文档内容
扬州中学高三化学月考试题 2024.01
试卷满分:100分 考试时间:75分钟
可能用到相对原子质量:H 1 O 16 C 12 N 14 Co 59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 材料是高新科技发展的物质基础,下列材料主要成分属于合金的是
A. 高性能铜箔 B. 半导体氮化镓 C. 快中子反应堆钠钾导热剂 D. 聚氨酯树脂
2. 某医用胶水的结构如图 ,下列说法正确的是
A. 第一电离能:N>C>O B. 分子中含π键数目为4
C. 合成单体中1-丁醇为非极性分子 D. 元素电负性:N>H>C
3. 化学家舍勒将软锰矿(主要成分是MnO )与浓盐酸作为原料制氯气。兴趣小组利用下列装置进行如下实
2
验,能达到预期目的的是
A.制取氯气 B.净化氯气 C.收集氯气 D.制备漂白液
4. 下列说法正确的是
A. 键角:ClO>OF B. 酸性:CHCOOH>CH FCOOH
2 2 3 2
C. 分子的极性:O>O D. 基态原子未成对电子数:Mn>Cr
2 3
阅读以下资料回答5~7题:
周期表中ⅥA族元素及其化合物应用广泛。O 具有杀菌、消毒、漂白等作用;HS是一种易燃的有毒
3 2
气体(燃烧热为562.2 kJ/mol),常用于沉淀重金属离子;氯化亚砜(SOCl )是重要的有机试剂;硒
2
( Se)和碲( Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,Se是人体不可或
34 52
缺的微量元素,工业上通过电解强碱性NaTeO 溶液制备Te。
2 3
5.下列说法不正确的是
A.16O、17O、18O互为同位素 B.HO+和SOCl 的的中心原子杂化轨道类型均为sp3
3 2
C.HO 为极性分子 D.CaO 中阴阳离子数目比为2:1
2 2 2
6.下列方程式书写正确的是
1
学科网(北京)股份有限公司A.SOCl 遇水强烈水解:SOCl +H O=2H++SO2-+2Cl-
2 2 2 3
B.HS与硫酸铜溶液反应:Cu2++H S=CuS↓+2H+
2 2
C.HS的燃烧:HS(g)+2O(g)=SO(g)+HO(l) △H= -562.2kJ/mol
2 2 2 3 2
D.工业制Te阴极反应:TeO 2-+6H++4e-=Te+3H O
3 2
7. 下列物质的性质与用途具有对应关系的是
A.浓硫酸有强氧化性,可用于实验室制乙烯
B.FeS 难溶于水,可用于工业制二氧化硫
2
C.二氧化硫有漂白性,可用于去除织物的石蕊污迹
D.NaSO 有还原性,可用于消除纺织品漂白后的残留氯
2 2 3
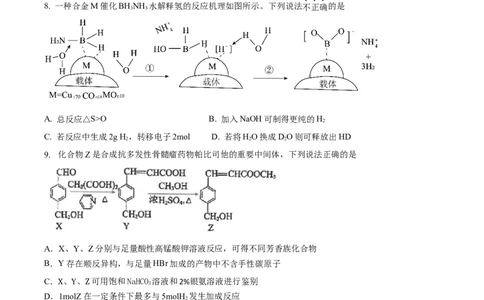
8. 一种合金M催化BHNH 水解释氢的反应机理如图所示。下列说法不正确的是
3 3
A. 总反应△S>O B. 加入NaOH可制得更纯的H
2
C. 若反应中生成2g H ,转移电子2mol D. 若将HO换成DO则可释放出HD
2 2 2
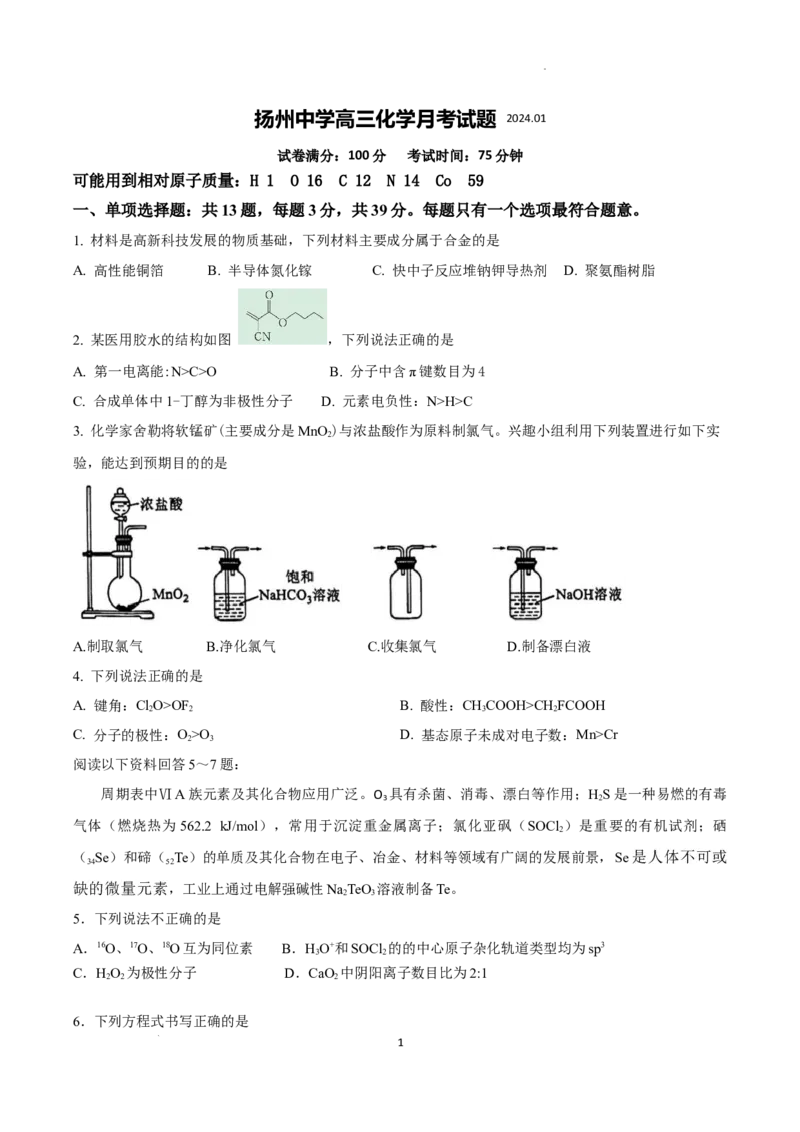
9. 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,下列说法正确的是
A.X、Y、Z分别与足量酸性高锰酸钾溶液反应,可得不同芳香族化合物
B.Y存在顺反异构,与足量HBr加成的产物中不含手性碳原子
C.X、Y、Z可用饱和NaHCO 溶液和2%银氨溶液进行鉴别
3
D.1molZ在一定条件下最多与5molH 发生加成反应
2
10.由含硒废料(主要含S、Se、Fe O、CuO、ZnO、SiO 等)制取硒的流程如下:
2 3 2
下列有关说法正确的是
2
学科网(北京)股份有限公司A.流程中的“分离”操作为蒸馏
B. “滤液”中主要存在的阴离子有:SO 、SiO 、SeSO
C. “酸化”时发生的离子反应方程式为SeSO +H O=Se↓+SO ↑+2OH-
2 2
D. SiO 晶胞如图所示,1个SiO 晶胞中有16个O原子
2 2
11.室温下,下列实验方案能达到探究目的的是
选项 实验方案 探究目的
向盛有饱和NaCO 溶液的试管中加入少量苯酚浊液,观
A 2 3 比较苯酚与碳酸的酸性强弱
察沉淀是否溶解、是否有气体生成
取某有机物(无环状结构单元)与KOH溶液混合加热充
B 分反应,冷却后取上层清液,加入硝酸酸化,再加入硝 该有机物中是否含有氯元素
酸银溶液,观察是否有白色沉淀生成
将Fe O 溶于盐酸所得溶液浓缩后,滴入酸性KMnO 溶
C 3 4 4 Fe O 中是否含Fe(Ⅱ)
液,观察溶液颜色的变化 3 4
比较Ksp(BaSO)、
用饱和NaCO 溶液浸泡BaSO 固体,过滤,将所得固体 4
D 2 3 4
溶于稀硝酸,观察沉淀是否溶解、是否有气体生成
Ksp(BaCO )大小
3
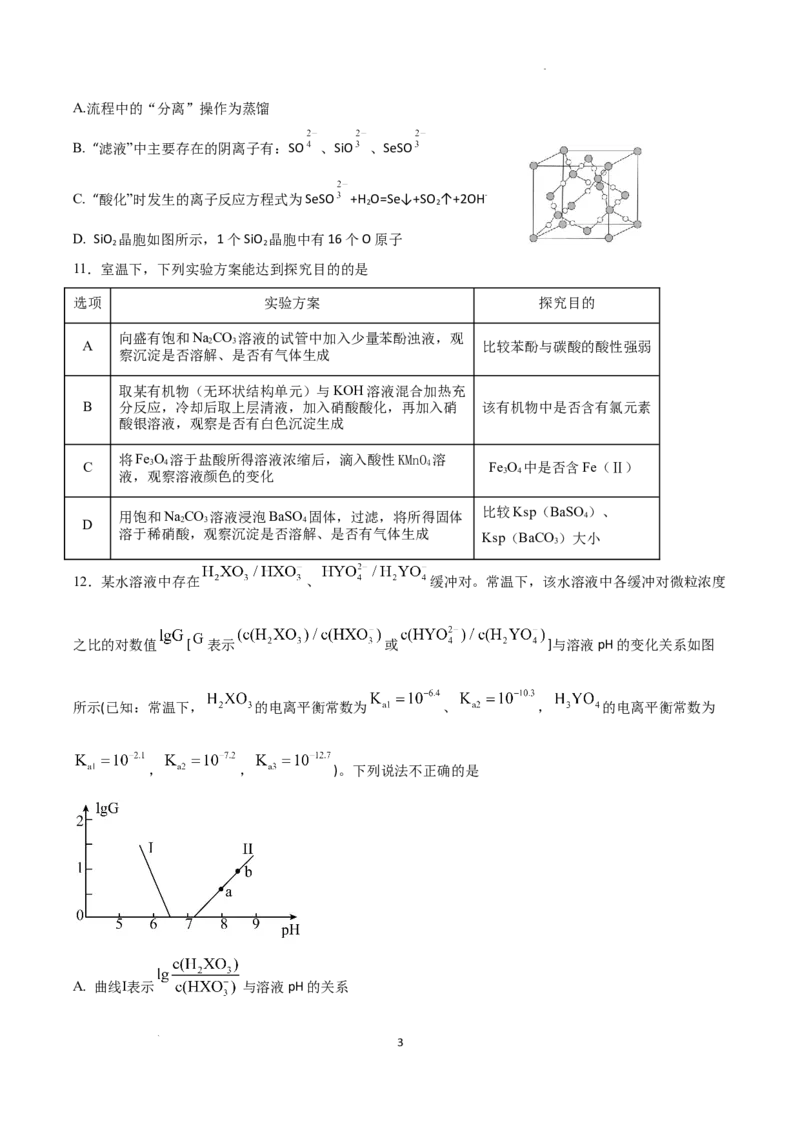
12.某水溶液中存在 、 缓冲对。常温下,该水溶液中各缓冲对微粒浓度
之比的对数值 [ 表示 或 ]与溶液pH的变化关系如图
所示(已知:常温下, 的电离平衡常数为 、 , 的电离平衡常数为
, , )。下列说法不正确的是
A. 曲线Ⅰ表示 与溶液pH的关系
3
学科网(北京)股份有限公司B. 的过程中,水的电离程度越来越大
C. 当溶液pH逐渐增大时, 逐渐减小
D. 当 时,
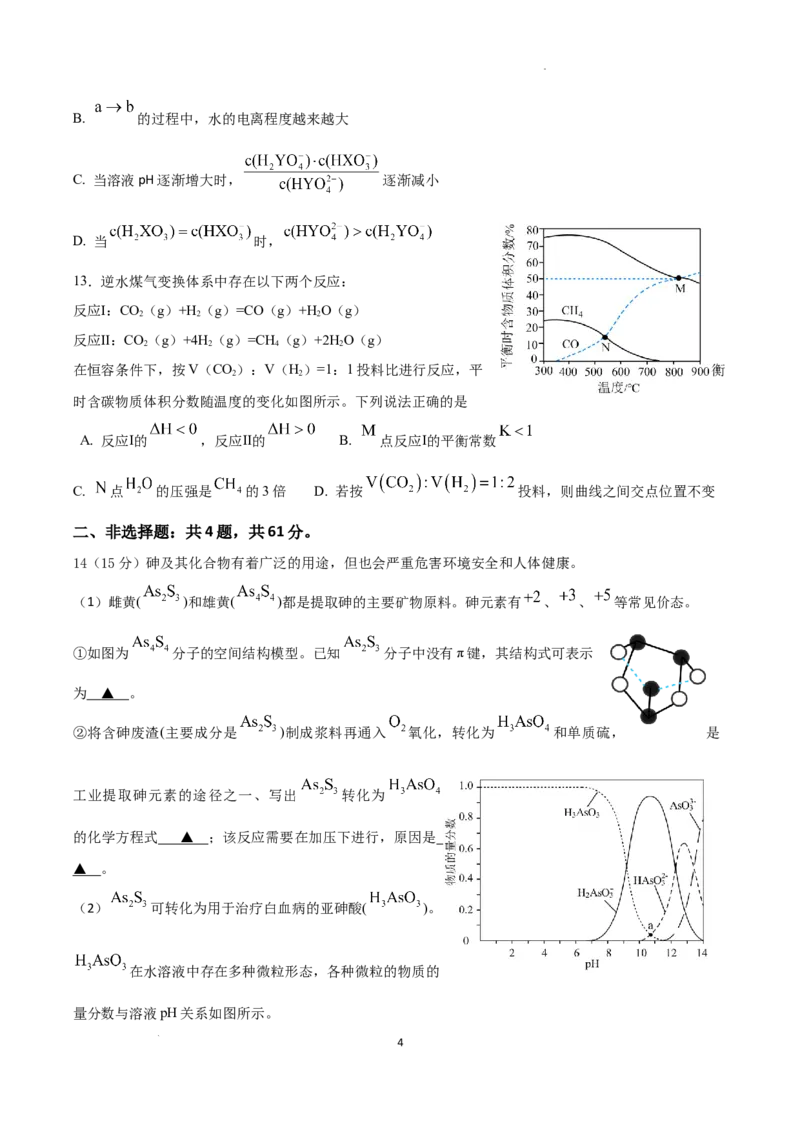
13.逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:CO(g)+H (g)=CO(g)+H O(g)
2 2 2
反应Ⅱ:CO(g)+4H (g)=CH (g)+2H O(g)
2 2 4 2
在恒容条件下,按V(CO):V(H)=1:1投料比进行反应,平 衡
2 2
时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
A. 反应Ⅰ的 ,反应Ⅱ的 B. 点反应Ⅰ的平衡常数
C. 点 的压强是 的3倍 D. 若按 投料,则曲线之间交点位置不变
二、非选择题:共4题,共61分。
14(15分)砷及其化合物有着广泛的用途,但也会严重危害环境安全和人体健康。
(1)雌黄( )和雄黄( )都是提取砷的主要矿物原料。砷元素有 、 、 等常见价态。
①如图为 分子的空间结构模型。已知 分子中没有π键,其结构式可表示
为 ▲ 。
②将含砷废渣(主要成分是 )制成浆料再通入 氧化,转化为 和单质硫, 是
工业提取砷元素的途径之一、写出 转化为
的化学方程式 ▲ ;该反应需要在加压下进行,原因是
▲ 。
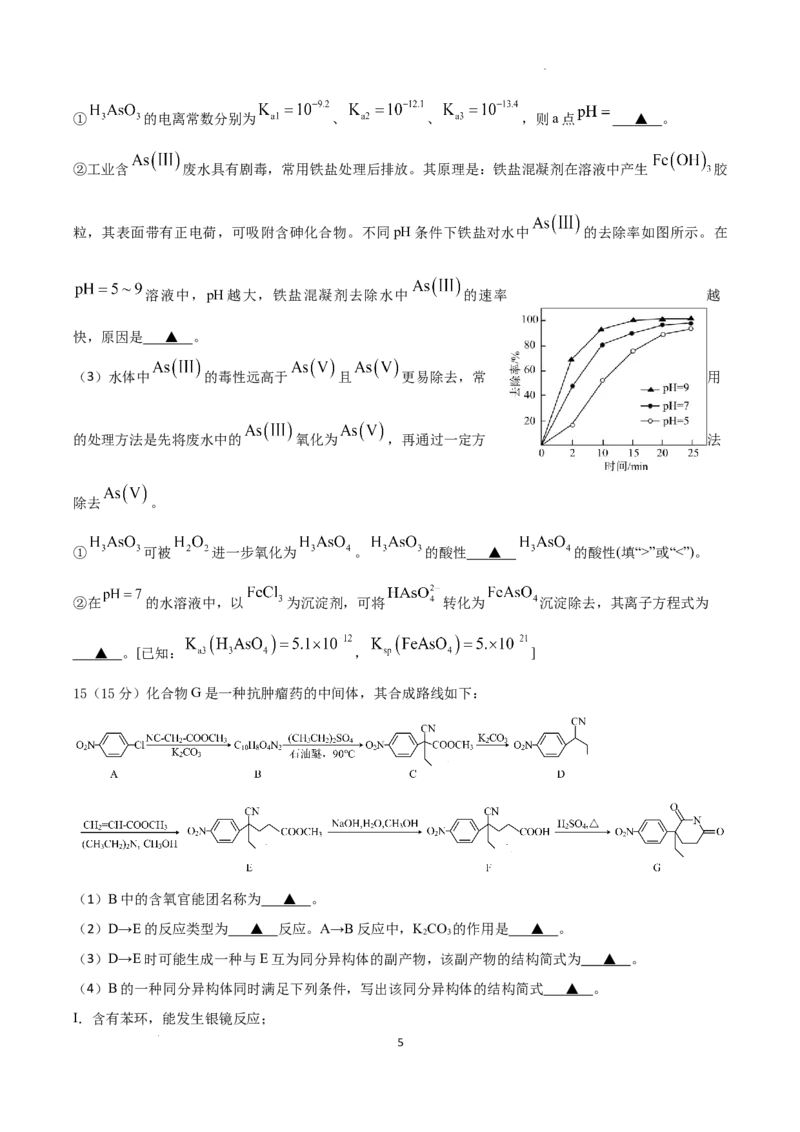
(2) 可转化为用于治疗白血病的亚砷酸( )。
在水溶液中存在多种微粒形态,各种微粒的物质的
量分数与溶液pH关系如图所示。
4
学科网(北京)股份有限公司① 的电离常数分别为 、 、 ,则a点 ▲ 。
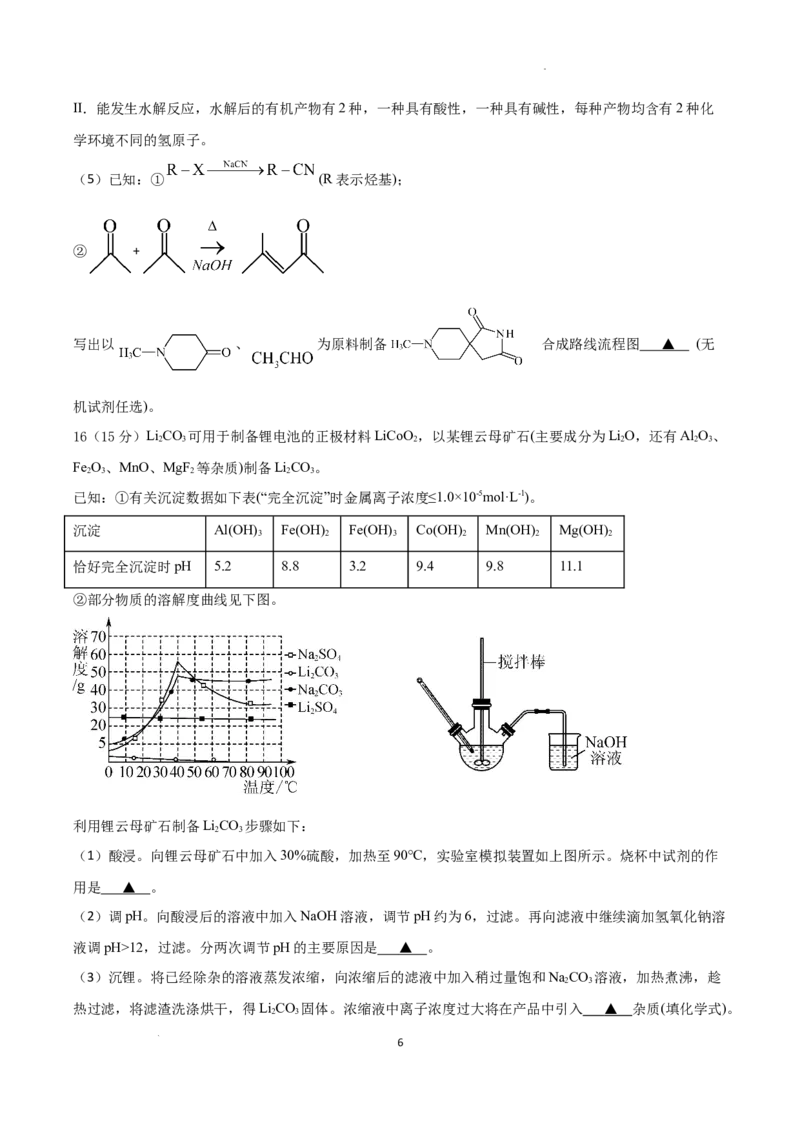
②工业含 废水具有剧毒,常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生 胶
粒,其表面带有正电荷,可吸附含砷化合物。不同pH条件下铁盐对水中 的去除率如图所示。在
溶液中,pH越大,铁盐混凝剂去除水中 的速率 越
快,原因是 ▲ 。
(3)水体中 的毒性远高于 且 更易除去,常 用
的处理方法是先将废水中的 氧化为 ,再通过一定方 法
除去 。
① 可被 进一步氧化为 。 的酸性 ▲ 的酸性(填“>”或“<”)。
②在 的水溶液中,以 为沉淀剂,可将 转化为 沉淀除去,其离子方程式为
▲ 。[已知: , ]
15(15分)化合物G是一种抗肿瘤药的中间体,其合成路线如下:
(1)B中的含氧官能团名称为 ▲ 。
(2)D→E的反应类型为 ▲ 反应。A→B反应中,KCO 的作用是 ▲ 。
2 3
(3)D→E时可能生成一种与E互为同分异构体的副产物,该副产物的结构简式为 ▲ 。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 ▲ 。
I.含有苯环,能发生银镜反应;
5
学科网(北京)股份有限公司Ⅱ.能发生水解反应,水解后的有机产物有2种,一种具有酸性,一种具有碱性,每种产物均含有2种化
学环境不同的氢原子。
(5)已知:① (R表示烃基);
② +
写出以 、 为原料制备 合成路线流程图 ▲ (无
的
机试剂任选)。
16(15分)LiCO 可用于制备锂电池的正极材料LiCoO ,以某锂云母矿石(主要成分为LiO,还有Al O、
2 3 2 2 2 3
Fe O、MnO、MgF 等杂质)制备LiCO。
2 3 2 2 3
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1)。
沉淀 Al(OH) Fe(OH) Fe(OH) Co(OH) Mn(OH) Mg(OH)
3 2 3 2 2 2
恰好完全沉淀时pH 5.2 8.8 3.2 9.4 9.8 11.1
②部分物质的溶解度曲线见下图。
利用锂云母矿石制备LiCO 步骤如下:
2 3
(1)酸浸。向锂云母矿石中加入30%硫酸,加热至90℃,实验室模拟装置如上图所示。烧杯中试剂的作
用是 ▲ 。
(2)调pH。向酸浸后的溶液中加入NaOH溶液,调节pH约为6,过滤。再向滤液中继续滴加氢氧化钠溶
液调pH>12,过滤。分两次调节pH的主要原因是 ▲ 。
(3)沉锂。将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和NaCO 溶液,加热煮沸,趁
2 3
热过滤,将滤渣洗涤烘干,得LiCO 固体。浓缩液中离子浓度过大将在产品中引入 ▲ 杂质(填化学式)。
2 3
6
学科网(北京)股份有限公司(4)LiCO 和Co O 混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO ,写出反应方程式:
2 3 3 4 2
▲ 。
(5)CoC O·2H O热分解可制备Co O 请补充完整由含c(Co2+)=0.1mol·L-1的浸出液(含有杂质Al3+、Fe3+、
2 4 2 3 4.
Fe2+)制备纯净的CoC O·2H O实验方案: ▲ ,干燥,得到CoC O·2H O晶体。(须使用的试剂:
2 4 2 2 4 2
NaClO,NaOH,AgNO 溶液,(NH )C O,蒸馏水)
3 3 4 2 2 4
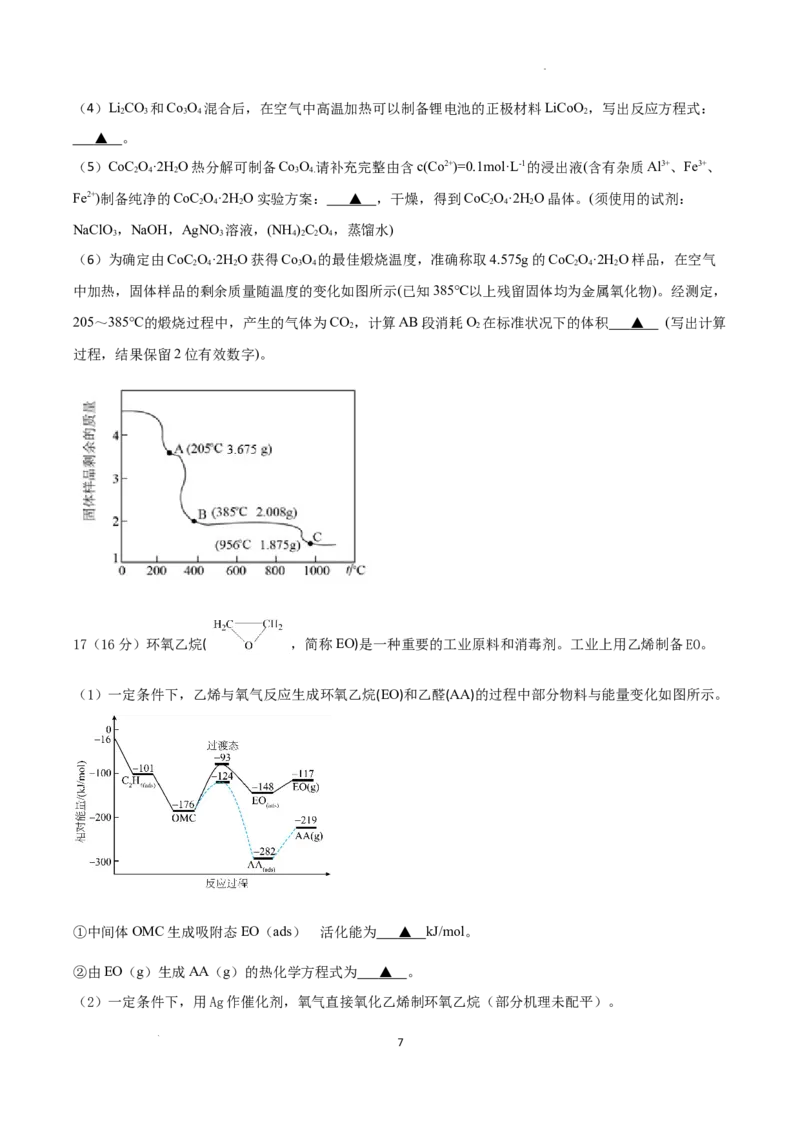
(6)为确定由CoC O·2H O获得Co O 的最佳煅烧温度,准确称取4.575g的CoC O·2H O样品,在空气
2 4 2 3 4 2 4 2
中加热,固体样品的剩余质量随温度的变化如图所示(已知385℃以上残留固体均为金属氧化物)。经测定,
205~385℃的煅烧过程中,产生的气体为CO,计算AB段消耗O 在标准状况下的体积 ▲ (写出计算
2 2
过程,结果保留2位有效数字)。
17(16分)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。工业上用乙烯制备EO。
(1)一定条件下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)的过程中部分物料与能量变化如图所示。
的
①中间体OMC生成吸附态EO(ads) 活化能为 ▲ kJ/mol。
②由EO(g)生成AA(g)的热化学方程式为 ▲ 。
(2)一定条件下,用Ag作催化剂,氧气直接氧化乙烯制环氧乙烷(部分机理未配平)。
7
学科网(北京)股份有限公司主反应:2CH=CH (g)+O (g)=2EO(g) △H=-213.8kJ/mol
2 2 2
副反应:C H(g)+3O (g)=2CO (g)+2H O(g)△H=-1323kJ/mol
2 4 2 2 2
催化机理:O+Ag(助剂)→O-(ads)+Ag+
2 2
O-(ads)+ CH=CH +Ag+→EO+ O(ads)+Ag
2 2 2
O(ads)+ CH=CH →CO+H O
2 2 2 2
①实际生产采用220-260℃的可能原因是 ▲ 。
②选择性S的定义:S(B)= ×100%,该生产中S(EO)= ▲ 。
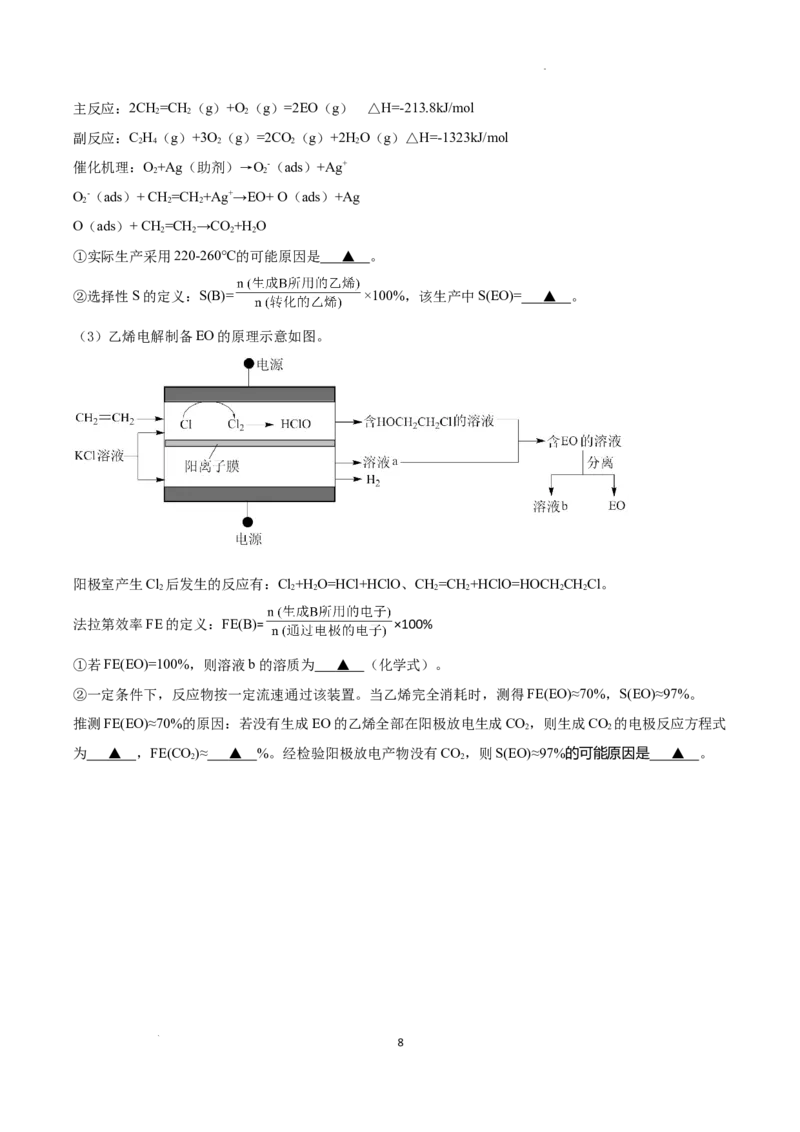
(3)乙烯电解制备EO的原理示意如图。
阳极室产生Cl 后发生的反应有:Cl+H O=HCl+HClO、CH=CH +HClO=HOCH CHCl。
2 2 2 2 2 2 2
法拉第效率FE的定义:FE(B)= ×100%
①若FE(EO)=100%,则溶液b的溶质为 ▲ (化学式)。
②一定条件下,反应物按一定流速通过该装置。当乙烯完全消耗时,测得FE(EO)≈70%,S(EO)≈97%。
推测FE(EO)≈70%的原因:若没有生成EO的乙烯全部在阳极放电生成CO,则生成CO 的电极反应方程式
2 2
为 ▲ ,FE(CO)≈ ▲ %。经检验阳极放电产物没有CO,则S(EO)≈97%的可能原因是 ▲ 。
2 2
8
学科网(北京)股份有限公司参考答案:
1C 2B 3D 4A 5D 6B 7D 8B 9C 10D 11B 12D 13C
14. (1) ①. ②.
③. 增大反应物 的浓度,加快 的转化速率
(2) ①. 10.65 ②. 增大,更多的 转变为 (或 中 的物
质的量分数增大),带负电荷的 更易被带正电荷的 胶粒吸附除去; 增大,
胶粒的量增多,吸附效果增强(3分)
(3) ①. < ②.
15. (1)硝基、酯基 (2)加成 吸收HCl,促进反应正向移动 (3)
(4)
9
学科网(北京)股份有限公司(5)
(5分)
16.(1)吸收HF,防止污染空气
(2)除尽Fe3+、Al3+; 防止铝元素转化为 ,无法去除
(3)NaSO (4)6LiCO+4Co O+O 12LiCoO +6CO
2 4 2 3 3 4 2 2 2
(5)向浸出液中边搅拌加入适量NaClO 氧化Fe2+,再滴加NaOH溶液调节pH的范围至5.2~7.4除去
3
Al3+、Fe3+。过滤,向滤液中加入(NH )C O 溶液至不再产生沉淀,过滤,用蒸馏水洗涤至取最后一次洗涤
4 2 2 4
的滤液加入AgNO 溶液不再出现沉淀为止 (4分)
3
(6)0.37L(3分)
4.575g样品中:n(CoC O·2H O)=0.025mol
2 4 2
其中:m(HO)=0.025mol×18g∙mol−1×2=0.9g,m(CoC O) =4.575g−0.9g=3.675g,则A点为CoC O,Co的
2 2 4 2 4
质量为0.025mol×59g∙mol−1=1.475g(1分)
根据385℃以上残留固体均为金属氧化物,则B点中氧的质量m(O)=2.008g−1.475g=0.533g,则n(O)=
0.033mol,则n(Co):n(O)=3:4,则B为Co O(1分)
3 4
A点到B点在空气中加热,其反应方程式为3CoC O+2O Co O+6CO,则消耗氧气物质的量为
2 4 2 3 4 2
(1分)
17.(1)①. 83 ②. EO(g)=AA(g)△H=-102kJ/mol
(2)①温度低与220℃,反应太慢;温度高于260℃,催化剂活性降低 ②85.7%
(3)①KCl ②CH+4HO-12e-=2CO+12H+ 13 溶液a与HOCHCHCl反应不完全
2 4 2 2 2 2
10
学科网(北京)股份有限公司