文档内容
专题 08 元素周期表与元素周期律
内容概览
考点01 元素周期表及其应用
考点02 元素周期律及其应用
考点03 有关元素周期表和周期律的综合考查
考点01 元素周期表及其应用
1.(23-24高一上·河南省开封市联考·期末)元素周期表中某区域的一些元素多用于制造半导体材料,它
们是
A.左下方区域的金属元素
B.右上方区域的非金属元素
C.金属元素和非金属元素分界线附近的元素
D.稀有气体元素
2.(23-24高一上·新疆乌鲁木齐市六校联考·期末)铼可用于制造航空发动机的核心部件。铼元素在周期
表中的信息如图所示。下列有关该元素说法错误的是
A.属于金属元素 B.元素符号为Re
C.质子数为75 D.相对原子质量为186.2g
3.(23-24高一上·天津市重点校·期末)根据元素周期律和周期表,下列推断不合理的是
A.第83号元素的最高化合价是+5价
B.在周期表中金属与非金属的分界处可以找到半导体材料
C.某元素原子最外电子层上只有两个电子,该元素一定是第Ⅱ 族元素
D.元素周期表中第3列的元素种类数最多
4.(23-24高一上·广东省广州市·期末)元素周期表的建立是化学发展史上的重要里程碑之一,下表列出
了A~G7种元素在周期表中的位置:
学科网(北京)股份有限公司请回答下列问题:
(1)画出A的原子结构示意图 ,写出化合物 的电子式 。
(2)到目前为止,元素周期表的第七周期已经被填满,如果发现第119号元素,则它的性质与表中
(填字母,从A~G中选择)元素的性质最相似。
(3)写出D的单质与B的氢氧化物的水溶液反应的化学方程式 ,若反应中产生6.72L气体(标
准状况),则消耗D的质量为 g。
(4)F、G元素氢化物的稳定性由大到小的顺序是 (写化学式),它们含有的化学键为
(填“非极性键”或“极性键”)。
(5)比较B、C的金属性大小: (填元素符号),请设计实验进行证明。
实验方案 预期现象
考点02 元素周期律及其应用
5.(23-24高一上·北京市东城区·期末)下列元素中,原子半径最大的是
A. B. C. D.
6.(23-24高一上·北京市朝阳区·期末)下列物质性质的比较中,不正确的是
A.酸性:HSO >HPO B.还原性: HCl>HBr
2 4 3 4
C.碱性:NaOH>Mg(OH) D.稳定性:HO>HS
2 2 2
7.(23-24高一上·广东省茂名市·期末)下列说法正确的是
A.碱性: B.半径:
C.酸性: D.最低负化合价:
8.(23-24高一上·吉林省部分名校·期末)下列事实不能用元素周期律解释的是
A.非金属性:N<O<F B.碱性:Al(OH) <Mg(OH) <NaOH
3 2
C.稳定性:HI<HBr<HCl D.酸性:HSO >HCO>HClO
2 3 2 3
9.(23-24高一上·吉林省部分名校·期末)下列关于元素金属性和非金属性强弱比较的说法错误的是
A.Fe投入 溶液中,能置换出Cu,说明Fe的金属性比Cu的强
B. 的酸性强于HF的酸性,说明Cl的非金属性强于F
学科网(北京)股份有限公司C.Na与冷水反应剧烈,而Mg与冷水反应缓慢,说明Na的金属性强于Mg
D.Si与 化合所需温度远高于S与 化合所需温度,说明S的非金属性强于Si
10.(23-24高一上·福建省福州市·期末)元素周期表和元素周期律可以指导人们进行规律性的推测和判
断。下列说法错误的是
A.若 和 白的核外电子层结构相同,则原子序数:X>Y
B.硫、硒为同主族元素,因此硒的主要化合价有-2、+4、+6
C. 和 分别位于第六周期IA和IIA族,碱性:
D.常温下,形状和大小相同的 、 与浓度相同的盐酸反应, 更剧烈
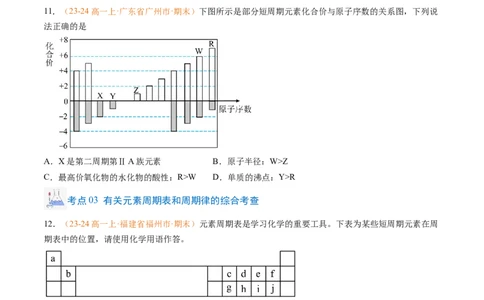
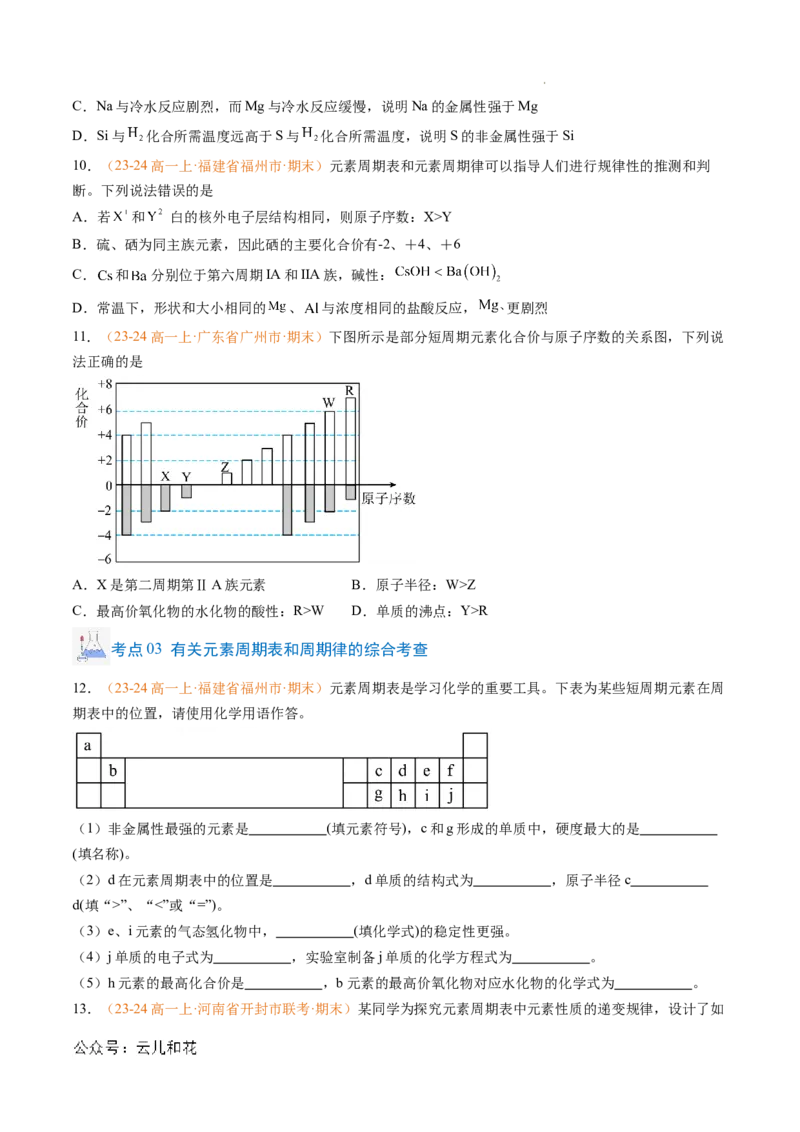
11.(23-24高一上·广东省广州市·期末)下图所示是部分短周期元素化合价与原子序数的关系图,下列说
法正确的是
A.X是第二周期第ⅡA族元素 B.原子半径:W>Z
C.最高价氧化物的水化物的酸性:R>W D.单质的沸点:Y>R
考点03 有关元素周期表和周期律的综合考查
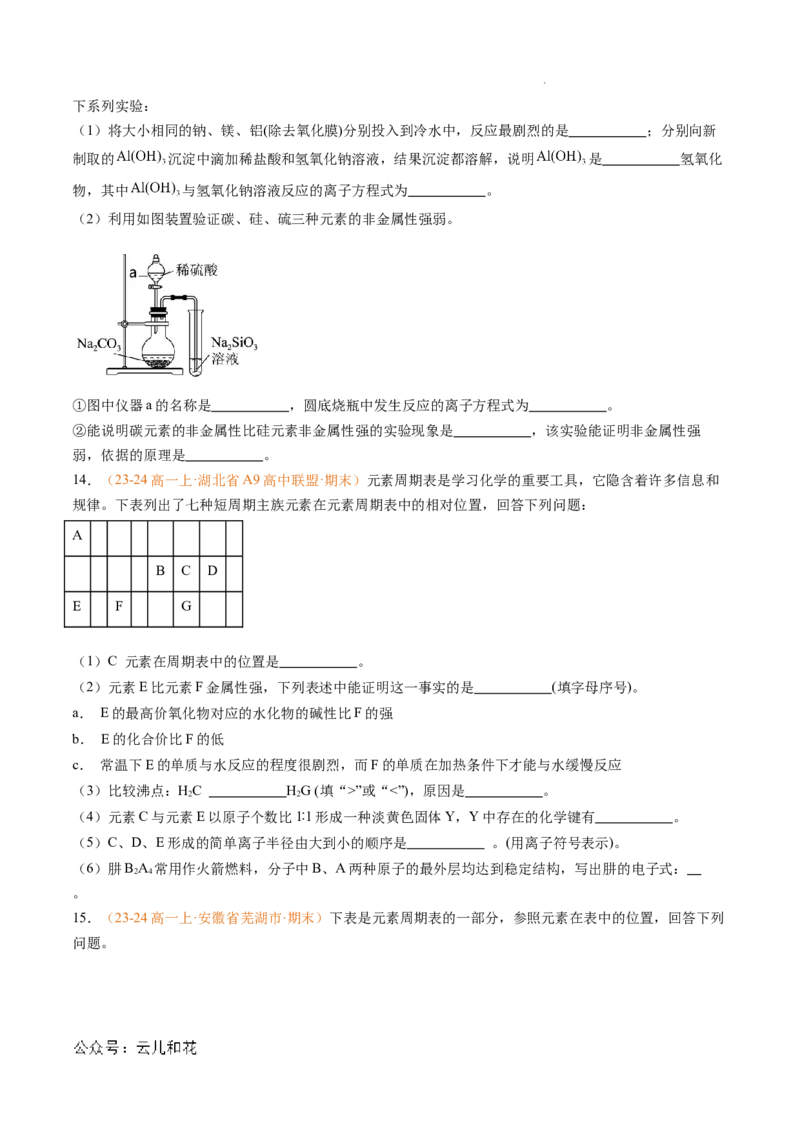
12.(23-24高一上·福建省福州市·期末)元素周期表是学习化学的重要工具。下表为某些短周期元素在周
期表中的位置,请使用化学用语作答。
(1)非金属性最强的元素是 (填元素符号),c和g形成的单质中,硬度最大的是
(填名称)。
(2)d在元素周期表中的位置是 ,d单质的结构式为 ,原子半径c
d(填“>”、“<”或“=”)。
(3)e、i元素的气态氢化物中, (填化学式)的稳定性更强。
(4)j单质的电子式为 ,实验室制备j单质的化学方程式为 。
(5)h元素的最高化合价是 ,b元素的最高价氧化物对应水化物的化学式为 。
13.(23-24高一上·河南省开封市联考·期末)某同学为探究元素周期表中元素性质的递变规律,设计了如
学科网(北京)股份有限公司下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是 ;分别向新
制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是 氢氧化
物,其中 与氢氧化钠溶液反应的离子方程式为 。
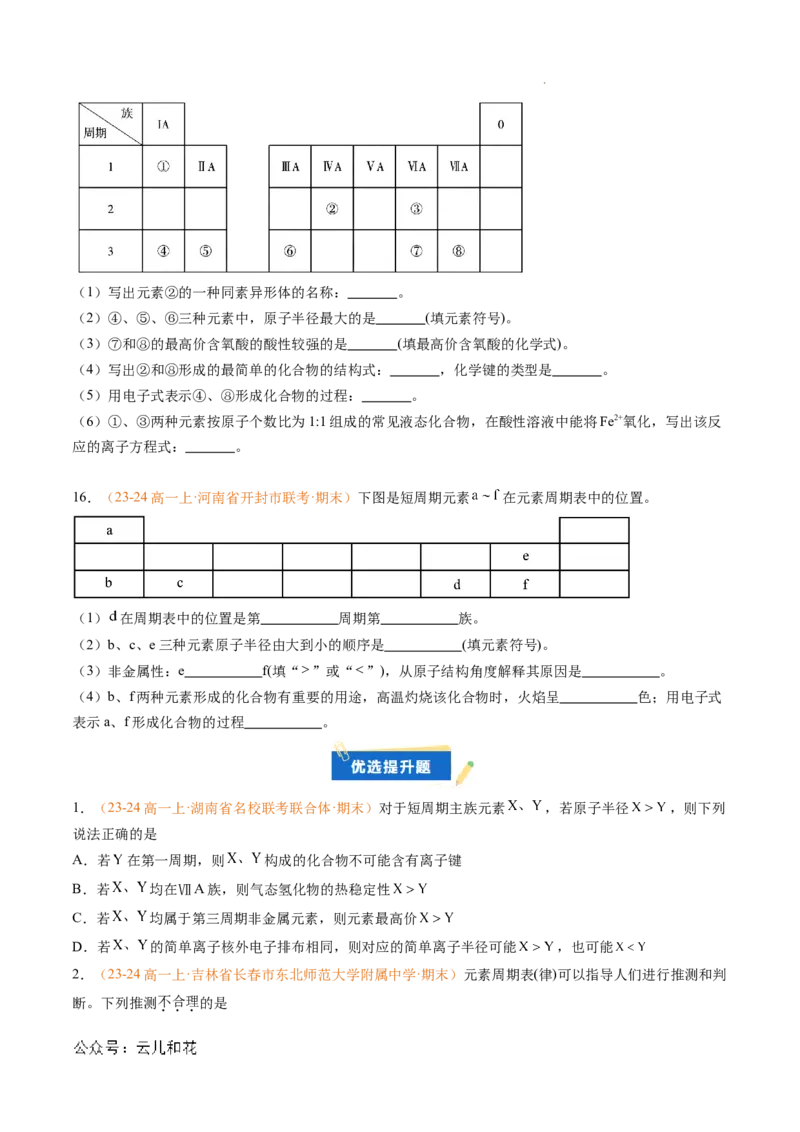
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
①图中仪器a的名称是 ,圆底烧瓶中发生反应的离子方程式为 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ,该实验能证明非金属性强
弱,依据的原理是 。
14.(23-24高一上·湖北省A9高中联盟·期末)元素周期表是学习化学的重要工具,它隐含着许多信息和
规律。下表列出了七种短周期主族元素在元素周期表中的相对位置,回答下列问题:
A
B C D
E F G
(1)C 元素在周期表中的位置是 。
(2)元素E比元素F金属性强,下列表述中能证明这一事实的是 (填字母序号)。
a. E的最高价氧化物对应的水化物的碱性比F的强
b. E的化合价比F的低
c. 常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水缓慢反应
(3)比较沸点:HC HG (填“>”或“<”),原因是 。
2 2
(4)元素C与元素E以原子个数比1∶1形成一种淡黄色固体Y,Y中存在的化学键有 。
(5)C、D、E形成的简单离子半径由大到小的顺序是 。(用离子符号表示)。
(6)肼B A 常用作火箭燃料,分子中B、A两种原子的最外层均达到稳定结构,写出肼的电子式:
2 4
。
15.(23-24高一上·安徽省芜湖市·期末)下表是元素周期表的一部分,参照元素在表中的位置,回答下列
问题。
学科网(北京)股份有限公司(1)写出元素②的一种同素异形体的名称: 。
(2)④、⑤、⑥三种元素中,原子半径最大的是 (填元素符号)。
(3)⑦和⑧的最高价含氧酸的酸性较强的是 (填最高价含氧酸的化学式)。
(4)写出②和⑧形成的最简单的化合物的结构式: ,化学键的类型是 。
(5)用电子式表示④、⑧形成化合物的过程: 。
(6)①、③两种元素按原子个数比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反
应的离子方程式: 。
16.(23-24高一上·河南省开封市联考·期末)下图是短周期元素 在元素周期表中的位置。
(1) 在周期表中的位置是第 周期第 族。
(2)b、c、e三种元素原子半径由大到小的顺序是 (填元素符号)。
(3)非金属性:e f(填“ ”或“ ”),从原子结构角度解释其原因是 。
(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈 色;用电子式
表示a、f形成化合物的过程 。
1.(23-24高一上·湖南省名校联考联合体·期末)对于短周期主族元素 ,若原子半径 ,则下列
说法正确的是
A.若 在第一周期,则 构成的化合物不可能含有离子键
B.若 均在ⅦA族,则气态氢化物的热稳定性
C.若 均属于第三周期非金属元素,则元素最高价
D.若 的简单离子核外电子排布相同,则对应的简单离子半径可能 ,也可能
2.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)元素周期表(律)可以指导人们进行推测和判
断。下列推测不合理的是
学科网(北京)股份有限公司A.若X+和Y2−的核外电子层结构相同,则原子序数:X>Y
B.由水溶液的酸性:HCl>HS,可推断元素的非金属性:Cl>S
2
C.Cs和Ba分别位于第六周期第IA和IIA族,则碱性:CsOH>Ba(OH)
2
D.IIA族元素依次为Be、Mg、Ca、Sr、Ba;MgSO4易溶于水,CaSO 微溶于水,则SrSO 可能难溶于水
4 4
3.(23-24高一上·广东省茂名市·期末)主族元素W、X、Y和Z在周期表中的相对位置如图所示,其中
元素X为Si,下列说法错误的是
W
X Y
Z
A.X的最高价氧化物与水反应生成强酸
B.W、Y两种元素的最简单氢化物之间能反应
C.可用单质Y、氢气、水为原料制取盐酸
D.Z原子的核外最外层电子数为6
4.(23-24高一上·广东省东莞市·期末)一种医药分子结构如下图所示。已知X、Y、Z、W、E的原子序
数依次增大,X是原子半径最小的元素,Y的最高正价与最低负价绝对值相等,Z的L层电子数是K层的
3倍,W、E的半径同周期最小(不考虑稀有气体原子)。下列说法正确的是
A.原子半径:Y<Z B. 含有非极性键
C.非金属性:W>Z D.该分子中所有原子的最外层都满足8电子结构
5.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)短周期主族元素W、X、Y、Z的原子序数
依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和
相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所
示。下列叙述正确的是
A.元素非金属性强弱的顺序为
B.离子半径关系
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
6.(23-24高一上·北京市东城区·期末)元素周期表与元素周期律在学习、研究和生产实践中有很重要的
作用。下表列出了5种元素在周期表中的位置,其中①~④代表4种元素。
学科网(北京)股份有限公司ⅠA ⅡA ⅢA ⅣA ⅤA ⅦA 0
3 ① ② ③
4 ④
(1)③的元素符号是 。
(2)下列能说明①比②失电子能力强的事实是 (填字母)。
a.单质①的密度比单质②的密度小
b.单质①比单质②更容易与水反应置换出氢气
c.最高价氧化物对应的水化物的碱性:①强于②
(3)依据元素周期律推测:
Ⅰ. 属于 (填“金属”或“非金属”)元素。
Ⅱ. 的最高价氧化物对应的水化物的化学式是 。
Ⅲ.气态氢化物的热稳定性: (填“强于”或“弱于”) 。
(4)某元素的原子结构示意图为 。下列关于该元素的说法正确的是 (填字
母)。
a.位于周期表中第五周期第ⅡA族 b.属于非金属元素
c.单质能与水反应 d.其碳酸盐难溶于水
7.(23-24高一上·广东省东莞市·期末)元素周期律和元素周期表,反映了元素性质与原子结构的关系,
在自然科学、生产实践等各方面都有重要意义。下图为部分短周期元素化合价与原子序数的关系图。
(1)b在元素周期表中的位置为 。
(2)f在半导体领域中有着重要应用,其原子结构示意图为 。
(3)h、g的气态氢化物稳定性由强到弱的顺序为 (填化学式)。
(4)c、d、e简单离子的半径从大到小为 (用化学式表示)。
(5)c与d形成的淡黄色化合物的电子式为 。
(6)X射线衍射法可以测定某些分子的结构,下列分子的结构模型正确是_______(填字母)。
学科网(北京)股份有限公司选项 A B C D
分子
平面正方形
直线形 直线形
直线形
结构
模型
(7)a、h的最高价氧化物的水化物酸性由强到弱的顺序为 (填化学式)。
(8)写出一条仅含a、b、c元素的氧化还原反应方程式 。
8.(23-24高一上·广东省茂名市·期末)元素周期律和周期表是我们研究、预测物质性质的重要工具。下
表是元素周期表中前四周期的5种元素的相关信息。
元
元素性质或原子结构
素
A
B B能形成多种单质,其中一种单质是硬度最大的物质
C 地壳中含量最高的金属元素,其合金可用于制造飞机外壳
D D的单质是一种黄绿色气体
E 用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃片)
回答下列问题:
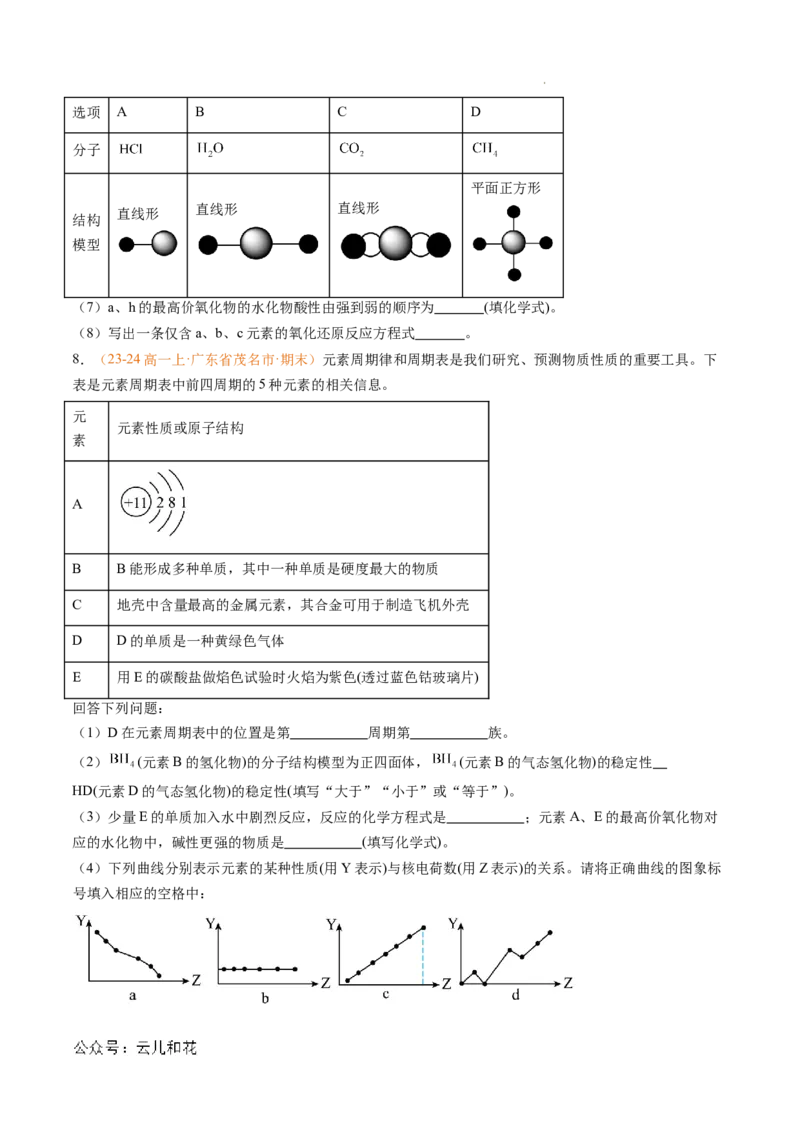
(1)D在元素周期表中的位置是第 周期第 族。
(2) (元素B的氢化物)的分子结构模型为正四面体, (元素B的气态氢化物)的稳定性
HD(元素D的气态氢化物)的稳定性(填写“大于”“小于”或“等于”)。
(3)少量E的单质加入水中剧烈反应,反应的化学方程式是 ;元素A、E的最高价氧化物对
应的水化物中,碱性更强的物质是 (填写化学式)。
(4)下列曲线分别表示元素的某种性质(用Y表示)与核电荷数(用Z表示)的关系。请将正确曲线的图象标
号填入相应的空格中:
学科网(北京)股份有限公司第ⅡA族元素的最外层电子数与核电荷数的关系为 ,第三周期主族元素的最高正化合价与核
电荷数的关系为 。
9.(23-24高一上·湖南省名校联考联合体·期末)元素周期表是学习物质结构和性质的重要工具。下表是
元素周期表的一部分,表中所列序号代表对应的元素。请回答下列问题:
(1)表中元素非金属性最强的是 (填元素符号),元素⑧在周期表中的位置是 。
(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是 (填物质名称)。
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序
是 (填离子符号)。
(4)①与⑤可形成 微粒,写出该微粒的电子式: 。
(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是 (填标号)。
a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与 化合的难易程度
c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③ ④(填“>”或“<”),元素④的单质可与元素③的最高价氧化物的水
化物反应,写出该反应的化学方程式: 。
10.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)结合元素周期表,回答下列问题:
族周
ⅠA 0
期
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨
(1)①、③、⑨按照原子个数比 构成化合物的结构式 。
(2)写出含有③、⑤元素且既具有离子键又具有非极性共价键化合物的电子式 。
(3)①②③⑤形成化合物在水溶液中的电离方程式 。
(4)下列事实能用元素周期律解释并正确的是 (填字母序号)。
a.对应阴离子还原性由强到弱的顺序为⑧>⑨>④
b.⑨的气态氢化物的稳定性大于④的氢化物
c.原子序数为35的元素最高价氧化物的水化的酸性比⑨最高价氧化物的水化的酸性强
d.③的简单氢化物的沸点高于⑧的氢化物
学科网(北京)股份有限公司e.原子半径由小到大的顺序为③<⑧<⑥<⑤
(5)②和⑦按照原子个数比 构成的固体化合物,易与水反应生成可燃性气体和白色沉淀。在相同条件
下,此气体密度是 密度的8倍。化合物与水反应的化学方程式为 。
(6)W是第Ⅷ族中原子序数最小的元素。W的单质可用于处理酸性废水中的 ,使其转换为 ,同
时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为 。
学科网(北京)股份有限公司