文档内容
哈三中 2024—2025 学年度下学期
高二学年月考考试 化学 试卷
可能用到的相对原子质量 H-1 C-12 O-16
I 卷(共 45 分)
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只
有一项符合题目要求。)
1.我国饮食注重营养均衡,讲究“色香味形”。下列说法错误的是
A.烹饪糖醋排骨用蔗糖炒出焦糖色,蔗糖属于二糖
B.端午时节用棕叶将糯米包裹成形,糯米中的淀粉可水解
C.凉拌黄瓜加醋使其具有可口酸味,食醋中含有极性分子
D.新鲜榨得的花生油具有独特油香,油脂属于芳香烃
2.下列化学用语或图示正确的是
A.3,3-二甲基戊烷的键线式: B.O 分子的球棍模型:
3
C.激发态H原子的轨道表示式: D.CO 的电子式:
2
3.下列有关化学概念或性质的判断错误的是
A.CH 分子是正四面体结构,则CH Cl 没有同分异构体
4 2 2
B.环己烷与苯分子中C—H键的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由R N+与PF-组成的离子液体常温下呈液态,与其离子的体积较大有关
4 6
4.化学用语可以表达化学过程,下列化学用语表达错误的是
A.用电子式表示Cl 的形成:
2
B.亚铜氨溶液除去合成氨原料气中的CO:
CuNH 2+ +CO+NH CuNH CO 2+
3 2 3 3 3
C.用电子云轮廓图示意p-pπ键的形成:
D.制备芳纶纤维凯芙拉:
高二化学 第1页 共8页
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}5.下列物质的结构或性质不能说明其用途的是
A.SiC的碳、硅原子间通过共价键形成空间网状结构,硬度大,故SiC可用作砂轮
磨料
B.具有网状结构的交联橡胶弹性好、强度高,故可用作汽车轮胎材料
C.葡萄糖分子结构中有多个羟基,故葡萄糖可与银氨溶液反应制作银镜
D.NaHCO 能中和酸并受热分解产生气体,故可用作加工馒头的膨松剂
3
6. 结构决定性质,性质决定用途。下列事实解释错误的是
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
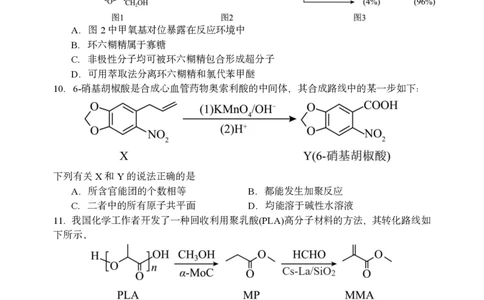
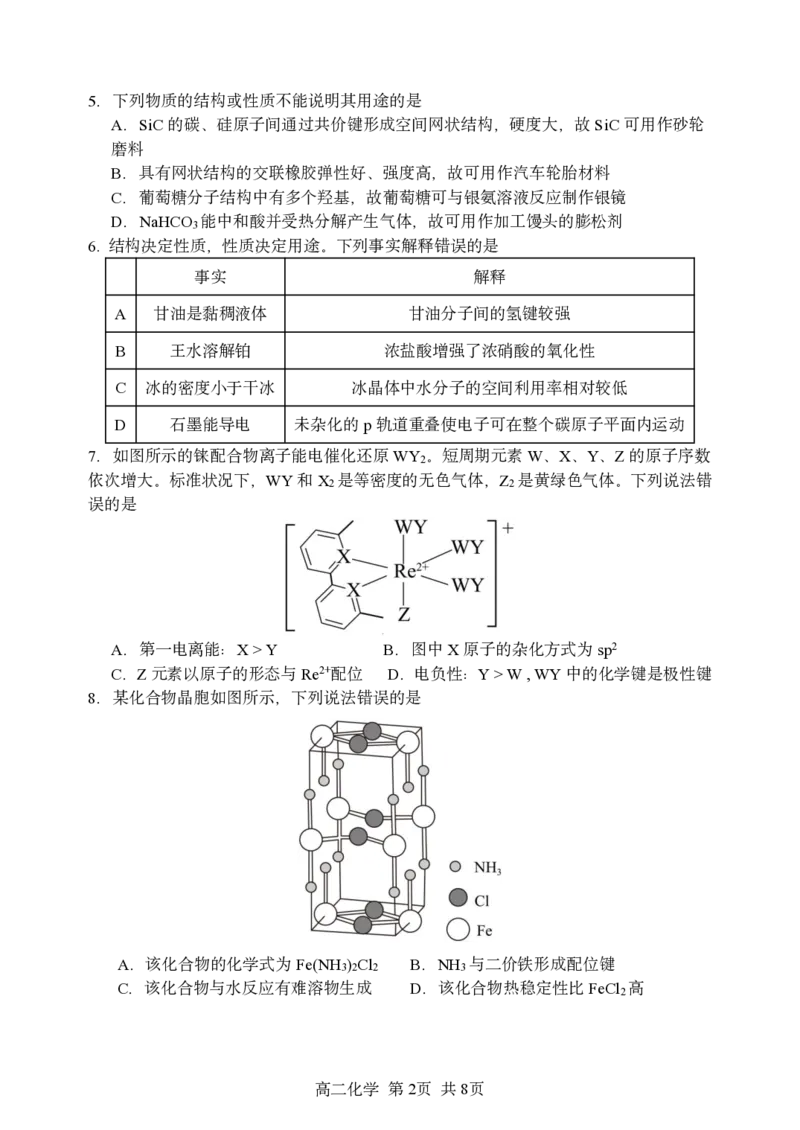
7.如图所示的铼配合物离子能电催化还原WY 。短周期元素W、X、Y、Z的原子序数
2
依次增大。标准状况下,WY和X 是等密度的无色气体,Z 是黄绿色气体。下列说法错
2 2
误的是
A.第一电离能:X>Y B.图中X原子的杂化方式为sp2
C.Z元素以原子的形态与Re2+配位 D.电负性:Y>W,WY中的化学键是极性键
8.某化合物晶胞如图所示,下列说法错误的是
A.该化合物的化学式为Fe(NH ) Cl B.NH 与二价铁形成配位键
3 2 2 3
C.该化合物与水反应有难溶物生成 D.该化合物热稳定性比FeCl 高
2
高二化学 第2页 共8页
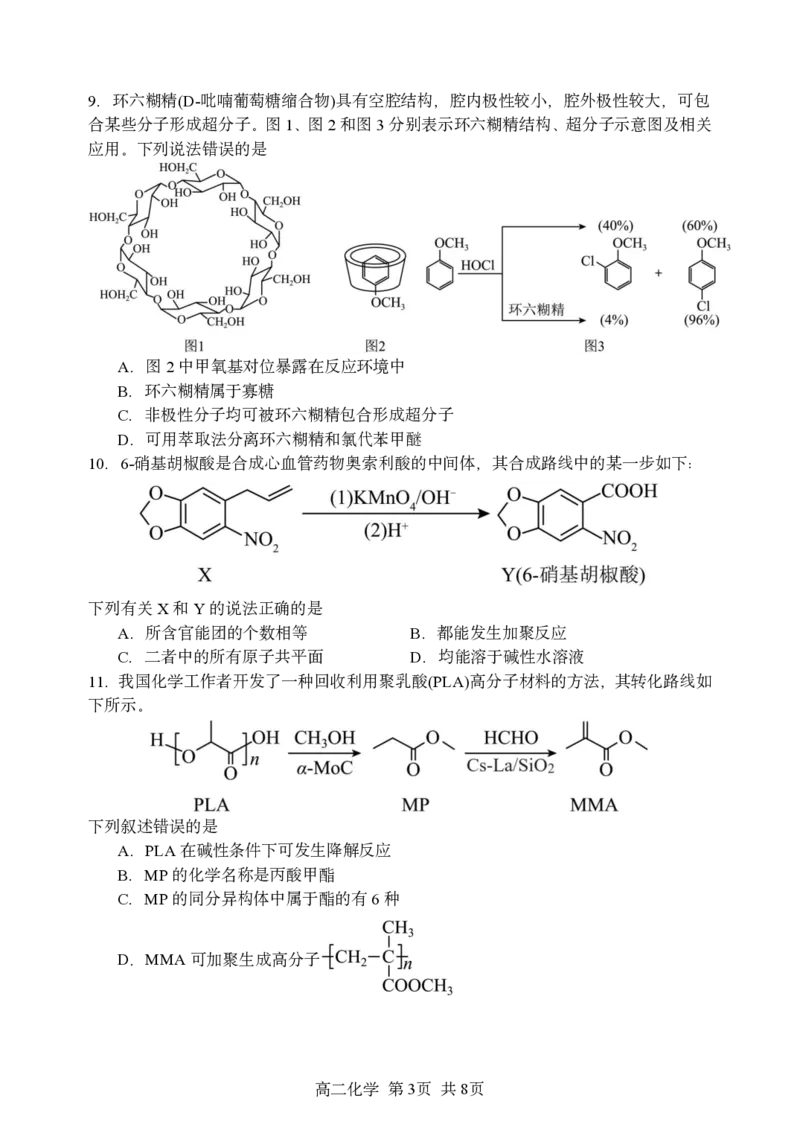
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}9.环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性较大,可包
合某些分子形成超分子。图1、图2和图3分别表示环六糊精结构、超分子示意图及相关
应用。下列说法错误的是
A.图2中甲氧基对位暴露在反应环境中
B.环六糊精属于寡糖
C.非极性分子均可被环六糊精包合形成超分子
D.可用萃取法分离环六糊精和氯代苯甲醚
10.6-硝基胡椒酸是合成心血管药物奥索利酸的中间体,其合成路线中的某一步如下:
下列有关X和Y的说法正确的是
A.所含官能团的个数相等 B.都能发生加聚反应
C.二者中的所有原子共平面 D.均能溶于碱性水溶液
11.我国化学工作者开发了一种回收利用聚乳酸(PLA)高分子材料的方法,其转化路线如
下所示。
下列叙述错误的是
A.PLA在碱性条件下可发生降解反应
B.MP的化学名称是丙酸甲酯
C.MP的同分异构体中属于酯的有6种
D.MMA可加聚生成高分子
高二化学 第3页 共8页
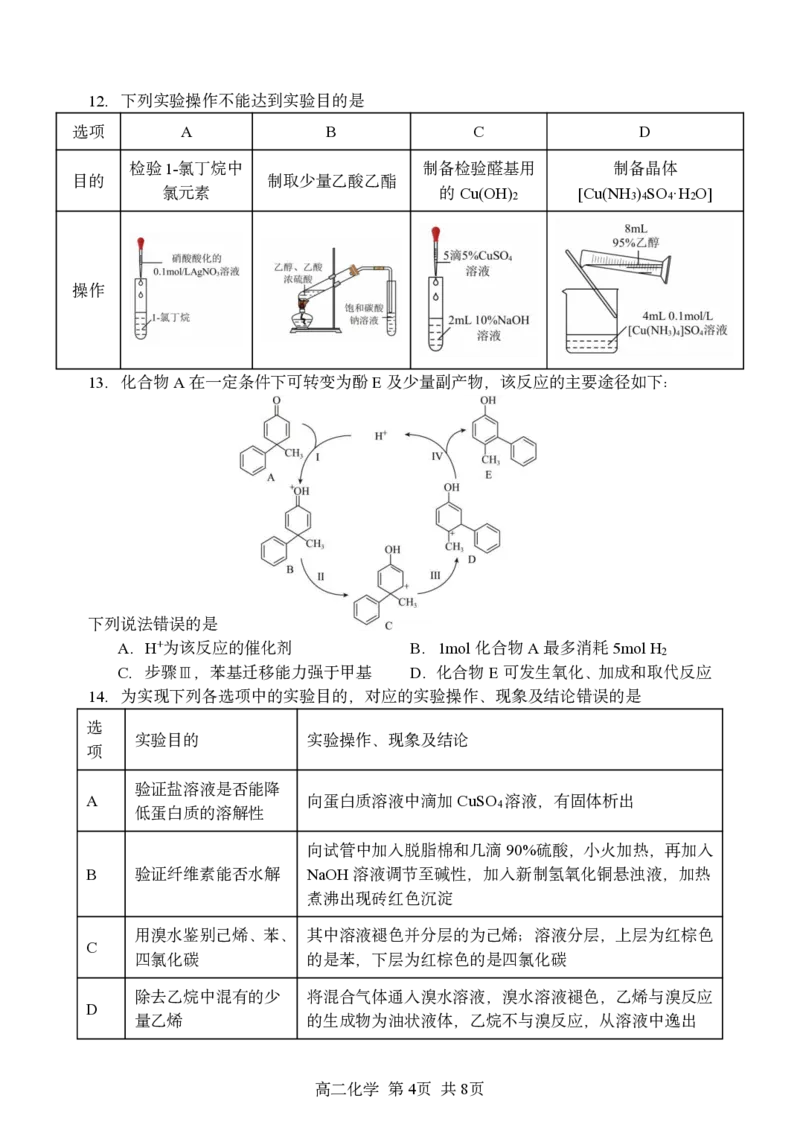
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}12.下列实验操作不能达到实验目的是
选项 A B C D
检验1-氯丁烷中 制备检验醛基用 制备晶体
目的 制取少量乙酸乙酯
氯元素 的Cu(OH) [Cu(NH ) SO ·H O]
2 3 4 4 2
操作
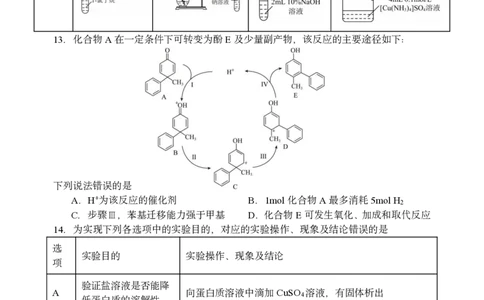
13.化合物A在一定条件下可转变为酚E及少量副产物,该反应的主要途径如下:
下列说法错误的是
A.H+为该反应的催化剂 B.1mol化合物A最多消耗5molH
2
C.步骤Ⅲ,苯基迁移能力强于甲基 D.化合物E可发生氧化、加成和取代反应
14.为实现下列各选项中的实验目的,对应的实验操作、现象及结论错误的是
选
实验目的 实验操作、现象及结论
项
验证盐溶液是否能降
A 向蛋白质溶液中滴加CuSO 溶液,有固体析出
4
低蛋白质的溶解性
向试管中加入脱脂棉和几滴90%硫酸,小火加热,再加入
B 验证纤维素能否水解 NaOH溶液调节至碱性,加入新制氢氧化铜悬浊液,加热
煮沸出现砖红色沉淀
用溴水鉴别己烯、苯、 其中溶液褪色并分层的为己烯;溶液分层,上层为红棕色
C
四氯化碳 的是苯,下层为红棕色的是四氯化碳
除去乙烷中混有的少 将混合气体通入溴水溶液,溴水溶液褪色,乙烯与溴反应
D
量乙烯 的生成物为油状液体,乙烷不与溴反应,从溶液中逸出
高二化学 第4页 共8页
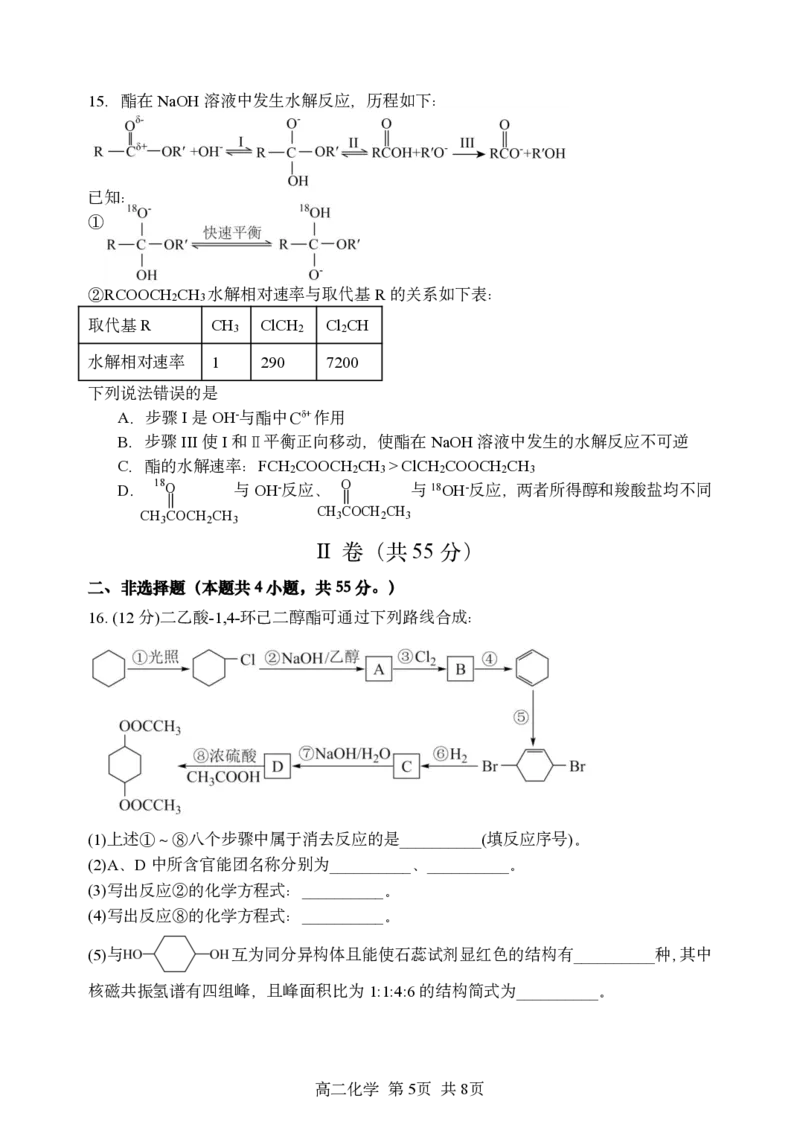
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}15.酯在NaOH溶液中发生水解反应,历程如下:
已知:
①
②RCOOCH
2
CH
3
水解相对速率与取代基R的关系如下表:
取代基R CH ClCH Cl CH
3 2 2
水解相对速率 1 290 7200
下列说法错误的是
A.步骤I是OH-与酯中Cδ+作用
B.步骤III使I和Ⅱ平衡正向移动,使酯在NaOH溶液中发生的水解反应不可逆
C.酯的水解速率:FCH COOCH CH >ClCH COOCH CH
2 2 3 2 2 3
D. 18O 与OH-反应、 O 与18OH-反应,两者所得醇和羧酸盐均不同
CH 3 COCH 2 CH 3 CH 3 COCH 2 CH 3
II 卷(共 55 分)
二、非选择题(本题共4小题,共55分。)
16.(12分)二乙酸-1,4-环己二醇酯可通过下列路线合成:
(1)上述①~⑧八个步骤中属于消去反应的是__________(填反应序号)。
(2)A、D中所含官能团名称分别为__________、__________。
(3)写出反应②的化学方程式:__________。
(4)写出反应⑧的化学方程式:__________。
(5)与 互为同分异构体且能使石蕊试剂显红色的结构有__________种,其中
核磁共振氢谱有四组峰,且峰面积比为1:1:4:6的结构简式为__________。
高二化学 第5页 共8页
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}17.(14分)2-硝基-1,3-苯二酚是重要的医药中间体。实验室常以间苯二酚为原料,经磺化、
硝化、去磺酸基三步合成:
部分物质相关性质如表:
名称 相对分子质量 性状 熔点/℃ 水溶性(常温)
间苯二酚 110 白色针状晶体 110.7 易溶
2-硝基-1,3-苯二酚 155 桔红色针状晶体 87.8 难溶
制备过程如下:
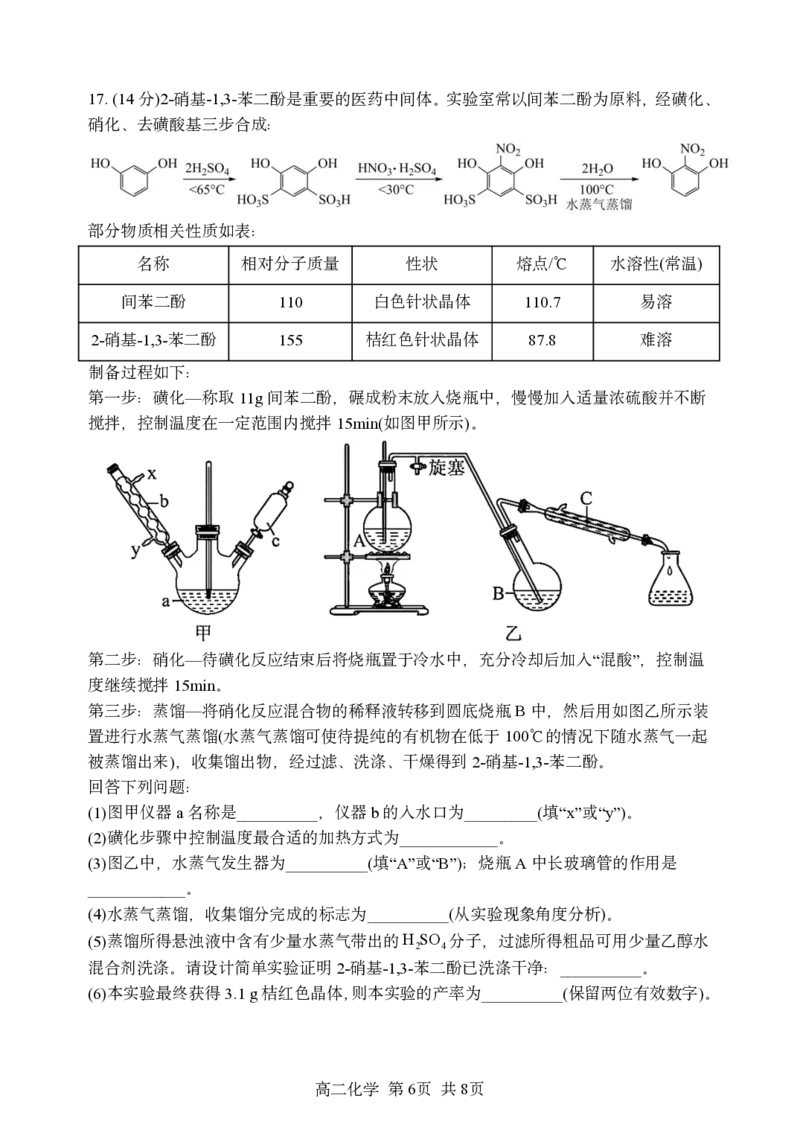
第一步:磺化—称取11g间苯二酚,碾成粉末放入烧瓶中,慢慢加入适量浓硫酸并不断
搅拌,控制温度在一定范围内搅拌15min(如图甲所示)。
第二步:硝化—待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温
度继续搅拌15min。
第三步:蒸馏—将硝化反应混合物的稀释液转移到圆底烧瓶B中,然后用如图乙所示装
置进行水蒸气蒸馏(水蒸气蒸馏可使待提纯的有机物在低于100℃的情况下随水蒸气一起
被蒸馏出来),收集馏出物,经过滤、洗涤、干燥得到2-硝基-1,3-苯二酚。
回答下列问题:
(1)图甲仪器a名称是__________,仪器b的入水口为_________(填“x”或“y”)。
(2)磺化步骤中控制温度最合适的加热方式为____________。
(3)图乙中,水蒸气发生器为__________(填“A”或“B”);烧瓶A中长玻璃管的作用是
____________。
(4)水蒸气蒸馏,收集馏分完成的标志为__________(从实验现象角度分析)。
(5)蒸馏所得悬浊液中含有少量水蒸气带出的H SO 分子,过滤所得粗品可用少量乙醇水
2 4
混合剂洗涤。请设计简单实验证明2-硝基-1,3-苯二酚已洗涤干净:__________。
(6)本实验最终获得3.1g桔红色晶体,则本实验的产率为__________(保留两位有效数字)。
高二化学 第6页 共8页
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}18. (14分)铟(In)是一种稀有金属,是电信、光电产品不可或缺的关键原材料。铟主要存
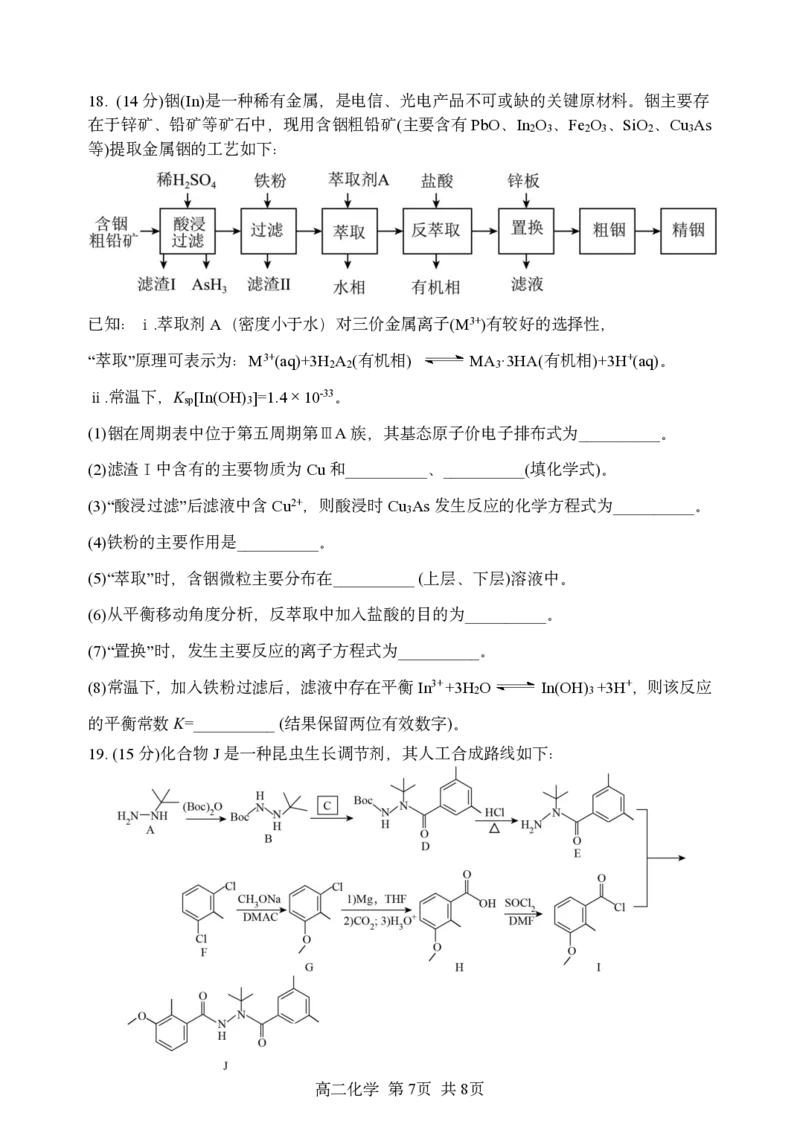
在于锌矿、铅矿等矿石中,现用含铟粗铅矿(主要含有PbO、In O 、Fe O 、SiO 、Cu As
2 3 2 3 2 3
等)提取金属铟的工艺如下:
已知:ⅰ.萃取剂A(密度小于水)对三价金属离子(M3+)有较好的选择性,
“萃取”原理可表示为:M3+(aq)+3H A (有机相) MA ·3HA(有机相)+3H+(aq)。
2 2 3
ⅱ.常温下,K
sp
[In(OH)
3
]=1.4×10-33。
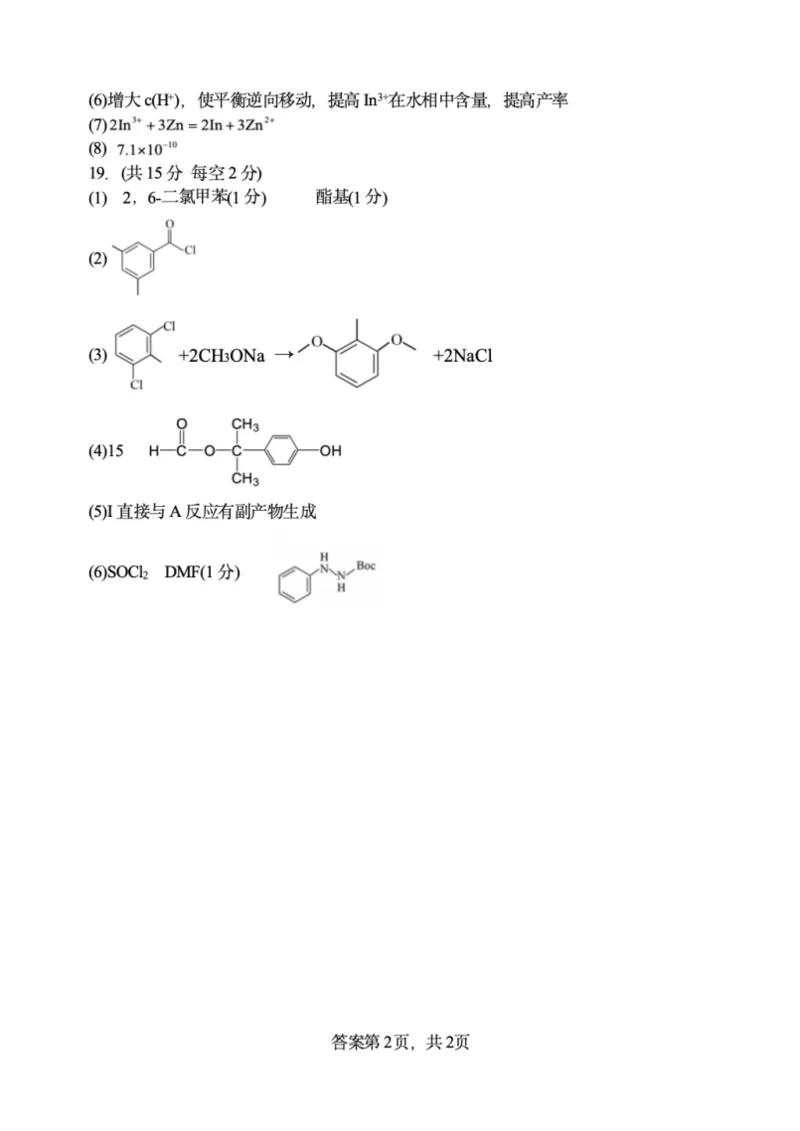
(1)铟在周期表中位于第五周期第ⅢA族,其基态原子价电子排布式为__________。
(2)滤渣Ⅰ中含有的主要物质为Cu和__________、__________(填化学式)。
(3)“酸浸过滤”后滤液中含Cu2+,则酸浸时Cu As发生反应的化学方程式为__________。
3
(4)铁粉的主要作用是__________。
(5)“萃取”时,含铟微粒主要分布在__________(上层、下层)溶液中。
(6)从平衡移动角度分析,反萃取中加入盐酸的目的为__________。
(7)“置换”时,发生主要反应的离子方程式为__________。
(8)常温下,加入铁粉过滤后,滤液中存在平衡In3++3H O In(OH) +3H+,则该反应
2 3
的平衡常数K=__________(结果保留两位有效数字)。
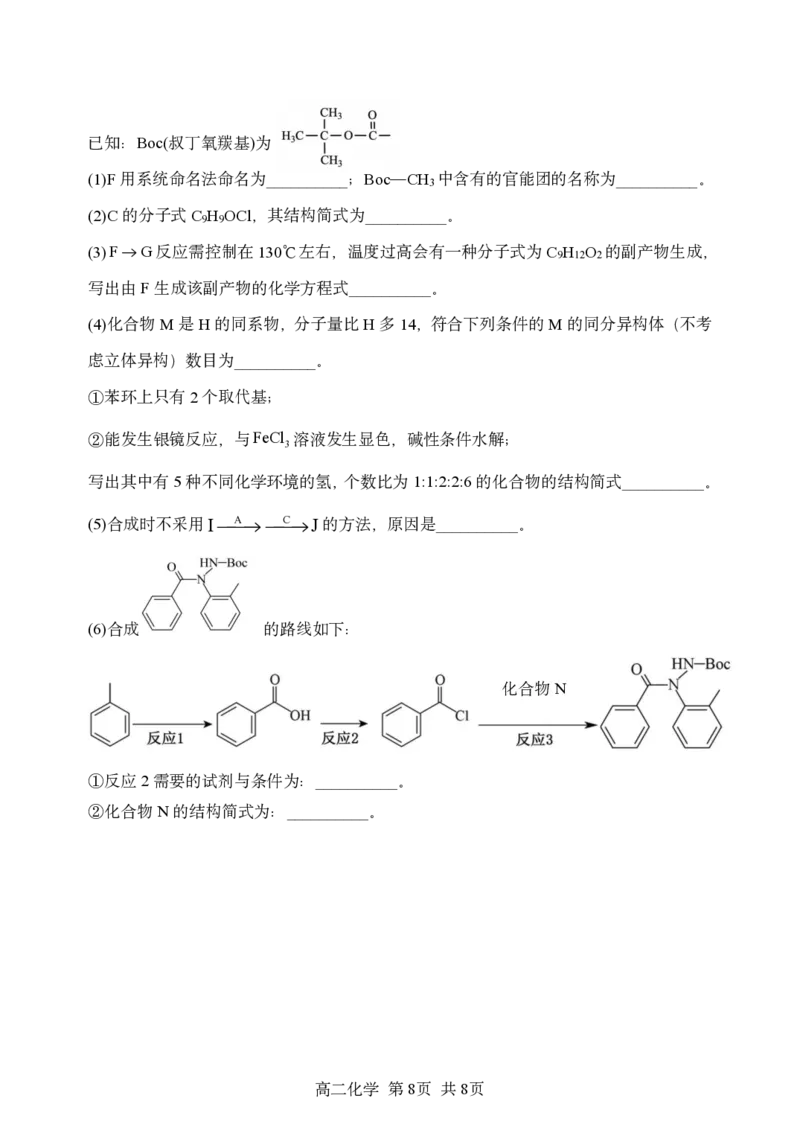
19.(15分)化合物J是一种昆虫生长调节剂,其人工合成路线如下:
高二化学 第7页 共8页
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}已知:Boc(叔丁氧羰基)为
(1)F用系统命名法命名为__________;Boc—CH 中含有的官能团的名称为__________。
3
(2)C的分子式C H OCl,其结构简式为__________。
9 9
(3)FG反应需控制在130℃左右,温度过高会有一种分子式为C
9
H
12
O
2
的副产物生成,
写出由F生成该副产物的化学方程式__________。
(4)化合物M是H的同系物,分子量比H多14,符合下列条件的M的同分异构体(不考
虑立体异构)数目为__________。
①苯环上只有2个取代基;
②能发生银镜反应,与FeCl 溶液发生显色,碱性条件水解;
3
写出其中有5种不同化学环境的氢,个数比为1:1:2:2:6的化合物的结构简式__________。
(5)合成时不采用IACJ的方法,原因是__________。
(6)合成 的路线如下:
化合物N
①反应2需要的试剂与条件为:__________。
②化合物N的结构简式为:__________。
高二化学 第8页 共8页
{#{QQABQYShwwowgEQACR6aRQEuCkgQkJCSJYouQUAQqAQrAAFABAA=}#}