文档内容
三明一中 2023—2024 学年上学期 12 月月考
高三化学试卷
(考试时长:75分钟满分:100分)
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 P-31 Mo-96
第Ⅰ卷
一、选择题(本题共10小题,每小题4分,共40分。每小题只有一个选项符合题意)
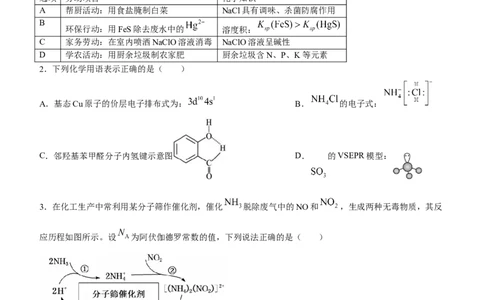
1.“致良知,知行合”。劳动有利于“知行合”。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 帮厨活动:用食盐腌制白菜 NaCl具有调味、杀菌防腐作用
B
环保行动:用FeS除去废水中的 溶度积:
C 家务劳动:在室内喷洒NaClO溶液消毒 NaClO溶液呈碱性
D 学农活动:用厨余垃圾制农家肥 厨余垃圾含N、P、K等元素
2.下列化学用语表示正确的是( )
A.基态Cu原子的价层电子排布式为: B. 的电子式:
C.邻羟基苯甲醛分子内氢键示意图 D. 的VSEPR模型:
3.在化工生产中常利用某分子筛作催化剂,催化 脱除废气中的NO和 ,生成两种无毒物质,其反
应历程如图所示。设 为阿伏伽德罗常数的值,下列说法正确的是( )
A. 溶液中含有 的数目为
B.常温下,4.6g二氧化氮气体中含有的分子数为
C. 中含有完全相同的 共价键的数目为:
学科网(北京)股份有限公司D.总反应中生成 (标准状况)时转移电子数为
4.铁是最常见的金属之一、纳米铁粉可用于处理酸性含氮废水(主要含) );铁易被腐蚀,经碱性发
蓝处理可增强其抗腐蚀性,方法为:用NaOH与 进行浸泡,在表面形成 的同时有 生成。
镍(Ni)与Fe单质化学性质相似,金属活动性比铁略低。酸性条件下, 的氧化性强于 , 的盐与碱
反应可以转化为不溶性的 。下列离子方程式正确的是( )
A.纳米铁粉处理酸性含 废水:
B.铁的发蓝处理:
C. 溶液中加少量氨水:
D. 与浓盐酸反应:
5.铼(Re)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主
族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质
反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法不正确的是
( )
A.元素第一电离能:
B.图中的阳离子与 互为等电子体,具有相同的空间结构
C.Q的最高价氧化物对应水化物可以和强碱反应
D.熔点:W晶体小于W、Y形成的晶体
6.维生素D含量越高,老年大脑的认知功能越好。目前已知的维生素D至少有10种分子,维生素D3是其
中重要的一种(结构如图),下列有关说法正确的是( )
学科网(北京)股份有限公司A.D3不存在手性碳原子 B.D3易溶于水,可溶解于水中服用
C.D3与溴水主要发生取代反应使其褪色 D.D3分子中虚线框内所含碳原子可能共平面
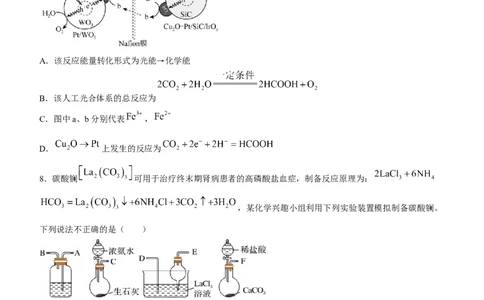
7.科研人员通过控制光沉积的方法构建 型复合材料光催化剂(光作用下生成 和
),然后以 和 离子渗透Nafion膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,
其反应机理如图。下列说法不正确的是( )
A.该反应能量转化形式为光能→化学能
B.该人工光合体系的总反应为
C.图中a、b分别代表 ,
D. 上发生的反应为
8.碳酸镧 可用于治疗终末期肾病患者的高磷酸盐血症,制备反应原理为:
,某化学兴趣小组利用下列实验装置模拟制备碳酸镧。
下列说法不正确的是( )
A.制备碳酸镧实验流程中导管从左向右的连接顺序为:F→A→B→D→E→C
B.X中盛放的试剂是浓硫酸,其作用为干燥
C.Y中发生反应的化学方程式为
D.Z中应先通入 ,后通入过量的
9.一种可充电的新型水系聚合物空气电池,其充放电时的工作原理如图所示。说法不正确的是( )
学科网(北京)股份有限公司A.放电时,电子由a极经用电器流向b极
B.放电过程时,b极区的pH变大
C.若有 参与电极反应,有 通过阳离子交换膜
D.充电时,电池总反应为
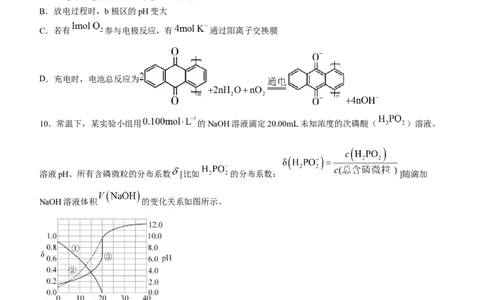
10.常温下,某实验小组用 的NaOH溶液滴定20.00mL未知浓度的次磷酸( )溶液。
溶液pH、所有含磷微粒的分布系数 [比如 的分布系数: ]随滴加
NaOH溶液体积 的变化关系如图所示。
下列说法错误的是( )
A.曲线①代表 ,曲线②代表
B. 的电离常数
C.滴定中用酚酞做指示剂
D.滴定终点时,溶液中
学科网(北京)股份有限公司第Ⅱ卷
二、非选择题(本题共4小题,共60分。)
11.(15分)次磷酸是一种一元弱酸,次磷酸钠( )是有机合成的常用还原剂,一般制备方法是
将黄磷( )和过量烧碱溶液混合、加热,生成次磷酸钠和 , 是一种无色、有毒的可燃性气体。
实验装置如图所示:
(1)在a中加入黄磷、活性炭粉末,打开 ,通入 一段时间,关闭 ,打开磁力加热搅拌器,滴加烧
碱溶液。
①仪器a的名称为______。
②活性炭粉末作为黄磷的分散剂,作用是______。
③a中反应的化学方程式为______。
(2)反应结束后,打开 ,继续通入 ,目的是______。
(3)碱性条件下,c中生成 和NaCl,c中反应的离子方程式为____________。相关物质溶解度
(S)如下:
NaCl 37 39
100 667
充分反应后,将a、c中溶液混合,将混合液(含极少量NaOH)蒸发浓缩,有大量晶体析出,该晶体主要成
分的化学式为______,然后______、再冷却结晶、过滤、洗涤、干燥,得到含 的粗产品。
(4)产品纯度测定:取产品1.50克配成250mL溶液,取25mL于锥形瓶中,酸化后加入25mL,0.10mol/L
碘水,于暗处充分反应后,以淀粉溶液做指示剂,用 溶液滴定至终点,平均消耗
18.00mL,相关反应方程式为: , 产品
纯度为______(保留3位有效数字)。
学科网(北京)股份有限公司12.(16分)Mo、Co均为重要战略性金属。以 为载体的钴钼废催化剂中含CoS、 及少量Fe、
Si、Ca等元素的物质,经系列处理可制取 、 ,工艺流程如图所示:
已知:①“焙烧”后各元素转化为相应氧化物,“酸浸”后钼元素转化为 。
②常温下, , , 。
③金属离子开始沉淀和完全沉淀时pH范围: , , 。
(1) 在空气中焙烧的化学方程式为______。
(2)“滤渣1”的主要成分为______。“滤渣2”的主要成分为 和 ,“调pH”中调节pH
的合理范围为______。
(3)“水相”经萃取后得钴的有机相,存在平衡: ,然后加反萃取剂进行反
萃取,可得含 的水溶液,可作为反萃取剂的一种常用物质为______(写化学式)溶液。
(4)“沉钴”过程中为防止 转化为 ,需控制溶液pH,转化过程存在平衡:
,该反应的平衡常数 ______
(结果保留一位小数)。
(5)氮化钼量子点可应用于电池及催化领域,其晶胞结构如图所示,氮化钼的化学式为______,钼原子周围
距离最近的氮原子有______个。若晶胞密度为 ,则晶胞参数 ______nm(设 为阿伏加德罗常
数的值)
学科网(北京)股份有限公司13.(14分)采取高效经济方式利用 对人类社会发展具有重要意义。以 和 为原料合成甲醇主要
发生反应Ⅰ和反应Ⅱ(不考虑其他反应):
Ⅰ.
Ⅱ.
回答以下问题:
(1)已知: ,则反应Ⅰ的 ______
。
(2)有利于提高 平衡转化率的措施有______(填标号)。
A.增大 投料比 B.增大压强
C.使用高效催化剂 D.及时将 分离
(3)在催化剂作用下,测得 平衡转化率(曲线Y)和平衡时 的选择性(曲线X)随温度变化
如图所示。(已知: 的选择性 )
① 加氢制 时,温度选择510~550K的原因为______。
②510K时,往恒容密闭容器中按 充入 和 ,若平衡时容器内
,则反应Ⅰ的平衡常数 ______(列计算式即可)。
(4) 和 在某催化剂表面合成甲醇(反应Ⅰ)的反应历程如图所示,其中吸附在催化剂表面上的物种
用*标注,“TS”表示过渡状态。
学科网(北京)股份有限公司①气体在催化剂表面的吸附是______(填“吸热”或“放热”)过程。
②该反应历程中反应速率最快步骤的化学方程式为______。
(5)甲醇催化制取丙烯( )的过程中发生如下反应:
Ⅰ.
Ⅱ.
反应Ⅰ的Arrhenius经验公式的实验数据如图所示,已知Arrhenius经验公式为 ( 为活化
能, 为速率常数,R和C为常数)。当改变外界条件时,实验数据由图中直线a变为直线b,则实验可能改
变的外界条件是______。
14.(15分)有机物F是合成抗肿瘤药物的重要中间体,其合成路线如下:
学科网(北京)股份有限公司已知:ⅰ.TBSCl为
ⅱ.
回答下列问题:
(1)化合物E中含氧官能团名称为______,A→B反应类型为______。
(2)F中碳原子的杂化类型为______,试剂a的结构简式为______。
(3)TBSCl的作用是______。
(4)B→C方程式为______。
(5)A在一定条件下与足量的乙酸发生酯化反应的化学方程式______。
(6)已知碳氧元素可形成类似 或 的环状有机物,请写出1种同时符合下列条件的化合物A的
同分异构体的结构简式(不包括立体异构体)______。
①分子中存在六元环;②不与钠反应;③H-NMR显示只有4种不同化学环境的氢原子
三明一中 2023—2024 学年上学期 12 月月考
高三化学参考答案
一、选择题(本题共10小题,每小题4分,共40分。每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10
答案 C A D B A D C B D B
二、非选择题(本题共5小题,共60分。)
11.(15分,第1空1分,其它每空2分)
(1)①三颈圆底烧瓶(三颈烧瓶)②使反应物充分混合(或增大反应物接触面积),加快反应速率
③
(2)排出装置中的未反应(或残留)的 ,使 被c装置(或NaClO溶液)吸收
(3) NaCl 趁热过滤 (4)93.9%
解析:(4)根据原子守恒有: ; , ;
据电子守恒有: ,即
学科网(北京)股份有限公司;1.50g产品中
;产品纯度为 。
12.(16分,每空2分)
(1) (2) 、
(3) (或 、HCl) (4) (5) 4
解析:(4)“沉钴”过程中为防止 转化为 ,需控制溶液pH,转化过程存在平衡:
,该反应的平衡常数
,
(5)氮化钼晶胞中,含有Mo数目为 ,含有N数目为 ,则氮化钼的化学式为
,从底面的面心钼原子观察,钼原子周围距离最近的氮原子有4个;若晶胞密度为 ,则
,晶胞参数 。
13.(14分,每空2分)
(1)-49.5 (2)BD (3)在510~550K之间 选择性和 转化率较高,且催化剂活性好,反应
速率较快
(4)吸热 (5)使用更高效的催化剂(增大催化剂比表面
积)解析:(3)① 加氢制 时,温度在510~550K之间 选择性和 转化率较高,且
催化剂活性好,反应速率较快,所以选择此温度区间;
②设 和 的物质的量分别为3m mol、mmol,则根据图中数据列三段式如下:
学科网(北京)股份有限公司起始(mol/L)m 3m 00
起始(mol/L)x 3x xx
平衡(mol/L)m-x 3m-3x xx
由 ,所以 ,则 ,
起始(mol/L)2.5 7.5 0 0
起始(mol/L)0.2 0.2 0.2 0.2
平衡(mol/L)1.5 4.9 0.2 1.0
;
(3)从该公式可以看到,活化能 就是直线斜率的相反数,a的斜率为 ,所以活化能就是
31kJ/mol;b相比a,斜率的相反数减小,也就是活化能降低,所以改变的外界条件是使用更高效的催化剂
(增大催化剂比表面积)。
14.(15分,第1空1分,其它每空2分)
(1)羟基 取代反应 (2) 杂化、 杂化
(3)保护“ ”,防止其被氧化
(4)2
(5)
(6) (任写1种)
学科网(北京)股份有限公司