文档内容
龙岩一中 2024 届高三上学期第三次月考
化 学
(满分:100 分 时间:75 分钟)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 Ca 40 Co 59 Fe 56 Mn 55
一、选择题(本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一项是符
合题目要求的)
1.我国古籍中蕴涵了许多化学知识。下列说法错误的是( )
..
A.“以磁石磨针锋,则能指南”中“磁石”的主要成分为Fe O
3 4
B.《本草纲目拾遗》中对强水的记载:性最猛烈,能蚀五金。强水为电解质
C.“欲试药金(铜锌合金),烧火有五色气起”,通过焰色反应可检验金属元素
D.“三月打雷麦谷堆”,在雷电作用下N 最终转化成能被农作物吸收的化合态氮
2
2.2-丁炔可发生如下转化,下列说法不正确的是
...
A.高分子Z可以使溴水褪色 B.X与酸性
1
K M n O
4
溶液反应可生成CH COOH
3
C.Y可以发生银镜反应 D.高分子Z可能存在顺式结构和反式结构
3.下列指定反应的离子方程式中,不正确的是( )
...
通电
A.工业上生产烧碱:2Cl−+2H O Cl +H +2OH−
2 2 2
B. Fe(OH) 和
3
N a C lO 的碱性溶液反应:3ClO−+2Fe(OH) +4OH− =2FeO2−+3Cl−+5H O
3 4 2
C.NaHSO 溶液和少量Ba(OH) 溶液反应:H++SO2−+Ba2++OH− =BaSO +H O
4 2 4 4 2
D.酸性KMnO 溶液和H O 溶液反应:2MnO−+5H O +6H+ =2Mn2++5O +8H O
4 2 2 4 2 2 2 2
4.2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼(Re)是生产飞机发动
机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其
中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到
铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
( )
A.元素第一电离能:Z>Y>W>Q
B.图中的阳离子存在三个共价键和一个配位键,四个键的
性质不同
C.熔点:W晶体大于W、Y形成的晶体
D.Q的最高价氧化物对应水化物可以和强碱反应
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}5.在碱性镀铜中电镀液的主要成分是Cu(NH ) SO ,其内界的电离与弱电解质类似,仅部分解
3 4 4
离为中心离子和配位体。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol/L Cu(NH ) SO 溶液中
3 4 4
2
C u ( N H
3
)
4
2 + 数目小于N
A
B.22.4L NH 含有的质子数目为10N
3 A
C.1mol C u ( N H
3
)
4
2 + 的配位键数目为2N
A
D.N 和H 合成1mol NH 转移电子数目为3N
2 2 3 A
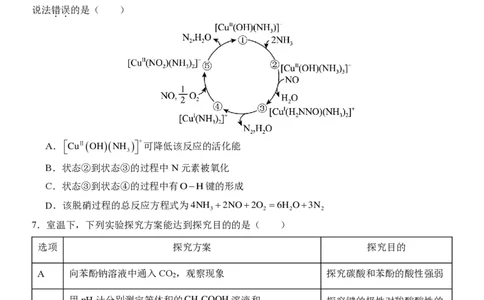
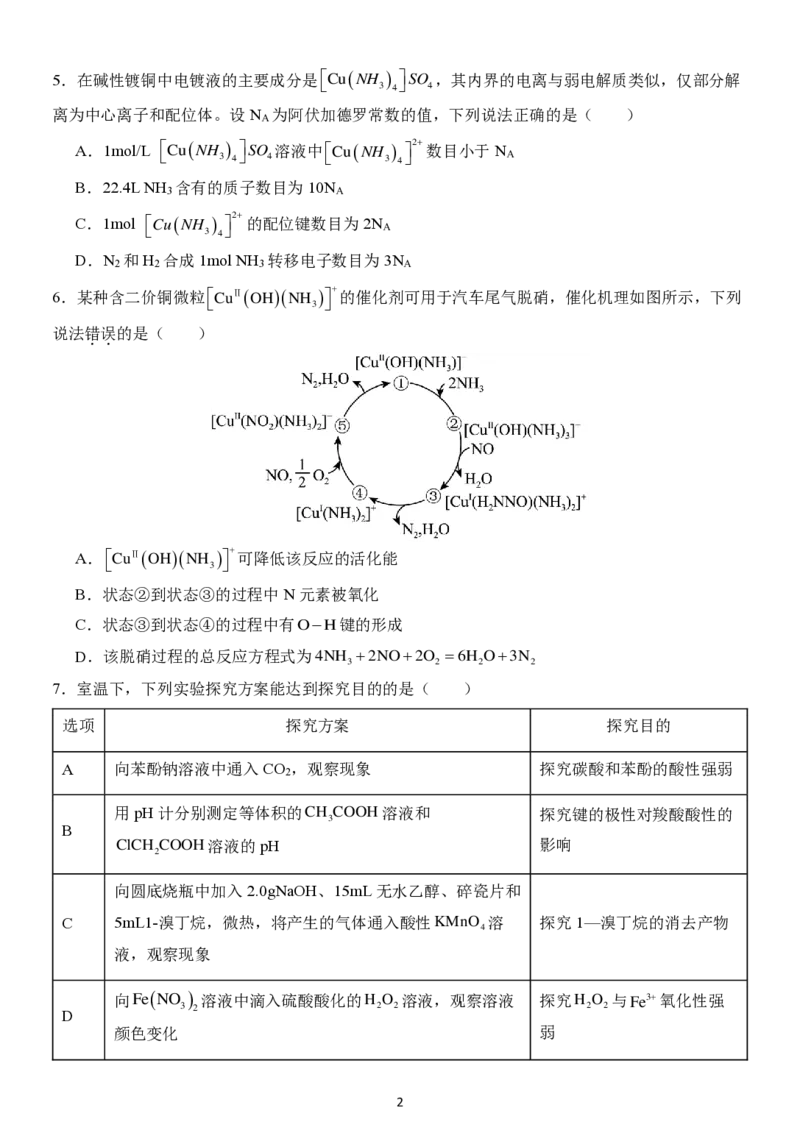
6.某种含二价铜微粒CuⅡ(OH)(NH ) + 的催化剂可用于汽车尾气脱硝,催化机理如图所示,下列
3
说法错误的是( )
..
A. C u Ⅱ ( O H ) ( N H
3
) + 可降低该反应的活化能
B.状态②到状态③的过程中N元素被氧化
C.状态③到状态④的过程中有 O − H 键的形成
D.该脱硝过程的总反应方程式为 4 N H
3
+ 2 N O + 2 O
2
= 6 H
2
O + 3 N
2
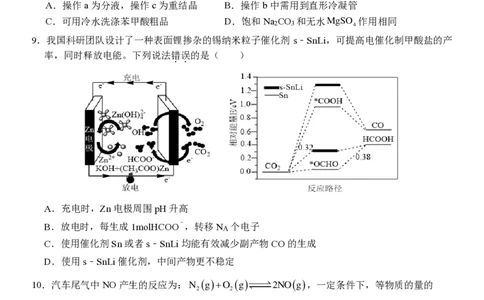
7.室温下,下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
A 向苯酚钠溶液中通入CO ,观察现象 探究碳酸和苯酚的酸性强弱
2
用pH计分别测定等体积的
B
C H
3
C O O H 溶液和 探究键的极性对羧酸酸性的
ClCH COOH溶液的pH 影响
2
向圆底烧瓶中加入2.0gNaOH、15mL无水乙醇、碎瓷片和
C 5mL1-溴丁烷,微热,将产生的气体通入酸性KMnO 溶 探究1—溴丁烷的消去产物
4
液,观察现象
向Fe(NO ) 溶液中滴入硫酸酸化的H O 溶液,观察溶液 探究H O 与Fe3+氧化性强
3 2 2 2 2 2
D
颜色变化 弱
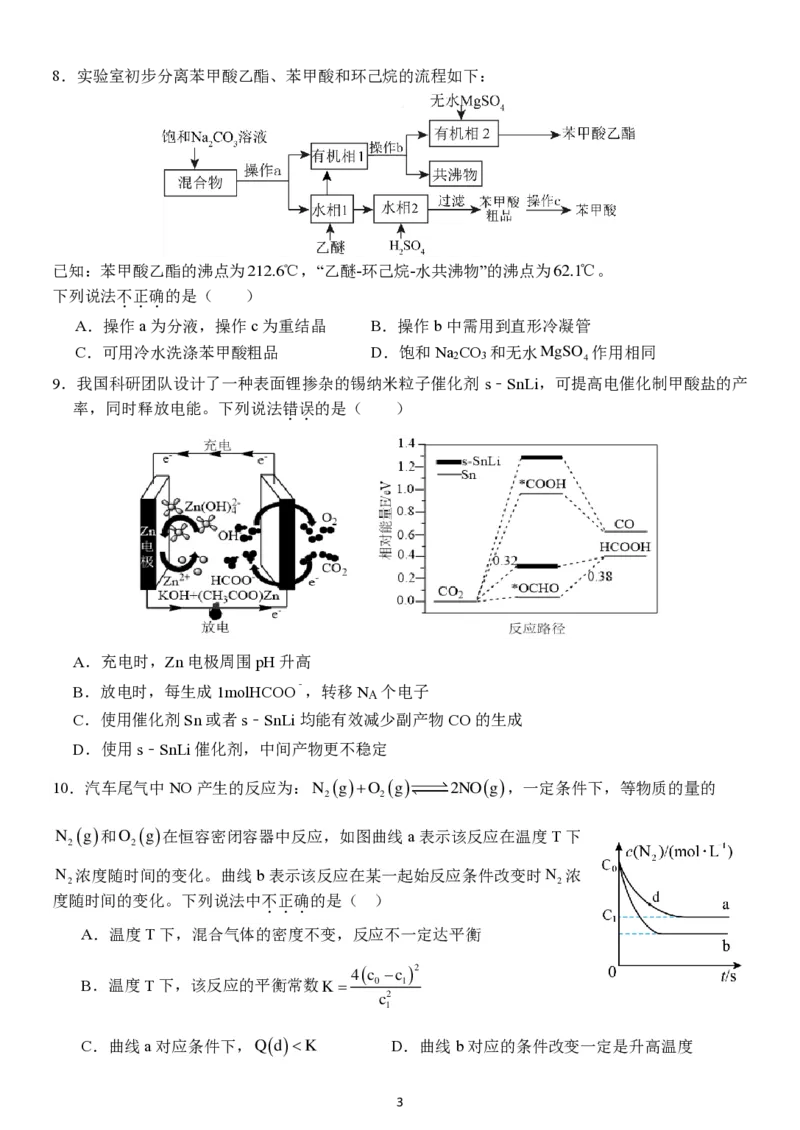
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}8.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为
3
2 1 2 .6 ℃ ,“乙醚-环己烷-水共沸物”的沸点为62.1℃。
下列说法不正确的是( )
...
A.操作a为分液,操作c为重结晶 B.操作b中需用到直形冷凝管
C.可用冷水洗涤苯甲酸粗品 D.饱和Na CO 和无水
2 3
M g S O
4
作用相同
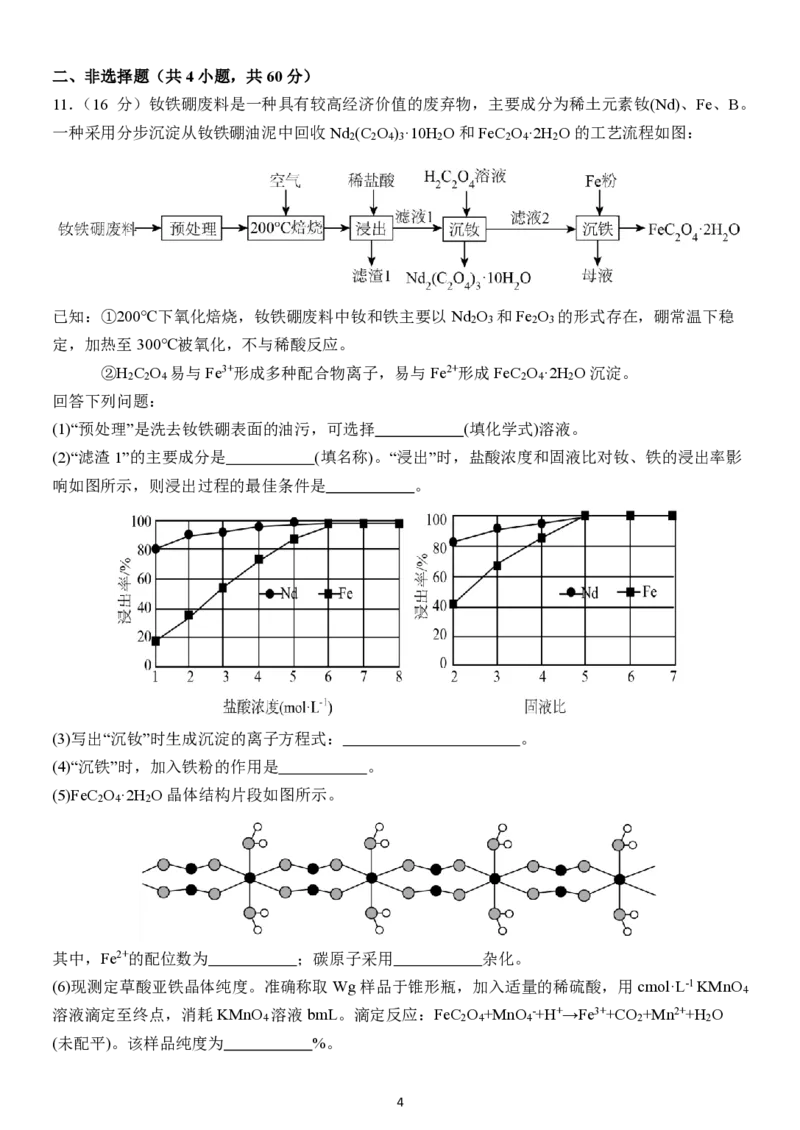
9.我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂 s﹣SnLi,可提高电催化制甲酸盐的产
率,同时释放电能。下列说法错误的是( )
..
A.充电时,Zn电极周围pH升高
B.放电时,每生成1molHCOO﹣,转移NA 个电子
C.使用催化剂Sn或者s﹣SnLi均能有效减少副产物CO的生成
D.使用s﹣SnLi催化剂,中间产物更不稳定
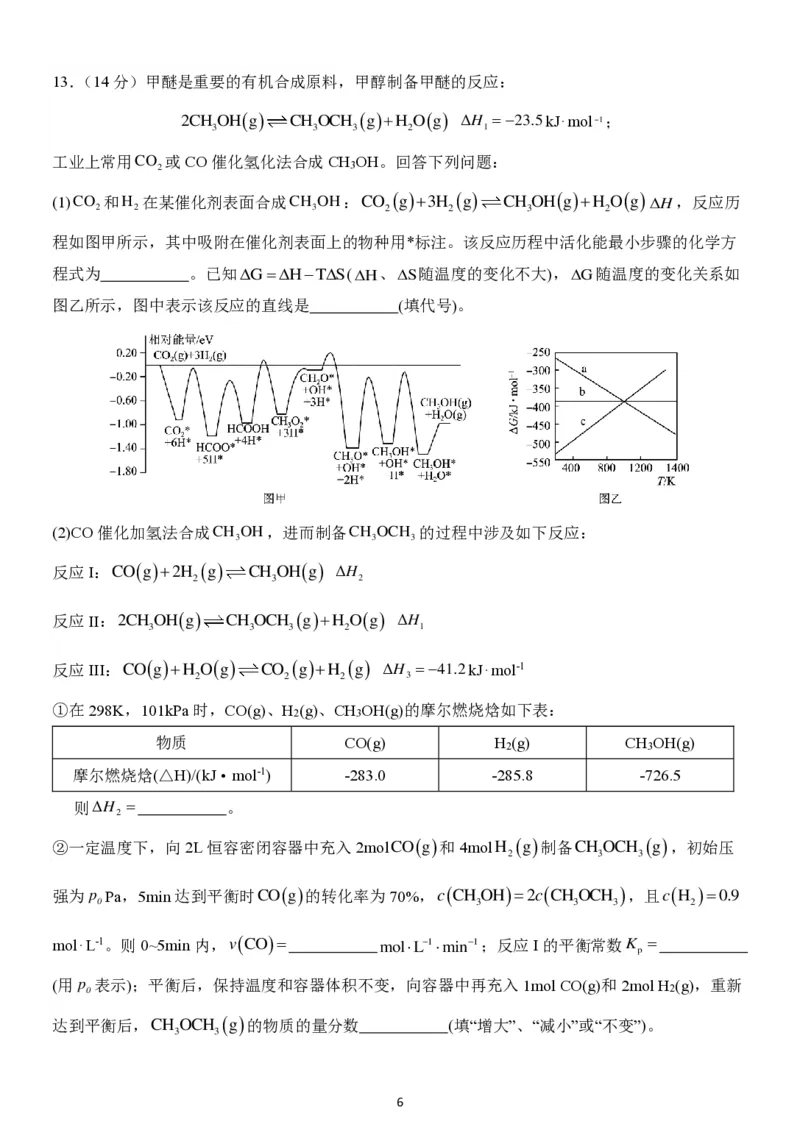
10.汽车尾气中NO产生的反应为: N
2
( g ) + O
2
( g ) 2 N O ( g ) ,一定条件下,等物质的量的
N
2
( g ) 和 O
2
( g ) 在恒容密闭容器中反应,如图曲线a表示该反应在温度T下
N
2
浓度随时间的变化。曲线b表示该反应在某一起始反应条件改变时 N
2
浓
度随时间的变化。下列说法中不正确的是( )
...
A.温度T下,混合气体的密度不变,反应不一定达平衡
4(c −c )2
B.温度T下,该反应的平衡常数K= 0 1
c2
1
C.曲线a对应条件下,Q(d)K D.曲线b对应的条件改变一定是升高温度
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}二、非选择题(共4小题,共60分)
11.(16 分)钕铁硼废料是一种具有较高经济价值的废弃物,主要成分为稀土元素钕(Nd)、Fe、B。
一种采用分步沉淀从钕铁硼油泥中回收Nd (C O ) ·10H O和FeC O ·2H O的工艺流程如图:
2 2 4 3 2 2 4 2
沉铁
已知:①200℃下氧化焙烧,钕铁硼废料中钕和铁主要以Nd O 和Fe O 的形式存在,硼常温下稳
2 3 2 3
定,加热至300℃被氧化,不与稀酸反应。
②H C O 易与Fe3+形成多种配合物离子,易与Fe2+形成FeC O ·2H O沉淀。
2 2 4 2 4 2
回答下列问题:
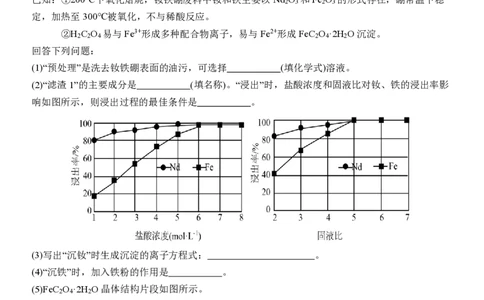
(1)“预处理”是洗去钕铁硼表面的油污,可选择 (填化学式)溶液。
(2)“滤渣1”的主要成分是 (填名称)。“浸出”时,盐酸浓度和固液比对钕、铁的浸出率影
响如图所示,则浸出过程的最佳条件是 。
(3)写出“沉钕”时生成沉淀的离子方程式: 。
(4)“沉铁”时,加入铁粉的作用是 。
(5)FeC O ·2H O晶体结构片段如图所示。
2 4 2
其中,Fe2+的配位数为 ;碳原子采用 杂化。
(6)现测定草酸亚铁晶体纯度。准确称取Wg样品于锥形瓶,加入适量的稀硫酸,用cmol·L-1 KMnO
4
溶液滴定至终点,消耗KMnO 溶液bmL。滴定反应:FeC O +MnO -+H+→Fe3++CO +Mn2++H O
4 2 4 4 2 2
(未配平)。该样品纯度为 %。
4
{#{QQABAYKU ggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}12.(14分)温和型供氧剂CaO 是白色固体,微溶于水,不溶于有机溶剂,可与水缓慢反应,易与
2
酸反应。某实验小组按如下流程和装置制取CaO :
2
第①步的装置如右图所示(夹持装置省略)。
请回答:
(1)盛装
5
H
2
O
2
溶液的恒压分液漏斗的支管的作用是 。
(2)如果用CaO固体替代 C a ( O H )
2
,结果得到 C a O
2
的量很少,原因
是 。
(3)取天然水的水样,分成等体积的甲、乙两份,甲经煮沸后密封冷却,乙无操作。向两份水样中加
入等质量的CaO (不足量),经分析发现,一段时间后甲水样中
2
O
2
的浓度较低。原因之一是煮沸除
去了甲水样中的溶解的O ,其它可能原因是 (写一个即可)。
2
(4)取1.4000g产品于烧杯,加过量盐酸并煮沸,冷却后加过量 N a
2
C
2
O
4
溶液,过滤、洗涤后将沉淀
转入锥形瓶中,加足量稀硫酸,用0.5000 mol/L KMnO 标准溶液滴定至终点,重复2~3次,平均
4
消耗标准溶液16.00mL。已知:
5 C a C
2
O
4
+ 2 K M n O
4
+ 8 H
2
S O
4
= 5 C a S O
4
+ K
2
S O
4
+ 2 M n S O
4
+ 1 0 C O
2
+ 8 H
2
O
①滴定操作可分解为如下几步,按实验操作先后顺序排序 (选填序号)。
A.用标准溶液润洗滴定管2~3次
B.固定盛有标准溶液的滴定管,转动旋塞使尖嘴处充满溶液
C.用标准溶液滴定至终点,读数
D.取标准溶液注入滴定管至“0”刻度线以上2~3cm处
E.调节液面至0刻度线以下,读数
②样品中CaO 的纯度是 %(结果保留一位小数)。
2
③根据计算结果,分析造成此结果的可能因素有 (选填序号)。
A.烘干时温度过高,少量CaO 分解为CaO B.转移
2
C a C
2
O
4
沉淀时,有固体残留在滤纸上
C.洗涤CaC O 沉淀时,未洗涤干净 D.滴定终点读数时,俯视读数
2 4
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}13.(14分)甲醚是重要的有机合成原料,甲醇制备甲醚的反应:
6
2 C H
3
O H ( g ) C H
3
O C H
3
( g ) + H
2
O ( g ) Δ H
1
= − 2 3 .5 kJ⋅mol−1;
工业上常用CO 或CO催化氢化法合成CH OH。回答下列问题:
2 3
(1) C O
2
和 H
2
在某催化剂表面合成 C H
3
O H : C O
2
( g ) + 3 H
2
( g ) C H
3
O H ( g ) + H
2
O ( g ) H,反应历
程如图甲所示,其中吸附在催化剂表面上的物种用*标注。该反应历程中活化能最小步骤的化学方
程式为 。已知G=H−TS( H 、 S 随温度的变化不大), G 随温度的变化关系如
图乙所示,图中表示该反应的直线是 (填代号)。
(2)CO催化加氢法合成 C H
3
O H ,进而制备 C H
3
O C H
3
的过程中涉及如下反应:
反应I: C O ( g ) + 2 H
2
( g ) C H
3
O H ( g ) Δ H
2
反应II: 2 C H
3
O H ( g ) C H
3
O C H
3
( g ) + H
2
O ( g ) Δ H
1
反应III: C O ( g ) + H
2
O ( g ) C O
2
( g ) + H
2
( g ) Δ H
3
= − 4 1 .2 kJ⋅mol-1
①在298K,101kPa时,CO(g)、H (g)、CH OH(g)的摩尔燃烧焓如下表:
2 3
物质 CO(g) H (g) CH OH(g)
2 3
摩尔燃烧焓(△H)/(kJ·mol-1) -283.0 -285.8 -726.5
则 Δ H
2
= 。
②一定温度下,向2L恒容密闭容器中充入2molCO(g)和4molH (g)制备
2
C H
3
O C H
3
( g ) ,初始压
强为 p
0
Pa,5min达到平衡时CO(g)的转化率为70%,c(CH OH)=2c(CH OCH ),且c(H )=0.9
3 3 3 2
mol⋅L-1。则0~5min内,v(CO)= molL−1min−1;反应I的平衡常数K =
p
(用 p 表示);平衡后,保持温度和容器体积不变,向容器中再充入1mol CO(g)和2mol H (g),重新
0 2
达到平衡后,CH OCH (g)的物质的量分数 (填“增大”、“减小”或“不变”)。
3 3
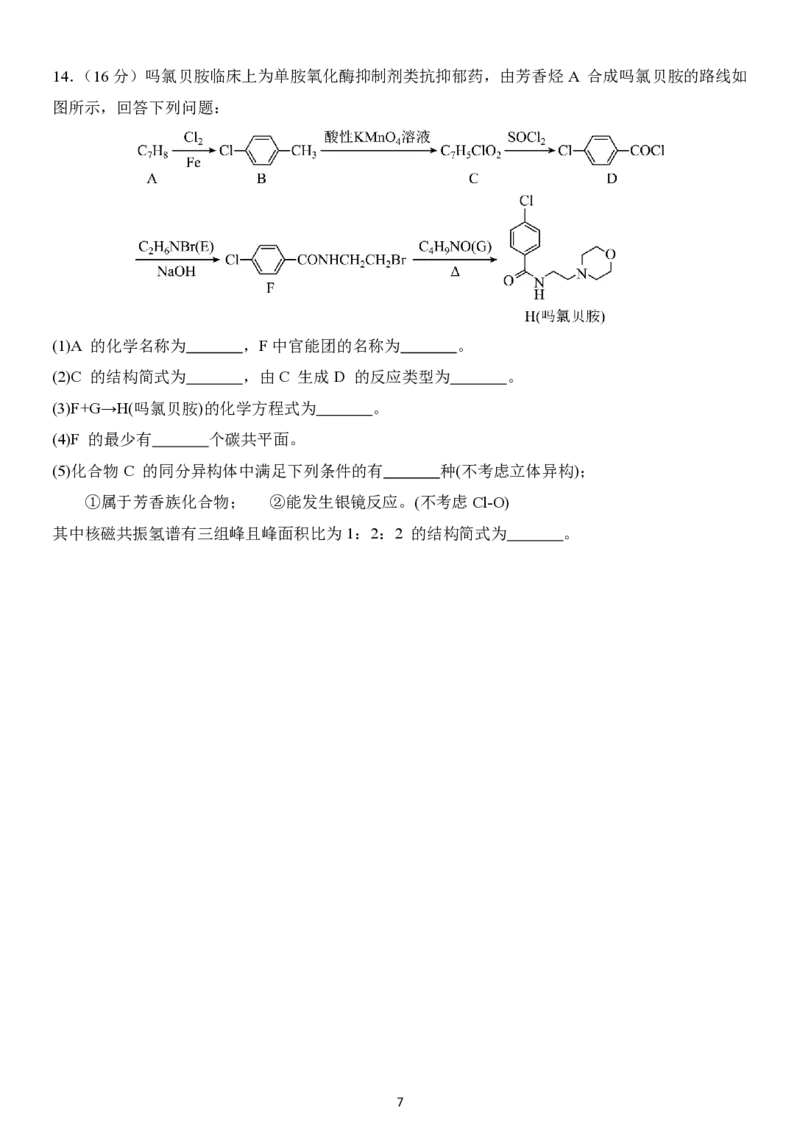
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}14.(16分)吗氯贝胺临床上为单胺氧化酶抑制剂类抗抑郁药,由芳香烃A 合成吗氯贝胺的路线如
图所示,回答下列问题:
(1)A 的化学名称为 ,F中官能团的名称为 。
(2)C 的结构简式为 ,由C 生成D 的反应类型为 。
(3)F+G→H(吗氯贝胺)的化学方程式为 。
(4)F 的最少有 个碳共平面。
(5)化合物C 的同分异构体中满足下列条件的有 种(不考虑立体异构);
①属于芳香族化合物; ②能发生银镜反应。(不考虑Cl-O)
其中核磁共振氢谱有三组峰且峰面积比为1:2:2 的结构简式为 。
7
{#{QQABAYKU ggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}龙岩一中2024届高三上学期第三次月考化学参考答案
1-5.BCCDD 6-10.DADBD
11.(16分) (1)NaOH(或热的Na CO )(2分)
2 3
(2)硼 (2分) 6mol/L的盐酸、固液比为5:1(2分)
(3)
8
2 N d 3 + + 3 H
2
C
2
O
4
+ 1 0 H
2
O = N d
2
( C
2
O
4
)
3
1 0 H
2
O + 6 H + (2分)
(4)将Fe(III)还原为Fe(II),与溶液中的草酸根生成FeC O ·2H O的沉淀(2分)
2 4 2
(5)6 (2分) sp2(2分) (6)
3 0
W
b c
(2分)
12. (14分) (1)平衡气压,使 H
2
O
2
易于滴下 (2分)
(2)CaO遇水快速放出大量热,导致H O 分解(2分)
2 2
(3)乙水样中溶解 C O
2
与 C a O
2
反应,增加了水体中 O
2
的浓度(3分)
(4)ADBEC (2分) 102.0 (3分) AC(2分)
13. (14分) (1) CH O*+OH*+3H*=CH O*+OH*+2H*(或CH O*+H*=CH O*) (2分) c
2 3 2 3
(2分)
(2) -128.1 kJ⋅mol-1(3分) 0.14(2分)
1
9
0
p
020
(3分) 增大 (2分)
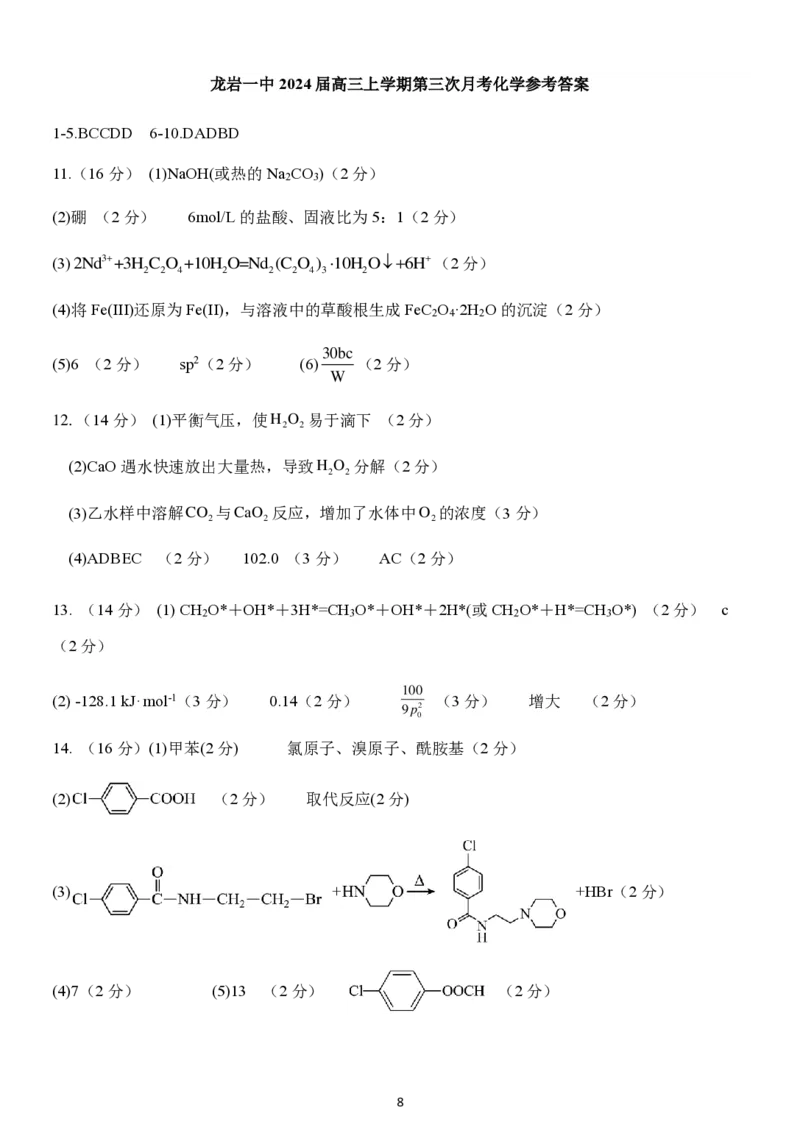
14. (16分)(1)甲苯(2分) 氯原子、溴原子、酰胺基(2分)
(2) (2分) 取代反应(2分)
(3) + +HBr(2分)
(4)7(2分) (5)13 (2分) (2分)
{#{QQABAYKUggAoABBAARgCUQW6CAGQkAACCAoOAFAMMAABwANABAA=}#}