文档内容
2026 届云南三校高考备考实用性联考卷(四)
化学评分细则
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
题号 1 2 3 4 5 6 7
答案 A D C A A C B
题号 8 9 10 11 12 13 14
答案 D C B D B B D
【解析】
1.煤的气化是将煤转化为可燃性气体的过程,主要发生的反应为 C+HO(g)=====CO+H ,
2 2
该过程属于化学变化,形成了新的化学键,A正确。硫酸铵使蛋白质发生盐析,而不是变
性,B错误。核电站反应堆所用铀棒中含有的 与 互为同位素,C错误。酚醛树脂
可由苯酚与甲醛缩聚得到,D错误。
2.NH Cl的电子式为 ,A错误。sp2杂化轨道由1个s轨道和2个p轨道杂化
4
形成,夹角为120°,题中示意图标注180°,为sp杂化特征,B错误。四氨合铜离子的结
构为 ,C错误。金属钠与水反应剧烈,需要护目镜保护眼睛;实验需
用小刀切金属钠,要防止划伤;氢氧化钠具有腐蚀性,实验结束需洗手;钠与水反应放
出氢气,需要通风,D正确。
3.标况下SO 为固体,不能用气体摩尔体积进行相关计算,A错误。未知溶液体积,无法确
3
定SO的数目,B错误。反应①的方程式为 SO +3HS=4S↓+3HO,反应中每断裂
3 2 2
0.6mol S—H键消耗0.3mol H S,故可以得到还原产物的数目为0.1N ,C正确。反应②的
2 A
离子方程式为 3S+6OH−=2S2−+SO+3HO,若有3mol S作氧化剂,转移电子数目为
2
6N ,D错误。
A
4.配制一定物质的量浓度的溶液时,溶质要放在烧杯中溶解,不能直接放在容量瓶中溶解,
A不合理。分液时,为了使液体顺利流下,需保持分液漏斗内部和外界大气压相等,所以分液时,先打开分液漏斗上方的玻璃塞,再打开下方的活塞,将下层液体从下口放出,
再将上层液体从上口倒出,操作方法正确,B合理。碘易升华,加热可使碘固体升华成为
碘蒸气,碘蒸气遇到冷的容器,又凝华成为碘固体,该装置可以提纯粗碘,C合理。用
HCl标准溶液滴定NaOH溶液时,眼睛应注视锥形瓶中溶液,以便观察溶液颜色的变化从
而判断滴定终点,D合理。
5.当NaOH吸收少量SO 时,应生成SO而非HSO,正确反应为2OH−+SO =SO+HO ,
2 2 2
A错误。乙醇与钠反应生成乙醇钠和氢气,化学方程式正确,B正确。C正确。 难溶
物不拆,HgS溶解度比 更小,沉淀转移,D正确。
6.合成X的单体为 、CH≡CH、CH=CH ,A错误。X的重复单元中连有苯基
2 2
的碳原子为手性碳原子,1mol X中存在n N 个手性碳原子,B错误。Y的重复单元中只
A
含有酯基一种官能团,C正确。Y为聚酯,碱性条件下可发生降解,X不可降解,D错误。
7.Al(OH) 既可与酸反应又可与碱反应,而Mg(OH) 只可与酸反应,则Mg(OH) 的碱性强
3 2 2
于 Al(OH) ,A 正确。CHCOONH 中 NH 水解,NH+HO NH ·HO+H+,会消耗
3 3 4 2 3 2
CHCOO−水解生成的OH−,测定相同浓度的CHCOONH 和NaHCO 溶液的pH,前者更
3 3 4 3
小,不能说明酸性:CHCOOH>H CO ,B错误。少量硫酸铜与铁反应产生铜单质并附着
3 2 3
在铁表面,形成原电池,加快了反应,所以电化学腐蚀速率更快,C正确。侯氏制碱法的
核心反应为NaCl+NH +CO +H O=NaHCO ↓+NHCl,碳酸氢钠(NaHCO )形成沉淀
3 2 2 3 4 3
的根本原因是碳酸氢钠在常温下的溶解度较小(约9.6 g/100 mL水),远低于氯化钠和碳
酸钠的溶解度,导致生成的NaHCO 浓度超过其饱和溶解度而析出 ,这一现象是侯氏制碱
3
法工艺设计的核心化学原理,D正确。
8.由图可知,反应①方程式为 ,A正确。由反应
③CHCH生成CH=CH ,应该还生成H+,或由④可知 生成 ,需要加
3 2 2
入H+,B正确。 在反应前添加,反应前后的质量和性质不变,是该反应的催化剂,
该反应总反应为CHCHOH――→CH=CH+H O,可用浓硫酸催化反应,C正确。反应
3 2 2 2 2
过程中有 配位键的形成和断裂,C—O等极性键的断裂,O—H等极性键的生成,
C—C非极性键的生成,但是没有非极性键的断裂,D错误。
9.X、Y、Z、W和Q是原子序数依次增大的前四周期非金属元素,五种元素位于四个不同
的周期,Q序数最大应为第四周期,据单质推出为液溴,Q为Br,Y、Z同周期,则X在
第一周期,Y、Z在第二周期,W在第三周期,再根据物质结构价键数得出,X是H元素,Y、Z、W元素分别为C、O、P。同周期第一电离能高于P的为Cl和Ar两种,A正确。
PCl 和PBr 中心原子相同,且价电子对数均为4,杂化方式相同,电负性Cl>Br,使P
3 3
—Cl成键电子对更远离中心原子,键之间斥力小,键角小,B正确。C H 为乙烯,平面
2 4
结构,为非极性分子,而NH 中两个为三角锥结构,为极性分子,据相似相溶,NH 更
2 4 2 4
易溶于极性溶剂水,且可与水分子间形成氢键,还能与水发生类似 NH 的反应,水溶性
3
C H负极,A正确。右侧 Fe为阴极,发生电极反应为 2H+
+2e−=H ↑,可用惰性电极代替,B错误。阴极消耗H+,导致溶液pH逐渐增大,生
2
成Fe(OH) 、Cr(OH) ,C正确。据转移电子守恒Cr O~6Fe2+~12e−~6H ,20mol Cr O需要
3 3 2 2 2
转移120mol Fe2+则电极上转移240mol电子,据电子利用率50%,则实际转移480mol电
子,消耗240mol H,标准状况下体积为22.4mol/L 240mol=5376L,D正确。
2
13.阳离子[Mg(H O) ]2+中 H—O—H 的键角大于 HO 中 H—O—H 的键角,因为
2 6 2
[Mg(H O) ]2+其中的O参与配位,孤电子对对成键电子的影响减小,A错误。符合题意,
2 6
B正确。据均摊法,晶胞中[Mg(H O) ]2+数目为 ,SO为4,单
2 6 2
位为1nm=10−7cm,晶胞密度为 ,C错误。阴离子SO的中心硫原子的
2
杂化方式为sp3,可以利用等电子体思想与SO对比,中心S杂化类型相同,D错误。
14.由图中点(9,−1.3),K [Mg(OH) ]=10−1.3 (10−5)2 = 10−11.3,数量级为10−12,A错误。M点
sp 2
时含碳微粒除了有 HCO 、HCO、CO 还有 MgCO ,据碳守恒 n(H CO)+n(HCO )+
2 3 3 2 3 3
n(CO)<0.2mol,B错误。P点c(Mg2+)均小于线上的c(Mg2+),为不饱和溶液,两个沉淀均
不产生,C错误。从图中可知pH=12时主要生成Mg(OH) 沉淀,D正确。
2二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分 ,共15分)
(1)
(2)4Cl− +MnO+PbS+4H+=PbCl+S+Mn2++2H O
2 2
(3)3.7≤pH < 6.2或3.7~6.2
(4)冰水(1分) PbCl (s)+2Cl−(aq) PbCl(aq) ΔH>0反应吸热,加入冰水温度降
2
低,反应逆向移动生成PbCl (s)
2
(5)1.6×103
(6)①PbCl+2e− =Pb+4Cl− ②0.4
【解析】“浸取”时PbS和MnO 在盐酸中发生氧化还原反应生成S、Mn2+、PbCl 加入的
2 2
NaCl促进反应PbCl (s)+2Cl−(aq) PbCl (aq)正向移动生成PbCl 进入溶液,据此分
2
析写出离子方程式;加入MnO调pH,使Fe3+转化为Fe(OH) 除去,但不能影响溶液中的
3
铅离子,所以调pH范围3.7≤pH<6.2;“沉降”时是为了把溶液中的PbCl 转化为
PbCl 沉淀,即需要让吸热反应PbCl (s)+2Cl−(aq) PbCl (aq)逆向移动,所以需要冰
2 2
水降温逆移;根据沉淀转化反应方程式,得到K的表达式为 ,用 即
可得出答案;“浸取”后的溶液含PbCl 据题目意思要从+2价Pb得电子还原为Pb单质,
据此写出电极反应式,生成41.4g Pb即0.2mol Pb时,转移0.4mol电子,通过质子交换
膜的H+为0.4mol。
16.(除特殊标注外,每空1分,共14分)
(1)三颈烧瓶
(2)抑制Ti(OH) 胶体形成、促进白色沉淀生成(2分)
4
(3)取最后一次洗涤液适量于试管中,滴加硝酸酸化的硝酸银溶液,无白色沉淀产生
(2分)
(4)检查装置气密性 ② ①
(5)碱石灰(合理答案给分) 防止固体堵塞导气管
(6) ====== (2分)
(7)60%或0.6(2分)
【解析】据题目信息 水解成Ti(OH) 胶体和盐酸,所以稀盐酸可抑制胶体形成、促
4进白色沉淀生成, 与水反应生成白色沉淀 ,将 洗涤,洗
去表面的盐酸,所以是否洗涤干净,检验氯离子即可。装置B中利用浓氨水和生石灰反
应制备NH ,利用装置C除去NH 中的水蒸气,则试剂X可以是碱石灰,提前通入NH
3 3 3
排出管式炉中空气后再进行加热,装置D中,NH 和 在800℃下反应生成
3
和 ,化学方程式为 ====== ,装置 E 中装有
CaCl , 可 以 吸 收 生 成 的 水 蒸 气 及 过 量 的 NH , 据 钛 原 子 守 恒 , 理 论 上
2 3
n(TiN)=n(TiCl =19mL× 1.7g/cm3 ÷190g/mol=0.17mol , 实 际 上
4)
n(TiN)=6.324g÷62g/mol=0.102 mol,所以产率为60%。
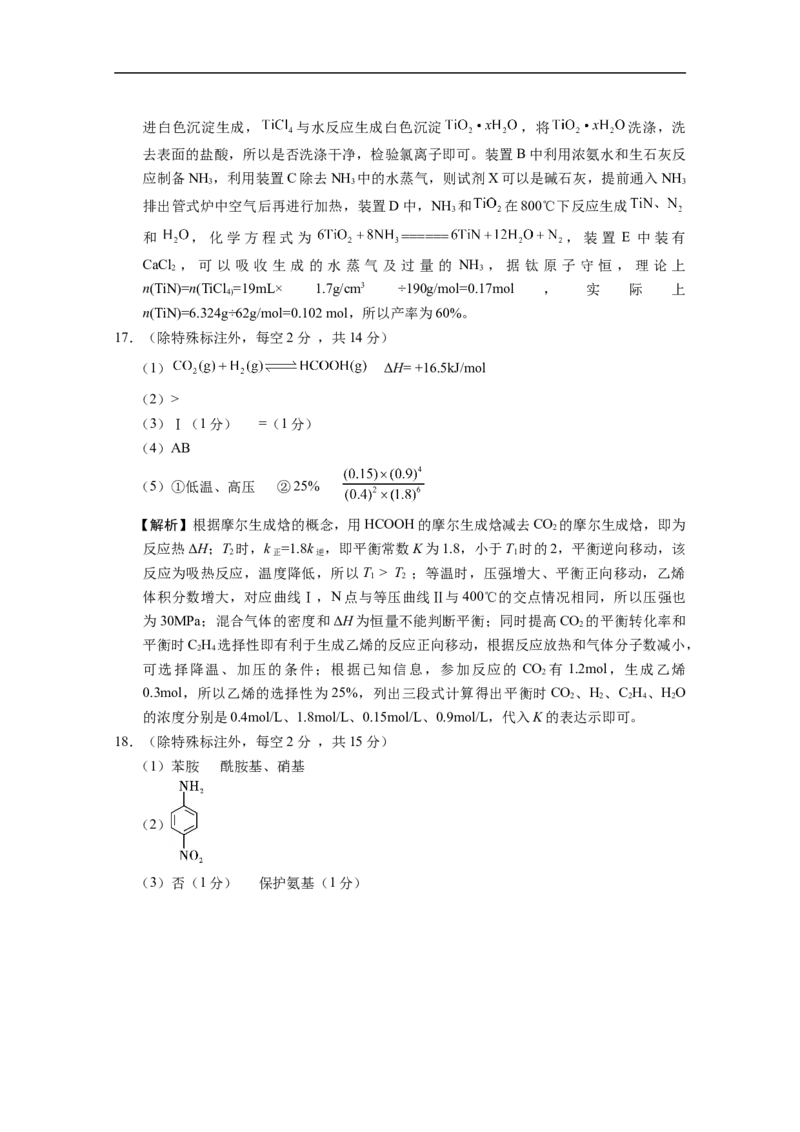
17.(除特殊标注外,每空2分 ,共14分)
(1) ΔH= +16.5kJ/mol
(2)>
(3)Ⅰ(1分) =(1分)
(4)AB
(5)①低温、高压 ②25%
【解析】根据摩尔生成焓的概念,用HCOOH的摩尔生成焓减去CO 的摩尔生成焓,即为
2
反应热ΔH;T 时,k =1.8k ,即平衡常数K为1.8,小于T 时的2,平衡逆向移动,该
2 正 逆 1
反应为吸热反应,温度降低,所以T > T ;等温时,压强增大、平衡正向移动,乙烯
1 2
体积分数增大,对应曲线Ⅰ,N点与等压曲线Ⅱ与400℃的交点情况相同,所以压强也
为30MPa;混合气体的密度和ΔH为恒量不能判断平衡;同时提高CO 的平衡转化率和
2
平衡时C H 选择性即有利于生成乙烯的反应正向移动,根据反应放热和气体分子数减小,
2 4
可选择降温、加压的条件;根据已知信息,参加反应的 CO 有 1.2mol,生成乙烯
2
0.3mol,所以乙烯的选择性为25%,列出三段式计算得出平衡时CO 、H 、C H 、HO
2 2 2 4 2
的浓度分别是0.4mol/L、1.8mol/L、0.15mol/L、0.9mol/L,代入K的表达示即可。
18.(除特殊标注外,每空2分 ,共15分)
(1)苯胺 酰胺基、硝基
(2)
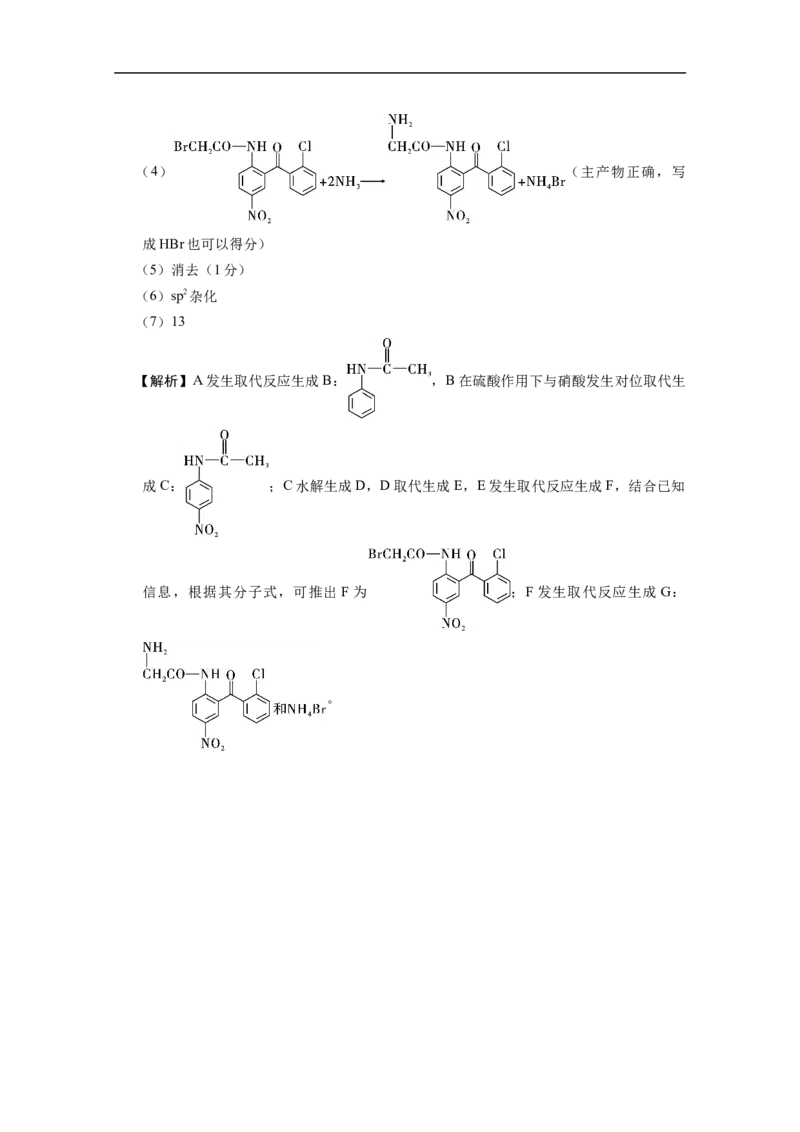
(3)否(1分) 保护氨基(1分)(4) (主产物正确,写
成HBr也可以得分)
(5)消去(1分)
(6)sp2杂化
(7)13
【解析】A发生取代反应生成B: ,B在硫酸作用下与硝酸发生对位取代生
成C: ;C水解生成D,D取代生成E,E发生取代反应生成F,结合已知
信息,根据其分子式,可推出F为 ;F发生取代反应生成G:
。