文档内容
2025 年湖北高考真题化学试题
一、单选题
1.下列与生活相关的叙述中,不涉及化学变化的是
A.干冰升华助力舞台云雾形成 B.珍珠遇酸后失去光泽
C.加酶洗衣粉清洗蛋白质污渍 D.植物油久置氧化变质
2.下列化学用语表达错误的是
A.甲醛(HCHO)的分子空间结构模型:
催化剂
B.制备聚乙炔:nH−C≡C−H →
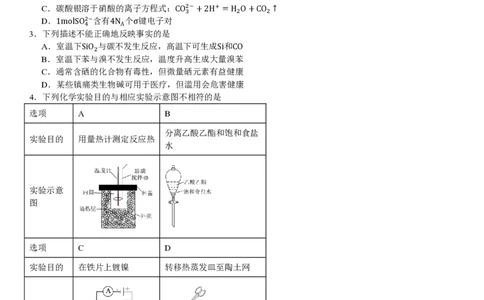
C.碳酸银溶于硝酸的离子方程式:CO2−+2H+ =H O+CO ↑
3 2 2
D.1molSO2−含有4N 个σ键电子对
4 A
3.下列描述不能正确地反映事实的是
A.室温下SiO 与碳不发生反应,高温下可生成Si和CO
2
B.室温下苯与溴不发生反应,温度升高生成大量溴苯
C.通常含硒的化合物有毒性,但微量硒元素有益健康
D.某些镇痛类生物碱可用于医疗,但滥用会危害健康
4.下列化学实验目的与相应实验示意图不相符的是
选项 A B
分离乙酸乙酯和饱和食盐
实验目的 用量热计测定反应热
水
实验示意
图
选项 C D
实验目的 在铁片上镀镍 转移热蒸发皿至陶土网
实验示意
图
A.A B.B C.C D.D
5.下列说法错误的是
A.胶体粒子对光线散射产生丁达尔效应
B.合成高分子是通过聚合反应得到的一类纯净物
C.配位化合物通过“电子对给予-接受”形成配位键
D.超分子可以由两种或两种以上的分子通过分子间相互作用形成
6.某化合物的分子式为XY Z。X、Y、Z三种元素位于同一短周期且原子序数依次增大,三者的原子核外电子层数
2
之和与未成对电子数之和相等,Z是周期表中电负性最大的元素。下列说法正确的是A.三者中Z的原子半径最大 B.三者中Y的第一电离能最小
C.X的最高化合价为+3 D.XZ 与NH 键角相等
3 3
7.下列关于物质性质或应用解释错误的是
选项 性质或应用 解释
A 石蜡油的流动性比水的差 石蜡油的分子间作用力比水的小
B NH 溶于水显碱性 NH 可结合水中的质子
3 3
C OF 可以氧化H O OF 中O显正电性
2 2 2
D 石墨作为润滑剂 石墨层间靠范德华力维系
A.A B.B C.C D.D
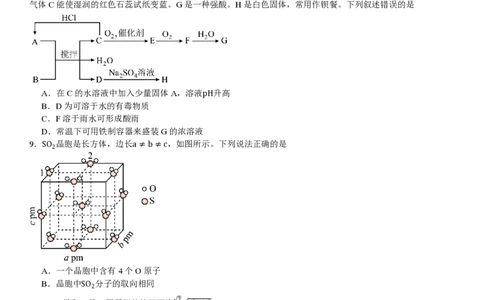
8.如图所示的物质转化关系中,固体A与固体B研细后混合,常温下搅拌产生气体C和固体D,温度迅速下降。
气体C能使湿润的红色石蕊试纸变蓝。G是一种强酸。H是白色固体,常用作钡餐。下列叙述错误的是
A.在C的水溶液中加入少量固体A,溶液pH升高
B.D为可溶于水的有毒物质
C.F溶于雨水可形成酸雨
D.常温下可用铁制容器来盛装G的浓溶液
9.SO 晶胞是长方体,边长a≠b≠c,如图所示。下列说法正确的是
2
A.一个晶胞中含有4个O原子
B.晶胞中SO 分子的取向相同
2
C.1号和2号S原子间的核间距为√2 √a2+b2pm
2
D.每个S原子周围与其等距且紧邻的S原子有4个
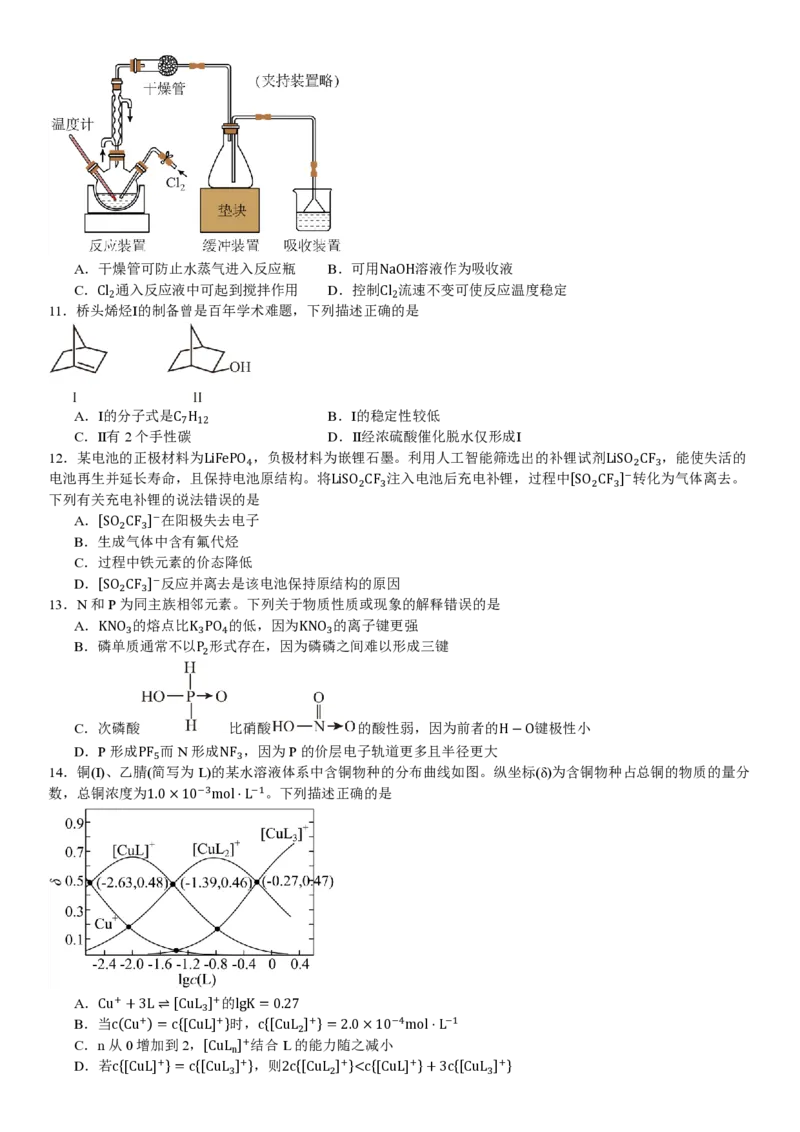
10.制备α-氯代异丁酸的装置如图。在反应瓶中加入异丁酸与催化剂(易水解),加热到70℃,通入Cl ,反应剧烈放
2
热,通气完毕,在120℃下继续反应。反应结束,常压蒸馏得产物。反应方程式:
下列说法错误的是A.干燥管可防止水蒸气进入反应瓶 B.可用NaOH溶液作为吸收液
C.Cl 通入反应液中可起到搅拌作用 D.控制Cl 流速不变可使反应温度稳定
2 2
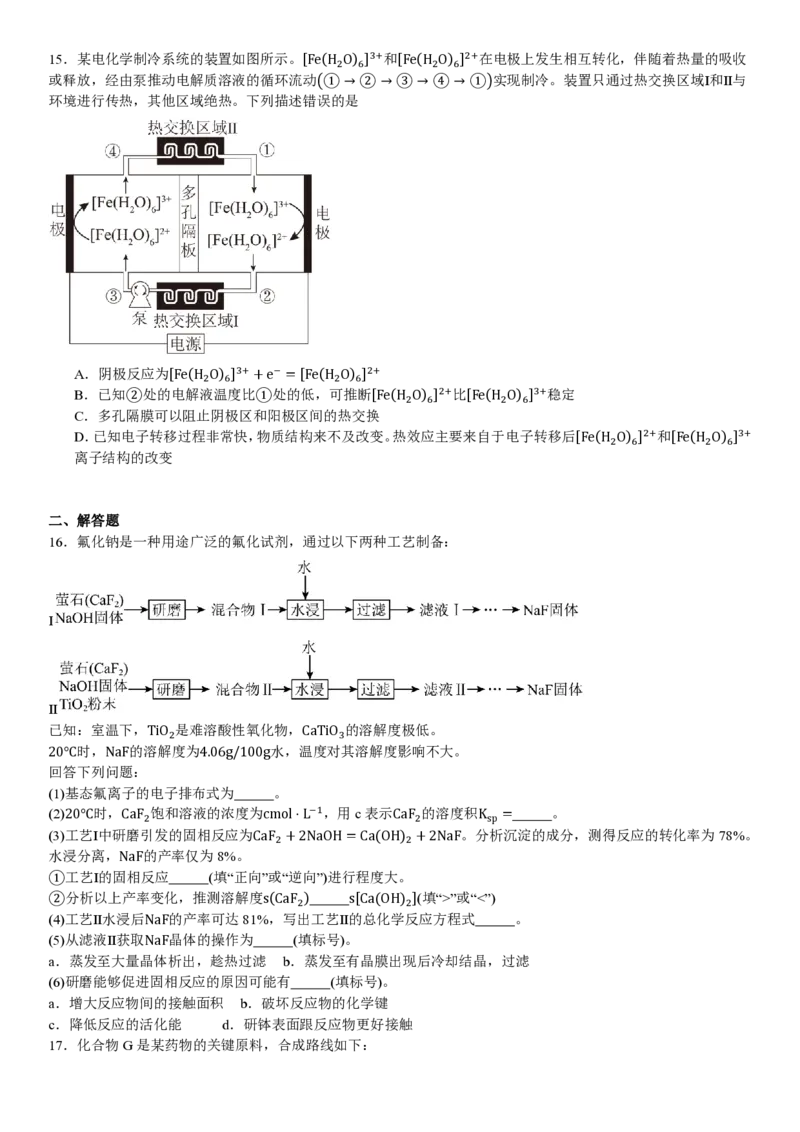
11.桥头烯烃Ⅰ的制备曾是百年学术难题,下列描述正确的是
A.Ⅰ的分子式是C H B.Ⅰ的稳定性较低
7 12
C.Ⅱ有2个手性碳 D.Ⅱ经浓硫酸催化脱水仅形成Ⅰ
12.某电池的正极材料为LiFePO ,负极材料为嵌锂石墨。利用人工智能筛选出的补锂试剂LiSO CF ,能使失活的
4 2 3
电池再生并延长寿命,且保持电池原结构。将LiSO CF 注入电池后充电补锂,过程中[SO CF ]−转化为气体离去。
2 3 2 3
下列有关充电补锂的说法错误的是
A.[SO CF ]−在阳极失去电子
2 3
B.生成气体中含有氟代烃
C.过程中铁元素的价态降低
D.[SO CF ]−反应并离去是该电池保持原结构的原因
2 3
13.N和P为同主族相邻元素。下列关于物质性质或现象的解释错误的是
A.KNO 的熔点比K PO 的低,因为KNO 的离子键更强
3 3 4 3
B.磷单质通常不以P 形式存在,因为磷磷之间难以形成三键
2
C.次磷酸 比硝酸 的酸性弱,因为前者的H−O键极性小
D.P形成PF 而N形成NF ,因为P的价层电子轨道更多且半径更大
5 3
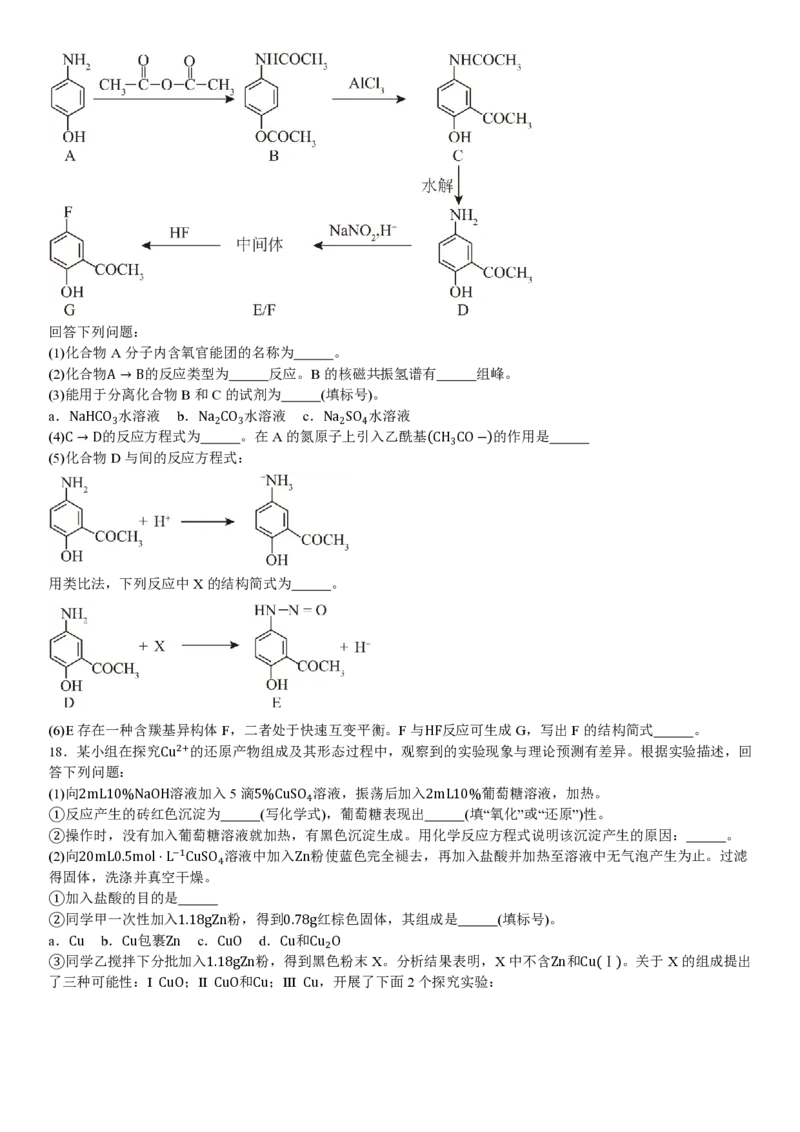
14.铜(I)、乙腈(简写为L)的某水溶液体系中含铜物种的分布曲线如图。纵坐标(δ)为含铜物种占总铜的物质的量分
数,总铜浓度为1.0×10−3mol⋅L−1。下列描述正确的是
A.Cu++3L⇌[CuL ]+的lgK=0.27
3
B.当c(Cu+)=c{[CuL]+}时,c{[CuL ]+}=2.0×10−4mol⋅L−1
2
C.n从0增加到2,[CuL ]+结合L的能力随之减小
n
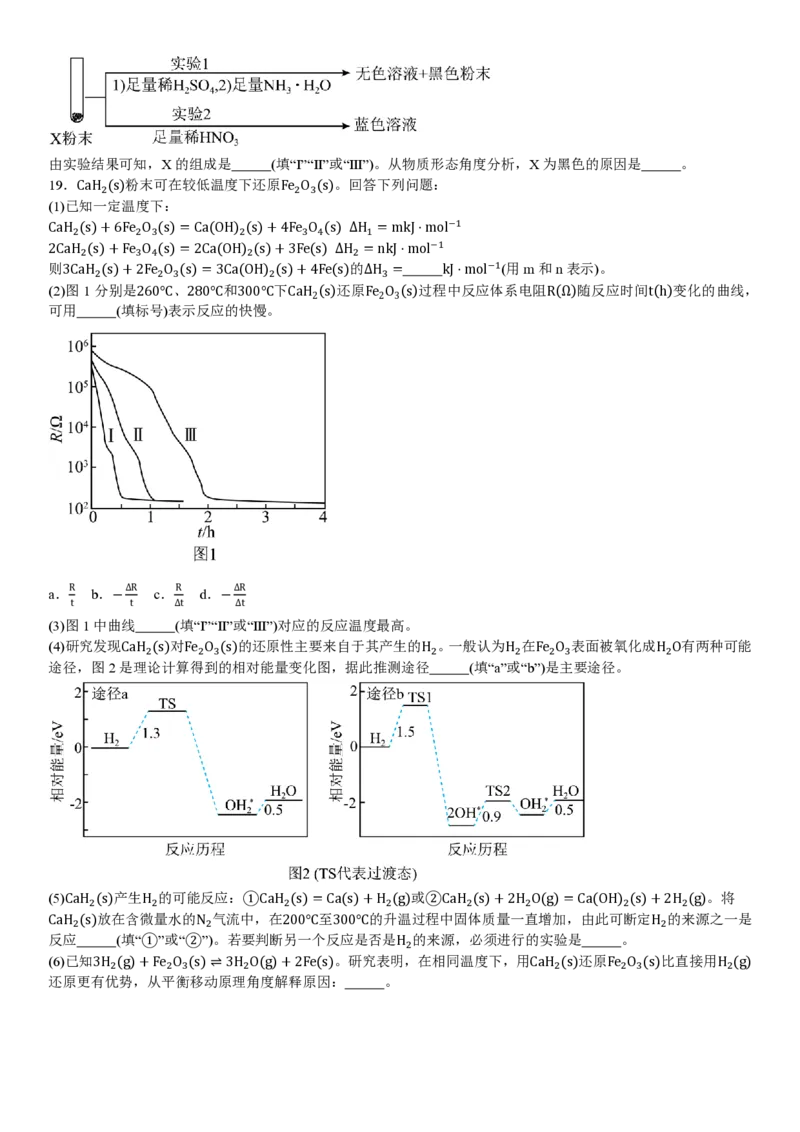
D.若c{[CuL]+}=c{[CuL ]+},则2c{[CuL ]+}”或“<”)
2 2
(4)工艺Ⅱ水浸后NaF的产率可达81%,写出工艺Ⅱ的总化学反应方程式 。
(5)从滤液Ⅱ获取NaF晶体的操作为 (填标号)。
a.蒸发至大量晶体析出,趁热过滤 b.蒸发至有晶膜出现后冷却结晶,过滤
(6)研磨能够促进固相反应的原因可能有 (填标号)。
a.增大反应物间的接触面积 b.破坏反应物的化学键
c.降低反应的活化能 d.研钵表面跟反应物更好接触
17.化合物G是某药物的关键原料,合成路线如下:回答下列问题:
(1)化合物A分子内含氧官能团的名称为 。
(2)化合物A→B的反应类型为 反应。B的核磁共振氢谱有 组峰。
(3)能用于分离化合物B和C的试剂为 (填标号)。
a.NaHCO 水溶液 b.Na CO 水溶液 c.Na SO 水溶液
3 2 3 2 4
(4)C→D的反应方程式为 。在A的氮原子上引入乙酰基(CH CO−)的作用是
3
(5)化合物D与间的反应方程式:
用类比法,下列反应中X的结构简式为 。
(6)E存在一种含羰基异构体F,二者处于快速互变平衡。F与HF反应可生成G,写出F的结构简式 。
18.某小组在探究Cu2+的还原产物组成及其形态过程中,观察到的实验现象与理论预测有差异。根据实验描述,回
答下列问题:
(1)向2mL10%NaOH溶液加入5滴5%CuSO 溶液,振荡后加入2mL10%葡萄糖溶液,加热。
4
①反应产生的砖红色沉淀为 (写化学式),葡萄糖表现出 (填“氧化”或“还原”)性。
②操作时,没有加入葡萄糖溶液就加热,有黑色沉淀生成。用化学反应方程式说明该沉淀产生的原因: 。
(2)向20mL0.5mol⋅L−1CuSO 溶液中加入Zn粉使蓝色完全褪去,再加入盐酸并加热至溶液中无气泡产生为止。过滤
4
得固体,洗涤并真空干燥。
①加入盐酸的目的是
②同学甲一次性加入1.18gZn粉,得到0.78g红棕色固体,其组成是 (填标号)。
a.Cu b.Cu包裹Zn c.CuO d.Cu和Cu O
2
③同学乙搅拌下分批加入1.18gZn粉,得到黑色粉末X。分析结果表明,X中不含Zn和Cu(Ⅰ)。关于X的组成提出
了三种可能性:Ⅰ CuO;Ⅱ CuO和Cu;Ⅲ Cu,开展了下面2个探究实验:由实验结果可知,X的组成是 (填“Ⅰ”“Ⅱ”或“Ⅲ”)。从物质形态角度分析,X为黑色的原因是 。
19.CaH (s)粉末可在较低温度下还原Fe O (s)。回答下列问题:
2 2 3
(1)已知一定温度下:
CaH (s)+6Fe O (s)=Ca(OH) (s)+4Fe O (s) ΔH =mkJ⋅mol−1
2 2 3 2 3 4 1
2CaH (s)+Fe O (s)=2Ca(OH) (s)+3Fe(s) ΔH =nkJ⋅mol−1
2 3 4 2 2
则3CaH (s)+2Fe O (s)=3Ca(OH) (s)+4Fe(s)的ΔH = kJ⋅mol−1(用m和n表示)。
2 2 3 2 3
(2)图1分别是260℃、280℃和300℃下CaH (s)还原Fe O (s)过程中反应体系电阻R(Ω)随反应时间t(h)变化的曲线,
2 2 3
可用 (填标号)表示反应的快慢。
a.R b.− ΔR c.R d.− ΔR
t t Δt Δt
(3)图1中曲线 (填“Ⅰ”“Ⅱ”或“Ⅲ”)对应的反应温度最高。
(4)研究发现CaH (s)对Fe O (s)的还原性主要来自于其产生的H 。一般认为H 在Fe O 表面被氧化成H O有两种可能
2 2 3 2 2 2 3 2
途径,图2是理论计算得到的相对能量变化图,据此推测途径 (填“a”或“b”)是主要途径。
(5)CaH (s)产生H 的可能反应:①CaH (s)=Ca(s)+H (g)或②CaH (s)+2H O(g)=Ca(OH) (s)+2H (g)。将
2 2 2 2 2 2 2 2
CaH (s)放在含微量水的N 气流中,在200℃至300℃的升温过程中固体质量一直增加,由此可断定H 的来源之一是
2 2 2
反应 (填“①”或“②”)。若要判断另一个反应是否是H 的来源,必须进行的实验是 。
2
(6)已知3H (g)+Fe O (s)⇌3H O(g)+2Fe(s)。研究表明,在相同温度下,用CaH (s)还原Fe O (s)比直接用H (g)
2 2 3 2 2 2 3 2
还原更有优势,从平衡移动原理角度解释原因: 。