文档内容
2025-2026 学年高一年级化学上学期第一次月考卷
(考试时间:90 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:专题一~专题二(苏教版 2019)。
5.难度系数:0.65。
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Ca 40
第Ⅰ卷(选择题 共 48 分)
一、选择题:本题共 16 个小题,每小题 3 分,共 48 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
2.下列概念之间存在如图所示关系的是
选项 A B C D
X 无机物 钠盐 碱溶液 中和反应
概念
Y 有机物 碳酸盐 碱性溶液 复分解反应
3.国外宇航员吃着“牙膏和砖块”时,中国宇航员已经在太空泡茶了,茶叶装在特制包装袋中,注水后用加
热器进行加热就可以喝了。下列说法正确的是
A.宇航员喝茶时注入的 2 mol H O 的摩尔质量是 36 g·mol-1
2
B.标准状况下,N 个 H O 分子所占体积为 22.4 L
A 2
C.含有 2N 个氧原子的水的质量为 36 g
A
/D.1 mol H O 中含有 3 mol 电子
2
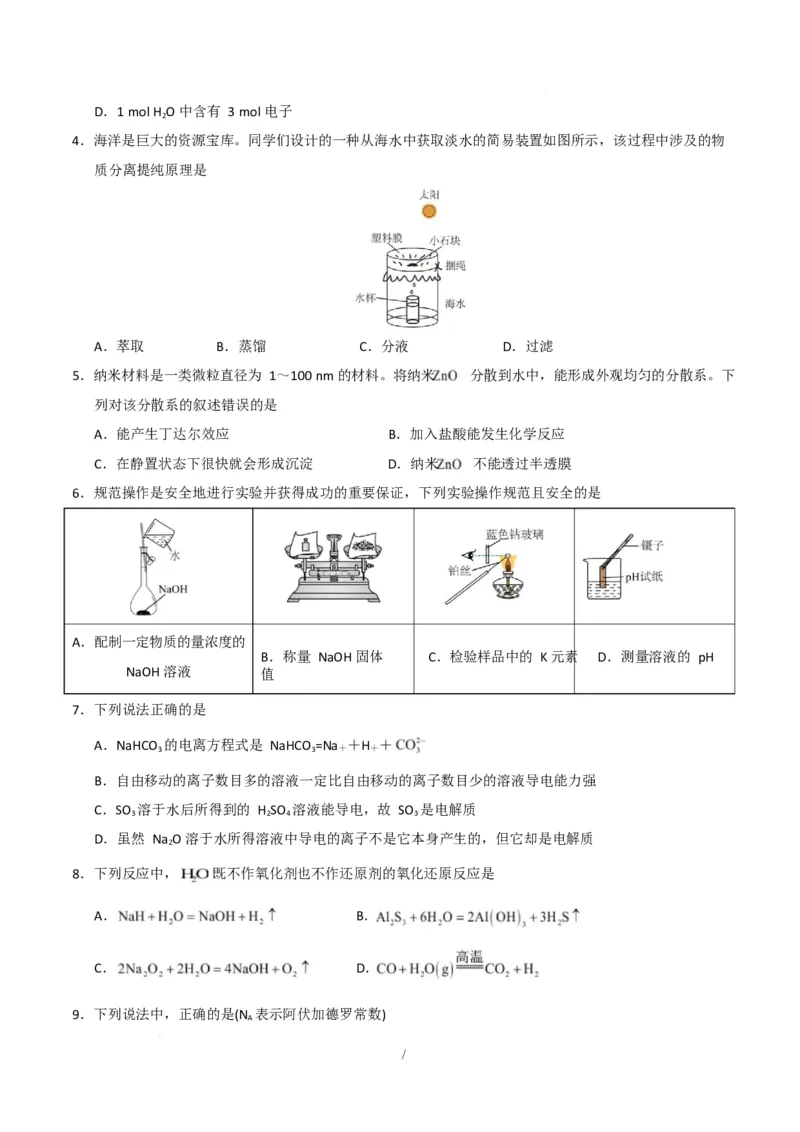
4.海洋是巨大的资源宝库。同学们设计的一种从海水中获取淡水的简易装置如图所示,该过程中涉及的物
质分离提纯原理是
A.萃取 B.蒸馏 C.分液 D.过滤
5.纳米材料是一类微粒直径为 1~100 nm 的材料。将纳米 分散到水中,能形成外观均匀的分散系。下
列对该分散系的叙述错误的是
A.能产生丁达尔效应 B.加入盐酸能发生化学反应
C.在静置状态下很快就会形成沉淀 D.纳米 不能透过半透膜
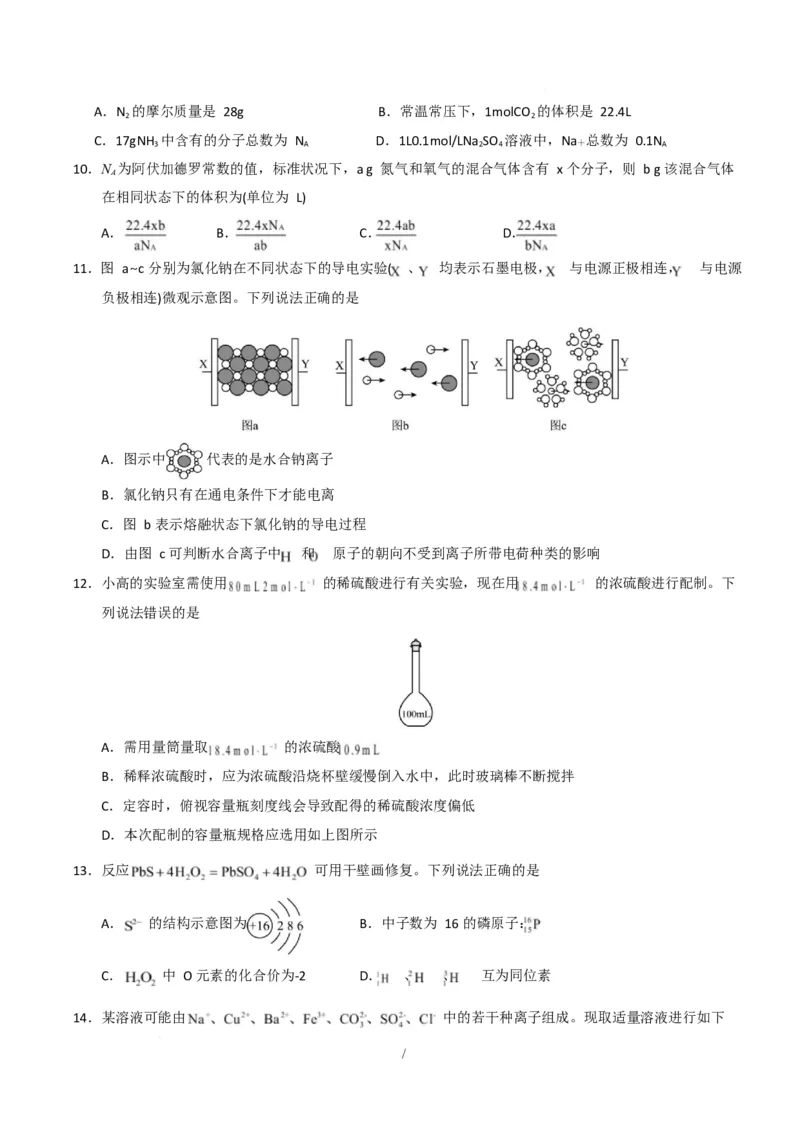
6.规范操作是安全地进行实验并获得成功的重要保证,下列实验操作规范且安全的是
A.配制一定物质的量浓度的
B.称量 NaOH 固体 C.检验样品中的 K 元素 D.测量溶液的 pH
NaOH 溶液 值
7.下列说法正确的是
A.NaHCO
3
的电离方程式是 NaHCO
3
=Na+ +H+ +
B.自由移动的离子数目多的溶液一定比自由移动的离子数目少的溶液导电能力强
C.SO 溶于水后所得到的 H SO 溶液能导电,故 SO 是电解质
3 2 4 3
D.虽然 Na O 溶于水所得溶液中导电的离子不是它本身产生的,但它却是电解质
2
8.下列反应中, 既不作氧化剂也不作还原剂的氧化还原反应是
A. B.
C. D.
9.下列说法中,正确的是(N 表示阿伏加德罗常数)
A
/A.N 的摩尔质量是 28g B.常温常压下,1molCO 的体积是 22.4L
2 2
C.17gNH
3
中含有的分子总数为 N
A
D.1L0.1mol/LNa
2
SO
4
溶液中,Na+ 总数为 0.1N
A
10.N 为阿伏加德罗常数的值,标准状况下,a g 氮气和氧气的混合气体含有 x 个分子,则 b g 该混合气体
A
在相同状态下的体积为(单位为 L)
A. B. C. D.
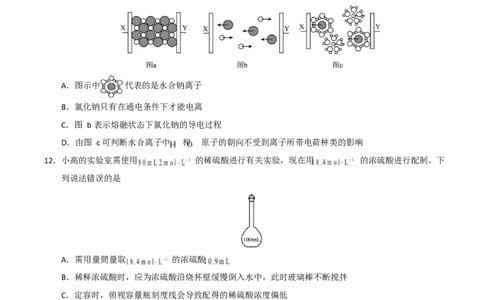
11.图 a∼c 分别为氯化钠在不同状态下的导电实验( 、 均表示石墨电极, 与电源正极相连, 与电源
负极相连)微观示意图。下列说法正确的是
A.图示中 代表的是水合钠离子
B.氯化钠只有在通电条件下才能电离
C.图 b 表示熔融状态下氯化钠的导电过程
D.由图 c 可判断水合离子中 和 原子的朝向不受到离子所带电荷种类的影响
12.小高的实验室需使用 的稀硫酸进行有关实验,现在用 的浓硫酸进行配制。下
列说法错误的是
A.需用量筒量取 的浓硫酸
B.稀释浓硫酸时,应为浓硫酸沿烧杯壁缓慢倒入水中,此时玻璃棒不断搅拌
C.定容时,俯视容量瓶刻度线会导致配得的稀硫酸浓度偏低
D.本次配制的容量瓶规格应选用如上图所示
13.反应 可用干壁画修复。下列说法正确的是
A. 的结构示意图为 B.中子数为 16 的磷原子:
C. 中 O 元素的化合价为-2 D. 、 、 互为同位素
14.某溶液可能由 中的若干种离子组成。现取适量溶液进行如下
/实验:
根据以上实验判断,下列推断错误的是
A.气体 1 可使澄清石灰水变浑浊 B.滤液 2 中加入 不产生白色沉淀
C.原溶液中一定存在 ,一定不存在 D.无色溶液说明不存在 、
15.科学家通过粒子加速器将钙离子加速到极高速度,撞击锎(Cf)靶核,成功合成了超重元素# (Og),该反
应的核反应方程式可表示为: 。Og 是一种极不稳定的超重元素,会迅速衰变
为更轻的元素。下列说法正确的是
A.Og 位于周期表第 7 周期 0 族 B. 可用作示踪原子研究化学反应历程
C. 和 互为同素异形体 D.Cf 元素的相对原子质量为 249
16.如图所示,向密闭容器内可移动活塞的两边分别充入 CO 、H 和 O 的混合气体(已知 CO 体积占整个容
2 2 2 2
器体积的 1/5),将 H 和 O 的混合气体点燃引爆。活塞先左弹,恢复室温过程中活塞右滑,最终左右
2 2
两侧气体体积相同。下列说法错误的是
A.反应前,活塞左右两边气体原子数之比为 3:8
B.原来 H 和 O 的体积之比为 1:1
2 2
C.反应后恢复到室温,活塞左测气体密度大于右侧气体
D.活塞移动情况说明 H 、O 燃烧放热,且该反应气体分子数减少
2 2
第 II 卷(非选择题 共 52 分)
二、非选择题(本题共 4 小题,共 52 分)
17.(10 分)回答下列问题:(1)今有 11 种物质:①盐酸;②石墨;③氯气;④ 晶体;⑤纯硫酸;⑥
金刚石;⑦碱石灰;⑧乙醇;⑨熔融的 ;⑩ ;其中:
①能导电的是(填序号,下同)_____________;
②属于电解质的是_____________;
(2)①19g 某二价金属氯化物( )中含有 ,则 的摩尔质量是______;
/②现有标准状况下 CO 和 混合气体 6.72L,其质量为 11.6g,则此混合气体中,CO 和 的物质的
量之比是______;
③质量相同的①HCl、② 、③ 、④ 四种气体中,在同温同压条件下,所占体积最小的是(填
序号)______。
18.(16 分)某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作顺序如下(设该药片中的其他成分
不与盐酸或氢氧化钠反应)。请回答下列问题:
①配制 稀盐酸和 NaOH 溶液:
②取 1 粒药片(每粒药片质量相同,均为 0.10g),研碎后加入 20.00mL 蒸馏水
③加入 25mL 稀盐酸
④用 NaOH 溶液中和过量的稀盐酸,记录所消耗 NaOH 溶液的体积。
(1)配制 250mL 的稀盐酸用到的玻璃仪器除量筒、烧杯、胶头滴管外,还需要用到的玻璃仪
器有___________、___________。
(2)用密度为 、质量分数为 36.5%的浓盐酸配制实验中所需的稀盐酸,则该浓盐酸的物质的量
浓度为___________,需用量筒量取浓盐酸的体积为___________。
(3)若配制 90mL NaOH 溶液,则需用托盘天平称 NaOH 固体___________g,配制过程中所涉
及的下列相关操作正确的是___________。
a. b. c. d.
(4)下列有关说法正确的是___________。
A.容量瓶上标有刻度线、温度(一般为 20℃)和容积,使用前先检查是否漏水
B.容量瓶要用蒸馏水洗净,待干燥后才能使用
C.定容时俯视刻度线,所配溶液浓度偏高
D.定容后摇匀、静置,发现液面下降,再加蒸馏水至刻度线
(5)某同学 4 次测定所消耗的 NaOH 溶液的体积如下:
测定次序 第 1 次 第 2 次 第 3 次 第 4 次
NaOH(ag)/mL 11.90 12.10 12.00 12.00
根据这位同学的实验数据,计算该药片中碳酸钙的质量分数为___________。
/19.(16 分)I.用 N 表示阿伏加德罗常数的值,按要求填空:
A
(1)在标准状况下,①6.72LCH ;②3.01×1023 个 HCl 分子;③13.6gH S;④0.2molNH 。下列关系表达正
4 2 3
确的是_______。
a.体积②>①>③>④ b.密度②>③>④>①
c.质量②>①>③>④ d.氢原子个数①>③>④>②
(2)8.4gN 与 9.6gR 的分子数目之比为 3:2,原子数目相同。则:9.6gR 的物质的量为_______mol。x
2 x x
值为_______,R 的相对原子质量是_______。
II.同温同压下,100mLX 气体与 50mLY 气体恰好完全反应,得到 100mLZ 气体。
2 2
(3)Z 的化学式为_______。
III.(4)将 2.3 钠投入足量水中,完全反应。冷却到标准状况,得到_______L 气体。
IV.在容积固定的密闭容器中,活塞可自由移动。在室温下,向 A 室充入一定量 H 、O 的混合气体,向
2 2
B 室充入 1mollN ,此时活塞的位置如图所示。
2
(5)A 室混合气体的物质的量为_______mol。
(6)实验测得 A 室混合气体的质量为 34g,则 A 室中 H 的物质的量为_______。
2
20.(10 分)Ⅰ.某无色透明溶液可能含有 Cu2+、Ca2+、K+ 、Ag+ 、SO 、CO 、Cl-中的几种,现进行如下实
验:
①滴加 BaCl 溶液,有白色沉淀产生,将沉淀滤出。
2
②向①沉淀中加入足量的稀硝酸,沉淀部分溶解。
③向①滤液中加入 AgNO 溶液,有白色沉淀生成,该沉淀不溶于稀 HNO 。
3 3
(1)试判断:该溶液中肯定有___________,肯定没有___________(填离子符号)。
(2)写出步骤②发生反应的离子方程式___________。
(3)若要检验溶液中可能存在的离子是否存在,进行的实验操作为___________。
Ⅱ.某溶液中含有较大量的 Cl-、CO 、OH-,如果只取一次该溶液就能够分别将 3 种阴离子依次检验
出来:
(4)下列实验操作顺序正确的是___________。(填写序号,可重复使用)
①滴加 Mg(NO ) 溶液 ②过滤 ③滴加 AgNO 溶液 ④滴加 Ba(NO ) 溶液
3 2 3 3 2
/