文档内容
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
C.硫酸溶液的导电性一定比醋酸溶液导电性强
2024-2025 学年高一化学上学期第一次月考卷
D.氯化氢溶于水能导电,但液态氯化氢不能导电
(考试时间:60分钟 试卷满分:100分) 3.下表中关于物质的分类正确的是
注意事项: 酸 碱 盐 碱性氧化物 酸性氧化物
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
A HSO NaOH BaCO CO CO
2 4 3 2
证号填写在答题卡上。
NaHCO
B HClO KOH CaO SO
2
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动, 3
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。 CHCOO C 3 NaCO CaCl NaO SO
H 2 3 2 2 3
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
NH·H
4.测试范围:第一章(人教版2019)。 D NaHSO 3 2 NaCl SiO CO
4 O 2
5.难度系数:0.65
A.A B.B C.C D.D
6.考试结束后,将本试卷和答题卡一并交回。
4.下列电离方程式正确的是
可能用到的相对原子质量:H 1 Na 11 N 14 O16 S 32 Cl 35.5
A.CuCl=Cu2++Cl- B.Ba(OH)=Ba2++2OH-
2 2
第Ⅰ卷(选择题 共 60 分)
C.NaHCO=Na++H++CO D.NH·HO=NH +OH-
3 3 2
一、选择题:本题共20个小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题目 5.如图所示装置中图1灯泡不亮,图2灯泡发亮,由此得出的结论是
要求的。
1.下列我国古代的技术应用中,其工作原理不涉及化学反应的是:
A.火药使用 B.粮食酿酒
A.固体NaCl不导电,是非电解质
B.电解质在电流的作用下才能发生电离
C.转轮排字 D.铁的冶炼 C.水是电解质,能产生大量的H+和OH-
D.NaCl溶液中存在大量自由移动的Na+和Cl-
6.下列各组物质能发生离子反应的是
2.下列关于电解质的叙述正确的是
A.NaCl溶液与盐酸 B.KNO 溶液与NaOH溶液
3
A.溶于水得到的溶液能导电的化合物都是电解质
C.硝酸银溶液与BaCl 溶液 D.NaSO 溶液与HNO 溶液
2 2 4 3
B.NaCl溶液在电流作用下电离成Na+与Cl-
试题 第15页(共48页) 试题 第16页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
B 实验室用大理石与稀盐酸反应制备二氧化碳 CO2-+2H+=HO+CO↑
7.不能用离子方程式 表示的反应是 3 2 2
HCOˉ+Ba2++OH-= BaCO ↓+
C NaHCO 溶液中加足量Ba(OH) 溶液 3 3 3 2 HO
A. 2
D 用氯化铁溶液刻蚀铜板 Fe3+ + Cu =Fe2++Cu2+ 此
B.
A.A B.B C.C D.D 卷
12.当光束通过下列分散系时,能观察到丁达尔效应的是
C. 只
A.NaCl溶液 B.蔗糖溶液 C.CuSO 溶液 D.AgI胶体
4
装
D.
13.下列反应既属于氧化还原反应,又属于离子反应的是
订
A.氯化钡与稀硫酸反应 B.氢氧化铝治疗胃酸过多
8.氧化还原反应的本质是
A.元素化合价的升降变化 B.电子的转移 C.金属铁放入硫酸铜溶液中 D.燃料的燃烧 不
14.在强酸性无色透明溶液中,能大量共存的离子组是
C.得失氧 D.有氧化反应必有还原反应
密
9.向下列物质中滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是
A.NH 、Mg2+、SO 、Cl- B.K+、OH-、NO 、Na+
封
A.BaCl B.Ba(OH) C.NaCO D.KOH
2 2 2 3
C.Al3+、Cu2+、SO 、Cl- D.Na+、Ca2+、Cl-、CO
10.在 溶液中,滴入 溶液,其导电能力随滴入溶液体积变化的曲线如图所示,下列分析不
15.下列变化不能通过一步反应实现的是
正确的是
A.NaCO→NaOH B.HO→HO C.Fe→FeO D.FeO→Fe(OH)
2 3 2 2 2 3 4 2 3 3
16.某溶液中含有较大量的Cl-、 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依
次检验出来。下列实验操作的操作顺序中,正确的是
①滴加Mg(NO) 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加Ba(NO) 溶液
3 2 3 3 2
A.①②④②③ B.④②①②③.
C.①②③②④ D.④②③②①
A. 的电离方程式是
17.下列“实验结论”与“实验操作及现象”相符的是( )
B.从滴入溶液开始到a点,溶液中的 和 的物质的量均减少
选项 实验操作及现象 实验结论
C.a点到b点的过程中,白色沉淀不断的增多
D.c点溶液呈酸性
A 向某溶液中加入AgNO 溶液,有白色沉淀生成 该溶液中一定含有Cl-
3
11.下列物质的用途或者制备中所涉及到的离子方程式书写正确的是( )
B 向某溶液中加入稀盐酸,产生无色无味气体 该溶液中一定含有CO
选项 用途或者制备 离子方程式
C 向某溶液中加入BaCl 溶液,有白色沉淀生成 该溶液中一定含有SO
2
A 用稀硫酸清洗铁锈 FeO+6H+=2Fe2++3HO
2 3 2
试题 第27页(共8页) 试题 第28页(共8页)………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
室温下向某溶液中加入几滴酚酞溶液,溶液变 (1)上述物质属于电解质的是 (填序号)。
D 该溶液一定呈碱性
红
(2)分别写出⑨、⑩在水中的电离方程式: 、 。
A.A B.B C.C D.D
(3)少量④与⑤的水溶液反应的化学方程式为 。
18.下列叙述中,正确的是
(4)⑧的水溶液与足量②的水溶液反应的化学方程式为 。
A.KNO 固体不导电,所以KNO 不是电解质
3 3 (5)氢氧化铁溶于②的水溶液反应的离子方程式为 。
B.铜丝、石墨均能导电,所以它们都是电解质
(6)选择两种属于不同基本反应类型的方法一步制取⑥(试剂任选),用化学方程式表示该方法: 、
C.熔融的MgCl 能导电,所以MgCl 是电解质
2 2
。
D.NaCl溶于水,在通电条件下才能发生电离
22.(8分)化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下8NH+3Cl=N+6NHCl。
3 2 2 4
19.世界卫生组织和中国卫健委公认二氧化氯 为新时代绿色消毒剂,其制备方程式: (1)NH 中N元素的化合价为 。Cl-的离子结构示意图为 。
3
(2)Cl 中的Cl元素 (填失电子或得电子),作还原剂的物质是 (写化学式,下同),上述反
2
,下列说法不正确的是 应中具有氧化性的反应物是 。
(3)反应每消耗3个Cl 时,转移 个电子,有 个NH (被氧化或被还原)。
2 3
A. 的消毒作用可能与其氧化性有关 B.氧化剂与还原剂的质量之比为
23.(6分)央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企
C. 具有还原性,反应中失去电子 D.生成 分子个数与转移电子个数之比为
业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水
20.双碱法脱除烟气中SO 的过程如图所示。下列说法中不正确的是
2
溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO) 中铬元素是+3价,则其中铁元素是 价。CrO 是一种酸根离子,则Fe(CrO)
2 2 2 2
属于 (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和KSO 溶液共同具备的性质是 (填序号)。
2 4
A.都不稳定,密封放置会产生沉淀
A.双碱法中的“双碱”是指NaOH和Ca(OH) B.二者均有丁达尔效应
2
B.过程Ⅰ和过程Ⅱ中碱的作用不同 C.分散质粒子可通过滤纸
C.脱除过程中硫元素的化合价一直没有变化 (3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中
D.脱除SO 的过程中,NaOH可以循环利用 的 (填序号)。
2
第 II 卷(非选择题 共 40 分)
二、填空题
21.(8分)完成下列填空:
①氯化钠溶液②氯化氢③铜④二氧化硫⑤氢氧化钠⑥硫酸亚铁⑦碳酸钙⑧纯碱⑨碳酸氢钠⑩碳酸铵
试题 第35页(共48页) 试题 第36页(共48页)
学学科科网网((北北京京))股股份份有有限限公公司司………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
②检验HO:向溶液A、B中分别滴加适量KMnO 溶液。
2 2 4
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO ,对其产生的原因 此
2
提出猜想: 卷
猜想1.KMnO,有氧化性,能被还原为MnO
4 2 只
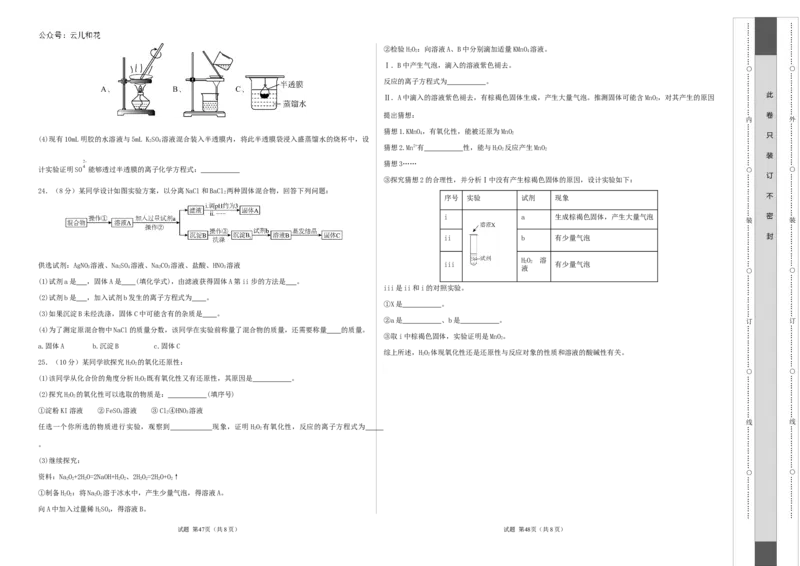
(4)现有10mL明胶的水溶液与5mL K SO 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设
2 4
猜想2.Mn2+有 性,能与HO 反应产生MnO
2 2 2
装
猜想3……
计实验证明SO 能够透过半透膜的离子化学方程式:
订
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
24.(8分)某同学设计如图实验方案,以分离NaCl和BaCl 两种固体混合物,回答下列问题:
2
序号 实验 试剂 现象 不
i a 生成棕褐色固体,产生大量气泡 密
ii b 有少量气泡 封
HO 溶
供选试剂:AgNO 溶液、NaSO 溶液、NaCO 溶液、盐酸、HNO 溶液 iii 2 2 有少量气泡
3 2 4 2 3 3 液
(1)试剂a是 ,固体A是 (填化学式),由滤液获得固体A第ii步的方法是 。
iii是ii和i的对照实验。
(2)试剂b是 ,加入试剂b发生的离子方程式为 。
①X是 。
(3)如果沉淀B未经洗涤,固体C中可能含有的杂质是 。
②a是 、b是 。
(4)为了测定原混合物中NaCl的质量分数,该同学在实验前称量了混合物的质量,还需要称量 的质量。
③取i中棕褐色固体,实验证明是MnO。
2
a.固体A b.沉淀B c.固体C
综上所述,HO 体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
2 2
25.(10分)某同学欲探究HO 的氧化还原性:
2 2
(1)该同学从化合价的角度分析HO 既有氧化性又有还原性,其原因是 。 2 2
(2)探究HO 的氧化性可以选取的物质是: (填序号)
2 2
①淀粉KI溶液 ②FeSO 溶液 ③Cl④HNO 溶液
4 2 3
任选一个你所选的物质进行实验,观察到 现象,证明HO 有氧化性,反应的离子方程式为
2 2
。
(3)继续探究:
资料:NaO+2HO=2NaOH+HO、2HO=2HO+O↑
2 2 2 2 2 2 2 2 2
①制备HO:将NaO 溶于冰水中,产生少量气泡,得溶液A。
2 2 2 2
向A中加入过量稀HSO,得溶液B。
2 4
试题 第47页(共8页) 试题 第48页(共8页)