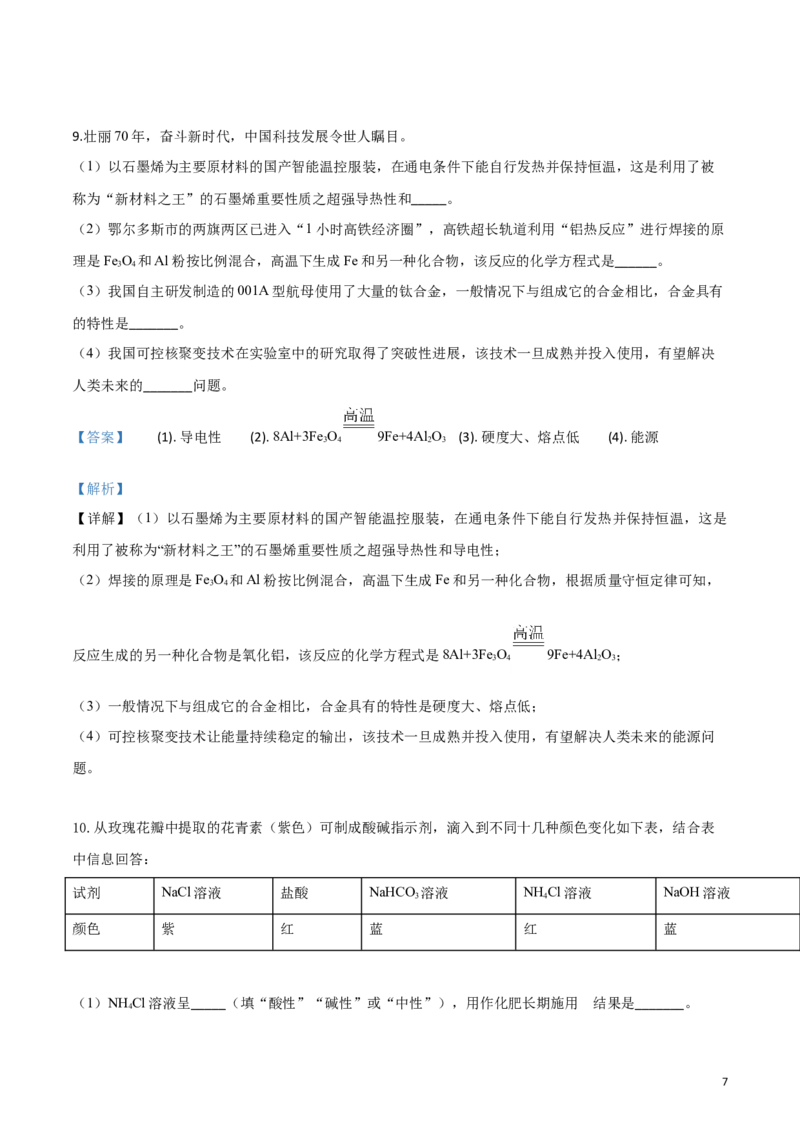文档内容
2019 年鄂尔多斯中考化学试题
1.绿水青山就是金山银山。下列做法不符合这一理念的是
A. 无纸化办公,低碳出行,减少资源消耗
B. 生活垃圾深埋处理,减少对地表的污染
C. 推广使用滴、喷灌技术,高效利用水资源
D. 退耕还草,植树造林,提高植被覆盖率
【答案】B
【解析】
【详解】A、无纸化办公,低碳出行,减少资源消耗,有利于保护环境,故A正确;
B、生活垃圾深埋处理,会污染土壤和地下水,不利于保护环境,故B错误;
C、推广使用滴、喷灌技术,高效利用水资源,有利于节约水资源,故C正确;
D、退耕还草,植树造林,提高植被覆盖率,有利于保护环境,故D正确。故选B。
2.学习化学要构建基本理念,对以下基本观念的认识,正确的是
A. 分类观:干冰和可燃冰都属于氧化物
B. 元素观:氧气和臭氧都由氧元素组成
C. 变化观:二氧化碳和一氧化碳不可以相互转化
D. 结构观:氖原子和氟原子最外层电子数相同,化学性质也相同
【答案】B
【解析】
【详解】A、干冰是二氧化碳,二氧化碳是由氧元素和另外一种元素组成的化合物,属于氧化物;可燃冰
的主要成分是甲烷,属于混合物,故A错误;
B、氧气和臭氧都由氧元素组成,故B正确;
C、二氧化碳在高温条件下与碳反应生成一氧化碳,一氧化碳在氧气中点燃生成二氧化碳,二氧化碳和一
氧化碳可以相互转化,故C错误;
D、氖原子和氟离子最外层电子数相同,但化学性质不相同,氟离子可以结合阳离子构成物质,氖原子性
质稳定,故D错误。故选B。
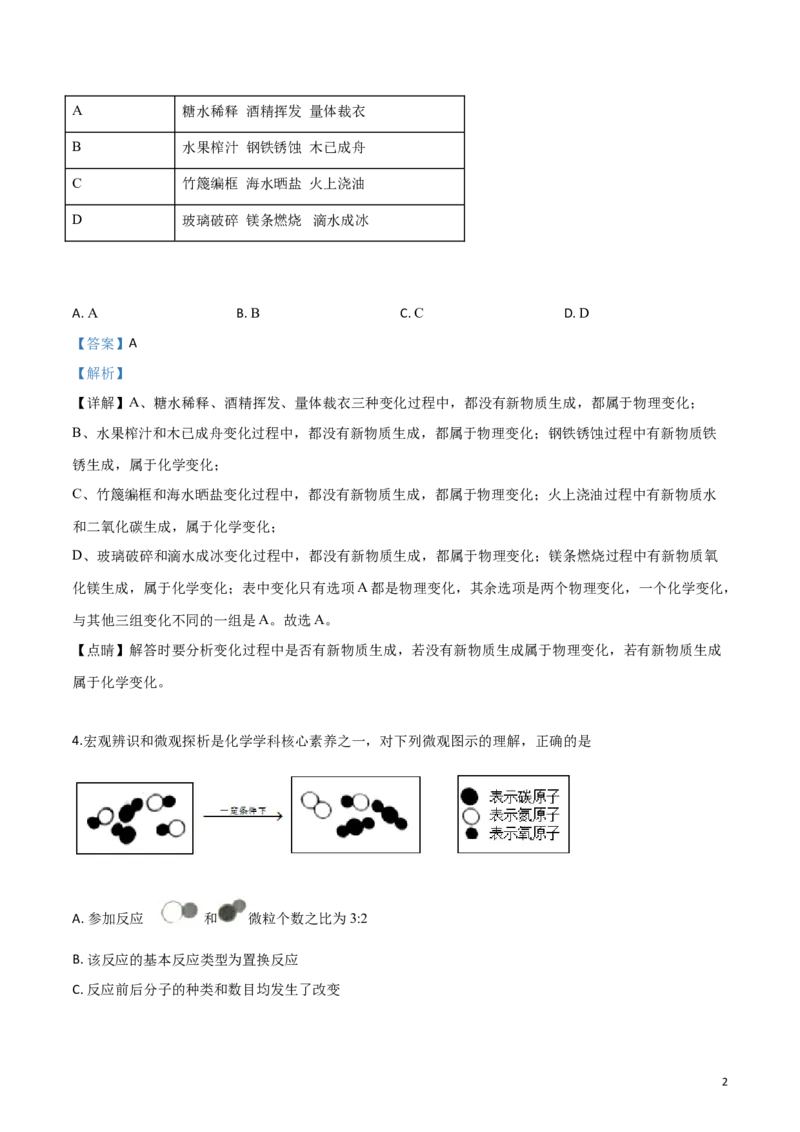
3.物质的变化是化学研究的重要内容,下表中与其他三组变化不同的一组是
组别 变化内容
1A 糖水稀释 酒精挥发 量体裁衣
B 水果榨汁 钢铁锈蚀 木已成舟
C 竹篾编框 海水晒盐 火上浇油
D 玻璃破碎 镁条燃烧 滴水成冰
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A、糖水稀释、酒精挥发、量体裁衣三种变化过程中,都没有新物质生成,都属于物理变化;
B、水果榨汁和木已成舟变化过程中,都没有新物质生成,都属于物理变化;钢铁锈蚀过程中有新物质铁
锈生成,属于化学变化;
C、竹篾编框和海水晒盐变化过程中,都没有新物质生成,都属于物理变化;火上浇油过程中有新物质水
和二氧化碳生成,属于化学变化;
D、玻璃破碎和滴水成冰变化过程中,都没有新物质生成,都属于物理变化;镁条燃烧过程中有新物质氧
化镁生成,属于化学变化;表中变化只有选项A都是物理变化,其余选项是两个物理变化,一个化学变化,
与其他三组变化不同的一组是A。故选A。
【点睛】解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成
属于化学变化。
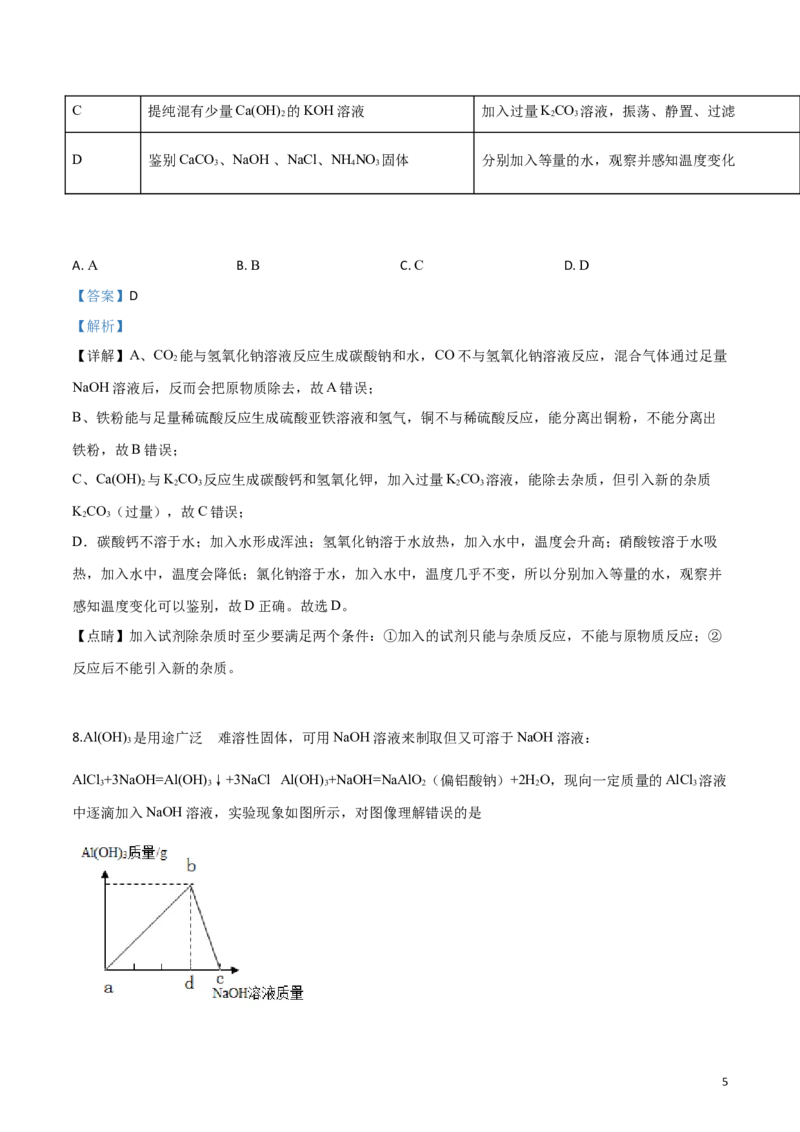
4.宏观辨识和微观探析是化学学科核心素养之一,对下列微观图示的理解,正确的是
A. 参加反应 的和 微粒个数之比为3:2
B. 该反应的基本反应类型为置换反应
C. 反应前后分子的种类和数目均发生了改变
2D. 由 和 分别构成的物质中同种元素化合价相同
【答案】C
【解析】
【分析】
由图中信息可知,反应的微观示意图表示两个NO分子与两个CO分子反应,通过C、N、O原子的重新结
合,形成了一个N 分子和两个CO 分子;反应的化学方程式为:2NO+2CO N +2CO 。
2 2 2 2
【详解】A、根据化学方程式可知,参加反应的 和 微粒个数之比为2:2(或1:1),故A错误;
B、该反应的反应物是两种化合物,生成物上一种单质和一种化合物,不符合置换反应的特征,故B错误;
C、根据化学方程式可知,反应前后分子的种类和数目均发生了改变,故C正确;
D、由 和 分别构成的物质中具有相同元素是碳元素, 中的碳元素化合价为+2价,
中碳元素化合价是+4价,由 和 分别构成的物质中同种元素化合价不相同,故D错误。故选
C。
【点睛】根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构
成与粒子个数关系,是解答本题的基本方法。
5.混合气体通过足量澄清石灰水后,经干燥再依次通过灼热的氧化铜、无水硫酸铜、澄清石灰水,若每个
环节均有明显现象,则符合条件的气体组合是
A. O CO N B. N H CO
2 2 2 2 2 2
C. H CO CO D. CO Ar CO
2 2 2
【答案】C
【解析】
【详解】无水硫酸铜遇水变蓝色,二氧化碳能使澄清石灰水变浑浊,一氧化碳、氢气会与灼热的氧化铜反
应。
A、O、N 都不能与澄清石灰水、灼热的氧化铜、无水硫酸铜反应,混合气体通过上述试剂后,不可能每
2 2
个环节均有明显现象,故A错误;
B、N 不能与澄清石灰水、灼热的氧化铜、无水硫酸铜反应,混合气体通过上述试剂后,不可能每个环节
2
3均有明显现象,故B错误;
C、二氧化碳能使澄清石灰水变浑浊,氢气、CO都能与灼热氧化铜反应,产生使黑色氧化铜变红的现象,
氢气与灼热氧化铜反应生成铜和水,CO与灼热氧化铜反应生成铜和二氧化碳,无水硫酸铜遇水变蓝色,
当混合气体为H 、CO、CO 组合时,通过足量澄清石灰水后,经干燥再依次通过灼热的氧化铜、无水硫
2 2
酸铜、澄清石灰水,会依次产生澄清石灰水变浑浊,黑色氧化铜变红,无水硫酸铜变蓝色,澄清石灰水变
浑浊的现象,故C正确;
D、Ar是稀有气体,化学性质稳定,不能与澄清石灰水、灼热的氧化铜、无水硫酸铜反应,混合气体通过
上述试剂后,不可能每个环节均有明显现象,故D错误。故选C。
6.金属M与Cu(NO ) 溶液发生反应:M+Cu(NO )=Cu+M(NO ),下列叙述不正确的是
3 2 3 2 3 2
A. 金属M不可能是铝
B. M一定发生反应:M+2AgNO =2Ag+M(NO )
3 3 2
C. 若M为镁,恰好完全反应后,溶液质量较反应前减少
D. 恰好完全反应后,M表面有红色固体析出,溶液一定由蓝色变为无色
【答案】D
【解析】
【详解】A、铝在形成硝酸盐时显+3价,该反应中的M显+2价,该金属不可能是铝,故A正确;
B、根据金属M与Cu(NO ) 溶液发生反应:M+Cu(NO )=Cu+M(NO ) 可知,M的金属活动性大于铜,所
3 2 3 2 3 2
以M的金属活动性大于银,M一定发生反应:M+2AgNO =2Ag+M(NO ),故B正确;
3 3 2
C、若M为镁,该反应的化学方程式为:Mg+Cu(NO )=Cu+Mg(NO ),根据化学方程式可知,每24份质
3 2 3 2
量的镁能置换出64份质量的铜,恰好完全反应后,溶液质量较反应前减少,故C正确;
D、恰好完全反应后,M表面有红色固体析出,溶液不一定由蓝色变为无色,因为M(NO) 溶液不一定呈
3 2
无色,例如铁与硝酸铜反应生成的磷酸亚铁呈浅绿色,故D错误。故选D。
的
【点睛】本题难度不大,明确M 金属活动性比铜强、M显+2价是正确解答本题的关键。
7.分离、提纯、除杂、鉴别是基本的实验技能,下列实验设计能达到实验目的的是
组别 实验目的 实验设计
A 除去CO 中混有的少量CO 通过足量NaOH溶液后,干燥,收集气体
2
B 分离铜粉和铁粉的混合物 加入足量稀硫酸充分反应后,过滤、洗涤、干燥
4C 提纯混有少量Ca(OH) 的KOH溶液 加入过量KCO 溶液,振荡、静置、过滤
2 2 3
D 鉴别CaCO 、NaOH 、NaCl、NH NO 固体 分别加入等量的水,观察并感知温度变化
3 4 3
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、CO 能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,混合气体通过足量
2
NaOH溶液后,反而会把原物质除去,故A错误;
B、铁粉能与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,能分离出铜粉,不能分离出
铁粉,故B错误;
C、Ca(OH) 与KCO 反应生成碳酸钙和氢氧化钾,加入过量KCO 溶液,能除去杂质,但引入新的杂质
2 2 3 2 3
KCO(过量),故C错误;
2 3
D.碳酸钙不溶于水;加入水形成浑浊;氢氧化钠溶于水放热,加入水中,温度会升高;硝酸铵溶于水吸
热,加入水中,温度会降低;氯化钠溶于水,加入水中,温度几乎不变,所以分别加入等量的水,观察并
感知温度变化可以鉴别,故D正确。故选D。
【点睛】加入试剂除杂质时至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②
反应后不能引入新的杂质。
的
8.Al(OH) 是用途广泛 难溶性固体,可用NaOH溶液来制取但又可溶于NaOH溶液:
3
AlCl +3NaOH=Al(OH) ↓+3NaCl Al(OH) +NaOH=NaAlO (偏铝酸钠)+2H O,现向一定质量的AlCl 溶液
3 3 3 2 2 3
中逐滴加入NaOH溶液,实验现象如图所示,对图像理解错误的是
5A. b点生成的Al(OH) 质量达到最大值
3
B. a、c点溶液中的溶质分别是AlCl 和NaAlO
3 2
C. bc段(不含端点)的铝元素存在于Al(OH) 和NaAlO 中
3 2
D. ad段和dc段消耗的NaOH质量比为3:1
【答案】B
【解析】
【详解】A、根据图像可知,b点生成的Al(OH) 质量达到最大值,故A正确;
3
B、根据题意可知a点溶液中的溶质是AlCl ,c点溶液中的溶质是Al(OH) 与NaOH反应生成的 NaAlO 和
3 3 2
ad段生成的氯化钠,故B错误;
C、bc段(不含端点)发生的反应是Al(OH) +NaOH=NaAlO (偏铝酸钠)+2H O,铝元素存在于Al(OH)
3 2 2 3
和NaAlO 中,故C正确;
2
D、设:一定质量的AlCl 溶液中AlCl 质量为m,ad段消耗的氢氧化钠质量为x,生成氢氧化铝的质量为
3 3
y。
x= ;
y= ;
设:dc段消耗的NaOH质量为z。
z= ;
ad段和dc段消耗的NaOH质量比= : =3:1,故D正确。故选B。
69.壮丽70年,奋斗新时代,中国科技发展令世人瞩目。
(1)以石墨烯为主要原材料的国产智能温控服装,在通电条件下能自行发热并保持恒温,这是利用了被
称为“新材料之王”的石墨烯重要性质之超强导热性和_____。
(2)鄂尔多斯市的两旗两区已进入“1小时高铁经济圈”,高铁超长轨道利用“铝热反应”进行焊接的原
理是Fe O 和Al粉按比例混合,高温下生成Fe和另一种化合物,该反应的化学方程式是______。
3 4
(3)我国自主研发制造的001A型航母使用了大量的钛合金,一般情况下与组成它的合金相比,合金具有
的特性是_______。
(4)我国可控核聚变技术在实验室中的研究取得了突破性进展,该技术一旦成熟并投入使用,有望解决
人类未来的_______问题。
【答案】 (1). 导电性 (2). 8Al+3Fe O 9Fe+4Al O (3). 硬度大、熔点低 (4). 能源
3 4 2 3
【解析】
【详解】(1)以石墨烯为主要原材料的国产智能温控服装,在通电条件下能自行发热并保持恒温,这是
利用了被称为“新材料之王”的石墨烯重要性质之超强导热性和导电性;
(2)焊接的原理是Fe O 和Al粉按比例混合,高温下生成Fe和另一种化合物,根据质量守恒定律可知,
3 4
反应生成的另一种化合物是氧化铝,该反应的化学方程式是8Al+3Fe O 9Fe+4Al O;
3 4 2 3
(3)一般情况下与组成它的合金相比,合金具有的特性是硬度大、熔点低;
(4)可控核聚变技术让能量持续稳定的输出,该技术一旦成熟并投入使用,有望解决人类未来的能源问
题。
10.从玫瑰花瓣中提取的花青素(紫色)可制成酸碱指示剂,滴入到不同十几种颜色变化如下表,结合表
中信息回答:
试剂 NaCl溶液 盐酸 NaHCO 溶液 NH Cl溶液 NaOH溶液
3 4
颜色 紫 红 蓝 红 蓝
的
(1)NH Cl溶液呈_____(填“酸性”“碱性”或“中性”),用作化肥长期施用 结果是_______。
4
7(2)向某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定不存在Na+、K+、Fe3+、NH +、NO -、
4 3
SO 2-离子中的______(填离子符号)。
4
(3)胃溃疡患者不用碳酸氢钠片治疗胃酸过多的原因是_______(用化学方程式表示)
【答案】 (1). 酸性 (2). 使土壤酸化、板结(写出其中之一即可) (3). Fe3+、NH + (4).
4
NaHCO +HCl=NaCl+H O+CO↑
3 2 2
【解析】
【详解】(1)盐酸呈酸性,从玫瑰花瓣中提取的花青素(紫色)在盐酸、NH Cl溶液中呈红色,所以
4
NH Cl溶液呈酸性,用作化肥长期施用的结果是使土壤酸化、板结;
4
(2)NaOH溶液呈碱性,溶液中存在OH-,从玫瑰花瓣中提取的花青素(紫色)在NaOH溶液呈蓝色,向
某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定存在OH-,Fe3+、NH +与不能共存,所以该溶液
4
不存在Fe3+、NH +;
4
(3)碳酸氢钠与胃酸(存在盐酸)反应产生二氧化碳气体,可能加重胃溃疡病,该反应的化学式方程式
为:NaHCO +HCl=NaCl+H O+CO↑;
3 2 2
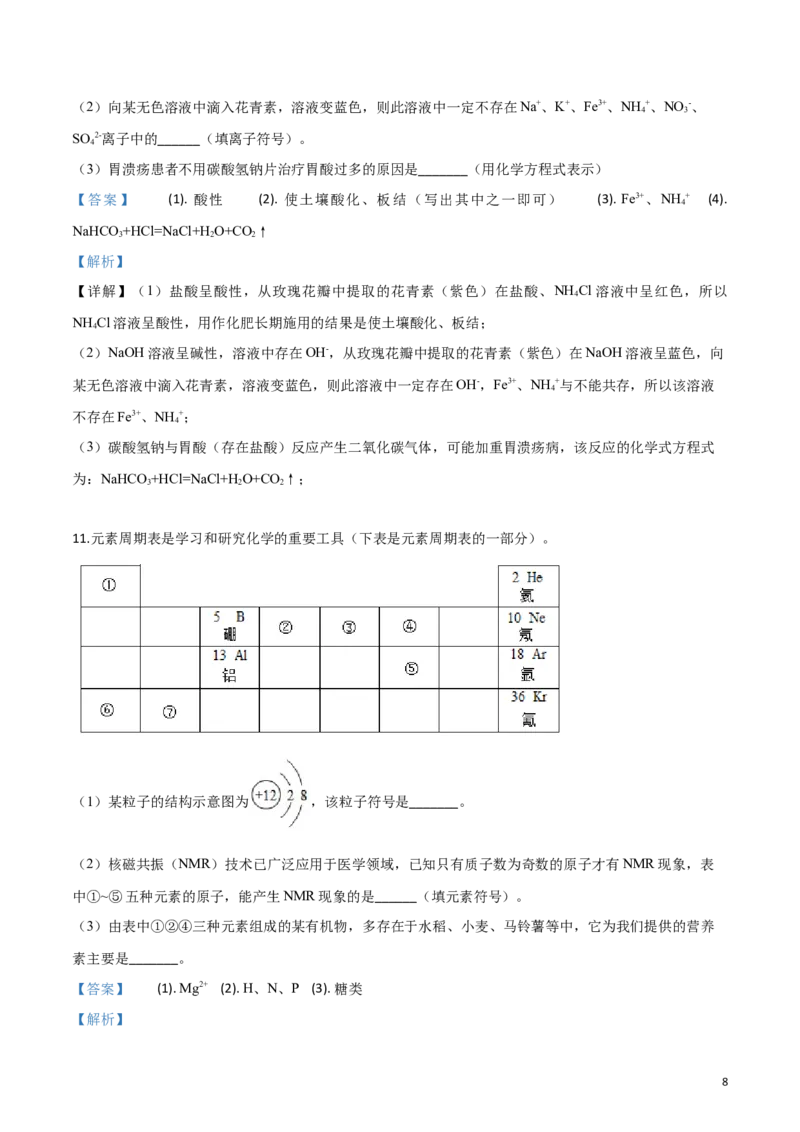
11.元素周期表是学习和研究化学的重要工具(下表是元素周期表的一部分)。
(1)某粒子的结构示意图为 ,该粒子符号是_______。
(2)核磁共振(NMR)技术已广泛应用于医学领域,已知只有质子数为奇数的原子才有NMR现象,表
中①~⑤五种元素的原子,能产生NMR现象的是______(填元素符号)。
(3)由表中①②④三种元素组成的某有机物,多存在于水稻、小麦、马铃薯等中,它为我们提供的营养
素主要是_______。
【答案】 (1). Mg2+ (2). H、N、P (3). 糖类
【解析】
8【详解】(1)根据核内质子数为12可知,该微粒是镁元素一种微粒,质子数比核外电子数多 2,说明该
微粒是带两单位正电荷,离子符号为Mg2+;
(2)表中①~⑤五种元素的原子,质子数为奇数的原子氢元素(质子数为1)、氮元素(质子数为7)、
磷元素(质子数为15),元素符号分别为:H、N、P;
(3)由表中①(氢元素)、②(碳元素)④(氧元素)三种元素组成的某有机物是淀粉,多存在于水稻、
小麦、马铃薯等中,它为我们提供的营养素主要是糖类。
12.为M、N两种固体物质的溶解度曲线,据图回答:
(1)b点表示的意义是_______。
(2)t℃时,将M溶液的状态由a点转化到b点,可采用的方法是_______和_______。
2
(3)将t℃时,M和N的饱和溶液各100g降温至t℃,过滤,得到滤液m和滤液n。关于m和n的说法
1 0
正确的是______(填序号)。
A 都是饱和溶液 B 溶液质量:m