文档内容
2025-2026 学年高一化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮 图 3 图 4
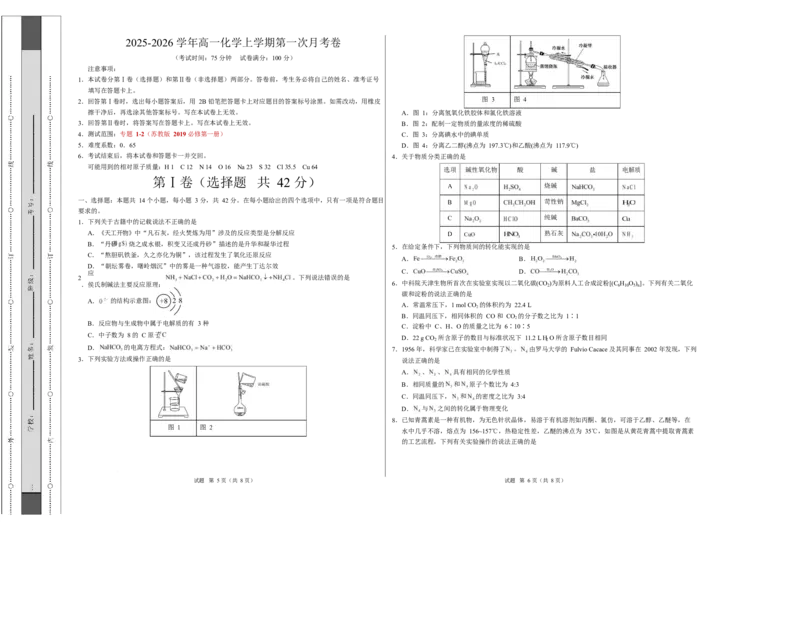
擦干净后,再选涂其他答案标号。写在本试卷上无效。 A.图 1:分离氢氧化铁胶体和氯化铁溶液
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。 B.图 2:配制一定物质的量浓度的稀硫酸
4.测试范围:专题 1-2(苏教版 2019 必修第一册) C.图 3:分离碘水中的碘单质
5.难度系数:0.65 D.图 4:分离乙二醇(沸点为 197.3℃)和乙酸(沸点为 117.9℃)
6.考试结束后,将本试卷和答题卡一并交回。 4.关于物质分类正确的是
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Cu 64
选项 碱性氧化物 酸 碱 盐 电解质
第Ⅰ卷(选择题 共 42 分)
A 烧碱
一、选择题:本题共 14 个小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是符合题目 B 苛性钠
要求的。
C 纯碱
1.下列关于古籍中的记载说法不正确的是
A.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应 D 熟石灰
B.“丹砂 烧之成水银,积变又还成丹砂”描述的是升华和凝华过程
5.在给定条件下,下列物质间的转化能实现的是
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应
A. B.
D.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效
应 C. D.
2 。下列说法错误的是
.侯氏制碱法主要反应原理: 6.中科院天津生物所首次在实验室实现以二氧化碳(CO 2 )为原料人工合成淀粉[(C 6 H 1 0 O 5 ) n ]。下列有关二氧化
碳和淀粉的说法正确的是
A. 的结构示意图:
A.常温常压下,1 mol CO 的体积约为 22.4 L
2
B.同温同压下,相同体积的 CO 和 CO 的分子数之比为 1∶1
2
B.反应物与生成物中属于电解质的有 3 种
C.淀粉中 C、H、O 的质量之比为 6∶10∶5
C.中子数为 8 的 C 原子
D.22 g CO 所含原子的数目与标准状况下 11.2 L H O 所含原子数目相同
2 2
D. 的电离方程式: 7.1956 年,科学家已在实验室中制得了 。 由罗马大学的 Fulvio Cacace 及其同事在 2002 年发现,下列
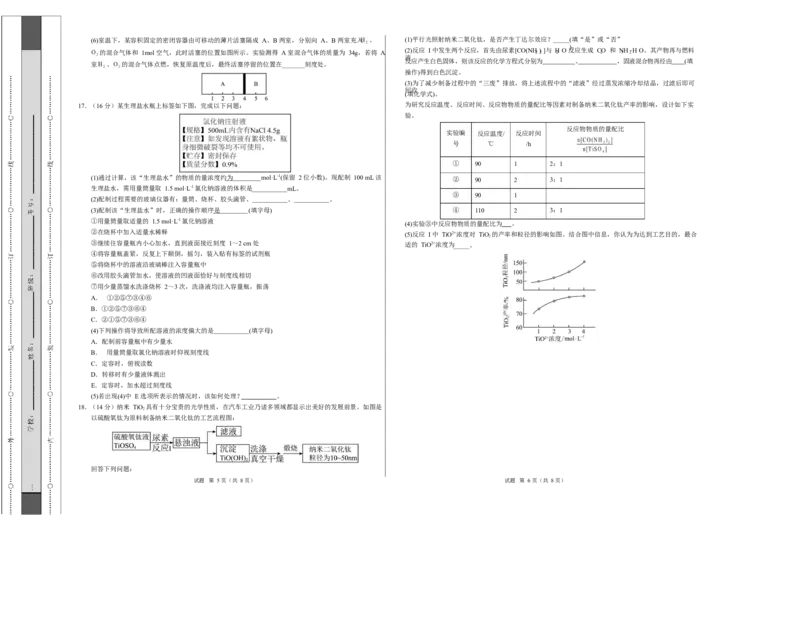
3.下列实验方法或操作正确的是 说法正确的是
A. 、 、 具有相同的化学性质
B.相同质量的 和 原子个数比为 4:3
C.同温同压下, 和 的密度之比为 3:4
D. 与 之间的转化属于物理变化
8.已知青蒿素是一种有机物,为无色针状晶体,易溶于有机溶剂如丙酮、氯仿,可溶于乙醇、乙醚等,在
图 1 图 2
水中几乎不溶,熔点为 156~157℃,热稳定性差,乙醚的沸点为 35℃,如图是从黄花青蒿中提取青蒿素
的工艺流程,下列有关实验操作的说法正确的是
试题 第 5 页(共 8 页) 试题 第 6 页(共 8 页)③200 mL2.0 mol·L 溶液 ④600 mL1.0 mol·L 溶液
下列说法正确的是
A.溶液的导电能力:①=②
B.Cl-的物质的量:②>③>④
C.标准状况下,将 22.4 L HCl 溶于 400 mL 水中可得①
A.研碎应该在烧杯中进行
D.②④中分别加入足量的铁粉,消耗的 Fe 的质量比为 5∶6
B.操作 I 是萃取,所用的玻璃仪器有烧杯、分液漏斗
13.在一定的温度下,用一可自由滑动的隔板将密闭容器分成左右两部分,向两边分别充入等质量的 和
C.操作 II 是蒸馏,所用玻璃仪器有蒸馏烧瓶、冷凝管、尾接管、锥形瓶
D.操作 III 是重结晶,具体为溶解、加热浓缩、冷却结晶、过滤 ,隔板处于如图位置。下列说法不正确的是
9.下列说法正确的是
A.将 40 g NaOH 溶于 1 L 水中,c(NaOH)=1 mol·L-1
B.从 1 L 1 mol·L-1 的碳酸钠溶液中取出 500 mL 后,剩余溶液的物质的量浓度为 0.5 mol·L-1
A.左侧充入的气体是
C.0.1 L 2.0 mol·L-1 的氨水中 n(NH )=0.2 mol
3
B.左右两侧的体积比是 2:1
D.100 mL 溶液中含有 28.4 g Na
2
SO
4
,则溶液中 c(Na+)=4.0 mol·L-1
C.左右两侧的气体密度比是 1:2
10.某实验需用 溶液,配制该 溶液的几个关键实验步骤和操作示意图如下。下列
D.左右两侧的原子个数之比是 5:2
说法正确的是
14.把 含有 和 的混合溶液分成 5 等份,取一份加入含 硫酸钠的溶液,恰好使钡离子
完全沉淀;另取一份加入 硝酸银的溶液,恰好使氯离子完全沉淀,则该混合溶液中钾离子浓度为
A. B.
C. D.
第 II 卷(非选择题 共 58
分)
二、非选择题:本题共 4 个小题,共 58 分。
A.用托盘天平和滤纸称取 氢氧化钠固体
15.(12 分)分类是认识和研究物质及其变化的一种常用的科学方法。现有以下物质:
B. 在烧杯中完全溶解后,立即转移到容量瓶中
① ②液氯③ 固体④硫酸⑤酒精⑥食盐水⑦铁⑧熔融硫酸钡⑨小苏打
C.上述操作的先后顺序是③②④⑥①⑤
(1) 是国际公认的高效安全灭菌消毒剂之一、 能被水吸收制备次氯酸(HClO),其化学反应方程
D.操作①时,若仰视容量瓶的刻度线,则所配的 溶液浓度偏高
11.由下列实验操作和现象得出的结论错误的是
式为: ;故从物质分类的角度看, 属于 (填“酸性氧化物”或“碱性氧化
物”)。
(2)以上属于电解质的有 (填序号,下同);属于非电解质有 ;上述条件下能导电
选
实验操作 实验现象 实验结论 的物质有 。
项
(3)请写出③在水溶液中的电离方程式: 。
将氢氧化钠固体放在表面皿上,露置于 氢氧化钠固体
16.(16 分)完成下面有关计算。
A 固体表面逐渐潮湿
空气中 具有吸水性
(1)常温常压下,160 g 的 气体含有的原子数为 。
B 向某溶液中滴加紫色石蕊溶液 溶液变红 该溶液呈酸性 (2)下列所给出的几组物质中:标准状况下体积最大的是 。(填序号)
① ;② 个 ;③ ;④标准状况下
将一根用砂纸打磨过的铝丝浸入硫酸铜 铝丝表面出现红色固 金属活动性:Cu
C (3) 中含有 mol 质子, 个电子。
溶液一段时间 体,溶液蓝色变浅 >Al
(4)在标准状况下 15 g CO 与 的混合气体,体积为 11.2 L。该混合气体中 CO 与 的物质的量比
向盛有半瓶水的锥形瓶中滴入一滴红墨 活性炭具有吸
为 。
D 溶液的红色褪去
水,投入几块活性炭,振荡 附性
(5)某溶液中只含有 、 、 、 四种离子,已知前三种离子的个数比为 ,则溶液中
12.现有下列四种溶液:
和 的离子个数比为 。
①400 mL2.5 mol·L HCl 溶液 ②250 mL4.0 mol·L HCl 溶液
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)(6)室温下,某容积固定的密闭容器由可移动的薄片活塞隔成 A、B 两室,分别向 A、B 两室充入 、 (1)平行光照射纳米二氧化钛,是否产生丁达尔效应? (填“是”或“否”
)。
的混合气体和 1mol 空气,此时活塞的位置如图所示。实验测得 A 室混合气体的质量为 34g,若将 A (2)反应 I 中发生两个反应,首先由尿素[CO(NH 2 ) 2 ]与 H 2 O 反应生成 C 2 O 和 N 3 H 2 ·H O。其产物再与燃料
液
反应产生白色固体,则该反应的化学方程式分别为 、 ,固液混合物再经由 (填
室 、 的混合气体点燃,恢复原温度后,最终活塞停留的位置在 刻度处。
操作)得到白色沉淀。
(3)为了减少制备过程中的“三废”排放,将上述流程中的“滤液”经过蒸发浓缩冷却结晶,过滤后即可
回收
(填化学式)。
17.(16 分)某生理盐水瓶上标签如下图,完成以下问题: 为研究反应温度、反应时间、反应物物质的量配比等因素对制备纳米二氧化钛产率的影响,设计如下实
验。
反应物物质的量配比
实验编 反应温度/ 反应时间
号 ℃ /h
① 90 1 2:1
(1)通过计算,该“生理盐水”的物质的量浓度约为 mol·L-1(保留 2 位小数)。现配制 100 mL 该 ② 90 2 3:1
生理盐水,需用量筒量取 1.5 mol·L-1 氯化钠溶液的体积是 mL。
③ 90 1
(2)配制过程需要的玻璃仪器有:量筒、烧杯、胶头滴管、 、 。
(3)配制该“生理盐水”时,正确的操作顺序是 (填字母) ④ 110 2 3:1
①用量筒量取适量的 1.5 mol·L-1 氯化钠溶液
(4)实验③中反应物物质的量配比为 。
②在烧杯中加入适量水稀释
(5)反应 I 中 TiO2+浓度对 TiO 的产率和粒径的影响如图。结合图中信息,你认为为达到工艺目的,最合
2
③继续往容量瓶内小心加水,直到液面接近刻度 1~2 cm 处 适的 TiO2+浓度为 。
④将容量瓶盖紧,反复上下颠倒,摇匀,装入贴有标签的试剂瓶
⑤将烧杯中的溶液沿玻璃棒注入容量瓶中
⑥改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切
⑦用少量蒸馏水洗涤烧杯 2~3 次,洗涤液均注入容量瓶,振荡
A. ①②⑤⑦③④⑥
B.①②⑤⑦③⑥④
C.②①⑤⑦③⑥④
(4)下列操作将导致所配溶液的浓度偏大的是 (填字母)
A.配制前容量瓶中有少量水
B. 用量筒量取氯化钠溶液时仰视刻度线
C.定容时,俯视读数
D.转移时有少量液体溅出
E.定容时,加水超过刻度线
(5)若出现(4)中 E 选项所表示的情况时,该如何处理? 。
18.(14 分)纳米 TiO 具有十分宝贵的光学性质,在汽车工业乃诸多领域都显示出美好的发展前景。如图是
2
以硫酸氧钛为原料制备纳米二氧化钛的工艺流程图:
回答下列问题:
试题 第 5 页(共 8 页) 试题 第 6 页(共 8 页)