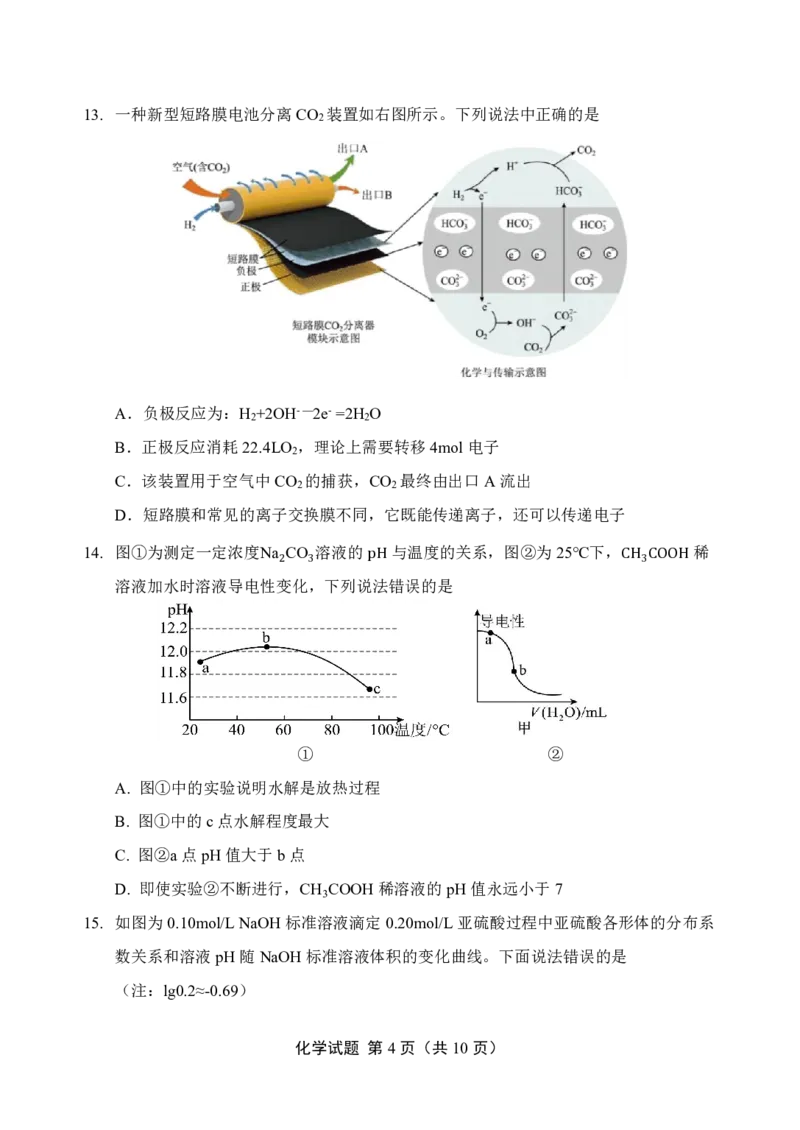
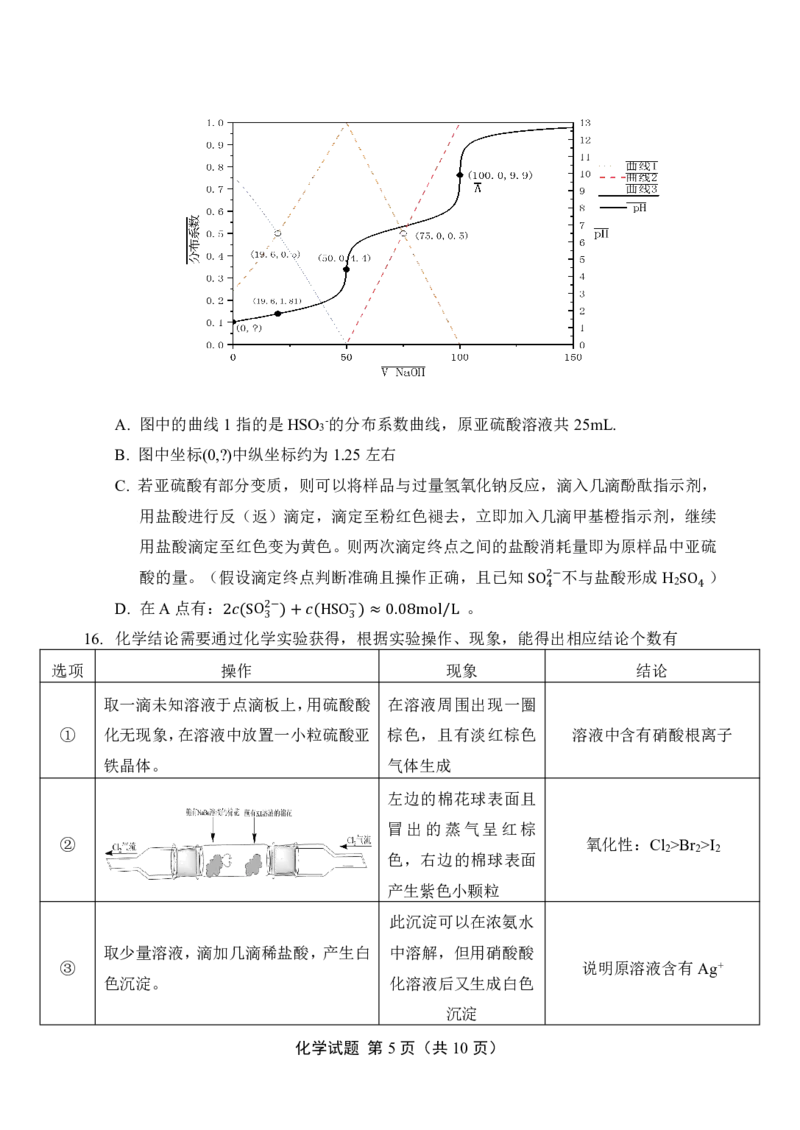
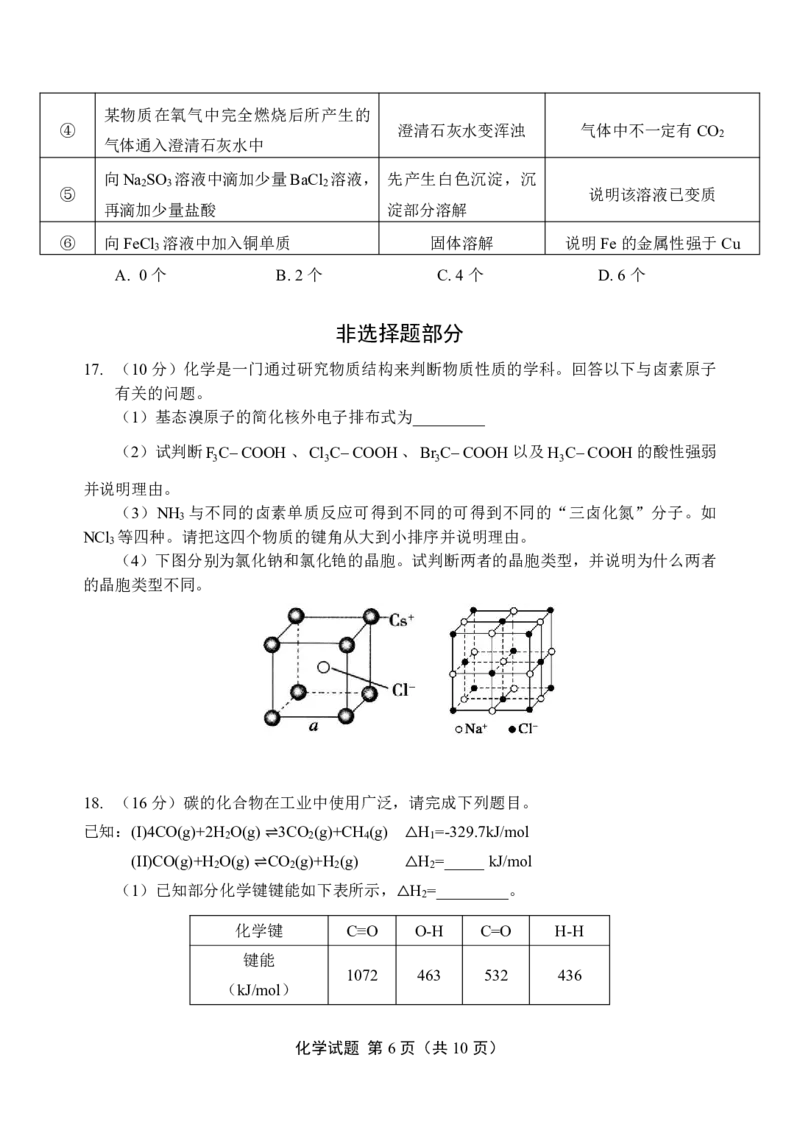
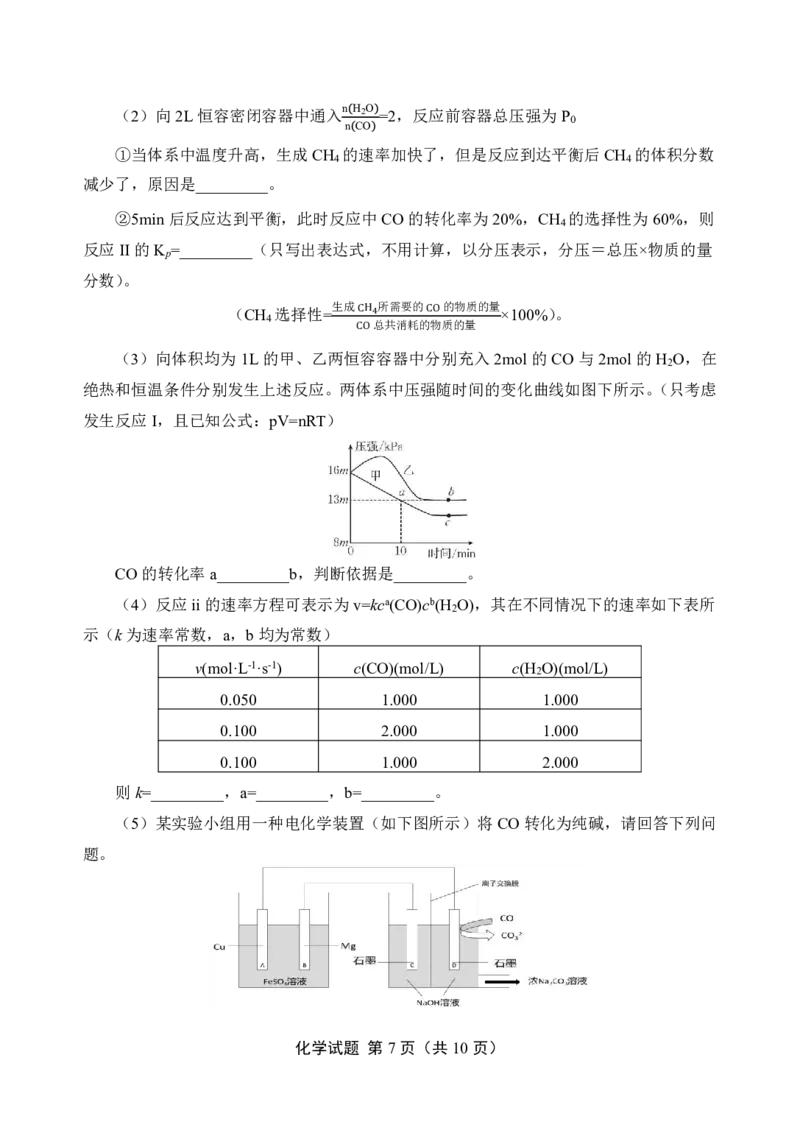
文档内容
机密★启用前
言蹊联考 2026 届新高三毕业班适应性检测
化学试题卷
2025.8
【命题人:鸣同学 zy小朋友 蔡蔡 水蓝蓝sama 张巍
审题人:隰有荷华 君喻 神阳 immediately】
注意事项:
1. 考生领到试题卷、答题卡后,请仔细核对试题卷、答题卡是否为当堂考试科目;检
1. 查无误后,请务必在规定区域内填写本人的姓名、准考证号。
2. 回答选择题时,在选出每小题答案后,需用2B铅笔将答题卡上对应的字母涂黑。
1. 改动时,清除已有答案后再选涂其他答案标号。回答非选择题时,须将答案写在答
1. 题卡上。写在试题卷、草稿纸上无效。
3. 试结束后答题卡需在规定时间内统一上传。后续发布统一渠道查阅个人成绩。
选择题部分
1. 中华典籍记载着先人对物质变化的深刻观察,如《考工记》言‘金锡美,火齐得’,道出
了合金冶炼的奥秘。古诗文中亦常暗含化学之理,或述物质转化,或言性质变迁。请
结合化学知识,下面对古诗文解释有错误的是
A. 《淮南万毕术》中“曾青涂铁,铁赤如铜”,指的是硫酸铜与铁反应得到金属铜。
A. 这说明铁的金属性强于铜。
B. 刘禹锡《浪淘沙》:“千淘万漉虽辛苦,吹尽狂沙始到金”,这说明自然界中部分金
B..属的提纯(如金)只发生物理变化。
C. 成语“水滴石穿”可以用来比喻一个人的恒心和毅力。其中水滴石穿的过程只发生
C. 物理变化。
D. 李商隐《无题》:“春蚕到死丝方尽,蜡炬成灰泪始干”其中发生了氧化还原反应。
2. 下列化学用语正确的是
A. 基态Cr原子的价层电子排布式:3d54s1
B. 二氧化硅的分子式:SiO
2
C. 硫化铜的化学式:Cu S
2
D. 碳的气态氢化物的空间填充模型:
化学试题 第1.页(共10.页)3. 下面四个选项中水解成酸性的盐是
A.NH I B.Na[Al(OH) ] C.C H OH D.NaHSO
4 4 2 5 3
4. 室温下,下列关于离子共存或离子反应的说法正确的是
A..0.1mol/LNaAlO 溶液中能大量存在:Fe3+、H+、Cl—、SO 2-
2 4
B. 向Ba(OH) 溶液中滴加NaHSO 溶液至溶液显中性:
2 4
..Ba2++2OH-+2H++SO 2-=BaSO +2H O
4 4 2
C. pH<7的溶液中能大量存在:Ca2+、Cu2+、SO 2-、Cl—
4
D. 由水电离出的c(H+)=1.0×10-12mol·L-1的溶液中能大量存在:NH +、Na+、SO 2-、Cl-
4 3
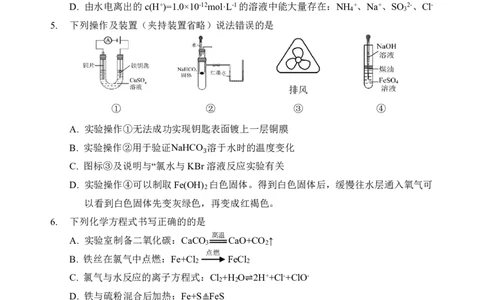
5. 下列操作及装置(夹持装置省略)说法错误的是
排风
① ② ③ ④
A. 实验操作①无法成功实现钥匙表面镀上一层铜膜
B. 实验操作②用于验证NaHCO 溶于水时的温度变化
C. 图标③及说明与“氯水与KBr3溶液反应实验有关
D. 实验操作④可以制取Fe(OH) 白色固体。得到白色固体后,缓慢往水层通入氧气可
2
..以看到白色固体先变灰绿色,再变成红褐色。
6. 下列化学方程式书写正确的的是
高温
A. 实验室制备二氧化碳:CaCO CaO+CO ↑
3 2
点燃
B. 铁丝在氯气中点燃:Fe+Cl FeCl
2 2
C. 氯气与水反应的离子方程式:Cl +H O 2H++Cl-+ClO-
2 2
D. 铁与硫粉混合后加热:Fe+S FeS ⇌
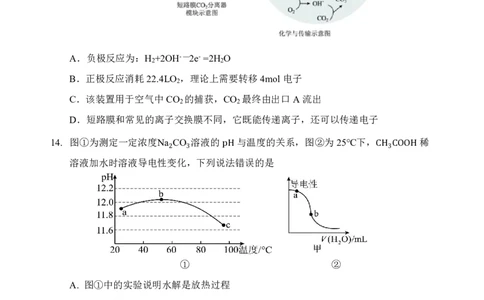
7. 2024年诺贝尔生理学或医学奖授 ≜ 予两位科学家,以表彰他们对于microRNA(微量核
糖核酸)及其在转录后基因调控中的作用的探索。尿嘧啶是RNA中的一种碱基,其结
构简式如右图所示,下列说法正确的是
A. 该物质不存在同分异构体是芳香化合物
B. 该物质所有原子均可在同一平面上
C.1mol该物质最多与3mol氢氧化钠溶液反应
D. 该物质中碳原子杂化方式有两种
化学试题 第2.页(共10.页)8. 某消炎药主要成分X中的组成元素是:A、B、C、D、E、F,这六种元素均为原子序
数依次增大的短周期元素,A是相对原子质量最小的元素,B的最外层原子是次外层
原子2倍,B、C、D、E同周期,E与F同主族,下列说法正确的是
A. 简单氢化物稳定性:BBr >I
2 2 2
色,右边的棉球表面
产生紫色小颗粒
此沉淀可以在浓氨水
取少量溶液,滴加几滴稀盐酸,产生白 中溶解,但用硝酸酸
③ 说明原溶液含有Ag+
色沉淀。 化溶液后又生成白色
沉淀
化学试题 第5.页(共10.页)某物质在氧气中完全燃烧后所产生的
④ 澄清石灰水变浑浊 气体中不一定有CO
2
气体通入澄清石灰水中
向Na SO 溶液中滴加少量BaCl 溶液, 先产生白色沉淀,沉
2 3 2
⑤ 说明该溶液已变质
再滴加少量盐酸 淀部分溶解
⑥ 向FeCl 溶液中加入铜单质 固体溶解 说明Fe的金属性强于Cu
3
A. 0个 B.2个 C.4个 D.6个
非选择题部分
17. (10分)化学是一门通过研究物质结构来判断物质性质的学科。回答以下与卤素原子
有关的问题。
(1)基态溴原子的简化核外电子排布式为_________
(2)试判断FCCOOH、Cl CCOOH、BrCCOOH以及H CCOOH的酸性强弱
3 3 3 3
并说明理由。
(3)NH 与不同的卤素单质反应可得到不同的可得到不同的“三卤化氮”分子。如
3
NCl 等四种。请把这四个物质的键角从大到小排序并说明理由。
3
(4)下图分别为氯化钠和氯化铯的晶胞。试判断两者的晶胞类型,并说明为什么两者
的晶胞类型不同。
18. (16分)碳的化合物在工业中使用广泛,请完成下列题目。
已知:(I)4CO(g)+2H O(g) 3CO (g)+CH (g) H =-329.7kJ/mol
2 2 4 1
(II)CO(g)+H O(g) CO (g)+H (g) H =_____kJ/mol
2 ⇌ 2 2 △ 2
(1)已知部分化学键键能如下表所示, H =_________。
⇌ △2
化学键 C≡O △ O-H C=O H-H
键能
1072 463 532 436
(kJ/mol)
化学试题 第6.页(共10.页)(2)向2L恒容密闭容器中通入n H2O =2,反应前容器总压强为P
0
n CO
①当体系中温度升高,生成CH 的速率加快了,但是反应到达平衡后CH 的体积分数
4 4
减少了,原因是_________。
②5min后反应达到平衡,此时反应中CO的转化率为20%,CH 的选择性为60%,则
4
反应II的K =_________(只写出表达式,不用计算,以分压表示,分压=总压×物质的量
p
分数)。
生成 所需要的 的物质的量
(CH 选择性= ×100%)。
4
总共消耗的物质的量
CH4 CO
CO
(3)向体积均为1L的甲、乙两恒容容器中分别充入2mol的CO与2mol的H O,在
2
绝热和恒温条件分别发生上述反应。两体系中压强随时间的变化曲线如图下所示。(只考虑
发生反应I,且已知公式:pV=nRT)
CO的转化率a_________b,判断依据是_________。
(4)反应ii的速率方程可表示为v=kca(CO)cb(H O),其在不同情况下的速率如下表所
2
示(k为速率常数,a,b均为常数)
v(mol·L-1·s-1) c(CO)(mol/L) c(H O)(mol/L)
2
0.050 1.000 1.000
0.100 2.000 1.000
0.100 1.000 2.000
则k=_________,a=_________,b=_________。
(5)某实验小组用一种电化学装置(如下图所示)将CO转化为纯碱,请回答下列问
题。
化学试题 第7.页(共10.页)①右池中的交换膜可能是_________。
①A. 阳离子交换膜 B. 阴离子交换膜
②写出D电极的电极方程式_________。
③A电极质量增加11.2g,理论上可以制备出_________gNa CO 溶液(忽略CO 2-水解)。
2 3 3
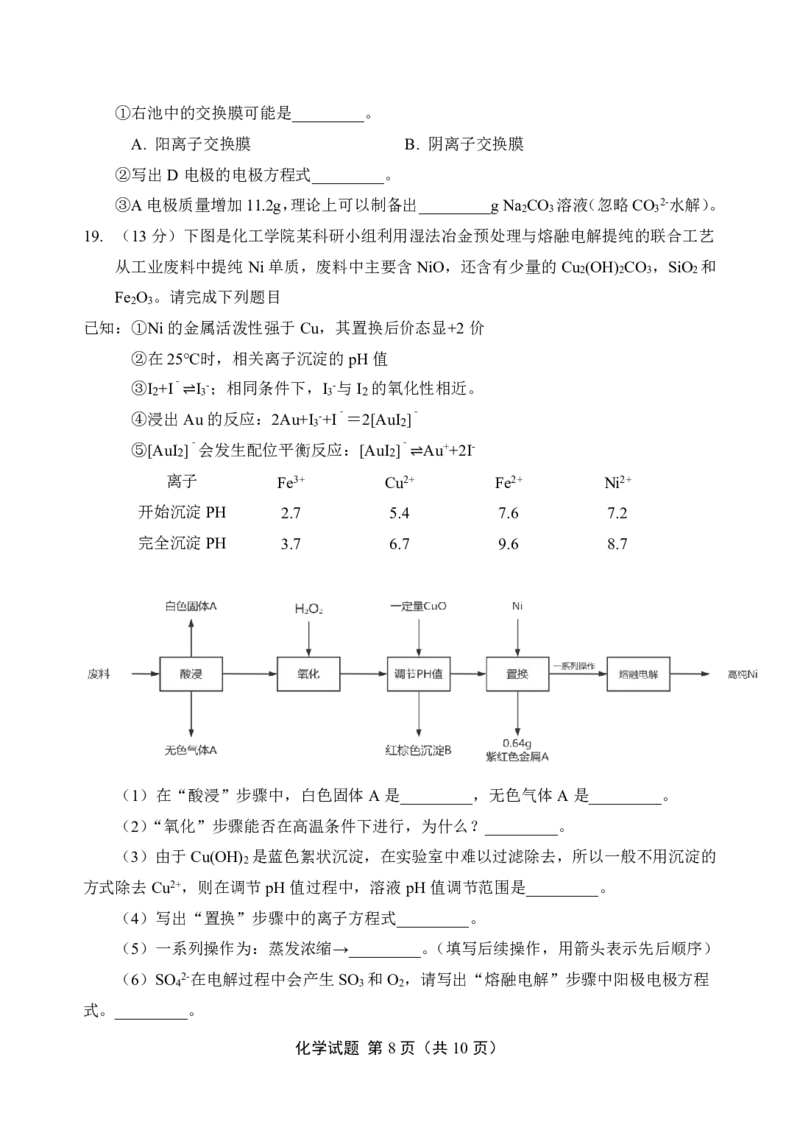
19. (13分)下图是化工学院某科研小组利用湿法冶金预处理与熔融电解提纯的联合工艺
从工业废料中提纯Ni单质,废料中主要含NiO,还含有少量的Cu (OH) CO ,SiO 和
2 2 3 2
Fe O 。请完成下列题目
2 3
已知:①Ni的金属活泼性强于Cu,其置换后价态显+2价
②在25℃时,相关离子沉淀的pH值
③I2+I ﹣ I
3
-;相同条件下,I
3
-与I2 的氧化性相近。
④浸出 ⇌Au的反应:2Au+I
3
-+I ﹣=2[AuI2] ﹣
⑤[AuI2] ﹣会发生配位平衡反应:[AuI2] ﹣ Au++2I-
离子 Fe3+ Cu2+⇌ Fe2+ Ni2+
开始沉淀PH 2.7 5.4 7.6 7.2
完全沉淀PH 3.7 6.7 9.6 8.7
(1)在“酸浸”步骤中,白色固体A是_________,无色气体A是_________。
(2)“氧化”步骤能否在高温条件下进行,为什么?_________。
(3)由于Cu(OH) 是蓝色絮状沉淀,在实验室中难以过滤除去,所以一般不用沉淀的
2
方式除去Cu2+,则在调节pH值过程中,溶液pH值调节范围是_________。
(4)写出“置换”步骤中的离子方程式_________。
(5)一系列操作为:蒸发浓缩→_________。(填写后续操作,用箭头表示先后顺序)
(6)SO 2-在电解过程中会产生SO 和O ,请写出“熔融电解”步骤中阳极电极方程
4 3 2
式。_________。
化学试题 第8.页(共10.页)(7)湿法冶金预处理法(方法一)与熔融电解提纯(方法二)在黄金提取中也有广泛
用途,化工学院某科研小组通过类比和探究,从上述流程的工艺中,研发了从电子废料(含
Cu和Au单质)中回收Au单质,发现了如下图所示的方法
①浸取一定时间后,应及时过滤,否则会降低金的浸出率,原因是_________。
②饱和碘水不能单独浸出Au,但是I2 ﹣KI溶液可以浸出Au,原因有:
i.I2 在KI溶液中的溶解度大,体系的氧化性强;
ii._________。
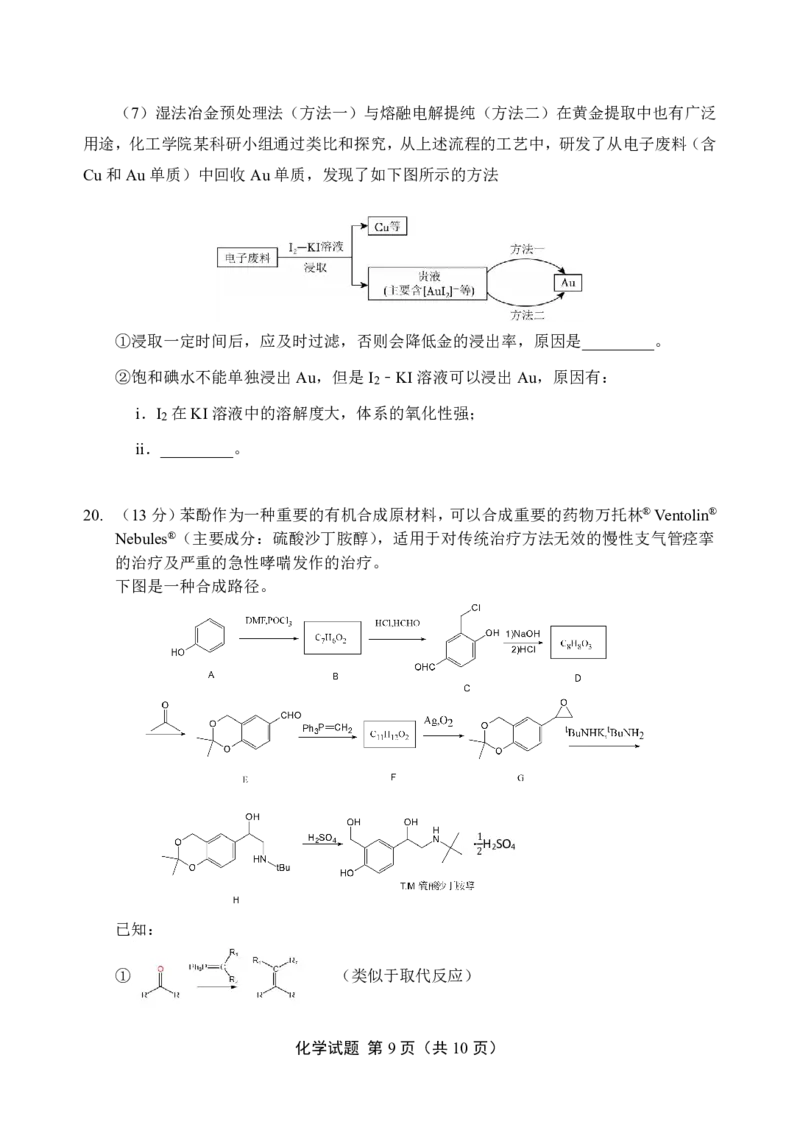
20. (13分)苯酚作为一种重要的有机合成原材料,可以合成重要的药物万托林®Ventolin®
Nebules®(主要成分:硫酸沙丁胺醇),适用于对传统治疗方法无效的慢性支气管痉挛
的治疗及严重的急性哮喘发作的治疗。
下图是一种合成路径。
· H 2 SO 4
1
2
已知:
① (类似于取代反应)
化学试题 第9.页(共10.页)②
③苯环与DMF、三氯氧磷反应,在对位取代一个基团。这个基团可以发生银镜反应。
(1)下面选项正确的是
(1)A. 图中所有下面标有英文大写字母的有机物均可以使三氯化铁溶液变色
(1)B. 从C生成D的反应类型是消去反应
(1)C. 最终得到的产物是一种盐,这种盐可以溶于水
(1)D. 从E变为F,分子式相比较,少了一个氧原子,多了1个碳原子,2个氢原子。
(2)化合物B的结构简式是_________。
(3)写出E→F的化学方程式:_________。
(4)步骤D→E的目的是_________。
(5)写出符合要求的D的同分异构体_________(三种,多写的根据前三个给分)。
..①分子中含有一个苯环
..②1H-NMR谱图有四组峰,面积比为1:2:2:3
..③不能与碳酸氢钠溶液反应
(6)利用图中所给信息,以苯酚为原料,合成 ,无机与有机试剂任选。
化学试题 第10.页(共10.页)