文档内容
2025-2026 学年(上)高三年级顶尖计划(一)
化学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将考生号条形
码粘贴在答题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答
题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 0 16 Na 23 S 32 Fe 56 Br 80
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
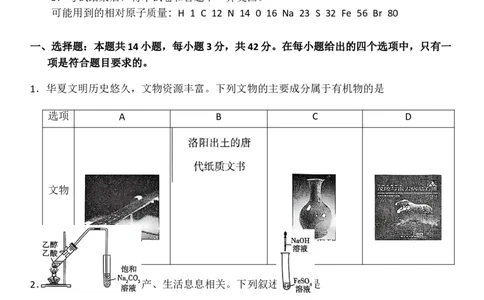
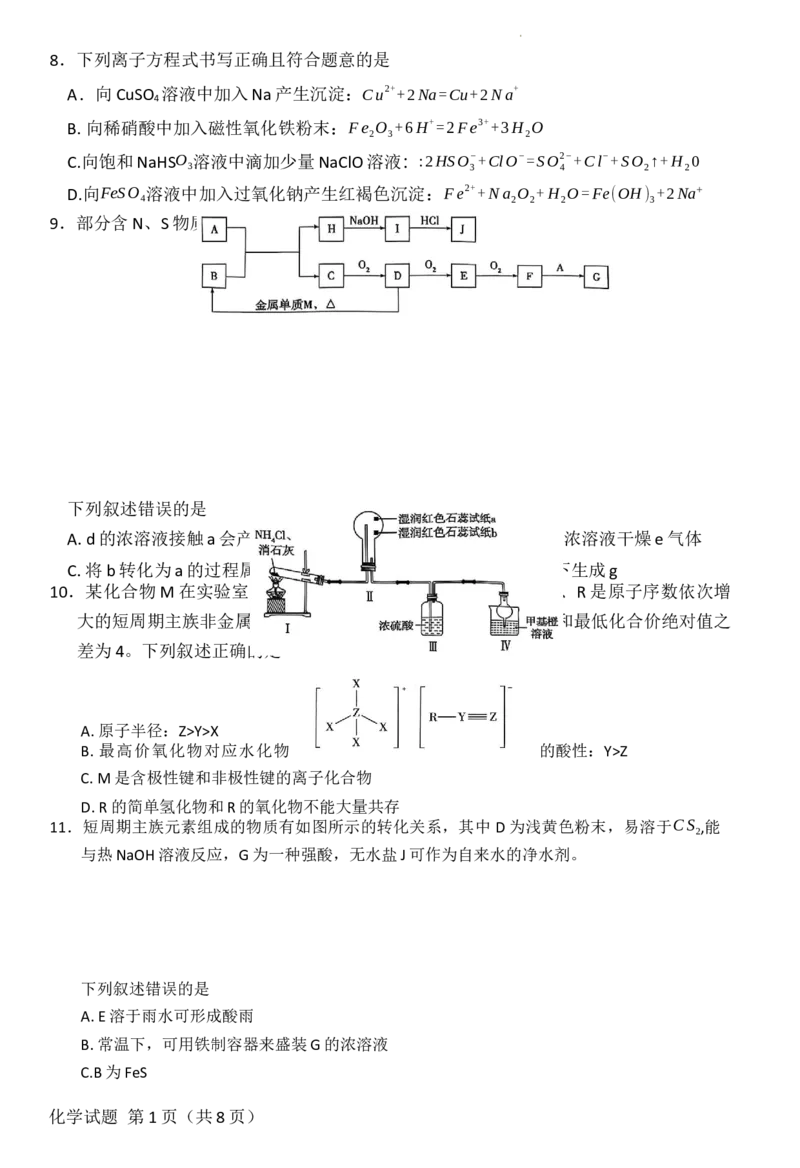
1.华夏文明历史悠久,文物资源丰富。下列文物的主要成分属于有机物的是
选项 A B C D
文物
秦始皇陵出土 北宋汝窑 茂陵霍去病墓
的青铜剑 天青釉瓷 前的石雕
2.有机高分子材料与生产、生活息息相关。下列叙述错误的是
A.聚乙烯由乙烯发生加聚反应合成,可用于药物等的包装材料
B.聚四氟乙烯(PTFE)可用于制造烧杯、坩埚等化学仪器
C.涤纶、芳纶等可用于制造“神舟”飞船航天服
D.天然橡胶的主要成分是聚异戊二烯,是一种纯净物
3.1934年H.R.克莱恩和C.C.劳伦斯首次报道制备了碳的放射性同位素碳-11❑ 11C),
6
在正电子发射断层显像技术中有着重要应用。已知碳元素相对原子质量为 12.01。下列
有关说法正确的是
A.❑ 11C的相对原子质量为12.01
6
化学试题 第1页(共8页)
学科网(北京)股份有限公司B.❑ 11C与❑ 14C互为同素异形体
6 6
C.❑ 13C发生衰变生成❑ 11C,发生的变化属于化学变化
6 6
D.碳元素最高价氧化物的空间结构为直线形
4.下列化学用语或图示错误的是
A.中子数为8的碳核素:❑ 14C
6
B.Na O 的 电 子 式:
2 2
C.NaCl固体溶于水形成的水合离子:
D.HCI的结构式:H-Cl
5.下列叙述正确的是
A.铁红呈红色,难溶于水,可用于制造红色颜料
B.二氧化硫有毒,在任何环境中二氧化硫都不能应用
C.纯碱属于碱,可用于去除油污
D.任何条件下,稀硫酸都能与铜发生反应生成硫酸铜
6.下列装置或操作能达到相应目的的是
A.制备乙酸乙酯 B.制备稳定的Fe(OH)2
C.比较Ni和Cu的金属性 D.证明Cl 和Cu反应
2
7.氮及其化合物的部分转化关系如图所示。设N 为阿伏加德罗常数的值。
A
下列说法正确的是
A.反应①每消耗2.24LN (标准状况),生成离子总数目为0.4N
2 A
B.反应②生成3.4g气态氢化物(全部逸出),消耗水分子数目为0.6N
A
C.1L0.2mol·L-1HNO 溶液中含HNO 分子数目为0.2N
3 3 A
D.反应④中产物还有H O和N ,反应④中1molN H NO 完全分解转移电子数目为1.5N
2 2 4 3 A
化学试题 第1页(共8页)
学科网(北京)股份有限公司8.下列离子方程式书写正确且符合题意的是
A.向CuSO 溶液中加入Na产生沉淀:Cu2++2Na=Cu+2Na+
4
B.向稀硝酸中加入磁性氧化铁粉末:Fe O +6H+=2Fe3++3H O
2 3 2
C.向饱和NaHSO 溶液中滴加少量NaClO溶液::2HSO−+ClO−=SO2−+Cl−+SO ↑+H 0
3 3 4 2 2
D.向FeSO 溶液中加入过氧化钠产生红褐色沉淀:Fe2++Na O +H O=Fe(OH) +2Na+
4 2 2 2 3
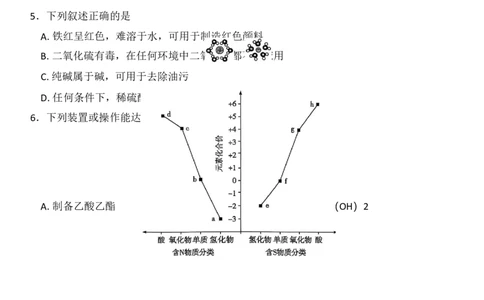
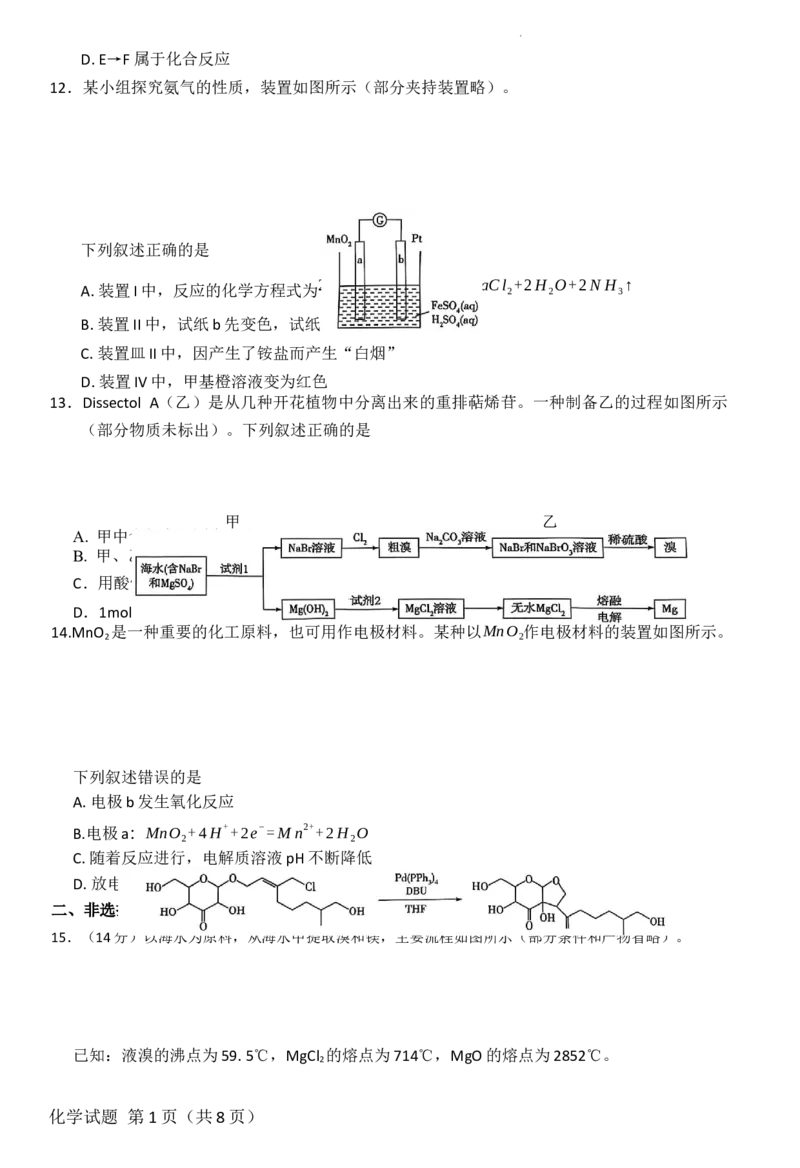
9.部分含N、S物质的“价-类”二维图如图所示。
下列叙述错误的是
A.d的浓溶液接触a会产生“白烟” B.实验室可以用h的浓溶液干燥e气体
C.将b转化为a的过程属于氮的固定 D.f与O 在点燃条件下生成g
2
10.某化合物M在实验室有广泛应用,其结构如图所示。X、Y、Z、R是原子序数依次增
大的短周期主族非金属元素。Y和Z位于同周期,R最高化合价和最低化合价绝对值之
差为4。下列叙述正确的是
A.原子半径:Z>Y>X
B.最高价氧化物对应水化物 的酸性:Y>Z
C.M是含极性键和非极性键的离子化合物
D.R的简单氢化物和R的氧化物不能大量共存
11.短周期主族元素组成的物质有如图所示的转化关系,其中 D为浅黄色粉末,易溶于CS ,能
2
与热NaOH溶液反应,G为一种强酸,无水盐J可作为自来水的净水剂。
下列叙述错误的是
A.E溶于雨水可形成酸雨
B.常温下,可用铁制容器来盛装G的浓溶液
C.B为FeS
化学试题 第1页(共8页)
学科网(北京)股份有限公司D.E→F属于化合反应
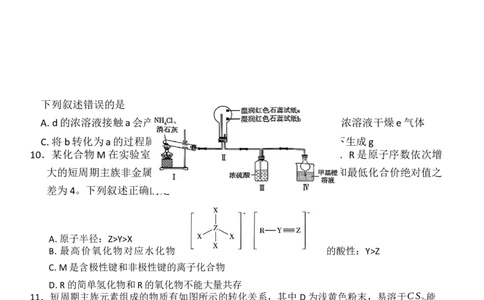
12.某小组探究氨气的性质,装置如图所示(部分夹持装置略)。
下列叙述正确的是
A.装置I中,反应的化学方程式为
2N H
4
Cl+Ca(OH)
2
∆CaCl
2
+2H
2
O+2N H
3
↑
→
B.装置II中,试纸b先变色,试纸a后变色
C.装置皿II中,因产生了铵盐而产生“白烟”
D.装置IV中,甲基橙溶液变为红色
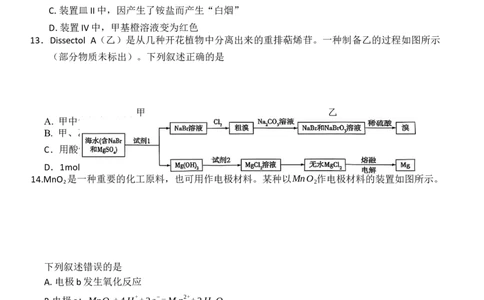
13.Dissectol A(乙)是从几种开花植物中分离出来的重排萜烯苷。一种制备乙的过程如图所示
(部分物质未标出)。下列叙述正确的是
甲 乙
A. 甲中含氧官能团有5种
B. 甲、乙均属于烃
C.用酸性KMnO 溶液可检验乙中的碳碳双键
4
D.1mol甲与足量钠反应能生成2molH
2
14.MnO 是一种重要的化工原料,也可用作电极材料。某种以MnO 作电极材料的装置如图所示。
2 2
下列叙述错误的是
A.电极b发生氧化反应
B.电极a:MnO +4H++2e−=Mn2++2H O
2 2
C.随着反应进行,电解质溶液pH不断降低
D.放电时,电子由电极b经外电路流向电极a
二、非选择题:本题共4小题,共58分。
15.(14分)以海水为原料,从海水中提取溴和镁,主要流程如图所示(部分条件和产物省略)。
已知:液溴的沸点为59.5℃,MgCl 的熔点为714℃,MgO的熔点为2852℃。
2
化学试题 第1页(共8页)
学科网(北京)股份有限公司回答下列问题:
(1)从产品来源和成本角度考虑,试剂1宜选择 (填字母)。
A.氨水 B.生石灰 C.NaOH
(2)上述提溴流程中,运用了元素周期律的事实是 (用
离子方程式表示)。
( 3 ) 用 Na CO 溶 液 吸 收 粗 溴 , 还 有 CO 生 成 , 其 离 子 方 程 式 为
2 3 2
。NaBr和NaBrO 反应制备Br ,氧化产物与还原产物的质量之比为 。
3 2
(4)如果上述流程中得到的粗溴中含少量Cl ,提纯溴的方法是 。
2
(5)制备无水 MgCl 分两步:第一步,采用结晶法提取 MgCl ⋅6H O;第二步,
2 2 2
MgCl ⋅6H O 和足量 SOCl 混合加热得到MgCl 。,写出第二步反应的化学方程式:
2 2 2 2
。
(6)工业上选择电解熔融MgCl 制备镁,而不选择 MgO,其主要原因是
2
。
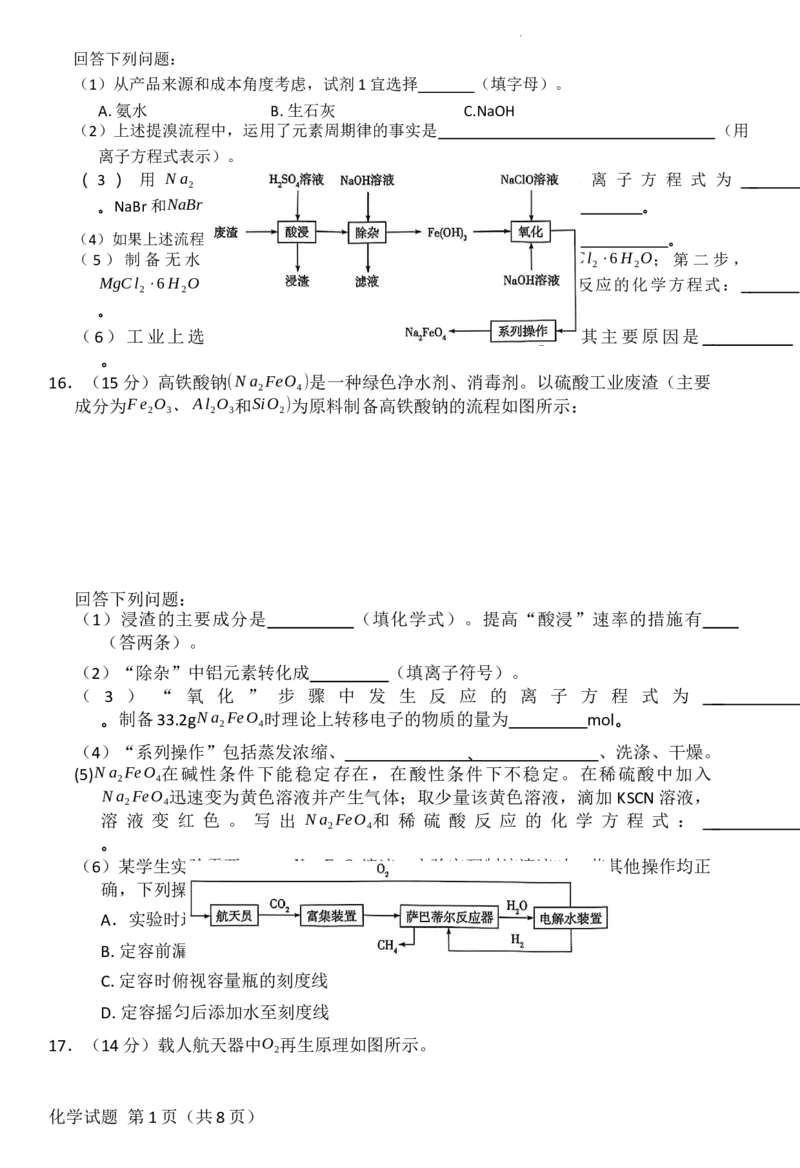
16.(15分)高铁酸钠(Na FeO )是一种绿色净水剂、消毒剂。以硫酸工业废渣(主要
2 4
成分为Fe O 、Al O 和SiO )为原料制备高铁酸钠的流程如图所示:
2 3 2 3 2
回答下列问题:
(1)浸渣的主要成分是 (填化学式)。提高“酸浸”速率的措施有
(答两条)。
(2)“除杂”中铝元素转化成 (填离子符号)。
( 3 ) “ 氧 化 ” 步 骤 中 发 生 反 应 的 离 子 方 程 式 为
。制备33.2gNa FeO 时理论上转移电子的物质的量为 mol。
2 4
(4)“系列操作”包括蒸发浓缩、 、 、洗涤、干燥。
(5)Na FeO 在碱性条件下能稳定存在,在酸性条件下不稳定。在稀硫酸中加入
2 4
Na FeO 迅速变为黄色溶液并产生气体;取少量该黄色溶液,滴加 KSCN溶液,
2 4
溶 液 变 红 色 。 写 出 Na FeO 和 稀 硫 酸 反 应 的 化 学 方 程 式 :
2 4
。
(6)某学生实验需要950mLNa FeO 溶液,实验室配制该溶液时,若其他操作均正
2 4
确,下列操作会使配制溶液浓度偏高的是 (填字母)。
A.实验时选择1000mL容量瓶
B.定容前漏掉“洗涤”步骤
C.定容时俯视容量瓶的刻度线
D.定容摇匀后添加水至刻度线
17.(14分)载人航天器中O 再生原理如图所示。
2
化学试题 第1页(共8页)
学科网(北京)股份有限公司i.CO (g)+4H (g)⇌CH (g)+2H O(g)(萨巴蒂尔反应)
2 2 4 2
ii.CO (g)+H (g)⇌CO(g)+H O(g)
2 2 2
回答下列问题:
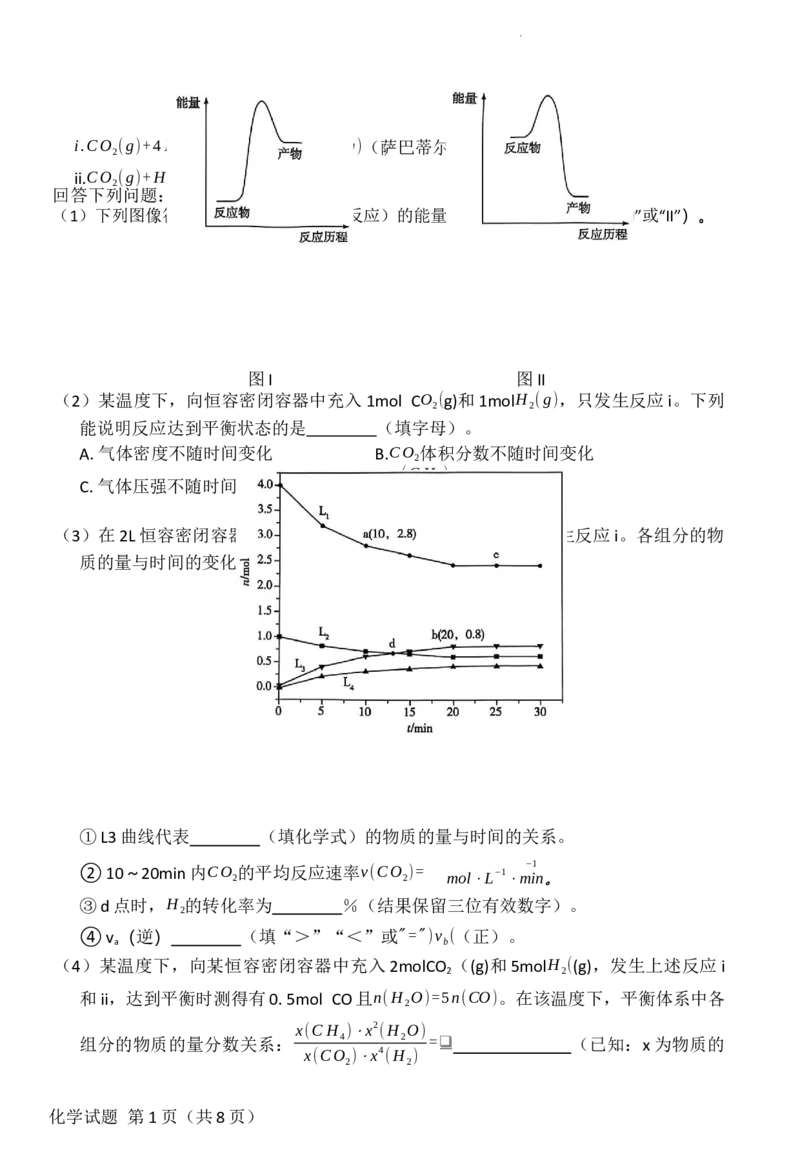
(1)下列图像符合萨巴蒂尔反应(放热反应)的能量变化的是图 (填“I”或“II”)。
图I 图II
(2)某温度下,向恒容密闭容器中充入 1mol CO (g)和1molH (g),只发生反应i。下列
2 2
能说明反应达到平衡状态的是 (填字母)。
A.气体密度不随时间变化 B.CO 体积分数不随时间变化
2
n(CH )
C.气体压强不随时间变化 D. 4 不随时间变化
n(H O)
2
(3)在2L恒容密闭容器中充入 1molCO ((g)和4 molH (g),只发生反应 i。各组分的物
2 2
质的量与时间的变化关系如图所示。
①L3曲线代表 (填化学式)的物质的量与时间的关系。
②10~20min内CO 2 的平均反应速率v(CO 2 )= mol⋅L−1 ⋅m − i 1 n。
③d点时,H 的转化率为 %(结果保留三位有效数字)。
2
④v (逆) (填“>”“<”或"=")v ((正)。
a b
(4)某温度下,向某恒容密闭容器中充入2molCO ((g)和5molH ((g),发生上述反应 i
2 2
和ii,达到平衡时测得有0.5mol CO且n(H O)=5n(CO)。在该温度下,平衡体系中各
2
x(CH )⋅x2 (H O)
组分的物质的量分数关系: 4 2 =❑ (已知:x为物质的
x(CO )⋅x4 (H )
2 2
化学试题 第1页(共8页)
学科网(北京)股份有限公司量分数)。
(5)上述产生的CH 可设计如图所示的燃料电池(电解质为熔融K CO )。
4 2 3
写出电极b的反应式: 。
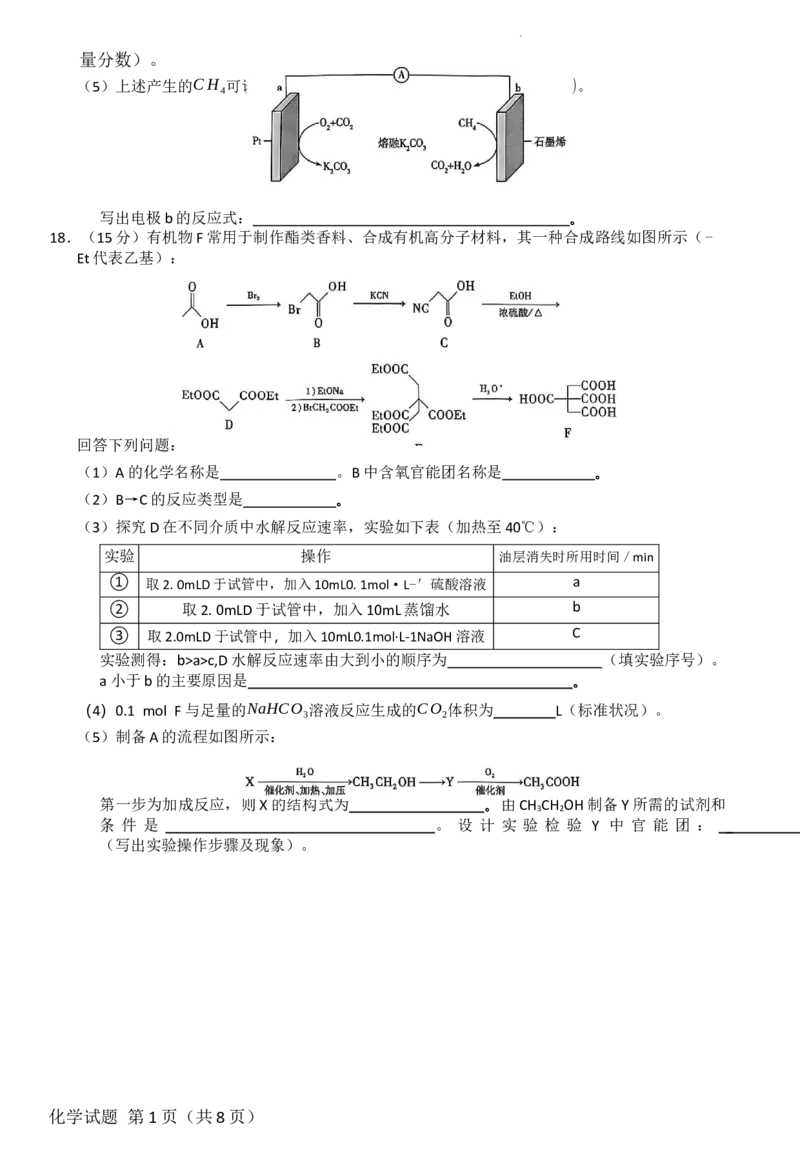
18.(15分)有机物F常用于制作酯类香料、合成有机高分子材料,其一种合成路线如图所示(-
Et代表乙基):
E
回答下列问题:
(1)A的化学名称是 。B中含氧官能团名称是 。
(2)B→C的反应类型是 。
(3)探究D在不同介质中水解反应速率,实验如下表(加热至40℃):
实验 操作 油层消失时所用时间/min
① 取2.0mLD于试管中,加入10mL0.1mol·L-'硫酸溶液 a
② 取2.0mLD于试管中,加入10mL蒸馏水 b
③ 取2.0mLD于试管中,加入10mL0.1mol·L-1NaOH溶液 C
实验测得:b>a>c,D水解反应速率由大到小的顺序为 (填实验序号)。
a小于b的主要原因是 。
(4)0.1 mol F与足量的NaHCO 溶液反应生成的CO 体积为 L(标准状况)。
3 2
(5)制备A的流程如图所示:
第一步为加成反应,则X的结构式为 。由CH CH OH制备Y所需的试剂和
3 2
条 件 是 。 设 计 实 验 检 验 Y 中 官 能 团 :
(写出实验操作步骤及现象)。
化学试题 第1页(共8页)
学科网(北京)股份有限公司