文档内容
2025-2026 学年高二年级化学上学期第一次月考卷 C.灼烧海带制海带灰 D.测定中和反应的反应热
75 100
(考试时间: 分钟 试卷满分: 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
4.对于反应 2SO (g)+O (g) 2SO (g) ΔH<0,下列说法正确的是
2 2 3
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
A.缩小体积使压强增大,增大了单位体积内活化分子的数目,但活化分子百分数不变
~第二章第二节(人教版 2019)
4.测试范围:第一章 。
B.增加氧气的浓度,能够增大活化分子百分数
65
5.难度系数:0.
C.只要选择适宜的条件,SO 和 O 就能全部转化为 SO
2 2 3
6.考试结束后,将本试卷和答题卡一并交回。
D.加入催化剂能加快反应速率,提高 SO 的平衡转化率
2
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39
5.下列依据热化学方程式得出的结论正确的是
Ca-40 Ti-48 Cr-52 Fe-56 Ni-59 Cu-64 Ba-137
A.正丁烷 异丁烷 ,则正丁烷比异丁烷稳定
第Ⅰ卷(选择题 共 45 分) B. ,则 的燃烧热为
一、选择题:本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合题目 C. ,则稀 和稀 完全反应生成
要求的。
时,放出 热量
1.化学与人类生产、生活密切相关,下列有关说法不正确的是
D. ; ,则
A.新冠病毒可用次氯酸钠溶液或双氧水消毒,其消毒原理不同
6.下列有关图像说法错误的是
B.燃煤中加入生石灰可以减少二氧化硫气体的排放
C.碳酸钠可用于去除餐具的油污,是因为碳酸钠溶液水解显碱性
D.“自嗨锅”加热食物是利用了化学反应的热效应
2.化学反应速率的调控被广泛应用于生活、生产中。下列操作可减慢化学反应速率的是
A.工业制硫酸时采用 400~500℃高温 B.向炉膛内鼓风可以使炉火更旺
C.用冰箱冷藏保鲜食物 D.工业合成氨使用催化剂
3.实验是学习化学的重要途径。下列实验操作对应的装置不正确的是 A.图①阴影部分面积表示反应物浓度的净减少量
A.配制一定浓度的 溶液 B.准确量取 稀盐酸
B.图②:等质量的石墨和金刚石完全燃烧释放的热量:石墨<金刚石
C.图③为可逆反应的物质的量—时间图,参与反应的各物质均为气体,化学反应方程式为
D.图④中装置实现了化学能转变为电能
7.下列事实中,能用勒夏特列原理解释的个数为
①夏天,打开啤酒瓶时会从瓶口逸出大量气体
②浓氨水中加入氢氧化钠固体时产生较多有刺激性气味的气体
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)③实验室可用排饱和食盐水的方法收集氯气
取 2mL0.5mol/LCuCl 溶液于试管中,加 反应[Cu(H O)]2++4Cl
C 2 加热后溶液变为黄绿色 2
④将盛有 和 混合气体的密闭容器置于冷水中,混合气体的颜色变浅 热 [CuCl ]2-+4H O 的△H>0
4 2
⑤对于 2HI(g) H (g)+I (g),达到平衡后,缩小容器容积可使体系颜色变深
2 2 减小生成物的浓度,平衡向正反
D K Cr O 溶液中滴加 NaOH 溶液 溶液由黄色变为橙色
2 2 7
A.2 B.5 C.4 D.3 应方向移动
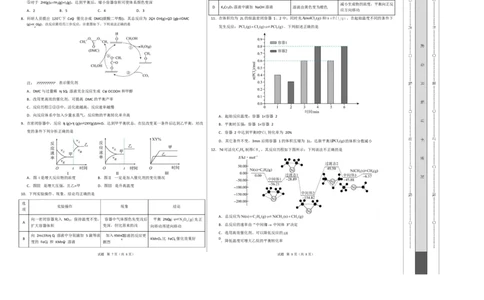
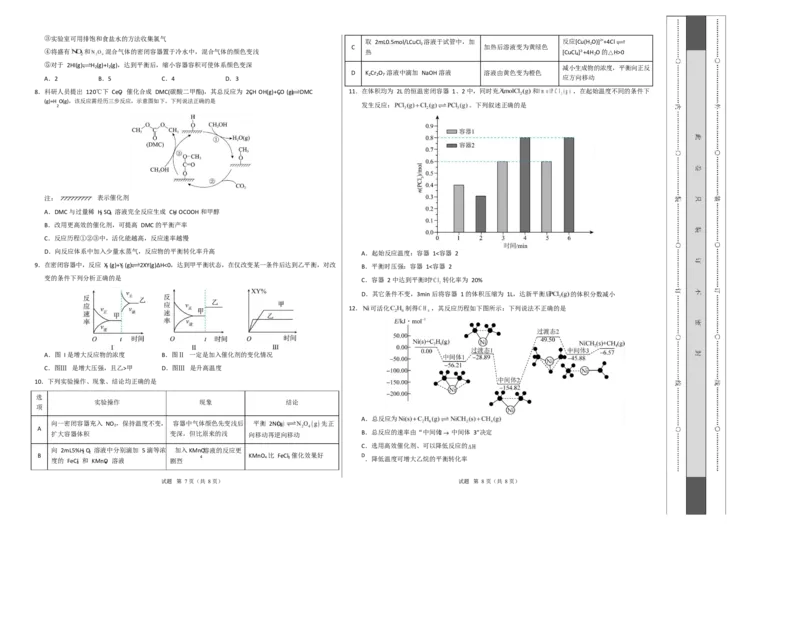
8.科研人员提出 120℃下 CeO 催化合成 DMC(碳酸二甲酯),其总反应为 2CH OH(g)+CO (g) DMC 11.在体积均为 2L 的恒温密闭容器 1、2 中,同时充入 和 ,在起始温度不同的条件下
2 3 2
(g)+H O(g),该反应需经历三步反应,示意图如下。下列说法正确的是
发生反应: 。下列叙述正确的是
2
注: 表示催化剂
A.DMC 与过量稀 H SO 溶液完全反应生成 CH OCOOH 和甲醇
2 4 3
B.改用更高效的催化剂,可提高 DMC 的平衡产率
C.反应历程①②③中,活化能越高,反应速率越慢
D.向反应体系中加入少量水蒸气,反应物的平衡转化率升高 A.起始反应温度:容器 1<容器 2
9.在密闭容器中,反应 X 2 (g)+Y 2 (g) 2XY(g)ΔH<0,达到甲平衡状态,在仅改变某一条件后达到乙平衡,对改 B.平衡时压强:容器 1<容器 2
变的条件下列分析正确的是
C.容器 2 中达到平衡时 转化率为 20%
D.其它条件不变,3min 后将容器 1 的体积压缩为 1L,达新平衡后 的体积分数减小
12. 可活化 制得 ,其反应历程如下图所示:下列说法不正确的是
A.图 I 是增大反应物的浓度 B.图Ⅱ 一定是加入催化剂的变化情况
C.图Ⅲ 是增大压强,且乙>甲 D.图Ⅲ 是升高温度
10.下列实验操作、现象、结论均正确的是
选
实验操作 现象 结论
项
A.总反应为
向一密闭容器充入 NO ,保持温度不变, 容器中气体颜色先变浅后 平衡 2NO 先正
2 2
A
扩大容器体积 变深,但比原来的浅 向移动再逆向移动 B.总反应的速率由“中间体 中间体 3”决定
C.选用高效催化剂、可以降低反应的
向 2mL5%H O 溶液中分别滴加 5 滴等浓 加入KMnO溶液的反应更
2 2
B 度的 FeCl 和 KMnO 溶液 剧烈 4 KMnO 4 比 FeCl 3 催化效果好 D .降低温度可增大乙烷的平衡转化率
3 4
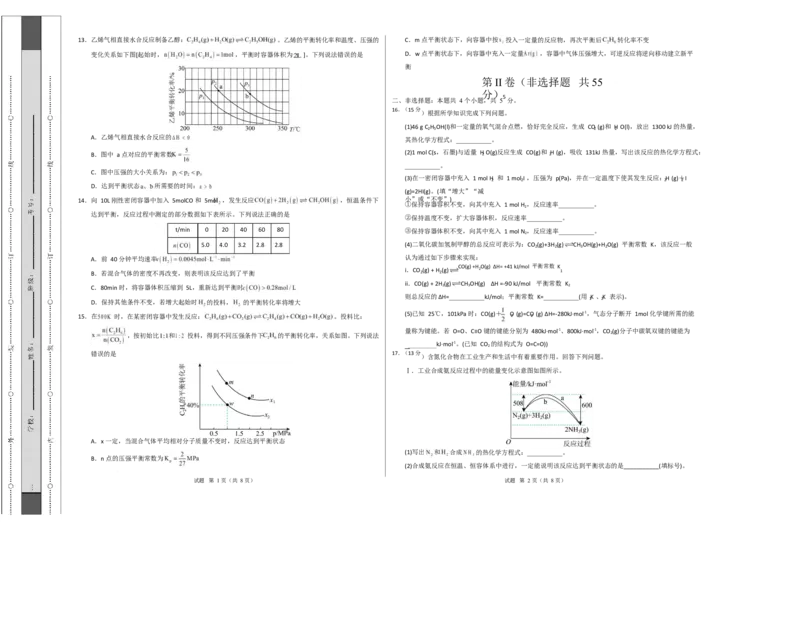
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)13.乙烯气相直接水合反应制备乙醇: 。乙烯的平衡转化率和温度、压强的 C.m 点平衡状态下,向容器中按 投入一定量的反应物,再次平衡后 转化率不变
变化关系如下图[起始时, ,平衡时容器体积为 ]。下列说法错误的是 D.w 点平衡状态下,向容器中充入一定量 ,容器中气体压强增大,可逆反应将逆向移动建立新平
衡
第 II 卷(非选择题 共 55
分)
5
二、非选择题:本题共 4 个小题,共 5 分。
16.(15 分
)根据所学知识完成下列问题。
(1)46 g C H OH(l)和一定量的氧气混合点燃,恰好完全反应,生成 CO (g)和 H O(l),放出 1300 kJ 的热量,
2 5 2 2
A.乙烯气相直接水合反应的
其热化学方程式:___________。
B.图中 a 点对应的平衡常数 (2)1 mol C(s,石墨)与适量 H 2 O(g)反应生成 CO(g)和 2 H (g),吸收 131kJ 热量,写出该反应的热化学方程式:
___________。
C.图中压强的大小关系为:
(3)在一密闭容器中充入 1 mol H 和 1 mol I ,压强为 p(Pa),并在一定温度下使其发生反应:H (g)+I
2 2 2 2
D.达到平衡状态 所需要的时间:
(g)=2HI(g)。(填“增大”“减
14.向 10L 刚性密闭容器中加入 5molCO 和 5mol ,发生反应 ,恒温条件下 小”或“不变”)
①保持容器容积不变,向其中充入 1 mol H ,反应速率___________。
2
达到平衡,反应过程中测定的部分数据如下表所示。下列说法正确的是
②保持温度不变,扩大容器体积,反应速率___________。
t/min 0 20 40 60 80 ③保持容器体积不变,向其中充入 1 mol N ,反应速率___________。
2
5.0 4.0 3.2 2.8 2.8 (4)二氧化碳加氢制甲醇的总反应可表示为:CO (g)+3H (g) CH OH(g)+H O(g) 平衡常数 K,该反应一般
2 2 3 2
A.前 40 分钟平均速率 认为通过如下步骤来实现:
CO(g) +H O(g) ΔH= +41 kJ/mol 平衡常数 K
B.若混合气体的密度不再改变,则表明该反应达到了平衡 i.CO 2 (g) + H 2 (g) 2 1
ii.CO(g) + 2H (g) CH OH(g) ΔH =-90 kJ/mol 平衡常数 K
C.80min 时,将容器体积压缩到 5L,重新达到平衡时 2 3 2
则总反应的ΔH=___________kJ/mol;平衡常数 K=___________(用 K 、K 表示)。
1 2
D.保持其他条件不变,若增大起始时 的投料, 的平衡转化率将增大
15.在 时,在某密闭容器中发生反应: 。投料比: (5)已知 25℃,101kPa 时:CO(g)+ O 2 (g)=CO 2 (g) ΔH=-280kJ·mol-1,气态分子断开 1mol 化学键所需的能
量称为键能。若 O=O、C≡O 键的键能分别为 480kJ·mol-1、800kJ·mol-1,CO (g)分子中碳氧双键的键能为
,按初始比 和 投料,得到不同压强条件下 的平衡转化率,关系如图。下列说法 2
_ __________kJ·mol-1。(已知 CO
2
的结构式为 O=C=O))
错误的是 17.(13 分
)含氮化合物在工业生产和生活中有着重要作用。回答下列问题。
Ⅰ.工业合成氨反应过程中的能量变化示意图如图所示。
A.x 一定,当混合气体平均相对分子质量不变时,反应达到平衡状态
(1)写出 和 合成 的热化学方程式:___________。
B.n 点的压强平衡常数为
(2)合成氨反应在恒温、恒容体系中进行,一定能说明该反应达到平衡状态的是___________(填标号)。
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)A. 、 、 的浓度之比为 1∶3∶2
B.单位时间内,消耗 amol 的同时生成 2amol
C.容器内气体的总压强保持不变
D.混合气体的密度保持不变
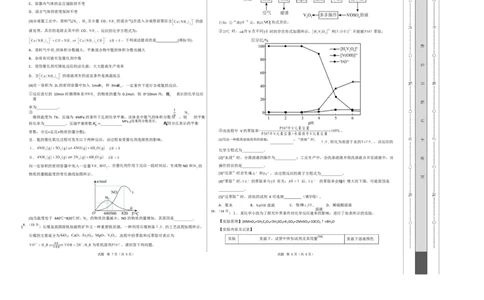
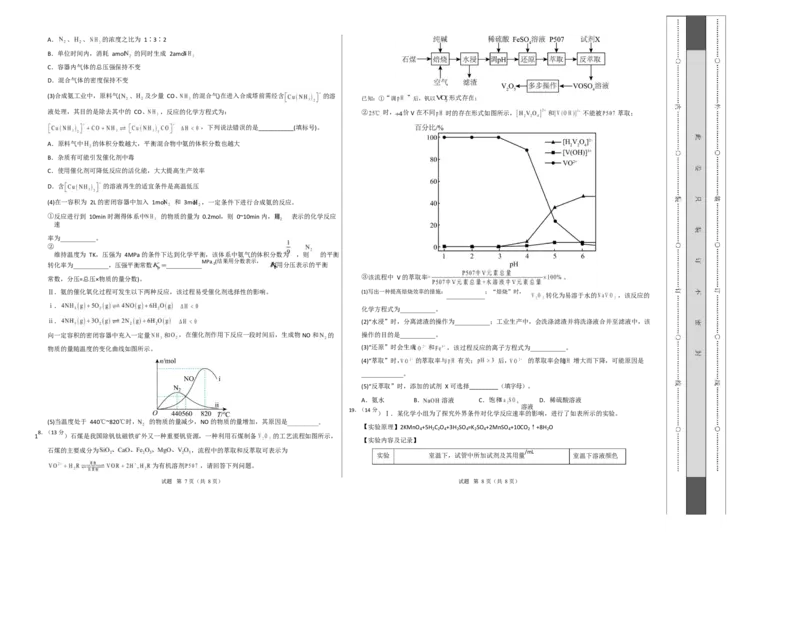
(3)合成氨工业中,原料气( 、 及少量 CO、 的混合气)在进入合成塔前需经含 的溶 已知:①“调 ”后,钒以 形式存在;
液处理,其目的是除去其中的 CO、 ,反应的化学方程式为: ② 时, 价V在不同 时的存在形式如图所示, 和 不能被 萃取;
,下列说法错误的是___________(填标号)。
A.原料气中 的体积分数越大,平衡混合物中氨的体积分数也越大
B.杂质有可能引发催化剂中毒
C.使用催化剂可降低反应的活化能,大大提高生产效率
D.含 的溶液再生的适宜条件是高温低压
(4)在一容积为 2L 的密闭容器中加入 1mol 和 3mol ,一定条件下进行合成氨的反应。
①反应进行到 10min 时测得体系中 的物质的量为 0.2mol,则 0~10min 内,用 表示的化学反应
速
率为___________。
②
维持温度为 TK,压强为 4MPa 的条件下达到化学平衡,该体系中氨气的体积分数为 ,则 的平衡
MPa (结果用分数表示,
转化率为___________,压强平衡常数 ___________ -2 为用分压表示的平衡
常数,分压=总压×物质的量分数)。 ③该流程中 V 的萃取率 。
Ⅱ.氨的催化氧化过程可发生以下两种反应,该过程易受催化剂选择性的影响。 (1)写出一种提高焙烧效率的措施: ;“焙烧”时,
____________ 转化为易溶于水的 ,该反应的
ⅰ.
化学方程式为___________。
ⅱ. (2)“水浸”时,分离滤渣的操作为___________;工业生产中,会洗涤滤渣并将洗涤液合并至滤液中,该
向一定容积的密闭容器中充入一定量 和 ,在催化剂作用下反应一段时间后,生成物NO 和 的 操作的目的是___________。
物质的量随温度的变化曲线如图所示。 (3)“还原”时会生成 和 ,该过程反应的离子方程式为___________。
(4)“萃取”时, 的萃取率与 有关; 后, 的萃取率会随 增大而下降,可能原因是
_____________。
(5)“反萃取”时,添加的试剂 X 可选择_________(填字母)。
A.氨水 B. 溶液 C.饱和 D.稀硫酸溶液
溶液
19.(14 分
)Ⅰ.某化学小组为了探究外界条件对化学反应速率的影响,进行了如表所示的实验。
(5)当温度处于 440℃~820℃时, 的物质的量减少,NO 的物质的量增加,其原因是 ___________。
【实验原理】2KMnO +5H C O +3H SO =K SO +2MnSO +10CO ↑+8H O
4 2 2 4 2 4 2 4 4 2 2
8.(13 分
1 )石煤是我国除钒钛磁铁矿外又一种重要钒资源,一种利用石煤制备 的工艺流程如图所示,
【实验内容及记录】
石煤的主要成分为 ,流程中的萃取和反萃取可表示为
/mL
实验 室温下,试管中所加试剂及其用量 室温下溶液颜色
为有机溶剂 ,请回答下列问题。
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)所示(实验中始终保持 V +V =50 mL),通过分析图像可知,做该实验时环境温度___________(填“高
编号 0.6mol•L-1H C O 0.2mol•L-1KMnO 3.0mol•L-1稀 褪至无色时所需 1 2
溶液 2 2 4 H 2 O 溶液 4 硫酸 时间 /min 于 于 ” ”或 “ “ 低 等于”)22℃,该 NaOH溶液的浓度约为___________ mol·L -1。
① 3.0 2.0 3.0 2.0 4.0
② 1.0 4.0 3.0 2.0 6.4
(1)实验目的是:
___________
。
(2)请解释实验②中加入 4.0mL 蒸馏水的原因是: ___________ 。
Ⅱ. 某学生通过测定反应过程中所放出的热量来计算中和反应反应热。他将 50 mL 0.50 mol·L-1 的盐酸
与 50 mL 0.55 mol·L-1 的 NaOH 溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题:
(3)从实验装置上看,图甲中尚缺少的一种玻璃仪器是 ___________。
(4)实验中改用 60 mL 0.50 mol·L-1 的盐酸与 50 mL 0.55 mol·L-1 的 NaOH 溶液进行反应,与上述实验相比,
(填“相等”或“不相等”);所求中和反应反应热的数值 (填“相等”或
所放出的热量___________ ___________
“不相
等”)。
(5)该同学做实验时有些操作不规范,造成测得的中和反应的ΔH偏大,请你分析可能的原因是___________
(填字母)。
A.测量盐酸的温度后,温度计没有用水冲洗干净,然后去测 NaOH 溶液的温度
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将 50 mL 0.55 mol·L-1 氢氧化钠溶液错取成了 50 mL 0.55 mol·L-1的氨水
(6)假设盐酸和氢氧化钠溶液的密度都是 1 g·cm-3,又知中和反应后生成溶液的比热容为:c=4.18 J·g-1·℃-1。
为了计算中和反应反应热,某学生实验记录数据如表:
起始温度 t /℃ 终止温度 t /℃
1 2
实验序
稀盐 氢氧化钠溶
号
混合溶液
酸 液
1 20.0 20.2 23.5
2 20.2 20.4 23.7
3 20.3 20.5 25.6
依据该学生的实验数据计算,该实验测得的中和反应反应热ΔH=___________(结果保留一位小数)。
(7)将 V mL 1.0 mol·L-1 盐酸和 V mL 未知浓度的 NaOH 溶液混合均匀后测量并记录温度,实验结果如图乙
1 2
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)