文档内容
2025-2026 学年度上学期月考
高三化学试题
本试卷分选择题和非选择题两部分,共 19 题,共 100 分,共 4 页。考试时间为 75 分钟。考试
结束后,只交答题卡。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Mg 24 P 31 Fe 56 Cu 64 Ga
70 As 75
第Ⅰ卷 选择题
一、选择题:本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项
符合题目要求。
1.化学与生产、生活、科技密切相关。下列说法正确的是( )
A.高吸水性树脂都含有羟基、烷基等亲水基团
B.含较多碳酸钠的盐碱地不利于农作物生长,可施加熟石灰进行改良
C.切开的土豆和茄子,切面处一段时间后会变色均是因为被氧化所致
D.北方冬季雪天路面上经常铺洒少量的融雪剂(一般含有氯化钙),目的是吸水
2.下列化学用语表示正确的是( )
A.HClO 的空间填充模型:
B.乙酰胺的结构简式:
C.基态 Fe2+的电子排布式:[Ar]3d54s1
D.HO 分子的形成过程:
2
3. 、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下: ;
。下列说法正确的是( )
A. X 的中子数为 2
B. X、Y 互为同位素
C. 、 可用作示踪原子研究化学反应历程
D. 自然界不存在 、 分子是因其化学键不稳定
4. 用下列装置进行实验,能达到实验目的的是( )A.装置甲:检查装置的气密性
B.装置乙:演示喷泉实验
C.装置丙:用明矾晶体制备 KAl(SO )
4 2
D.装置丁:制备 NH 并测量其体积
3
5.已知在酸性条件下,硫代硫酸钠会发生歧化反应:HSO +Na SO=Na SO +SO↑+S↓+H O。设 N 为阿
2 4 2 2 3 2 4 2 2 A
伏加德罗常数的值,下列说法正确的是
A.常温常压下,20 g DO 中含有的氧原子的数目为 N
2 A
B.pH=2 的 H
2
SO
4
溶液中,含有的 H+ 数目为 0.02N
A
C.常温下,向 100 mL 18 mol L-1 浓硫酸中加入足量的 Cu,该过程转移电子的数目为 1.8N
A
D.32 g SO 与足量的 O 充分反应,生成的 SO 分子总数为 0.5N
2 2 ⋅ 3 A
6.下列说法不正确的是( )
A.冠醚、杯酚、RNA 和蛋白质都是超分子
B.甲苯、甘油都与浓硝酸发生取代反应分别生成 TNT 和硝化甘油
C.只用新制氢氧化铜(可加热)就能区分乙醇、乙醛、己烷、四氯化碳、葡萄糖
D.疫苗一般采用冷藏存放,以避免蛋白质变性
7.下列关于有机化合物的说法正确的是( )
A.乙烯使酸性高锰酸钾溶液褪色是发生了加成反应
B.乙烯、苯、乙酸分子中的所有原子都在同一平面上
C.C H 属于芳香烃的同分异构体共有 4 种
8 10
D.蛋白质水解最终产物是氨基酸和甘油
8.立体异构包括顺反异构、对映异构等。有机物 M(2—甲基—2—丁醇)存在如图转化关系,下列说法错误的
是( )
A.N 分子不存在顺反异构
B.L 的任一同分异构体最多有 1 个手性碳原子
C.M 的同分异构体中,能被氧化为酮的醇有 4 种
D.L 的同分异构体中,含两种化学环境氢的只有 1 种
9.科学家合成出一种新化合物(如图所示),其中 W、X、Y、Z 四种元素,X、Y、Z 为同一短周期的元素,Z
核外最外层电子数是 X 核外电子数的一半,W 与 Z 的简单离子具有相同的电子层排布。下列叙述正确的是( )
A.WZ 的水溶液呈碱性
B. 是共价化合物,X 原子轨道杂化类型为 杂化C.原子半径大小顺序为:W>Z>Y>X
D. 的空间构型为平面三角形,Y 的价层电子对数为 4
10.实验室用 MnO 等原料制取 KMnO 粗品的实验流程如下。下列说法正确的是( )
2 4
A.“熔融”时,应先将 MnO 和 KClO 混合加热一段时间后再加入 KOH
2 3
B.通入 CO“歧化”时,氧化剂与还原剂的物质的量之比为 2∶1
2
C.“过滤”时,为加快分离速率可采用减压过滤
D.制得的 KMnO 粗品可能会含有 KCO,可以向粗品中滴加盐酸观察是否有气泡来检验是否含有 KCO
4 2 3 2 3
11.FeBr 溶液中通入一定量的 Cl,发生反应的离子方程式为 aFe2++bBr-+cCl→dFe3++eBr +fCl-,下列选项
2 2 2 2
中的数字与离子方程式的 a、b、c、d、e、f 一一对应,其中不符合反应实际的是( )
A.2 4 3 2 2 6 B.0 2 1 0 1 2
C.2 0 1 2 0 2 D.2 2 2 2 1 4
12.仅用下表提供的仪器和药品,就能达到相应实验目的是( )
编
仪器 药品 实
号 验目的
托盘天平(带 配制一定质
A 砝码)、胶头 NaCl 固体、 量分数的
滴管、量筒、 蒸馏水
NaCl
烧杯、
溶液
药匙、玻璃
棒
B 分液漏斗、烧瓶、锥形瓶、导管及橡皮塞 盐酸、大理石、硅酸钠溶液 证明非金属性:Cl>C>Si
酸式滴定 已 知 浓 度 测定 NaOH
C 管、胶头滴 的 盐 酸 、 溶液的物质
管、 待 测 的
铁架台(带 NaOH 溶液 量浓度
铁夹)
待 提 纯 的 提 纯 混 有 MgCl 杂 质 的
2
D 烧杯、 AlCl 溶 液
分液漏斗、 、 3 AlCl 3 溶液
胶头滴管、
铁架台 NaOH 溶液
A.A B.B C.C D.D
13.某学习小组为探究氯化铜与亚硫酸钠的反应,设计了如下实验:
已知 。下列分析中,错误的是( )A.2 mL 0.2 溶液中含 数目小于 ( 为阿伏加德罗常数的值)。
B.由实验可知,生成橙黄色沉淀的速率较快,而生成白色沉淀的反应趋势更大。
C.已知橙黄色沉淀中只含有 ,可利用稀硫酸检验其中的 ,若溶液变蓝,则说明含有
D.本 实 验 中 , 溶 液 和 溶 液 的 总 反 应 离 子 方 程 式 为
:
14.砷化镓是一种立方晶系如图甲所示,将 Mn 掺杂到晶体中得到稀磁性半导体材料如图乙所示,砷化镓的晶
体密度为ρ g·cm-3。下列说法错误的是( )
A.1 mol 砷化镓中配位键的数目是 N
A
B.掺入 Mn 的晶体中 Mn、Ga、As 的原子个数比为
C.沿体对角线 a→b 方向投影图如丙,若 c 在 11 处,则 As 的位置为 7、9、11、13
D.该晶体中距离最近的两个镓原子之间的距离为
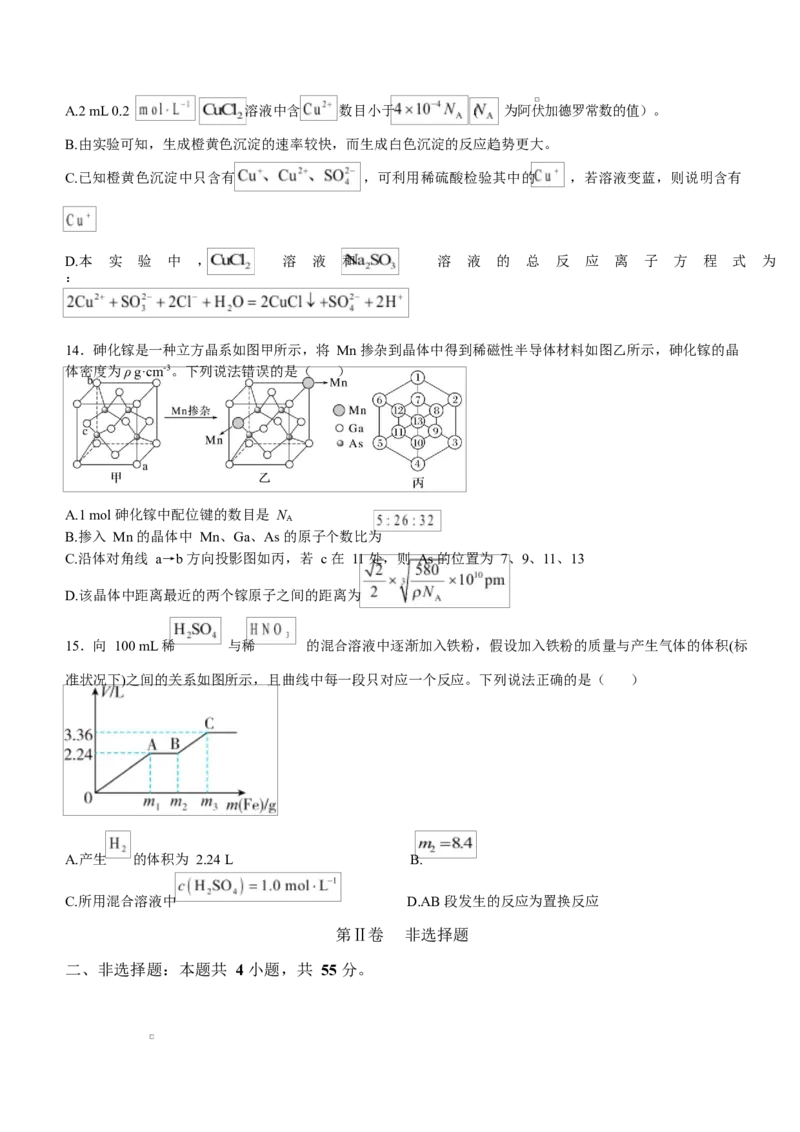
15.向 100 mL 稀 与稀 的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标
准状况下)之间的关系如图所示,且曲线中每一段只对应一个反应。下列说法正确的是( )
A.产生 的体积为 2.24 L B.
C.所用混合溶液中 D.AB 段发生的反应为置换反应
第Ⅱ卷 非选择题
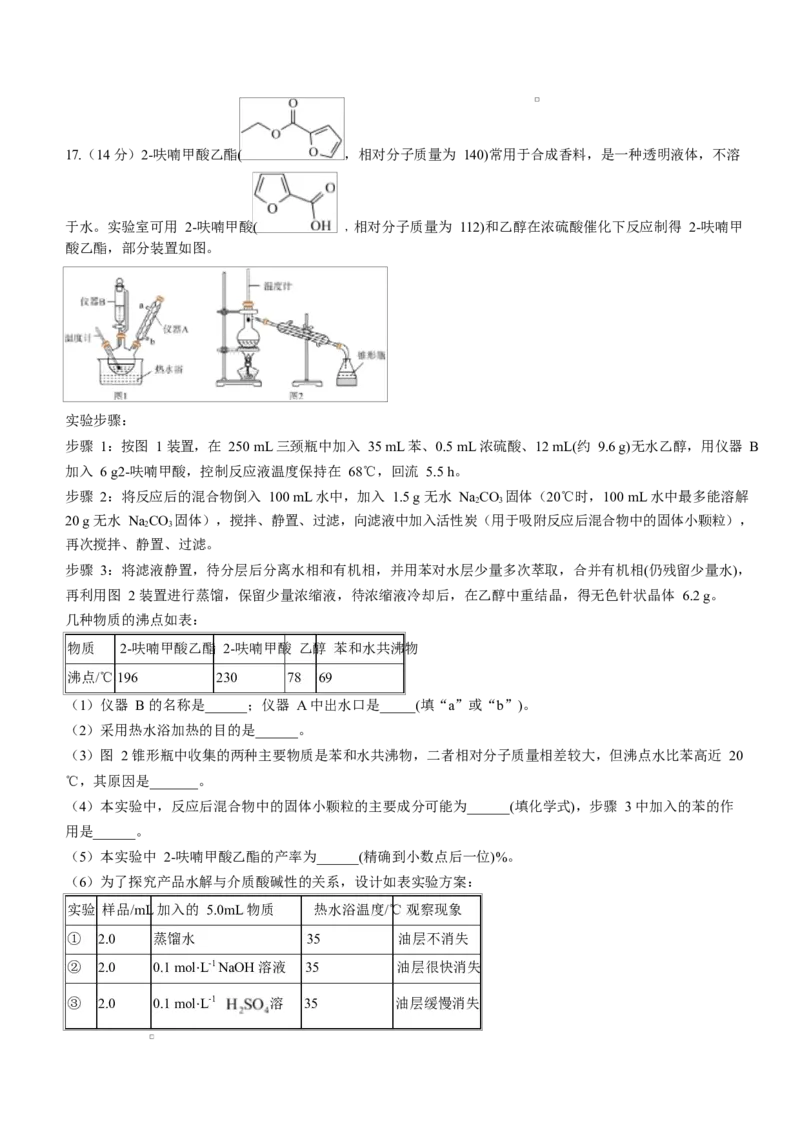
二、非选择题:本题共 4 小题,共 55 分。16.(14 分)磷酸亚铁锂是比亚迪“刀片电池”的电极材料,可以硫铁矿(主要成分是 ,含少量 、
和 )为原料制备,流程如图:
已知几种金属离子沉淀的 pH 如表所示:
金属氢氧化物
开始沉淀的 pH 2.3 7.5 4.0
完全沉淀的 pH 4.1 9.7 5.2
请回答下列问题:
(1)将硫铁矿磨成粉末的目的是____________________。
(2)从焙烧到氧化要经历一系列步骤,请从下列步骤选择正确的步骤并合理排序__________________。
(3)“试剂 R”是一种氧化剂,最好选择____________。
(4)流程中在“高温煅烧”条件下,由 制备 的化学方程式为____________。不能用铁粉代
替草酸,其原因是____________________。
(5)检验产品中是否混有 或 杂质的实验操作是_____________。
(6)产品 纯度的测定。分别取 7.000 g 试样,用稀硫酸溶解,滴加二苯胺磺酸钠指示剂,用 0.3000
溶液滴定至溶液由浅绿变为蓝紫,平均消耗 溶液 20.00 mL。
①产品的纯度为____________。(精确到 0.01%)
②测定结果偏低的原因不可能是____________。
A.产品在空气中放置时间过长 B.滴定前仰视读数
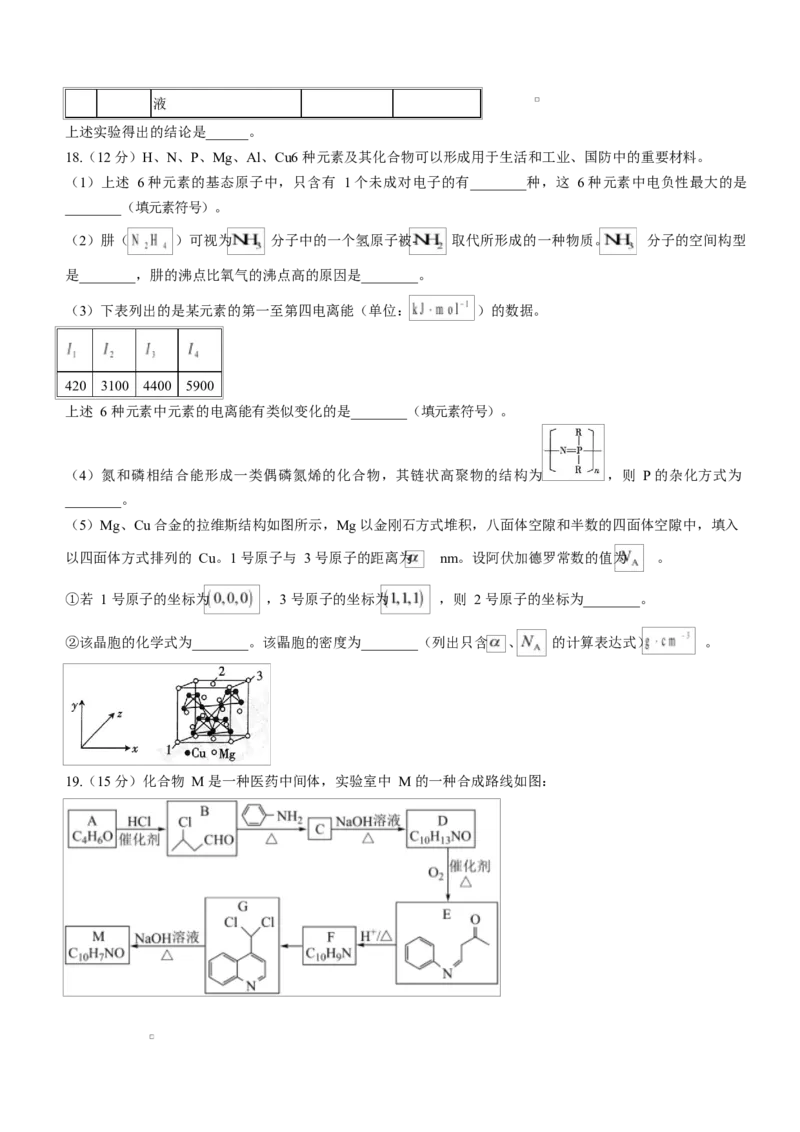
C.滴定达终点时发现滴定管尖嘴内有气泡生成 D.滴定管没有用标准液润洗17.(14 分)2-呋喃甲酸乙酯( ,相对分子质量为 140)常用于合成香料,是一种透明液体,不溶
于水。实验室可用 2-呋喃甲酸( ﹐相对分子质量为 112)和乙醇在浓硫酸催化下反应制得 2-呋喃甲
酸乙酯,部分装置如图。
实验步骤:
步骤 1:按图 1 装置,在 250 mL 三颈瓶中加入 35 mL 苯、0.5 mL 浓硫酸、12 mL(约 9.6 g)无水乙醇,用仪器 B
加入 6 g2-呋喃甲酸,控制反应液温度保持在 68℃,回流 5.5 h。
步骤 2:将反应后的混合物倒入 100 mL 水中,加入 1.5 g 无水 NaCO 固体(20℃时,100 mL 水中最多能溶解
2 3
20 g 无水 NaCO 固体),搅拌、静置、过滤,向滤液中加入活性炭(用于吸附反应后混合物中的固体小颗粒),
2 3
再次搅拌、静置、过滤。
步骤 3:将滤液静置,待分层后分离水相和有机相,并用苯对水层少量多次萃取,合并有机相(仍残留少量水),
再利用图 2 装置进行蒸馏,保留少量浓缩液,待浓缩液冷却后,在乙醇中重结晶,得无色针状晶体 6.2 g。
几种物质的沸点如表:
物质 2-呋喃甲酸乙酯 2-呋喃甲酸 乙醇 苯和水共沸物
沸点/℃ 196 230 78 69
(1)仪器 B 的名称是______;仪器 A 中出水口是_____(填“a”或“b”)。
(2)采用热水浴加热的目的是______。
(3)图 2 锥形瓶中收集的两种主要物质是苯和水共沸物,二者相对分子质量相差较大,但沸点水比苯高近 20
℃,其原因是______。
(4)本实验中,反应后混合物中的固体小颗粒的主要成分可能为______(填化学式),步骤 3 中加入的苯的作
用是______。
(5)本实验中 2-呋喃甲酸乙酯的产率为______(精确到小数点后一位)%。
(6)为了探究产品水解与介质酸碱性的关系,设计如表实验方案:
实验 样品/mL 加入的 5.0mL 物质 热水浴温度/℃ 观察现象
① 2.0 蒸馏水 35 油层不消失
② 2.0 0.1 molL-1 NaOH 溶液 35 油层很快消失
③ 2.0 0.1 mol ⋅ L-1 溶 35 油层缓慢消失
⋅液
上述实验得出的结论是______。
18.(12 分)H、N、P、Mg、Al、Cu6 种元素及其化合物可以形成用于生活和工业、国防中的重要材料。
(1)上述 6 种元素的基态原子中,只含有 1 个未成对电子的有________种,这 6 种元素中电负性最大的是
________(填元素符号)。
(2)肼( )可视为 分子中的一个氢原子被- 取代所形成的一种物质。 分子的空间构型
是________,肼的沸点比氧气的沸点高的原因是________。
(3)下表列出的是某元素的第一至第四电离能(单位: )的数据。
420 3100 4400 5900
上述 6 种元素中元素的电离能有类似变化的是________(填元素符号)。
(4)氮和磷相结合能形成一类偶磷氮烯的化合物,其链状高聚物的结构为 ,则 P 的杂化方式为
________。
(5)Mg、Cu 合金的拉维斯结构如图所示,Mg 以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入
以四面体方式排列的 Cu。1 号原子与 3 号原子的距离为 nm。设阿伏加德罗常数的值为 。
①若 1 号原子的坐标为 ,3 号原子的坐标为 ,则 2 号原子的坐标为________。
②该晶胞的化学式为________。该晶胞的密度为________(列出只含 、 的计算表达式) 。
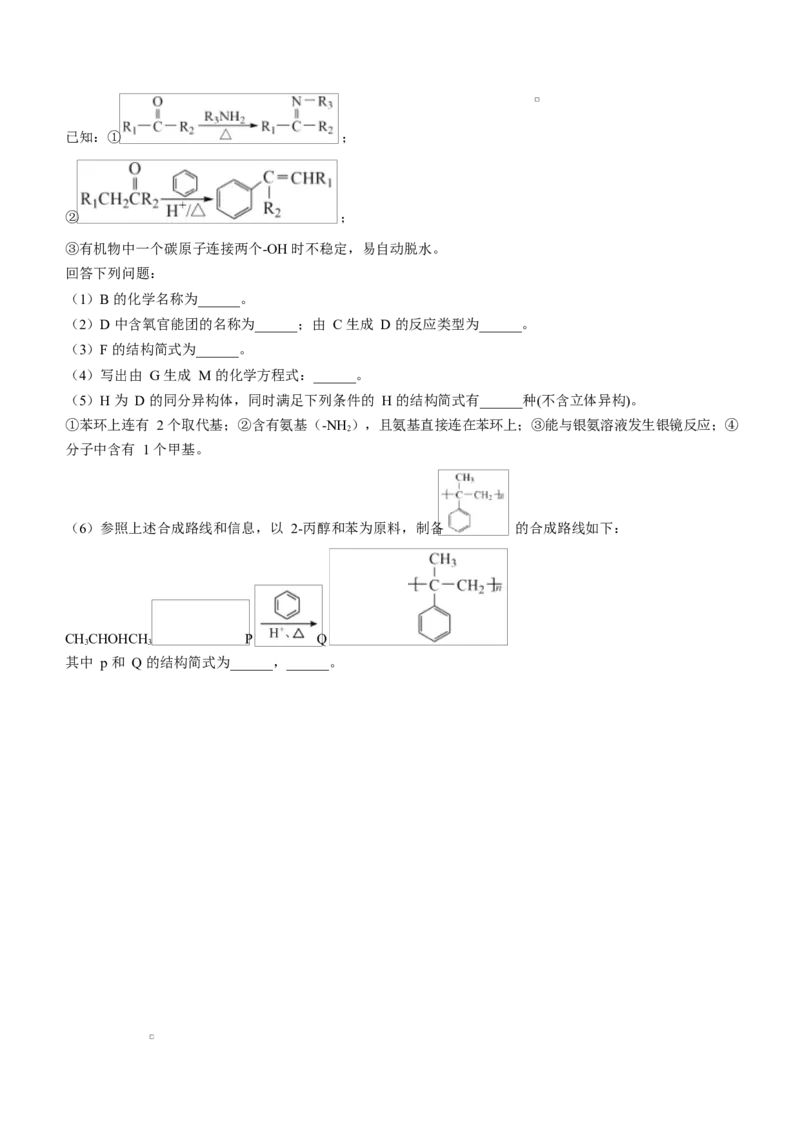
19.(15 分)化合物 M 是一种医药中间体,实验室中 M 的一种合成路线如图:已知:① ;
② ;
③有机物中一个碳原子连接两个-OH 时不稳定,易自动脱水。
回答下列问题:
(1)B 的化学名称为______。
(2)D 中含氧官能团的名称为______;由 C 生成 D 的反应类型为______。
(3)F 的结构简式为______。
(4)写出由 G 生成 M 的化学方程式:______。
(5)H 为 D 的同分异构体,同时满足下列条件的 H 的结构简式有______种(不含立体异构)。
①苯环上连有 2 个取代基;②含有氨基(-NH ),且氨基直接连在苯环上;③能与银氨溶液发生银镜反应;④
2
分子中含有 1 个甲基。
(6)参照上述合成路线和信息,以 2-丙醇和苯为原料,制备 的合成路线如下:
CHCHOHCH P Q
3 3
其中 p 和 Q 的结构简式为______,______。参考答案
1.【答案】C
【解析】
A.烷基不属于亲水基团,A 错误;
B.熟石灰为强碱,不利于盐碱地改良,B 错误;
C.茄子中存在一类叫“酚氧化酶”的物质,它遇到氧气之后,发生化学反应产生一些有色的物质。反应时间越
长,颜色越深;土豆变色的原因类似。C 正确;
D.铺融雪剂是为了降低水的熔点,D 错误;
故选 C。
2.【答案】A
【解析】
A.次氯酸的结构式为 H—O—Cl,Cl 原子半径最大,H 原子半径最小,空间填充模型为 ,故 A 正确;
B.乙酰胺的结构简式: ,故 B 错误;
C.铁元素为 26 号元素,核外电子排布为 1s22s22p63s23p63d64s2,基态 Fe2+的电子排布是为 1s22s22p63s23p63d6
或[Ar]3d6,故 C 错误;
D.HO 为共价化合物,氧原子最外层只有 6 个电子,HO 的形成过程中,2 个 H 原子与 1 个 O 原子各形成 1
2 2
对共用电子对,用电子式表示形成过程为: ,故 D 错误;
故选 A。
3.【答案】B
4.【答案】C
【解析】
A.装置中长颈漏斗处没有封闭,所以用手捂锥形瓶的方法不能达到检验装置气密性的目的,A 错误;
B. 不溶于水也不与氢氧化钠反应,无法演示喷泉实验,B 错误;
C.明矾晶体在坩埚中灼烧失去结晶水得到 KAl(SO ),C 正确;
4 2
D.氨气极易溶于水,不能用装水的量气管确定其体积,D 错误;
故选 C。
5.【答案】A
【解析】
A.DO 的相对分子质量为 20,20 g DO 的物质的量为 1 mol,含有的氧原子的数目为 N ,A 正确;
2 2 A
B.pH=2 的硫酸溶液中氢离子浓度为 mol/L,选项中未说明硫酸的体积,无法得知氢离子的数目,B
错误;
C.常温下,浓硫酸和铜不反应,没有电子转移,C 错误;
D.32 g SO 为 0.5 mol,SO 与 O 反应生成 SO 的反应为可逆反应,则最终生成的 SO 分子数小于 0.5N ,D
2 2 2 3 3 A错误;
故答案选 A。
6.【答案】A
【解析】
A.超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。冠醚、杯酚是超分子,RNA 和
蛋白质是高分子,A 错误;
B.甲苯与浓硝酸发生取代反应生成三硝基甲苯,即 TNT;甘油与浓硝酸发生取代反应生成硝化甘油,B 正确;
C.乙醇与新制氢氧化铜溶液互溶;己烷密度比水小,与新制氢氧化铜溶液分层,无色层在上层;四氯化碳密度
比水大,与新制氢氧化铜溶液分层,无色层在下层;乙醛在加热条件下与新制氢氧化铜反应均生成砖红色沉淀,
葡萄糖与新制氢氧化铜,先生成蓝色溶液,加热出现砖红色沉淀,可以区分,C 正确;
D.低温可防止蛋白质变性,疫苗一般采用冷藏存放,D 正确;
故选 A。
7.【答案】C
解析乙烯使酸性高锰酸钾溶液褪色,发生了氧化还原反应,A 项错误;乙烯、苯为平面结构,乙酸中含甲基,
甲基为四面体结构,则乙酸中所有原子不可能在同一平面上,B 项错误;C H 的芳香烃满足 C H 的通式,
8 10 n 2n-6
取代基可为 1 个乙基或两个甲基,同分异构体有
C 项正确;蛋白质水解的最终产物是氨基酸,D 项错误。
答案 C
8.【答案】C
【解析】
A.顺反异构是指化合物分子中由于具有自由旋转的限制因素,使各个基团在空间的排列方式不同而出现的非对
映异构现象, 、 都不存在顺反异构,故 A 正确;
B.手性碳原子是指与四个各不相同原子或基团相连的碳原子,L 的同分异构体结构及手性碳原子(用*标记)为
、 、 、 、 、 、
、 ,任一同分异构体中最多含有 1 个手性碳原子,故 B 正确;
C.当与羟基相连的碳原子上只有 1 个氢原子时,醇发生催化氧化反应生成酮,羟基取代戊烷同分异构体中含有
2 个氢原子的碳原子上 1 个氢原子即满足条件,满足条件的结构有: 、 、,共 3 种,故 C 错误;
D.连接在同一碳原子上的氢原子等效,连接在同一碳原子上的甲基等效,由 B 项解析可知,L 的同分异构体中,
含有 2 种化学环境的氢原子的结构为 ,故 D 正确;
综上所述,说法错误的是 C,故答案为:C。
9.【答案】B
【解析】
W、X、Y、Z 四种元素,X、Y、Z 为同一短周期元素,由化合物结构式可知 X 可以形成四个共价键则其为 C
或者 Si,Z 核外最外层电子数是 X 核外电子数的一半,若 X 为 C 则 Z 为 B,若 X 为 Si 则 Z 为 Cl,Z形成了
一个共价键则 Z 为 Cl,Y 形成两个共价键,化合物中阴离子带一个单位负电荷,阴离子中只含有一个 Y,所
以 Y 为 P,需要从外界得到一个电子而稳定,W 与 Z 的简单离子具有相同的电子层排布,由化合物结构式可知 W
失去一个电子,则 W 为 K,W、X、Y、Z 分别为 K、Si、P、Cl。
A.WZ 的水溶液为氯化钾溶液,强酸强碱盐呈中性,故 A 错误;
B. 是 SiCl ,是共价化合物,中心原子价层电子对数为 ,根据价层电子对互斥理论 Si 原子轨
4
道杂化类型为 杂化,故 B 正确;
C.原子半径同周期从左到右半径减小, , ,故 C 错误;
D. 为 PCl ,价电子对数为 ,根据价层电子对互斥理论的空间构型 P 原子轨道杂化类型为
3
杂化,孤电子对数为 1, 的空间构型为三角锥形,故 D 错误;
故选:B。
10.【答案】C
【解析】
A.“熔融”时,应先将 MnO 和 KClO 混合加热一段时间后,KClO 会分解;
2 3 3
B.通入 CO“歧化”时,氧化剂与还原剂的物质的量之比为 1∶2
2
C.“过滤”时,为加快分离速率可采用减压过滤,加快过滤速度
D.制得的 KMnO 粗品可能会含有 KCO,向粗品中滴加盐酸时会和 KMnO 反应产生氯气,也观察有气泡不
4 2 3 4
能确定含有 KCO
2 3
故选 C。
11.【答案】B
【解析】略
12.【答案】A【解析】
13.【答案】C【解析】略
14.【答案】B
【解析】
解析由图甲知,砷化镓的化学式为 GaAs,砷化镓中砷提供孤电子对,镓提供空轨道形成配位键,则 1 mol 砷
化镓中配位键的数目是 N ,A 正确;掺入 Mn 的晶体中 Ga 个数为 ,As 有 4 个位于体内,
A
Mn 个数为 ,Mn、Ga、As 的原子个数比为 ,B 错误;由砷化镓晶胞结
构可知,c 位于侧面的面心,沿体对角线 a→b 方向投影图如丙,则 As 的位置为 7、9、11、13,C 正确;由晶
胞结构可知,距离最近的两个镓原子之间的距离为面对角线长的一半,晶胞中含 4 个 Ga 和 4 个 As,晶胞质
量为 g,晶胞体积为 cm3,则晶胞边长为 pm,两个镓原子之间的最近距离为
pm,D 正确。
15.【答案】B
【解析】OA 段稀硝酸和铁反应生成 Fe3+和 NO,AB 段发生 Fe3+和 Fe 反应生成 Fe2+,BC 段发生 H+ 和 Fe+ 反应
生成 H
2
16.14 分(除标注外其它 2 分)【答案】(1)增大接触面积使焙烧更充分(1 分) (2)cade
(3)过氧化氢(1 分)
(4) 防止生成杂质
(5)取样品,加入稀盐酸溶解,滴加 KSCN 溶液,若不变色则不含三价铁杂质,或变色则含三价铁杂质
(6) D
【解析】
硫铁矿焙烧后加入硫酸酸溶,除去不反应的二氧化硅等物质,过滤滤液加入 FeS 进行还原操作,将铁离子转
化为亚铁离子同时生成硫单质,过滤除去滤渣,滤液再加入氧化亚铁调节溶液 pH 除去铝,过滤滤液进行氧化
操作将二价铁转化为三价铁,加入磷酸氢二铵生成 沉淀, 和碳酸锂、草酸反应生成 ;
(1)焙烧过程的目的是将 转化为氧化铁和二氧化硫,能够除去硫;
(2)由表格可知,三价铁离子和铝离子的沉淀范围有重叠,从焙烧到氧化要经历一系列步骤,此步骤需要除
去铝杂质且需要将三价铁转化为二价铁,防止沉铝过程中导致铁损失,故应该焙烧后首先加入稀硫酸溶解金属
氧化物后除去不反应的二氧化硅等物质,滤液加入 FeS 进行还原操作,将铁离子转化为亚铁离子同时生成硫
单质,过滤除去滤渣,滤液再加入氧化亚铁调节溶液 pH 除去铝,过滤滤液进行氧化操作,故正确的步骤并合
理排序为:cade;
(3)“试剂 R”是一种氧化剂,需要将二价铁转化为三价铁且不引入新杂质,最好选择过氧化氢;( 4)“高 温 煅 烧 ”条 件 下 , 由 和 碳 酸 锂 、 草 酸 反 应 生 成 , 化 学 方 程
式 为
;铁粉极易和空气中氧气生成氧化铁,不能
用铁粉代替草酸,其目的是防止生成杂质导致产品不纯;
(5)铁离子会和 KSCN 溶液变红色,故检验产品中是否混有 或 杂质的实验操作是:取样品,
加入稀盐酸溶解,滴加 KSCN 溶液,若不变色则不含三价铁杂质,或变色则含三价铁杂质;
( 6) ① 具 有 氧 化 性 会 把 亚 铁 离 子 氧 化 为 铁 离 子 , 根 据 电 子 守 恒 、 质 量 守
恒 配 平 可 得 :
, 则 产 品 的 纯 度 为
;
②A.产品在空气中放置时间过长,部分二价铁转化为三价铁,导致标准液用量减小,测定结果偏低,A 符不合
题意;
B.滴定前仰视读数,导致标准液用量数值偏小,测定结果偏低,B 不符合题意;
C.滴定达终点时发现滴定管尖嘴内有气泡生成,使得标准液读数偏小,测定结果偏低,C 不符合题意;
D.滴定管没有用标准液润洗,导致标准液用量增大,测定结果偏大,D 符合题意;
故选 D。
17.14 分(除标注外其它 2 分)【答案】(1)恒压(滴液)漏斗(1 分) a(1 分)
(2)使反应混合物受热均匀,温度容易控制
(3)水分子间存在氢键,苯分子间为范德华力 (4)C 作萃取剂
(5)82.7
(6)酸、碱都能催化酯水解,碱的催化效率高于酸
【解析】
如图 1 为反应发生装置,其中仪器 A 为球形冷凝管,用于冷凝回流,仪器 B 为恒压滴液漏斗,可以平衡三口
烧 瓶 和 漏 斗 中 的 气 压 , 使 液 体 顺 利 滴 下 , 步 骤 1 发 生 反 应 的 化 学 方 程 式 为
,其中浓硫酸作催化剂和吸水剂;步骤 2 加入碳酸钠是为
了除去硫酸等;利用图 2 蒸馏时,冷却水从下口进,上口出,温度计水银球置于支管口;
(1)如图 1 为反应发生装置,其中仪器 A 为球形冷凝管,用于冷凝回流,冷却水从 b 口进 a 口出,仪器 B 为
恒压滴液漏斗;故答案为:恒压(滴液)漏斗;a;
(2)热水浴加热的优点有:加热平稳,不像直接加热那样剧烈,易控制,加热均匀。适宜需要严格控制温度
的反应;故答案为:使反应混合物受热均匀,温度容易控制;(3)水分子间存在氢键,苯分子间为范德华力
(4)步骤 1 制取 2-呋喃甲酸乙酯时加入了浓硫酸,浓硫酸具有强脱水性,易使含 C、H、O 的有机物炭化,
所以该固体小颗粒为 C;步骤 3 中加入苯是为了从水相中萃取出产物,减少损失,所以苯作萃取剂;故答案为:
C;作萃取剂;
(5)由题意,12 mL(约 9.6 g)无水乙醇,物质的量为 ,6 g 2-呋喃甲酸的物质的量为
,根据反应 ,可知乙醇
过量,按 2-呋喃甲酸的的量计算,设理论上生成的 2-呋喃甲酸乙酯的质量为 x,则有 ,解得
,则 2-呋喃甲酸乙酯的产率为 ;故答案为:82.7%;
(6)根据表中数据,其他条件相同时,中性环境中产品不水解,在酸和碱性环境中,产品均水解,且碱性环
境中酯的水解效率较高;故答案为:酸、碱都能催化酯水解,碱的催化效率高于酸。
18.12 分(除标注外其它 2 分)【答案】(1)3(1 分),N(1 分)
(2)三角锥形(1 分),肼分子间形成了氢键(1 分)
(3) (1 分)
(4) (1 分)
(5)① ,② ,
19.15 分(除标注外其它 2 分)【答案】(1)3-氯丁醛
(2)羟基取代反应(1 分)
(3)
(4)
(5)9
(6CHCOCH
3 3
【解析】B 的分子式为 ,对比 A 的分子式可知 A 到 B 为加成反应;由已知①可推出 C 的结构简式为
;C 到 D 为卤代烃的水解,D 的结构简式为 ;D 到
E 为仲醇的催化氧化;根据已知②,可推断出 F 的结构简式为 ;根据 G 的结构简式可推出,F 到
G 为取代反应,条件为氯气、光照;G 到 M 为水解反应,因为两个羟基不能连在同一个碳上,脱水形成醛基,
M 的结构简式为 ,以此解题。
(1)根据 B 的结构简式可知,起名称为:3-氯丁醛;根据 B 的结构简式,用“*”标出物质 B 中的手性碳原
子: ,可知 B 分子中手性碳原子有 1 个;
(2)由分析可知 D 的结构简式为 ,则其中的含氧官能团的名称为羟基;
和氢氧化钠溶液加热生成 ,该反应为取代反
应;
(3)由分析可知,F 的结构简式为 ;
(4)由 G 生成 M 的反应为卤代烃的水解反应,则由 G 生成 M 的化学方程式为
;
(5)苯环上连有 2 个取代基;②既含-NH ,又能与银氨溶液发生银镜反应,说明含有-CHO;且-NH 直接与
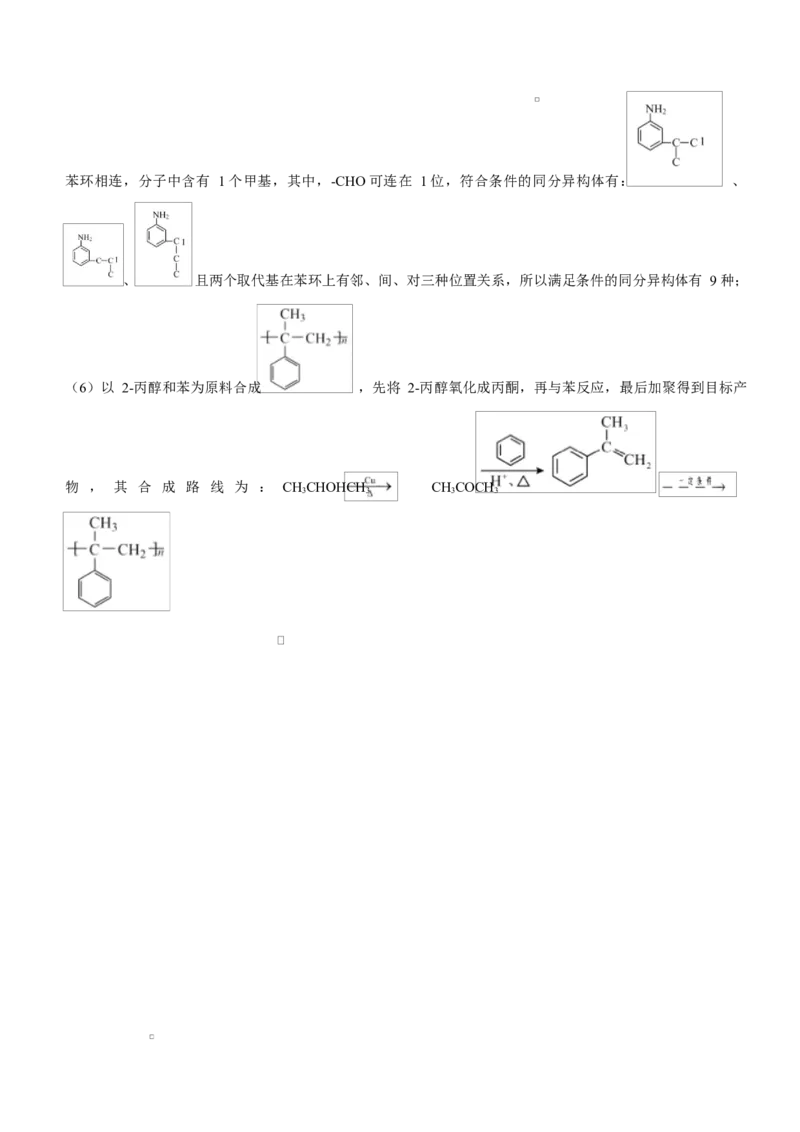
2 2苯环相连,分子中含有 1 个甲基,其中,-CHO 可连在 1 位,符合条件的同分异构体有: 、
、 且两个取代基在苯环上有邻、间、对三种位置关系,所以满足条件的同分异构体有 9 种;
(6)以 2-丙醇和苯为原料合成 ,先将 2-丙醇氧化成丙酮,再与苯反应,最后加聚得到目标产
物 , 其 合 成 路 线 为 : CHCHOHCH CHCOCH
3 3 3 3