文档内容
C. 反应③中 与足量 反应转移电子的数目为
六安一中 2026 届高三年级第二次月考
D. 溶液中, 的数目为
化学试卷
4.下列离子方程式书写正确的是( )
A.向(NH ) Fe(SO ) 溶液中加入过量NaOH溶液:2NH +Fe3++5OH-=2NH ↑+2H O+Fe(OH) ↓
4 2 4 2 3 2 3
B.用稀氢碘酸除去铁制品表面的铁锈:Fe O +6H+=2Fe3++3H O
2 3 2
时间:75分钟 满分:100分
C.泡沫灭火器使用时发生的反应:Al3++3HCO =Al(OH) ↓+3CO ↑
3 2
D.向饱和碳酸钠溶液中通入过量的二氧化碳气体:CO +CO + H O=2HCO
2 2
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27
5.某班同学对一定物质的量浓度溶液配制进行实验。甲组:用碳酸钠晶体(Na CO •10H O)来配
2 3 2
S:32 Cl:35.5 Ca:40 Fe:56 Cu:64 制1.0mol•L-1Na CO 溶液480mL;乙组:用98%的浓硫酸(ρ=1.85g/cm3)配制0.5mol•L-1稀硫酸
2 3
500mL。假如其他操作都准确无误,下列说法正确的是( )
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求。 A.定容后,将容量瓶振荡摇匀、静置发现液面低于刻度线,又加少量水至刻度线
1. 化学应用体现在生活的方方面面,下列用法不合理的是( ) B.甲组需称取空气中久置的碳酸钠晶体143.0g;乙组需用量筒量取浓硫酸13.67mL
A. 用明矾净化黄河水 C.使用前容量瓶中有水珠,无需干燥即可立即使用
B.含铁元素的硫酸铁是一些补血药剂的主要成分 D.甲组定容时仰视刻度线,配制浓度偏低;乙组量筒量取时仰视刻度线,配制浓度偏低
C.镁合金密度小,硬度和强度大,常用作制造火箭、飞机的部件 6.下列实验产生的废液中,可能大量存在的粒子组是( )
D.碳酸氢钠溶液呈碱性,故可以用作胃药起到中和胃酸的作用
A. 稀硝酸与铜片制 的溶液中:
2. 实验室中,下列试剂保存方法正确的是( )
B. 硫酸与 制 的溶液中:
A. 液溴加水封保存在广口试剂瓶中 B. 硝酸银溶液保存在棕色细口试剂瓶中
C. 浓盐酸与 制 的溶液中:
C. 高锰酸钾与苯酚存放在同一药品柜中 D. 金属锂保存在盛有煤油的广口试剂瓶中
D. 双氧水与 溶液制 的溶液中:
3. 钠及其化合物的部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是(
7.某碳酸钠固体样品中,可能含有固体氯化钠、碳酸钙、硫酸铜中的一种或几种杂质。为探究
)
其成分组成,现取10.6g该固体样品,向其中加入100g一定质量分数的稀盐酸,固体样品全
部溶解,得到无色溶液,同时生成mg气体。下列说法错误的是( )
A.该固体样品中一定没有硫酸铜
B.若 ,则该固体样品一定是纯净物
A. 反应①生成的气体,每11.2L(标准状况)含原子的数目为
C.若 ,则该固体样品中一定含有氯化钠
B. 反应②中2.3gNa完全反应生成的产物中含非极性键的数目为
1
学科网(北京)股份有限公司D.若 ,则该固体样品中一定含有碳酸钙
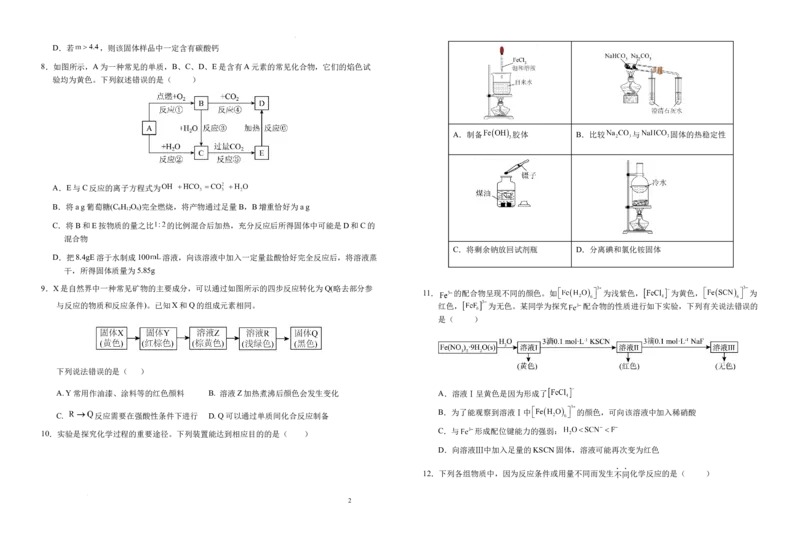
8.如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色试
验均为黄色。下列叙述错误的是( )
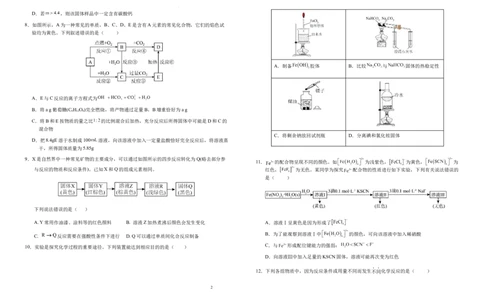
A.制备 胶体 B.比较 与 固体的热稳定性
A.E与C反应的离子方程式为
B.将a g葡萄糖(C H O )完全燃烧,将产物通过足量B,B增重恰好为a g
6 12 6
C.将B和E按物质的量之比 的比例混合后加热,充分反应后所得固体中可能是D和C的
混合物
C.将剩余钠放回试剂瓶 D.分离碘和氯化铵固体
D.把8.4gE溶于水制成100 溶液,向该溶液中加入一定量盐酸恰好完全反应后,将溶液蒸
干,所得固体质量为5.85g
9.X是自然界中一种常见矿物的主要成分,可以通过如图所示的四步反应转化为Q(略去部分参
11. 的配合物呈现不同的颜色。如 为浅紫色, 为黄色, 为
与反应的物质和反应条件)。已知X和Q的组成元素相同。 红色, 为无色。某同学为探究 配合物的性质进行如下实验,下列有关说法错误的
是( )
下列说法错误的是( )
A. Y常用作油漆、涂料等的红色颜料 B. 溶液Z加热煮沸后颜色会发生变化 A.溶液Ⅰ呈黄色是因为形成了
B.为了能观察到溶液Ⅰ中 的颜色,可向该溶液中加入稀硝酸
C. 反应需要在强酸性条件下进行 D. Q可以通过单质间化合反应制备
C.与 形成配位键能力的强弱:
10.实验是探究化学过程的重要途径。下列装置能达到相应目的的是( )
D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色
12.下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是( )
2
学科网(北京)股份有限公司① 与 ② 与 ③ 与 ④ 溶液与氨水
⑤ 与 溶液 ⑥ 与硝酸 ⑦ 溶液与氨水 二、非选择题:本题共四小题,共58分。
A.除③④外 B.除③⑦外 C.除③外 D.除⑥⑦外 15.(14分)填写下列空白:
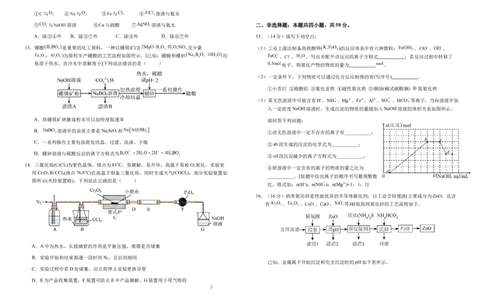
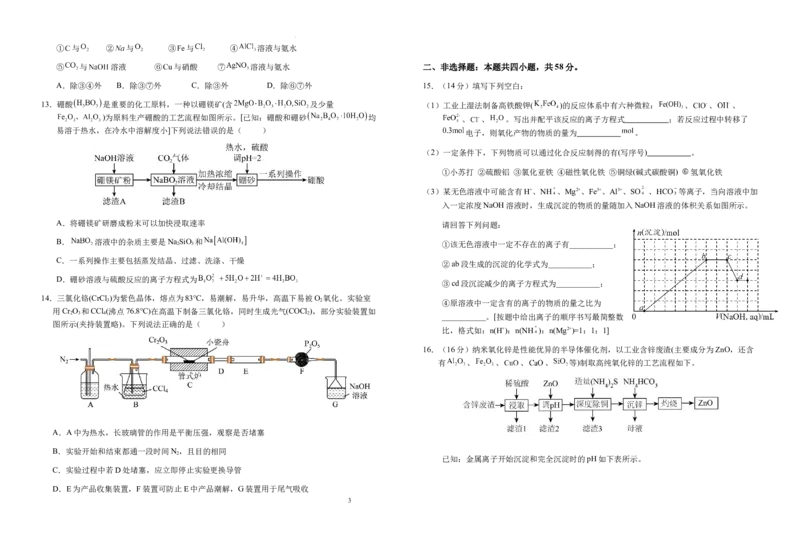
13.硼酸 是重要的化工原料,一种以硼镁矿(含 及少量 (1)工业上湿法制备高铁酸钾( )的反应体系中有六种微粒: 、 、 、
)为原料生产硼酸的工艺流程如图所示。[已知:硼酸和硼砂 均 、 、 。写出并配平该反应的离子方程式 ;若反应过程中转移了
易溶于热水,在冷水中溶解度小]下列说法错误的是( )
电子,则氧化产物的物质的量为 。
(2)一定条件下,下列物质可以通过化合反应制得的有(写序号) 。
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)某无色溶液中可能含有H+、NH 、Mg2+、Fe3+、Al3+、SO 、HCO 等离子,当向溶液中加
入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
A.将硼镁矿研磨成粉末可以加快浸取速率 请回答下列问题:
B. 溶液中的杂质主要是Na SiO 和
2 3 ①该无色溶液中一定不存在的离子有___________;
C.一系列操作主要包括蒸发结晶、过滤、洗涤、干燥
②ab段生成的沉淀的化学式为___________;
D.硼砂溶液与硫酸反应的离子方程式为
③cd段沉淀减少的离子方程式为___________;
14.三氯化铬(CrCl )为紫色晶体,熔点为83℃,易潮解,易升华,高温下易被O 氧化。实验室
3 2 ④原溶液中一定含有的离子的物质的量之比为
用Cr O 和CCl (沸点76.8℃)在高温下制备三氯化铬,同时生成光气(COCl ),部分实验装置如
2 3 4 2 ___________。[按题中给出离子的顺序书写最简整数
图所示(夹持装置略)。下列说法正确的是( )
比,格式如:n(H+):n(NH ):n(Mg2+)=1:1:1]
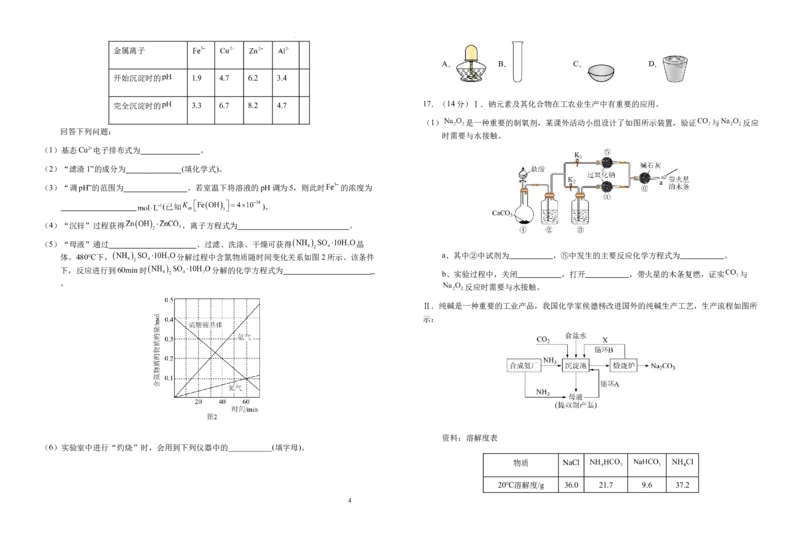
16.(16分)纳米氧化锌是性能优异的半导体催化剂,以工业含锌废渣(主要成分为ZnO,还含
有 、 、 、 、 等)制取高纯氧化锌的工艺流程如下。
A.A中为热水,长玻璃管的作用是平衡压强,观察是否堵塞
B.实验开始和结束都通一段时间N ,且目的相同
2
已知:金属离子开始沉淀和完全沉淀时的pH如下表所示。
C.实验过程中若D处堵塞,应立即停止实验更换导管
D.E为产品收集装置,F装置可防止E中产品潮解,G装置用于尾气吸收
3
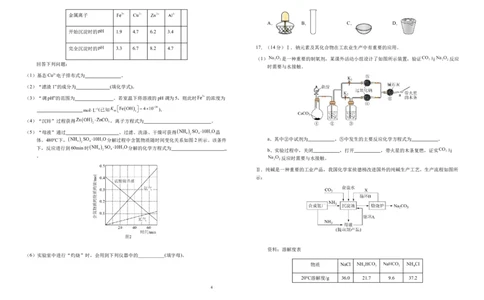
学科网(北京)股份有限公司金属离子
A. B. C. D.
开始沉淀时的 1.9 4.7 6.2 3.4
完全沉淀时的 3.3 6.7 8.2 4.7 17.(14分)Ⅰ.钠元素及其化合物在工农业生产中有重要的应用。
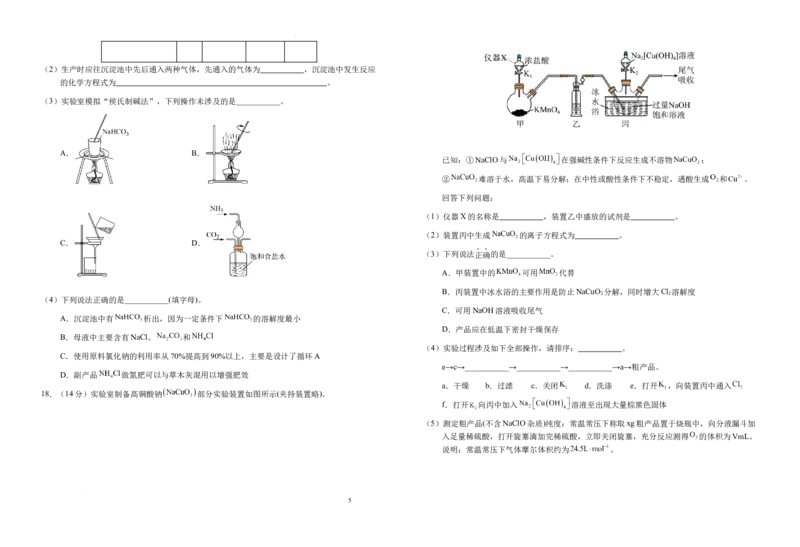
(1) 是一种重要的制氧剂,某课外活动小组设计了如图所示装置,验证 与 反应
回答下列问题:
时需要与水接触。
(1)基态Cu2+电子排布式为 。
(2)“滤渣1”的成分为 (填化学式)。
(3)“调pH”的范围为 。若室温下将溶液的pH调为5,则此时 的浓度为
(已知 )。
(4)“沉锌”过程获得 ,离子方程式为 。
(5)“母液”通过 、过滤、洗涤、干燥可获得 晶
体。480℃下, 分解过程中含氮物质随时间变化关系如图2所示。该条件 a、其中②中试剂为 ,⑤中发生的主要反应化学方程式为 。
下,反应进行到60min时 分解的化学方程式为
b、实验过程中,关闭 ,打开 ,带火星的木条复燃,证实 与
。
反应时需要与水接触。
Ⅱ.纯碱是一种重要的工业产品,我国化学家侯德榜改进国外的纯碱生产工艺,生产流程如图所
示:
资料:溶解度表
(6)实验室中进行“灼烧”时,会用到下列仪器中的___________(填字母)。
物质 NaCl
20℃溶解度/g 36.0 21.7 9.6 37.2
4
学科网(北京)股份有限公司(2)生产时应往沉淀池中先后通入两种气体,先通入的气体为 ,沉淀池中发生反应
的化学方程式为 。
(3)实验室模拟“侯氏制碱法”,下列操作未涉及的是___________。
A. B.
已知:①NaClO与 在强碱性条件下反应生成不溶物 ;
② 难溶于水,高温下易分解;在中性或酸性条件下不稳定,遇酸生成 和 。
回答下列问题:
(1)仪器X的名称是 ,装置乙中盛放的试剂是 。
(2)装置丙中生成 的离子方程式为 。
C. D.
(3)下列说法正确的是___________。
A.甲装置中的 可用 代替
B.丙装置中冰水浴的主要作用是防止NaCuO 分解,同时增大Cl 溶解度
2 2
(4)下列说法正确的是___________(填字母)。
C.可用NaOH溶液吸收尾气
A.沉淀池中有 析出,因为一定条件下 的溶解度最小
D.产品应在低温下密封干燥保存
B.母液中主要含有NaCl、 和
(4)实验过程涉及如下全部操作,请排序: 。
C.使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了循环A
e→c→___________→___________→___________→a→粗产品。
D.副产品 做氮肥可以与草木灰混用以增强肥效
a.干燥 b.过滤 c.关闭 d.洗涤 e.打开 ,向装置丙中通入
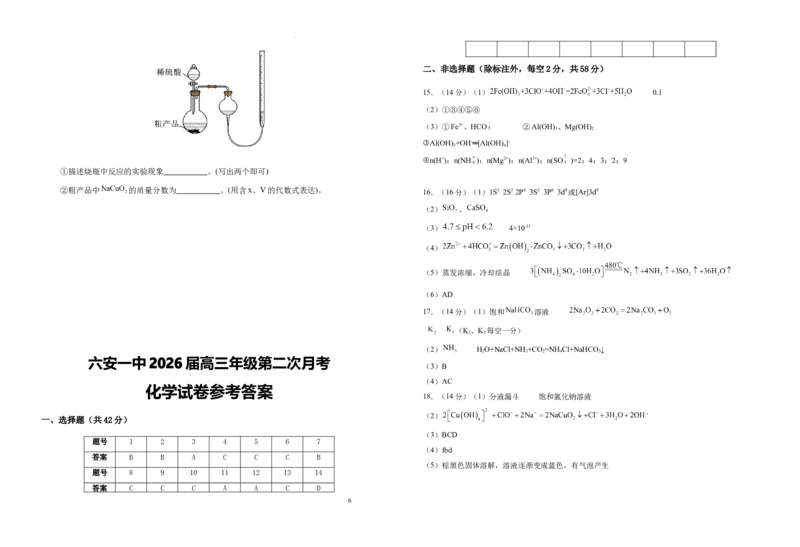
18.(14分)实验室制备高铜酸钠 部分实验装置如图所示(夹持装置略)。
f.打开 向丙中加入 溶液至出现大量棕黑色固体
(5)测定粗产品(不含NaClO杂质)纯度:常温常压下称取xg粗产品置于烧瓶中,向分液漏斗加
入足量稀硫酸,打开旋塞滴加完稀硫酸,立即关闭旋塞,充分反应测得 的体积为VmL。
说明:常温常压下气体摩尔体积约为 。
5
学科网(北京)股份有限公司二、非选择题(除标注外,每空2分,共58分)
15.(14分)(1) 0.1
(2)①③④⑤⑥
(3)①Fe3+、HCO ②Al(OH) 、Mg(OH)
3 2
③Al(OH) +OH-═[Al(OH) ]-
3 4
④n(H+):n(NH ):n(Mg2+):n(Al3+):n(SO )=2:4:3:2:9
①描述烧瓶中反应的实验现象 。(写出两个即可)
②粗产品中 的质量分数为 。(用含x、V的代数式表达)。 16.(16分)(1)1S2 2S2 2P6 3S2 3P6 3d9或[Ar]3d9
(2) 、
(3) 4×10-11
(4)
(5)蒸发浓缩,冷却结晶
(6)AD
17.(14分)(1)饱和 溶液
(K、K 每空一分)
2 1
(2) HO+NaCl+NH +CO =NHCl+NaHCO ↓
2 3 2 4 3
六安一中 2026 届高三年级第二次月考
(3)B
(4)AC
化学试卷参考答案
18.(14分)(1)分液漏斗 饱和氯化钠溶液
(2) -
一、选择题(共42分)
(3)BCD
题号 1 2 3 4 5 6 7
(4)fbd
答案 B B A C C C B
(5)棕黑色固体溶解,溶液逐渐变成蓝色,有气泡产生
题号 8 9 10 11 12 13 14
答案 C C C A A C D
6
学科网(北京)股份有限公司2NH +Fe2++4OH-=2NH·H O+Fe(OH) ↓,故A错误;
3 2 2
B. 反应生成的Fe3+能氧化I-,正确的离子方程式为:Fe O+6H++2I-=2Fe2++3H O+I ,故B错误;
2 3 2 2
C. 泡沫灭火器的原理是利用Al (SO ) 与NaHCO 的双水解反应生成氢氧化铝和CO,则离子方程式
2 4 3 3 2
正确,故C正确;D. 向饱和碳酸钠溶液中通入过量的二氧化碳气体,会生成NaHCO ,由于NaHCO
3 3
的质量比碳酸钠大,且溶解度比碳酸钠小,反应消耗了溶剂水,则会有NaHCO 晶体析出,则正确的
3
离子方程式为:NaCO+CO + H O=2NaHCO ↓,故D错误;
2 3 2 2 3
5.C
【详解】A.摇匀后加水,会导致配制结果偏低,A错误;
详解 B.甲组应称取Na 2 CO 3 •10H 2 O晶体143g(m=nM=0.5mol×286g/mol=143g),但空气中久置会变质;乙组
需用量筒量取浓硫酸的体积,但是量筒是粗量器、不能量取13.67mL,B错误;
1.B
C.使用前容量瓶中有水不影响配制,C正确;D.甲组定容时仰视刻线,水加多,配制浓度偏低;
【解析】A.明矾水解生成氢氧化铝胶体可吸附水中悬浮杂质,可用于净水,A正确;
乙组量筒量取时俯视刻度线,浓硫酸取少,配制浓度偏低,D错误
B.含铁元素的硫酸亚铁是一些补血药剂的主要成分,故B错误;
6.C
C.镁合金密度小,硬度和强度大,耐腐蚀等方面的优点,常用作制造火箭、飞机的部件,故B正
【详解】A.稀硝酸与铜反应生成 和NO,NO难溶于水,无法大量存在,A不符合
确;
题意;B.70%硫酸与NaSO 反应生成SO ,溶液中应含 ,但 在强酸性条件
2 3 2
D.碳酸氢钠溶液弱碱性,可用作胃药,故D正确; 下会转化为SO 2 和H 2 O,无法大量存在,B不符合题意;C.浓盐酸与KMnO 4 反应生成Cl 2 ,产物为
、 、 和 ,这些离子在酸性环境中稳定共存,无后续反应干扰,C符合题意;D.
2.B
FeCl 催化HO 分解生成O,溶液中应含Fe3+而非Fe2+,D不符合题意;
3 2 2 2
【详解】A.液溴为液体,应使用细口瓶保存,广口瓶通常用于固体,加水封正确但试剂瓶选择错
7.B
误,A错误;B.硝酸银溶液见光易分解,棕色细口瓶避光且适合液体保存,B正确;
【详解】A.硫酸铜溶液呈蓝色,而反应后得到无色溶液,说明样品中不含硫酸铜,A正确;
C.高锰酸钾是强氧化剂,苯酚有还原性,两者混合可能反应,不能放在同一药品柜中,C错误;
B.若m=4.4g,纯碳酸钠10.6g恰好生成4.4g CO。若样品为碳酸钠、碳酸钙和氯化钠的混合物,因
2
D.锂密度小于煤油,无法被煤油浸没隔绝空气,保存方法错误,应保存在固体石蜡中,D错误;
为等质量的碳酸钙比碳酸钠生成的二氧化碳多,而氯化钠不反应,所以可以通过调整三者的比例,使
3.A 10.6g混合物恰好生成4.4g二氧化碳,B错误;
【详解】A.反应①电解熔融NaCl生成 ,标准状况下11.2L 为0.5mol,含0.5×2=1mol原子,即 C.若m<4.4g,说明杂质生成的CO 2 比同质量碳酸钠少或不生成。碳酸钙生成的CO 2 比同质量碳酸钠
,A正确;B.2.3g Na(0.1mol)与氧气加热反应生成0.05mol ,每个 含1个O-O 多,因此杂质中必须含有氯化钠(可能同时含碳酸钙和氯化钠,但必须有氯化钠),C正确;
非极性键,所以非极性键数目为 ,B错误;
D.等质量的碳酸钙与稀盐酸反应产生二氧化碳的质量比碳酸钠多,若m>4.4,说明等质量的杂质与
C. 与水反应生成氢氧化钠和氧气,化学方程式为 ,1mol 稀盐酸反应产生二氧化碳的能力比碳酸钠强,所以该固体样品中一定含有碳酸钙,D正确;答案选
与水反应转移1mol电子,数目为 ,C错误; B。
D.ClO⁻在水中会水解,故 数目小于 ,D错误; 8.C
4.C 【分析】A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色试验均为黄
色,则为钠的单质或钠的化合物,所以A为Na,结合转化关系可知,B为 ,C为NaOH,D为
【详解】A. (NH)Fe(SO ) 溶液中为Fe2+,而不是Fe3+,则加入过量NaOH溶液,正确的离子方程式为
4 2 4 2
7
学科网(北京)股份有限公司,E为 ,据此分析作答; D.氯化铵受热易分解生成氨气和氯化氢,遇冷后氨气和氯化氢又重新化合生成氯化铵,碘易升华,
加热碘和氯化铵固体混合物后,升华的碘遇冷重新变为固体,所以不能用该方法分离碘和氯化铵固
【详解】A.E为 ,C为NaOH,两者反应生成碳酸钠和水,离子方程式为
体,D错误;
,A正确;
11.A
B.有机物在氧气中完全燃烧生成 ,产物通过足量 ,发生反应
、 , 固体增加的质量相当于吸收的 【详解】A.Ⅰ中溶液显黄色,原因是 水解成黄色的[Fe(H O) (OH)]2+,故A错误;
2 5
CO和H 的质量。由C H O:6CO+6H 可知m(C H O)=6CO+6H ,将a g葡萄糖(C H O)完全燃烧
2 6 12 6 2 6 12 6 2 6 12 6
B.为了观察浅紫色,需要抑制 的水解,为了防止 的干扰,需要加入稀硝酸,故B正确;
后,将产物通过足量B,B增重为a g,B正确;
C.溶液Ⅰ中含有 ,向其中滴入几滴KSCN溶液,溶液变为红色,说明 转
C.将 和 按物质的量之比 的比例混合后加热,设 的物质的量为2mol,
化为了 ,即 与 的配位能力强于HO;溶液Ⅱ呈红色,说明含有
2
NaO 的物质的量为1mol,则发生反应 ,生成1mol 和1mol ,加入几滴NaF,溶液颜色由红色变为无色,说明 转化成 ,即 与 的配位
2 2
能力强于 ,故C正确;D.向溶液Ⅲ中加入足量KSCN固体,可使平衡
,1mol 优先与1mol 反应,方程式为 ,恰好完全反应生成
正向移动,溶液可能再次变为红色,故D正确。
1mol ,C错误;
12.A
D.把8.4g 溶于水制成100 溶液,向该溶液中加入一定量盐酸恰好完全反应,加入盐酸
【详解】① 与 :氧气足量生成二氧化碳,不足生成一氧化碳,符合条件;
后,溶质是氯化钠,n(NaCl)=n(Na+)= =0.1mol,质量为0.1mol×58.5g/mol=5.85g,将溶液蒸
② 与 :常温生成氧化钠,加热生成过氧化钠,符合条件;
干,所得固体质量为5.85g,D正确; 故选B。
③ 与 :无论条件如何均生成氯化铁,不符合;
9.C
④ 与氨水:无论氨水量多少均生成氢氧化铝沉淀,不符合;
【分析】X是自然界中一种常见矿物的主要成分,根据溶液 Z、R、Q的颜色可知X中含有铁元素,
根据固体颜色可知X是FeS,Y是Fe O,溶液中Z含有Fe3+、溶液R中含有Fe2+,Q是FeS。 ⑤ 与 :二氧化碳足量生成碳酸氢钠,二氧化碳少量生成碳酸钠,符合条件;
2 2 3
【详解】A.Fe O 可用作油漆、涂料等的红色颜料,A正确; ⑥ 与硝酸:与浓硝酸反应放出二氧化氮,稀硝酸放出一氧化氮,符合条件;
2 3
B.含有Fe3+的溶液加热转化为Fe(OH) 胶体,溶液颜色发生变化,B正确; ⑦ 与氨水:氨水量不同分别生成氢氧化银沉淀(会分解生成氧化银)或银氨溶液,符合条
3
件。
C.FeS可溶于酸,所以R→Q反应不能在酸性溶液中进行,C错误;
综上,①、②、⑤、⑥、⑦符合条件,排除③④,选A。
D.在加热条件下Fe和S化合生成FeS,D正确;
13.C
10.C
【分析】生成 的流程为将硼镁矿加NaOH溶液碱浸,其中难溶于NaOH溶液的 、 形
【详解】A.制备 胶体时应向沸腾的蒸馏水中逐滴滴加饱和氯化铁溶液,继续煮沸至液体呈
成滤渣A过滤除去,能溶于NaOH溶液中的 、 、 生成 、 、
红褐色,不能用自来水,自来水中杂质会使得胶体聚沉,A错误;
进入滤液,然后通入 气体将 、 转化为 和 沉
B.碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,碳酸钠受热不分解,比较碳酸钠、碳酸氢钠固体 淀形成滤渣B过滤除去,将滤液蒸发浓缩,冷却结晶,再加入硫酸调节pH,得到硼砂,最后经过处
的热稳定性时,应将碳酸氢钠置于小试管中,碳酸钠置于大试管中,小试管中碳酸氢钠分解生成的气 理得到硼酸,据此分析解答。
体能使澄清的石灰水变浑浊,大试管中产生的气体不能使澄清的石灰水变浑浊,则题给装置设计不合
【详解】A.硼镁矿研磨成粉末可以增大固体的表面积,有利于增大反应物的接触面积,加快浸取速
理,B错误:
率,A正确;B.由分析可知,硼酸钠溶液中的主要杂质为硅酸钠和四羟基合铝酸钠,B正确;
C.钠的性质非常活泼,随意丢弃易发生事故,实验室中剩余的钠要放回试剂瓶,钠的密度大于煤
C.由分析可知,得到硼酸的一系列操作为冷却结晶、过滤、洗涤、干燥,C错误;
油,可放回盛装煤油的试剂瓶中,C正确;
8
学科网(北京)股份有限公司D.由分析可知,加入热水和稀硫酸调节溶液 为2的目的是将硼砂转化为硼酸,反应的离子方程式 ⑥由反应4Fe(OH) +O +2H O=4Fe(OH) 可得出,氢氧化铁可以通过化合反应制得;
2 2 2 3
为 ,D正确。
由以上分析可知,①③④⑤⑥符合题意。
14.D
(3)无色溶液,则一定不含Fe3+,加入NaOH溶液后,在0-a段没有生成沉淀,说明溶液中一定存在
【分析】氮气经浓硫酸干燥后通入后续装置除去反应装置内的空气,与装置B挥发出的CCl 一起进 H+或HCO 离子,由于后面有沉淀生成及部分沉淀溶解可知,溶液中一定存在Al3+,由于HCO 和
4
入管式炉,Cr O 与CCl 在管式炉内高温反应得到光气和无水三氯化铬气体,经过装置E时,无水三 Al3+会发生双水解而不能共存,则只能存在H+,a-b段生成沉淀消耗了6a体积氢氧化钠,又c-d段部
2 3 4
氯化铬冷却凝华,光气则通过球形干燥管进入NaOH溶液被吸收,据此分析; 分沉淀溶解,可知溶液中一定存在Mg2+、Al3+,根据图象Al(OH) 的物质的量与剩余的沉淀的物质的
3
量相等,由OH-~[Al(OH) ]-可知消耗溶解氢氧化铝消耗了a体积氢氧化钠,所以生成氢氧化铝沉淀消
4
【详解】A.由题干可知三氯化铬( )易潮解,所以整个装置应保持无水的状态,所以A中装的应
耗了3a体积氢氧化钠,Mg2+生成的沉淀的量也消耗3a体积氢氧化钠,b-c段沉淀的物质的量不变,说
是浓硫酸,除 中的水蒸气,A错误;
明氢氧根离子与铵离子发生了反应,即溶液中一定存在NH ,根据溶液呈电中性可知,溶液中一定
B.反应前先通入氮气,排除空气的干扰,而反应结束后还需要持续通入N 一段时间,从而将COCl 存在SO ;综上所述,原溶液中含有的阳离子是H+、NH 、Mg2+、Al3+、SO ,一定不存在Fe3+、
2 2
完全排入装置D被充分吸收,并使CrCl 在氮气氛围中冷却进入装置E,即前后两次的作用不相同,B HCO ,据此分析解答
3
错误;
①含Fe3+溶液为黄色,由分析可知,该无色溶液中一定不存在的离子有Fe3+、HCO ;
C.实验过程中若D处出现堵塞,因 易升华,应对D处导管用酒精灯加热即可,C错误;
②根据以上分析,溶液中一定存在Mg2+、Al3+,所以ab段生成沉淀的化学式为:Al(OH) 、
3
D.由题干可知三氯化铬( )易潮解,F中的无水PO 可防止G中的水进入装置中,光气可与氢氧 Mg(OH) ,故答案为:Al(OH) 、Mg(OH) ;
2 5 2 3 2
化钠溶液反应COCl₂ + 4NaOH → Na₂CO₃ + 2NaCl + 2H₂O,G装置可用于光气的吸收,D正确;
③cd段沉淀减少是氢氧化铝与氢氧化钠反应,反应的离子方程式为:Al(OH) +OH-═[Al(OH) ]-
3 4
15.(1) 0.1 +2H O,故答案为:Al(OH) +OH-═[Al(OH) ]-;
2 3 4
(2)①③④⑤⑥ ④原溶液中含有的阳离子是H+、NH 、Mg2+、Al3+,根据消耗的氢氧化钠的物质的量可以认为
n(H+)=a,n(Al3+)=a,n(Mg2+)=1.5a,n(NH )=2a,根据电荷守恒,n(SO )=4.5a,n(H+):n(NH ):
(3)①Fe3+、HCO
n(Mg2+):n(Al3+):n(SO )=2:4:3:2:9。
②Al(OH) 、Mg(OH)
3 2
③Al(OH) +OH-═[Al(OH) ]-
3 4 16.(1)1S2 2S2 2P6 3S2 3P6 3d9或[Ar]3d9
④n(H+):n(NH ):n(Mg2+):n(Al3+):n(SO )=2:4:3:2:9
(2) 、
【详解】(1)制备 ,使用以下六种微粒: 、 、 、 、 、 。则
(3) 4×10-11
是还原剂, 是氧化剂,Cl-是还原产物,该反应的离子方程式为
;由此可建立关系式:2FeO 4 2-——6e-,若反应过程中转移 (4)
了 电子,则氧化产物(FeO2-)的物质的量为0.1 。
4
(5)蒸发浓缩,冷却结晶
(2)①由反应NaCO+CO +H O=2NaHCO 可得出,小苏打可以通过化合反应制得;
2 3 2 2 3
②硫酸铝通常由铝或氧化铝与硫酸反应制得,反应为置换反应或复分解反应;
(6)AD
③由反应2FeCl +Fe=3FeCl 可得出,氯化亚铁可以通过化合反应制得;
3 2 【分析】含锌废渣主要成分为ZnO,还含有 、 、 、 、 等。向粉碎后的含锌
废渣中先加入稀硫酸“浸取”,将金属元素转化为硫酸盐,二氧化硅不反应,硫酸钙微溶,过滤得到
④由反应3Fe+2O Fe O 可得出,磁性氧化铁可以通过化合反应制得;
2 3 4
含有二氧化硅、硫酸钙的滤渣1和滤液;向滤液中加入氧化锌调节溶液pH在4.7—6.2范围内,将溶
⑤由反应2Cu+O +CO +H O=Cu (OH) CO 可得出,铜绿(碱式碳酸铜) 可以通过化合反应制得;
2 2 2 2 2 3 液中的铁离子、铝离子、铜离子转化为氢氧化铁、氢氧化铝、氢氧化铜沉淀,过滤得到含有氢氧化
铁、氢氧化铝、氢氧化铜的滤渣2和滤液;向滤液中加入硫化铵,将溶液中剩余的铜离子转化CuS沉
9
学科网(北京)股份有限公司淀“深度除铜”,过滤得到CuS沉淀和滤液;向滤液中加入碳酸氢铵溶液,将溶液中的锌离子转化为
循环使用,煅烧炉中发生2NaHCO NaCO+CO ↑+H O,X为二氧化碳可循环使用,以此来解答。
3 2 3 2 2
Zn(OH) ∙ZnCO 沉淀,过滤得到母液和Zn(OH) ∙ZnCO ;碱式碳酸锌煅烧分解生成氧化锌。母液中溶
2 3 2 3
质主要为硫酸铵,“母液”通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥可获得
【详解】(1)a.其中②中试剂为饱和碳酸氢钠溶液,目的是除去二氧化碳气体中的氯化氢,⑤中发
晶体。
生的主要反应化学方程式为:2NaO+2CO =2Na CO+O ;
2 2 2 2 3 2
【详解】(1)Cu是29号元素,基态Cu2+:1S2 2S2 2P6 3S2 3P6 3d9或[Ar]3d9。故答案为:1S2 2S2 2P6
b.实验过程中,关闭K、打开K,生成的CO 未被干燥,带火星的木条复燃,证实CO 与NaO 反
2 1 2 2 2 2
3S2 3P6 3d9或[Ar]3d9;
应时需要与水接触;
(2)向粉碎后的含锌废渣中先加入稀硫酸“浸取”,将金属元素转化为硫酸盐,二氧化硅不反应,
(2)生产时应往沉淀池中先后通入两种气体,氨气极易溶于水,二氧化碳溶解度不大,先通入的气
硫酸钙微溶,“滤渣1”的主要成分为 、 。故答案为: 、 ;
体为NH ,再通入CO,沉淀池中发生的反应为:HO+NaCl+NH +CO =NHCl+NaHCO ↓;
3 2 2 3 2 4 3
(3)“调pH”的目的是除去铜离子、铝离子和铁离子,为不影响锌离子,“调pH”的范围为
(3)由流程图可知,实验室模拟“侯氏制碱法”,未涉及的操作是蒸发结晶,故答案为:B;
。若室温下将溶液的pH调为5,c(OH-)=10-9mol/L,则此时 的浓度为4×10-38/(1×10-
9)3 =4×10-11 。故答案为: ;4×10-11; (4)A.沉淀池中发生反应:HO+NaCl+NH +CO =NHCl+NaHCO ↓,有NaHCO 析出,因为该条件
2 3 2 4 3 3
下NaHCO 的溶解度最小,故A正确;
3
(4)“沉锌”过程获得 ,“沉锌”过程中硫酸锌和碳酸氢铵反应生成
、二氧化碳、水、和硫酸铵,离子方程式为 B.滤液中主要含有NaCl、NaHCO 和NH Cl,故B错误;
3 4
。故答案为:
C.使用原料氯化钠的利用率从70%提高到90%以上,图中转化关系可知,主要是设计了循环A,故
;
C正确;
(5)母液中溶质主要为硫酸铵,“母液”通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥可获得
D.副产品NH Cl做氮肥,不能与草木灰(显碱性)混用,二者混合发生双水解反应,肥效减小,故D
4
晶体。480℃下, 分解过程中含氮物质随时间变化关系如图2
错误;故答案为:AC。
所示,60min时,∆n ∶∆n( )∶∆n( )=3∶1∶4,即三者化学剂量数之比为3:1:
18.(1)分液漏斗 饱和氯化钠溶液
4,根据原子守恒得该条件下 分解的化学方程式为
(2) -
。
(3)BCD
(6)实验室中进行“灼烧”固体时,会用到下列仪器中的A酒精灯和D坩埚。
(4)fbd
17.(1)饱和 溶液
(5)棕黑色固体溶解,溶液逐渐变成蓝色,有气泡产生
(2) HO+NaCl+NH +CO =NHCl+NaHCO ↓
2 3 2 4 3
(3)B
(4)AC
【分析】装置甲中高锰酸钾和浓盐酸反应生成氯气,装置乙中盛有饱和食盐水,作用是除去氯气中混
有的HCl气体,装置丙中 与 在强碱性条件下反应生成 ,以此解答;
【分析】Ⅰ.验证CO 与NaO 反应时需要与水接触,由实验装置可知:①中盐酸和碳酸钙反应生成
2 2 2
二氧化碳,②用于除去HCl,应为饱和碳酸氢钠溶液,③应为浓硫酸,④⑤为对比试验,用于判断干
【详解】(1)仪器X的名称是分液漏斗,装置乙中盛放的试剂是饱和氯化钠溶液,用来除去氯气中
燥的二氧化碳是否与过氧化钠反应,⑥可避免空气中的水、二氧化碳进入④⑤,最后用带火星的木条
混有的HCl气体;
检验是否生成氧气,以此分析解答;
(2)装置丙中首先氯气和氢氧化钠反应生成氯化钠和次氯酸钠,随后 与 在强
Ⅱ.因二氧化碳在水中溶解度不大,则沉淀池中,向饱和食盐水先通入氨气,后通入二氧化碳,有利
碱性条件下反应生成 ,该反应中Cl元素化合价由+1价下降到-1价,Cu元素化合价由+2价上
于析出NaHCO ,沉淀池中发生反应为:HO+NaCl+NH +CO =NHCl+NaHCO ↓,母液中含氯化铵可
3 2 3 2 4 3
升到+3价,根据得失电子守恒和原子守恒配平离子方程式为:
10
学科网(北京)股份有限公司-;
(3)A.甲装置中的 不可用 代替, 与浓盐酸反应制取氯气需要加热,A错误;
B.丙装置中冰水浴的主要作用是防 高温分解,同时增大 溶解度,B正确;
C.尾气中含氯气,可用NaOH溶液吸收,C正确;
D.产品高温下易分解,在中性或酸性条件下不稳定,故应在低温下密封干燥保存,D正确;
故选BCD;
(4)打开 ,向装置丙中通入 ,一段时间后,关闭 ,打开 向丙中加入 溶液
至出现大量棕黑色固体,过滤、洗涤、干燥得粗产品,故顺序fbd;
(5)①因 难溶于水;在中性或酸性条件下不稳定,遇酸生成 和 ,故烧瓶中反应的实
验现象有气泡产生、棕黑色固体溶解溶液逐渐变成蓝色;
② 难溶于水,在中性或酸性条件下不稳定,遇酸生成 和 ,
,根据关系式可知, , 的质量分数为
。
11
学科网(北京)股份有限公司