文档内容
高途高中·化学
点睛卷
2024
河北省-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024 年河北省普通高中学业水平选择性考试模拟测试卷
化学
本试卷共 8页,18小题,满分 100分,考试用时 75分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28 Cl-35.5 Fe-56 Zn-65 Br-80
一、选择题:本题共 14小题,每小题 3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
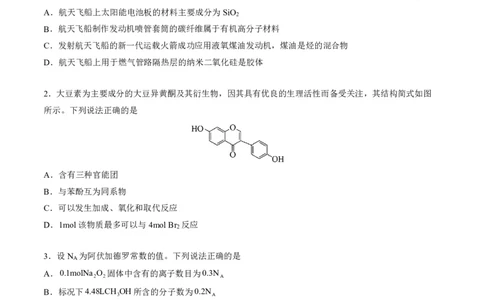
1.2023年中国航天大会的主题是“格物致知,叩问苍穹”。下列关于航天飞船上所用材料说法正确的是
A.航天飞船上太阳能电池板的材料主要成分为SiO
2
B.航天飞船制作发动机喷管套筒的碳纤维属于有机高分子材料
C.发射航天飞船的新一代运载火箭成功应用液氧煤油发动机,煤油是烃的混合物
D.航天飞船上用于燃气管路隔热层的纳米二氧化硅是胶体
2.大豆素为主要成分的大豆异黄酮及其衍生物,因其具有优良的生理活性而备受关注,其结构简式如图
所示。下列说法正确的是
A.含有三种官能团
B.与苯酚互为同系物
C.可以发生加成、氧化和取代反应
D.1mol该物质最多可以与4molBr 反应
2
3.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.0.1molNa O 固体中含有的离子数目为0.3N
2 2 A
B.标况下4.48LCH OH所含的分子数为0.2N
3 A
C.一定条件下,0.5molSO 与足量的O 反应,转移的电子数为N
2 2 A
D.1L 0.1molL1Na SO 溶液中含有的氧原子数为0.4N
2 4 A
4.已知某种核反应方程为30X+1HW Y+1n,其中X的次外层电子数是最外层电子数的2倍,X、Y的
Z 1 Z+1 0
最外层电子数之和为9。下列叙述正确的是
A.X、Y元素在自然界中均存在游离态
B.X的原子半径小于Y的
C.Y的简单气态氢化物的空间构型为平面三角形
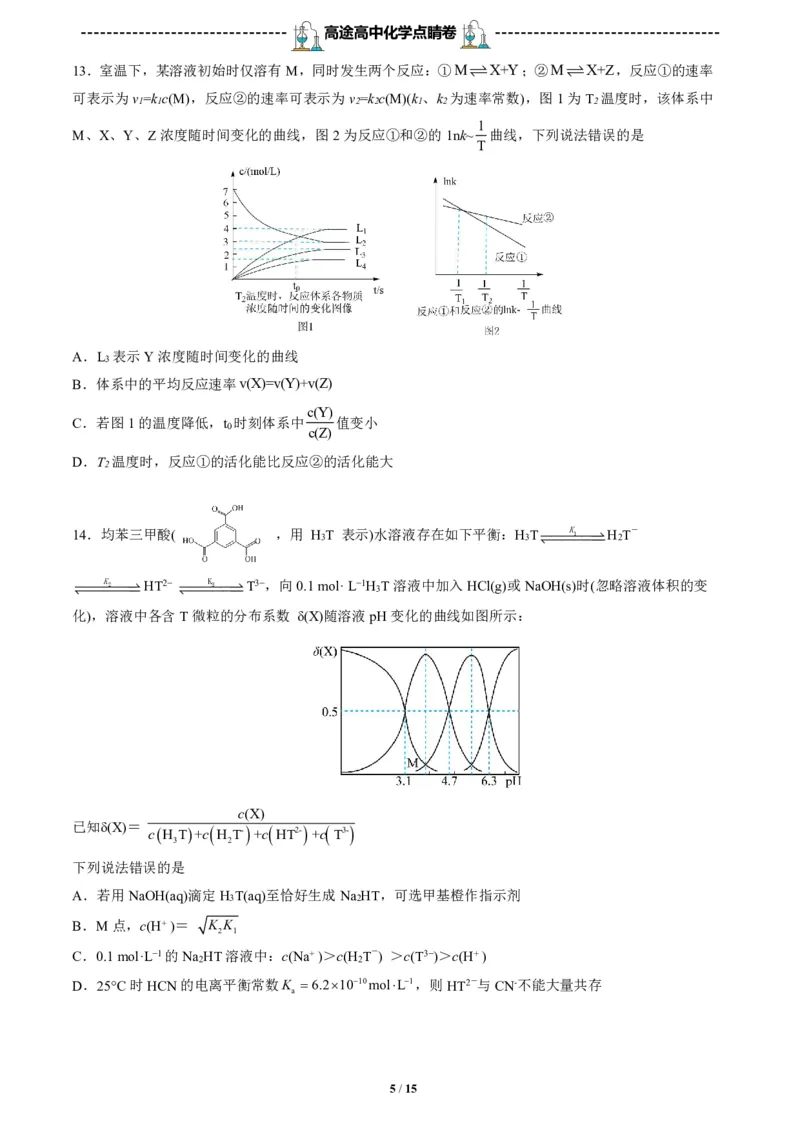
D.最高价氧化物对应的水化物的酸性:X0,存在:v
正
=k
正
•p2(CH
4
)、v
逆
=k
逆
•p(C
2
H
2
)•p3(H
2
),
(k为速率常数),部分数据如表所示。
p(C H )/MPa p(H )/MPa v /(MPa•min-1)
2 2 2 逆
0.05 p 4.8
1
p p 19.2
2 1
p 0.15 8.1
2
表中p = ,该温度下k = MPa-3•min-1;温度升高,速率常数增大的倍数:k k (填“>”“<”
2 逆 正 逆
或“=”)。
(3)我国科技工作者发明了一种电化学分解甲烷的直流电源方法,从而实现了碳和水的零排放方式生产氢
气,电化学反应机理如图丙所示。阳极的电极反应式为 。
7/15-------------------------------- 高途高中化学点睛卷 -----------------------------------
(4)大量研究表明Pt Ni、Sn Ni、Cu Ni三种双金属合金团簇均可用于催化DRM反应
12 12 12
(CH +CO 2CO+2H ),在催化剂表面涉及多个基元反应,其中甲烷逐步脱氢过程的能量变化如图甲所
4 2 2
示(吸附在催化剂表面上的物种用*标注,TS1、TS2、TS3、TS4分别表示过渡态1、过渡态2、过渡态3、
过渡态4)。Pt Ni、Sn Ni、Cu Ni催化甲烷逐步脱氢过程的速率分别为v 、v 、v ,则脱氢过程的速率由
12 12 12 1 2 3
小到大的关系为 。
18.(15分)某研究小组按下列路线合成药物利培酮。
已知:①
②
请回答:
(1)化合物 的名称是 。
(2)E→F的过程中涉及两步反应,其反应类型依次为 。
(3)G的结构简式为 。
(4)写出同时符合下列条件的化合物A的一种同分异构体的结构简式 。
①1HNMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,没有C=N键和氮氧键
②分子中有一个含氧六元环 ,无其他环
(5)设计以CH CN、 和NH 为原料合成 的路线 (用流程图表示,其它无机试
3 3
剂任选)。
8/15-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2024 年河北省普通高中学业水平选择性考试模拟测试卷
化学参考答案
1.【答案】C
【详解】A.Si是一种良好的半导体材料,用于制造载人飞船上太阳能电池板的半导体材料主要成分为Si,
选项A不正确;
B.碳纤维为新型无机非金属材料,不是有机化合物,选项B不正确;
C.煤油的主要成分是烃的混合物,选项C正确;
D.纳米二氧化硅只有分散到水中才能形成胶体分散系,选项D不正确;答案选C。
2.【答案】C
【详解】A.该有机物含有四种官能团,分别为碳碳双键、羟基、醚键和酮羰基,A错误;
B.与苯酚不是差若干个-CH -,故不是同系物;
2
C.该有机物含有苯环和碳碳双键,故能发生加成反应,该有机物含有酚羟基,能发生取代反应和氧化反应
,C正确;
D该有机物含有两个酚羟基,且酚羟基的邻位碳上都有氢原子,1mol该物质能与4molBr 发生取代反应,该
2
有机物含有一个碳碳双键,1mol该物质能与1molBr 发生加成反应,则1mol该物质最多能与5molBr 发生反
2 2
应,故D错误; 故选C。
3.【答案】A
【详解】A.1molNa O 中含2mol阳离子(Na+)和1mol阴离子(O2-),A正确;
2 2 2
B.标况下,CH OH为液体,B错误;
3
C.SO 与O 反应可逆,C错误;
2 2
D.Na SO 溶液中还需要考虑水中的氧原子,D错误。故答案为A。
2 4
4.【答案】D
【分析】X的次外层电子数是最外层电子数的2倍,结合X质量数为30可知X为Si,Z=14,X、Y的最外层电
子数之和为9,则Y为P。
【详解】A.X为Si,自然界中以化合态(硅酸盐和氧化物)的形式存在,Y为P,自然界中主要以化合态(磷酸
盐)形式存在,A错误;
B.X为Si,Y为P,二者均为第三周期元素,同周期从左往右原子半径逐渐减小,则Si的原子半径大于P,B
错误;
C.Y的简单气态氢化物为PH ,中心原子为sp3杂化且有一对孤对电子,故空间构型为三角锥形,C错误;
3
D.非金属性XHCN,则HT2
a
与CN能发生反应生成HCN,不能大量共存,故D正确;
故选:C。
15.【答案】(1)蒸馏烧瓶 吸收未反应完的溴 3、2、5 管式炉5中无固体剩余或仪器6中无液体
滴下 无尾气处理装置
(2)蒸馏 关闭K 打开K
1 2
269m
(3)
2100%
60m
1
【分析】1、2、3为HBr生成装置,4为除杂装置除去混合气体中的溴蒸汽,5为反应装置,6、7、8、9为提
纯装置。
【详解】(1)装置6为蒸馏烧瓶,装置4中溴化亚铁能和溴单质反应将未反应的溴单质吸收,应先预热HBr
生成装置,再将溴单质通入生成装置,减少4中溴化亚铁在反应前的消耗,等HBr制得后再加热5,故加热顺
12/15-------------------------------- 高途高中化学点睛卷 -----------------------------------
序为3、2、5,反应结束时5中固体消耗殆尽且6中不再有液体产生,溴单质和溴化氢都有毒需要增加尾气处
理装置;
(2)利用产物体系中各组分沸点不同蒸馏提纯,提纯时为了让液体能顺利流下应关闭K 打开K ;
1 2
(3)样品最终经过水解、干燥、灼烧、冷却得到二氧化硅,269gSiHBr ~60gSiO ,则样品中SiHBr 质量为
3 2 3
269m 269m
2 g,样品纯度为 2100%。
60 60m
1
Δ
16.【答案】(1)将阳极泥粉碎或搅拌 Cu S+2O 2CuO+SO
2 2 2
(2)Pt、Au 防止生成的氮氧化物排放到空气中
(3)静置,向上层清液中滴加NaCl溶液,若无沉淀产生,则沉淀完全
(4)分液 HNO
3
(5)6.0×103
(6)2[Ag(S 2 O 3 ) 2 ]3-+S 2 O2 4 -+4OH-=2Ag+2SO 3 2-+4S 2 O 3 2-+2H 2 O
【分析】焙烧时,除了Pt、Au外,阳极泥中物质转化为对应氧化物,故进入酸浸氧化步骤的物质有:CuO
、Ag O、Pt、Au,由于Pt、Au与HNO 不反应,故滤渣Ⅰ的成分为Pt、Au,CuO、Ag O溶解转化为Cu(NO )
2 3 2 3 2
、AgNO ,则滤液Ⅰ中含Cu(NO ) 、AgNO 、HNO (过量),加入NaCl获得AgCl沉淀,即滤渣Ⅱ为AgCl,滤液
3 3 2 3 3
Ⅱ含Cu(NO ) 、NaNO ,加入萃取剂萃取Cu2+,可实现与Na+的分离,再经过反萃取获得Cu(NO ) 溶液,滤渣
3 2 3 3 2
Ⅱ中加入Na S O 后,AgCl转化为[Ag(S O ) ]3-,最后经过还原获得Ag单质。
2 2 3 2 3 2
【详解】(1)固体表面积、反应物浓度、温度等因素都会影响反应速率,则加快“焙烧”速率的措施:将阳极
Δ
泥粉碎或搅拌;焙烧时Cu S和O 反应生成CuO和SO ,反应的方程式Cu S+2O 2CuO+SO ;
2 2 2 2 2 2
(2)由分析知,滤渣Ⅰ的成分为Pt、Au;由于HNO 此时可能发生氧化还原反应产生氮的氧化物,通入O 可
3 2
使氮氧化物又转化为HNO 而溶解,故通入氧气的目的是防止生成的氮氧化物排放到空气中;
3
(3)证明银离子沉淀完全即检验滤液中银离子是否存在,实验操作是静置,向上层清液中滴加NaCl溶液,
若无沉淀产生,则沉淀完全;
(4)萃取后得到有机相的操作方法是分液;反萃取即使萃取平衡逆向移动,此时可向体系中加入酸,由于
最终是获得Cu(NO ) ,所以为了不引入新杂质,最好选用HNO ;
3 2 3
(5)对应反应AgCl(s)+2S 2 O 3 2-(aq) [Ag(S 2 O 3 ) 2 ]3-(aq)+Cl-(aq)平衡常数
c Cl- c AgS O 3- c Cl- ⇌ c Ag+ c AgS O 3-
K′= c2 S O2- 2 3 2 = c2 S O2- c Ag+ 2 3 2 =K sp (AgCl)K2.010103.01013 6.0103;
2 3 2 3
(6)由分析知,滤液Ⅲ中[Ag(S O ) ]3-被Na S O 还原为Ag,自身被氧化为Na SO ,根据得失电子守恒初步
2 3 2 2 2 4 2 3
配平方程式为:2[Ag(S 2 O 3 ) 2 ]3-+S 2 O2 4 -→2Ag+2SO 3 2-+4S 2 O 3 2-,结合流程知,可在左边添加4个OH-配平电荷守
恒,右边添加2个H O配平元素守恒,得完整方程式为:
2
2[Ag(S 2 O 3 ) 2 ]3-+S 2 O2 4 -+4OH-=2Ag+2SO 3 2-+4S 2 O 3 2-+2H 2 O。
50
17.【答案】(1)+247.3kJ/mol (2)① 66.7% ②0.2 12000 >
81
(3)CH -4e-+2O2-=CO +2H (4) v