文档内容
2025—2026学年第一学期10月高三三校联考
化学试卷
本试卷共8页,20小题,满分100分。考试用时75分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56 Co59
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的。
1. 文房用品是传统文化的重要组成部分。下列文房用品的主要材质属于金属材料的是
A.玉杆斗笔 B.铜质笔架 C.御制宣纸 D.五彩瓷砚
2. 广东是岭南文化的集萃地。下列有关岭南文化的说法不正确的是
A. “海丝文化”:海上丝绸贸易用于交易的银锭中存在金属键
B. “茶艺文化”:沏泡功夫茶利用了萃取原理,水作萃取剂
C. “建筑文化”:制作博古梁架时,在木材上雕刻花纹的过程主要发生化学变化
D. “戏剧文化”:现代粤剧舞台上灯光光柱的形成是因为丁达尔效应
3. 2025年7月15日,搭载天舟九号货运飞船的长征七号运载火箭在海南文昌发射升空,体现了我国强大
科技力量。下列说法正确的是
A. “天舟九号”为空间站送去电推进氙气瓶, 与 互为同位素
B. “天舟九号”配有半刚性太阳电池阵“翅膀”,工作时将化学能转化为电能
C. “长征七号”采用液氧、煤油等作为推进剂,液氧、煤油是纯净物
D. “长征七号”使用碳纤维材料减轻火箭质量,碳纤维属于有机高分子材料
4. 劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识A FeCl 溶液作腐蚀液制作印刷电路板 Fe3+氧化性强于Cu2+
3
B 用硫酸钡做钡餐检查胃病 BaSO 既不溶于水,也不溶于酸
4
C 用福尔马林制作生物标本 甲醛有强还原性
D 用84消毒液消毒
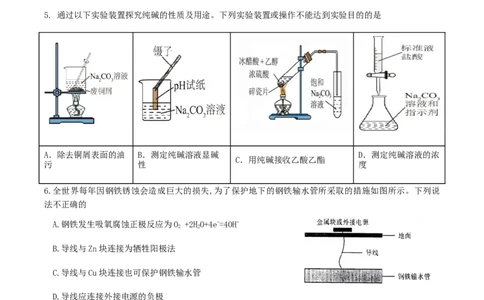
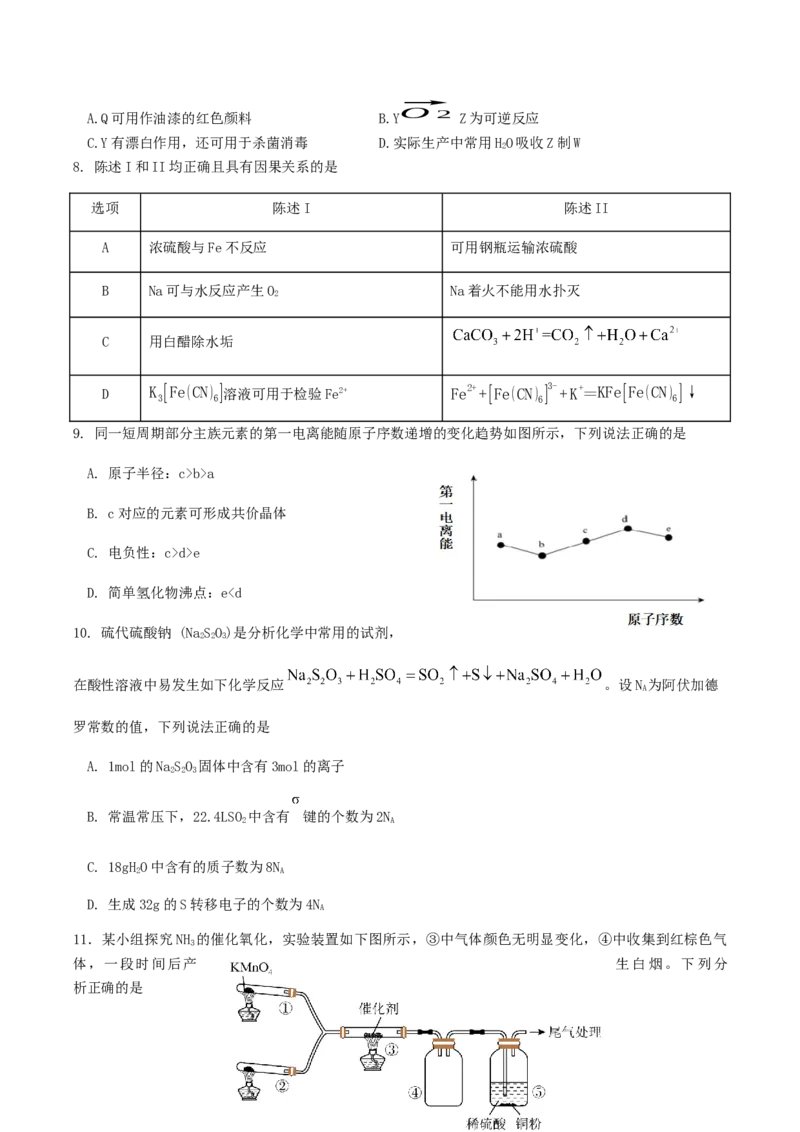
5. 通过以下实验装置探究纯碱的性质及用途。下列实验装置或操作不能达到实验目的的是
A.除去铜屑表面的油 B.测定纯碱溶液显碱 D.测定纯碱溶液的浓
C.用纯碱接收乙酸乙酯
污 性 度
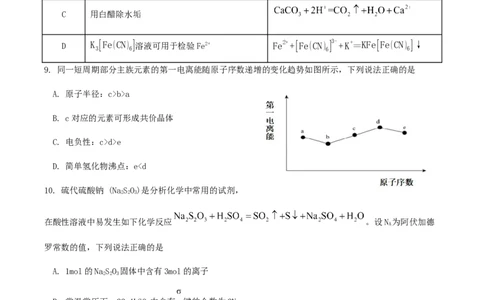
6.全世界每年因钢铁锈蚀会造成巨大的损失,为了保护地下的钢铁输水管所采取的措施如图所示。下列说
法不正确的
A.钢铁发生吸氧腐蚀正极反应为O +2HO+4e-=4OH-
2 2
B.导线与Zn块连接为牺牲阳极法
C.导线与Cu块连接也可保护钢铁输水管
D.导线应连接外接电源的负极
7.黄色固体X是一种金属矿石的主要成分,可发生如下图所示的转化关系(部分应略去反应
条件 ), 其中 Q为红棕色
固 体 ,W 是一种强酸
下列说法不正确的是A.Q可用作油漆的红色颜料 B.Y
⃗O
2 Z为可逆反应
C.Y有漂白作用,还可用于杀菌消毒 D.实际生产中常用HO吸收Z制W
2
8. 陈述I和II均正确且具有因果关系的是
选项 陈述I 陈述II
A 浓硫酸与Fe不反应 可用钢瓶运输浓硫酸
B Na可与水反应产生O Na着火不能用水扑灭
2
C 用白醋除水垢
D K [Fe(CN) ]溶液可用于检验Fe2+ Fe2++[Fe(CN) ] 3- +K+==KFe[Fe(CN) ]↓
3 6 6 6
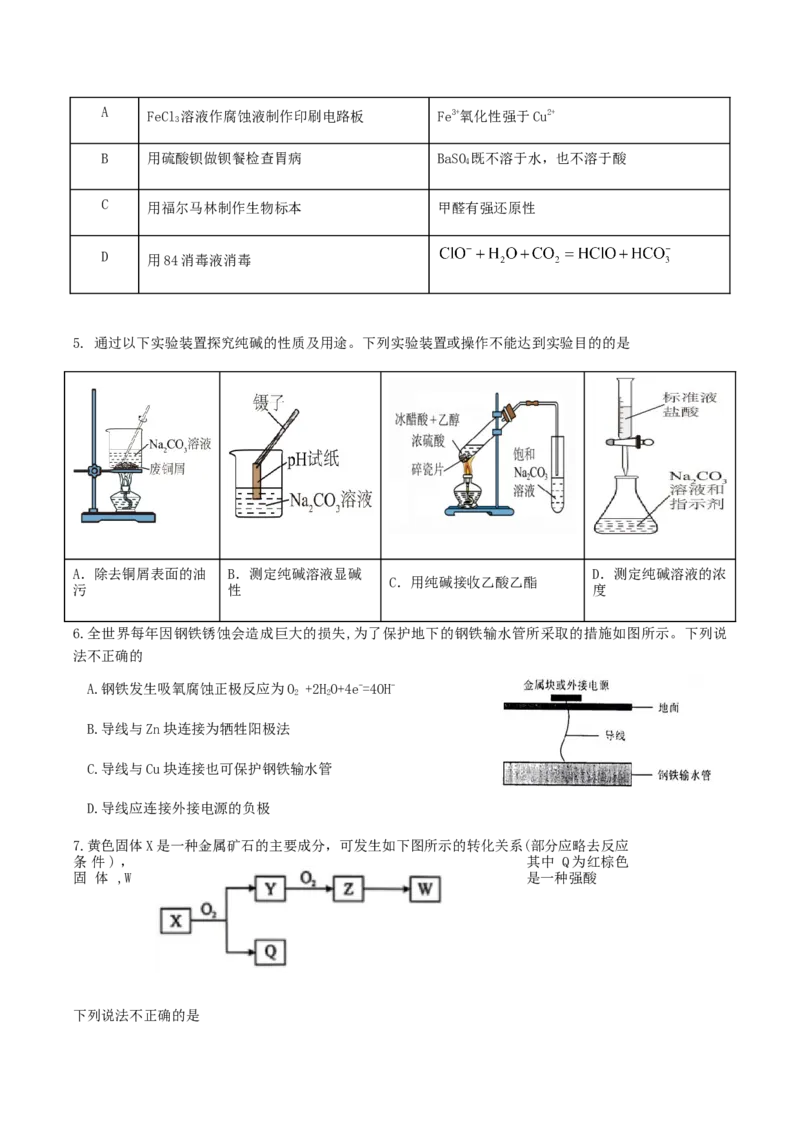
9. 同一短周期部分主族元素的第一电离能随原子序数递增的变化趋势如图所示,下列说法正确的是
A. 原子半径:c>b>a
B. c对应的元素可形成共价晶体
C. 电负性:c>d>e
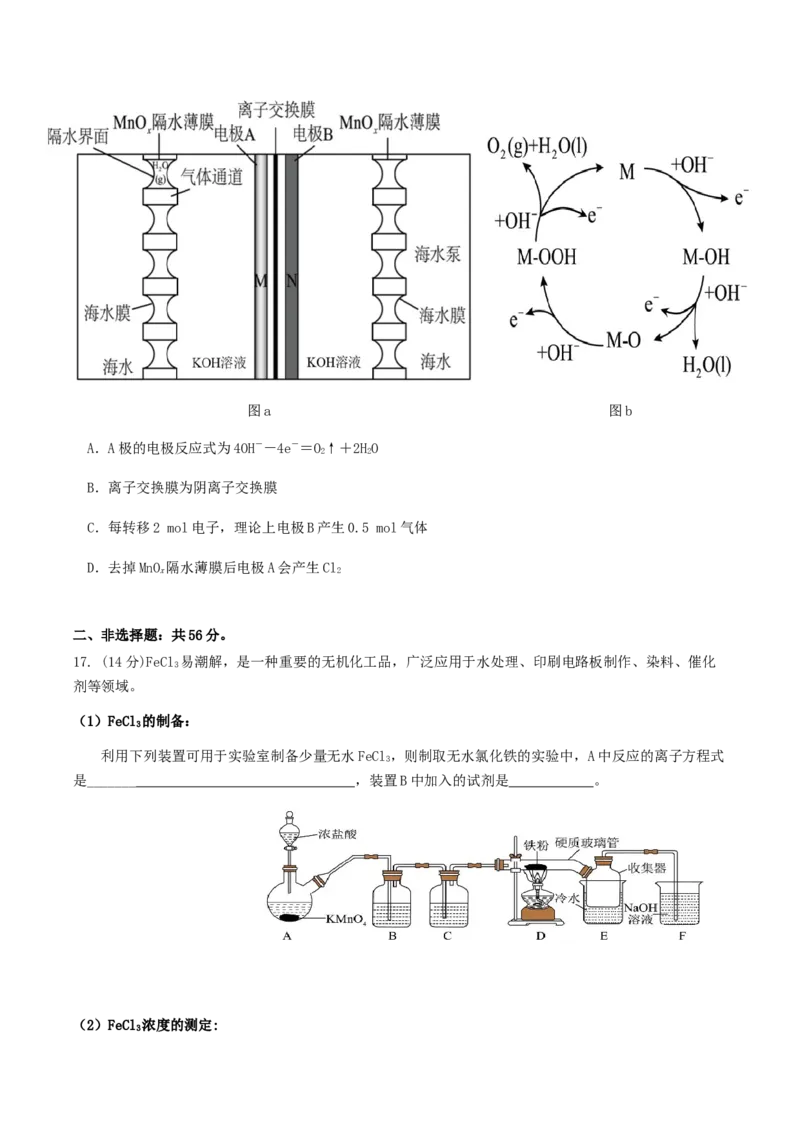
D. 简单氢化物沸点:e ClO-
iV.常温下,Ksp(CoCO)=1.6×10-13 , Ksp(CoCO)=6.3×10-8 当离子浓度≤10-5时可视为沉淀完全。
3 2 4
回答下列问题:
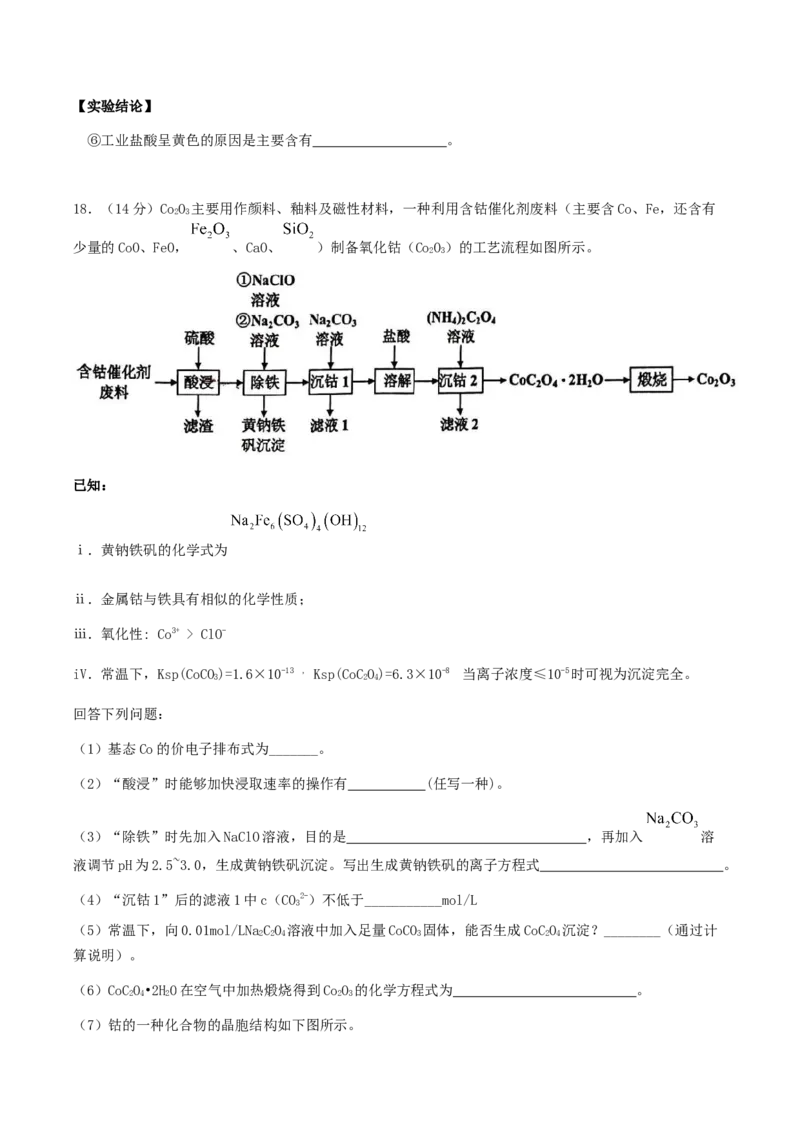
(1)基态Co的价电子排布式为_______。
(2)“酸浸”时能够加快浸取速率的操作有 (任写一种)。
(3)“除铁”时先加入NaClO溶液,目的是 ,再加入 溶
液调节pH为2.5~3.0,生成黄钠铁矾沉淀。写出生成黄钠铁矾的离子方程式 。
(4)“沉钴1”后的滤液1中c(CO2-)不低于___________mol/L
3
(5)常温下,向0.01mol/LNaCO 溶液中加入足量CoCO 固体,能否生成CoCO 沉淀?________(通过计
2 2 4 3 2 4
算说明)。
(6)CoCO•2HO在空气中加热煅烧得到CoO 的化学方程式为 。
2 4 2 2 3
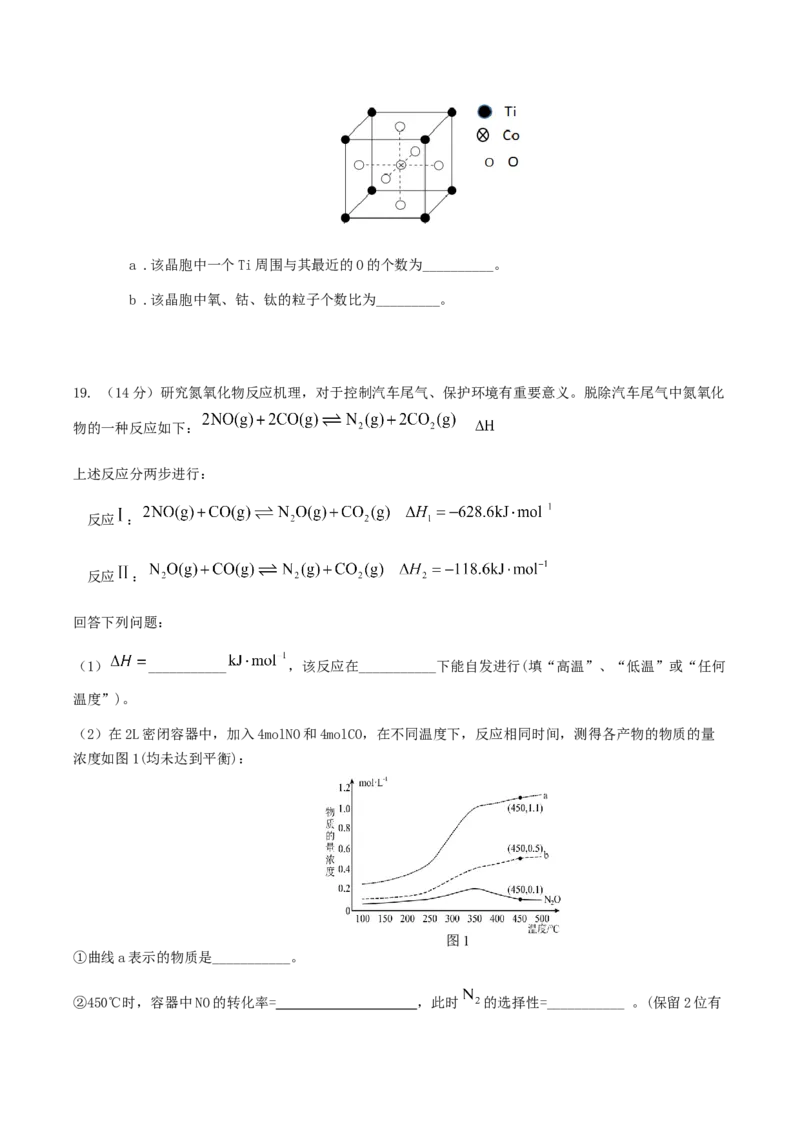
(7)钴的一种化合物的晶胞结构如下图所示。a .该晶胞中一个Ti周围与其最近的O的个数为__________。
b .该晶胞中氧、钴、钛的粒子个数比为_________。
19. (14分)研究氮氧化物反应机理,对于控制汽车尾气、保护环境有重要意义。脱除汽车尾气中氮氧化
物的一种反应如下:
上述反应分两步进行:
反应 :
反应 :
回答下列问题:
(1) ___________ ,该反应在___________下能自发进行(填“高温”、“低温”或“任何
温度”)。
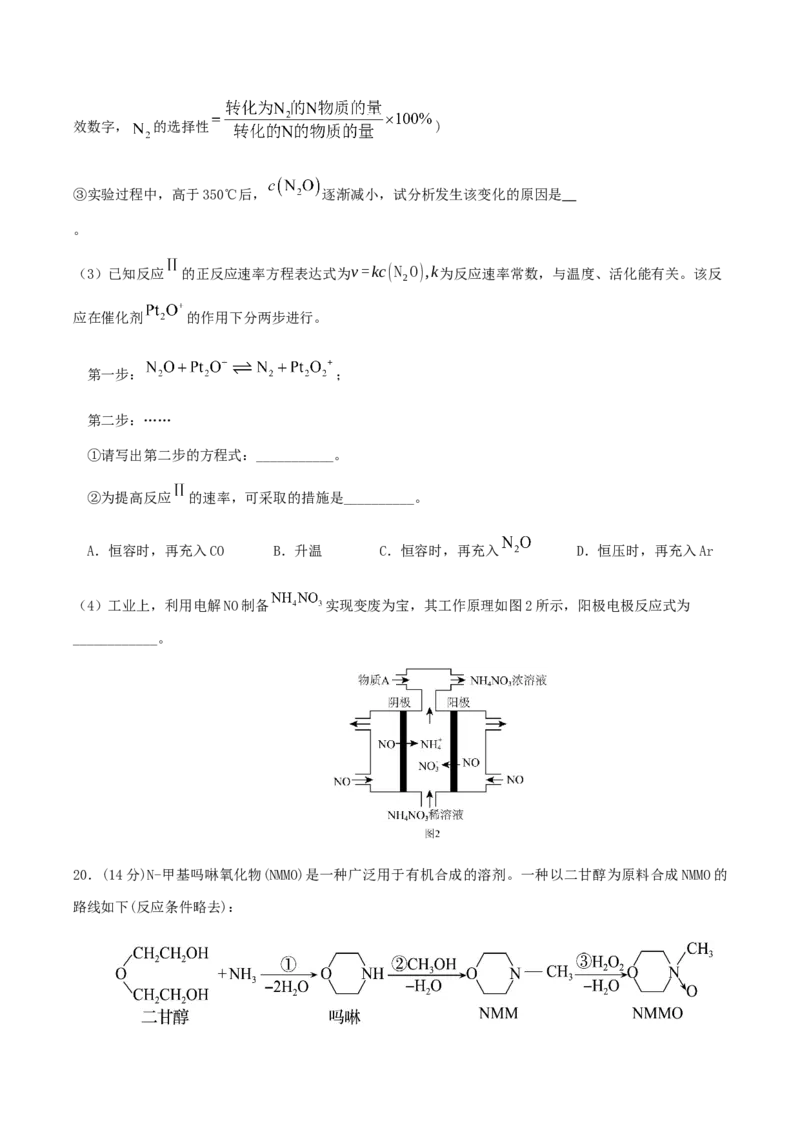
(2)在2L密闭容器中,加入4molNO和4molCO,在不同温度下,反应相同时间,测得各产物的物质的量
浓度如图1(均未达到平衡):
图1
①曲线a表示的物质是___________。
②450℃时,容器中NO的转化率= ,此时 的选择性=___________ 。(保留2位有效数字, 的选择性 )
③实验过程中,高于350℃后, 逐渐减小,试分析发生该变化的原因是
。
(3)已知反应 的正反应速率方程表达式为v=kc(N O),k为反应速率常数,与温度、活化能有关。该反
2
应在催化剂 的作用下分两步进行。
第一步: ;
第二步:……
①请写出第二步的方程式:___________。
②为提高反应 的速率,可采取的措施是__________。
A.恒容时,再充入CO B.升温 C.恒容时,再充入 D.恒压时,再充入Ar
(4)工业上,利用电解NO制备 实现变废为宝,其工作原理如图2所示,阳极电极反应式为
____________。
20.(14分)N-甲基吗啉氧化物(NMMO)是一种广泛用于有机合成的溶剂。一种以二甘醇为原料合成NMMO的
路线如下(反应条件略去):(1)二甘醇的分子式为____________,所含官能团名称为_______。
(2)吗啉的同分异构体X中含有-CONH 结构的共有 种,其中核磁共振氢谱图显示有3组峰,且
2
峰面积比为1:2:6的结构简式为
(3)下列说法不正确的是
A.在二甘醇分子中,存在手性碳原子,并有7个原子采取sp3杂化
B.吗啉易溶解于水,吗啉能与水形成分子间氢键
C.NMM所有碳原子在同一平面内
D.在反应③中,有存在σ键的断裂与形成
(4)酸碱质子理论认为:凡是能接受氢离子的分子或离子称为碱。胺类化合物中氮原子含孤电子对,氮
原子上的电子云密度越大,碱性越强。下列三种物质的碱性由强到弱的是_______(用序号表示)。
① ② ③
(5)以乙烯为含碳原料,利用①、②的反应原理,合成 。基于你设计的合成路线,回答下
列问题:
a.最后一步反应中,有机反应物是 和 (写结构简式)。
b.乙烯一步制得乙醇反应的化学方程式为________________________________________。
c. 在相关步骤中涉及二元卤代烃转化为二元醇的化学方程式为____________________(注明反应条
件)。化学参考答案
一、单项选择题:第1~10小题,每小题2分;第11~16小题,每小题4分,共44分。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
B C A C B C D D B A D B B C A C
二、非选择题:共56分。
17.(14分)
(1) 2MnO—+10Cl—+16H+=5Cl↑+2Mn2++8HO(2分) 饱和氯化钠溶液 (1分)
4 2 2
(2)①. 溶液(1分) ②. 或者 (1分)
(3)
①. 0.005 (1分)
②. (1分)
③. 10滴蒸馏水 (1分)
④. 向 溶液加入 固体,溶液黄色加深(其他合理表述也给分)
(2分)
⑤. 或 (3分)
100.01 100.01
(正确计算表达式答案给2分,如: ×104×10、 ×105等)
10−6.31 10−6.31
⑥. 主要是含有 (1分)
18.(14分)
(1) 3d7 4s2 (1分)(2)适当增大硫酸的浓度、搅拌、加热等(1分) (其他合理答案也给分)
(3)把亚铁离子氧化为铁离子(1分)
6Fe3+ + 6CO2-+ 2Na+ + 4SO2-+6HO=NaFe(SO)(OH) ↓ + 6CO↑(2分)
3 4 2 2 6 4 4 12 2
2Na++6Fe3++4SO2-+12HO=NaFe(SO)(OH) ↓+12H+ (1分)
4 2 2 6 4 4 12
(4)1.6×10-8(2分)
(5)CoCO 饱和溶液中c(Co2+)= = =4×10−7mol/L,
3
Q=c(Co2+)×c(CO2-)=4×10−7×0.01=4×10−9①>② (2分)(5) a.CHCHOH 和 (全对给1分)
3 2
b. (1分)
c. (2分)