文档内容
江西省十校协作体 2025 届高三第二次联考化学试卷
(其中:-Ph表示 ), 下列说法不正确的是( )
命题人:昌河中学 刘细莲 审题人:昌河中学 彭立红
考试时长:75 分钟 试卷分值:100 分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Fe-56 Co-59 A.该化合物中有离子键和共价键
一、单选题:本大题共14小题,共42分。
B.从化学键角度解释左侧离子带正电荷可能是因为碳-碳单电子键少了一个电子
1.2025年我国迎来了首个“非遗版”春节,央视春晚节目精彩纷呈,下列说法正确的是( )
C.该碳-碳单电子键键长应比普通碳-碳单键键长要短
A. 景德镇“春碗”:釉料中的二氧化硅是两性氧化物
D.依据价层电子对互斥理论,负离子III的中心碘原子孤电子对数为3
B.《迎福》植物染技艺使用的竹材:纤维素与淀粉互为同分异构体
6.用下列仪器或装置进行相应实验,不能达到实验目的的是( )
C. 军歌《青春奔赴》中士兵服饰材质:聚四氟乙烯(PTFE)具有极强的耐化学腐蚀性
D.《星汉耀江城》烟花:金属粉末在燃烧时会发出耀眼的光,是因为发生了焰色反应
2. 绿矾FeSO ·7H O可写成[Fe(H O) ]SO ·H O,其结构可表示为 下列
4 2 2 6 4 2
有关绿矾的说法正确的是( ) A.制备 CuSO B.制备无水FeCl
4 3
A.绿矾晶体中含有离子键、配位键、氢键等化学键 B.电负性:O>S>H>Fe
C.1个[Fe(H O) ]2+离子中有12个σ键 D.键角:SO 2— >SO
2 6 4 3
3.《哪吒 2之魔童闹海》中太乙真人使用藕粉为哪吒和敖丙重塑肉身。尼克酸是藕的主要成分之一,其结
构如图所示 与苯环相似)。下列说法错误的是( )
A. 尼克酸分子中有两个手性碳原子 B. 尼克酸的分子式为C6H5NO₂ C.除去CO
2
中少量的HCl D.可用于Cl
2
制备
C. 尼克酸的所有原子可能共平面 D. 尼克酸能发生取代、加成和氧化反应
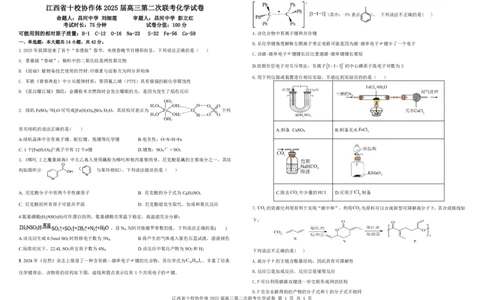
7.CO 的资源化利用有利于实现“碳中和”。利用CO 为原料可以合成新型可降解高分子P,其合成路线如
2 2
4.氨基磺酸(H2NSO3H)可作漂白助剂。氨基磺酸在常温下稳定,高温能完全分解:
下;
。设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.该反应生成0.5molSO 时转移电子数为3N B.将产生的气体通入紫色石蕊试液,溶液褪色
2 A
C.标准状况下,22.4LSO₃所含原子数为4N D.该反应中氧化产物为SO 和H
A 2 2 下列说法不正确的是( )
5.2024年《自然》杂志上报道了一种含有碳—碳单电子键的化合物,其化学式为C H I ,丰富了经典 A.高分子P的主链含酯基结构,因此具有可降解性
38 30 3
化学键理论。该物质的结构如下图,虚线和圆点表示仅有1个共用电子的键。 B.反应①是加成反应,反应②是缩聚反应
C.P可以利用碳碳双键进一步交联形成网状结构
D.P完全水解得到的产物的分子式和Y的分子式不相同
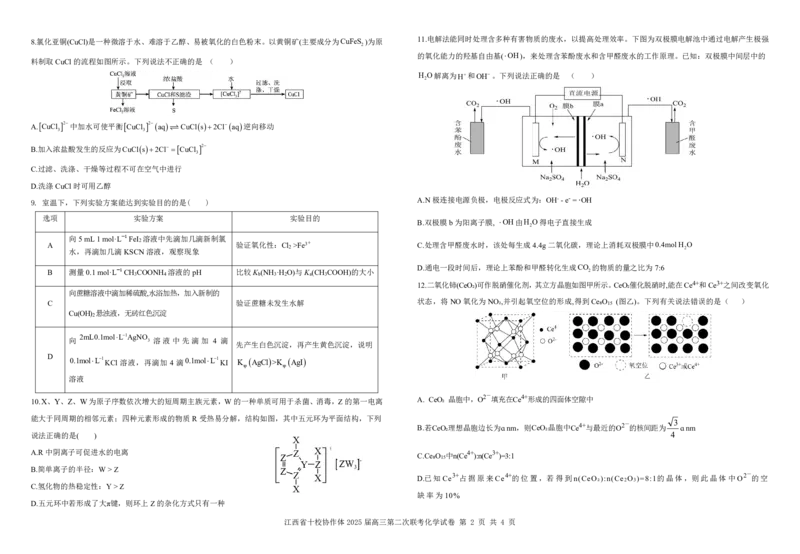
江西省十校协作体2025届高三第二次联考化学试卷 第 1 页 共 4 页8.氯化亚铜(CuCl)是一种微溶于水、难溶于乙醇、易被氧化的白色粉末。以黄铜矿(主要成分为CuFeS )为原
11.电解法能同时处理含多种有害物质的废水,以提高处理效率。下图为双极膜电解池中通过电解产生极强
2
的氧化能力的羟基自由基(OH),来处理含苯酚废水和含甲醛废水的工作原理。已知:双极膜中间层中的
料制取CuCl的流程如图所示。下列说法不正确的是 ( )
H O解离为H和OH。下列说法正确的是 ( )
2
A. CuCl 2中加水可使平衡CuCl 2aq CuCls2Claq逆向移动
3 3
B.加入浓盐酸发生的反应为CuCls2Cl CuCl 2
3
C.过滤、洗涤、干燥等过程不可在空气中进行
D.洗涤CuCl时可用乙醇
9. 室温下,下列实验方案能达到实验目的的是( )
A.N极连接电源负极,电极反应式为:OH--e-=·OH
选项 实验方案 实验目的
B.双极膜b为阳离子膜, OH由H O得电子直接生成
2
向5mL1mol·L-1FeI 溶液中先滴加几滴新制氯
2
A 验证氧化性:Cl >Fe3+ C.处理含甲醛废水时,该处每生成4.4g二氧化碳,理论上消耗双极膜中0.4molH O
水,再滴加几滴KSCN溶液,观察现象 2 2
D.通电一段时间后,理论上苯酚和甲醛转化生成CO 的物质的量之比为7:6
B 测量0.1mol·L-1CH COONH 溶液的pH 比较K (NH ·H O)与K (CH COOH)的大小 2
3 4 b 3 2 a 3
12.二氧化铈(CeO₂)可作脱硝催化剂,其立方晶胞如图甲所示。CeO₂催化脱硝时,能在Ce4+和Ce3+之间改变氧化
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的
C 验证蔗糖未发生水解 状态,将NO氧化为NO₂,并引起氧空位的形成,得到Ce₈O 15 (图乙)。下列有关说法错误的是( )
Cu(OH) 悬浊液,无砖红色沉淀
2
2mL0.1molL1AgNO
向 3 溶液中先滴加 4 滴
先产生白色沉淀,再产生黄色沉淀,说明
D
0.1molL1 KCl 溶液,再滴加 4 滴0.1molL1 KI K AgCl>K AgI
sp sp
溶液
10.X、Y、Z、W为原子序数依次增大的短周期主族元素,W的一种单质可用于杀菌、消毒,Z的第一电离 A. CeO₂ 晶胞中,O 2- 填充在Ce 4+形成的四面体空隙中
能大于同周期的相邻元素;四种元素形成的物质R受热易分解,结构如图,其中五元环为平面结构,下列
B.若CeO₂理想晶胞边长为ɑnm,则CeO₂晶胞中Ce 4+与最近的O 2- 的核间距为 3 ɑnm
说法正确的是( ) 4
A.R中阴离子可促进水的电离 C.Ce₈O 中n(Ce 4+ ):n(Ce 3+ )=3:1
15
B.简单离子的半径:W>Z
D.已知Ce 3+占据原来Ce 4+的位置,若得到n(CeO₂):n(Ce O )=8:1的晶体,则此晶体中O 2- 的空
2 3
C.氢化物的热稳定性:Y>Z
缺率为10%
D.五元环中若形成了大π键,则环上Z的杂化方式只有一种
江西省十校协作体2025届高三第二次联考化学试卷 第 2 页 共 4 页13.某试液中只可能含有K+、NH、Fe2+、Al3+、Cl-、SO2、CO2、[Al(OH) ]-中的若干种离子,离子浓度 (4)准确量取VmLc molL1NaHSO 溶液于锥形瓶中,加入mg乙醛试样,待乙醛完全反应后,再用c molL1
4 4 3 4 1 1 3 2
均为0.1mol•L-1,某同学进行了如下实验,下列说法不正确的是( )
碘标准溶液滴定过量NaHSO 溶液至终点,整个过程涉及以下反应:
3
Ⅰ:CH CHONaHSO CH CHOHSO Na;Ⅱ:NaHSO I H O 2HI NaHSO。
3 3 3 3 3 2 2 4
①滴定所用的指示剂为 (填名称),滴定终点的现象是 。
②经多次滴定,平均消耗碘标准溶液VmL,则乙醛的纯度为 (填写含c、V计算式)。
2
A.气体A遇空气变为红棕色 B.原试液中一定不含有K+
16.(14分)LiCoO (钴酸锂)难溶于水,具有强氧化性,可用作锂电池正极材料,
C.沉淀C为BaCO D.原试液中存在的阳离子有NH、Fe2+和Al3+ 2
3 4
某锂离子二次电池的正极材料主要为LiCoO ,还含有少量Al、Fe、Mn、Ni的化合物。通过如下流程利用
2
14.25℃时向10mL某浓度新制氯水中滴入0.1molL1的NaOH溶液,滴定曲线如图所示。已知次氯酸的
废旧锂离子电池制取Co O 。
3 4
电离平衡常数为K 2.5108。下列说法正确的是( )
a
A.该实验过程可以用PH试纸测量溶液的PH值
B.甲点溶液中存在:
n Cl +n HClO +n Cl- +n ClO- =0.01N →Co 3 O 4
2 A
C.丙点溶液中:c Na c Cl c ClO cHClOc H 已知:常温下,该工艺条件下,有关金属离子沉淀完全(c=1×10-5mol·L-1)的pH见下表
D.氯水中存在平衡: 离子 Co2+ Fe3+ Fe2+ Al3+ Mn2+ Ni2+
Cl aqH O1 HaqClaqHClOaq该反应的平衡常数K的数量级为10-6 pH 9.4 3.2 9.0 4.7 10.1 8.9
2 2
二、简答题:本大题共4小题,共58分。
(1)“酸浸还原”时为减少环境污染,应如何滴入Na S O 溶液? 。
2 2 3
15.(14分)某小组用40%乙醛溶液制备无水乙醛,并对乙醛的性质进行探究,设计装置如下。已知:乙醛
(2)“酸浸还原”时,LiCoO 发生的反应中氧化产物为硫酸盐的化学方程式为 。
的沸点为20.8℃,易挥发、易被氧化。回答下列问题: 2
(3)水解净化过程中生成“滤渣”的离子方程式为 。
(1)仪器N的名称是 ,M装置的作用
是 。 (4)氧化沉铁锰:若浸取液中c Co2 0.1molL1,为使钴不损失,则常温下须调节溶液pH不大于 ;
(2)实验时水浴温度超过40℃,乙醛溶液才开始沸腾, 在调好pH后,加入NaClO溶液,随着锰和铁的沉淀率逐渐增大,钴的损失量也随之增大,可能的原因
试从结构的角度分析该温度明显高于乙醛沸点的主要 是 。
原因可能是 。 (5)萃取、反萃取:该工艺设计萃取、反萃取的目的是 。
(3)向溴水中滴加足量的乙醛溶液,观察到溴水褪色,
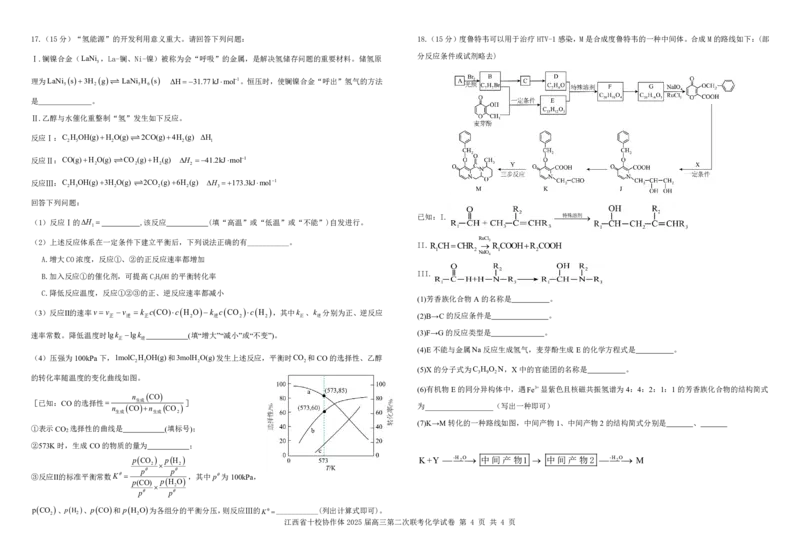
(6)制Co O :CoC O 2H O在空气中加热时固体残留物质质量与
3 4 2 4 2
该反应的化学方程式为 。
温度关系如右图所示,写出900°C时,残留固体的化学式为______。
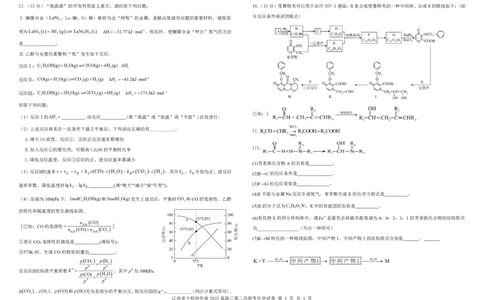
江西省十校协作体2025届高三第二次联考化学试卷 第 3 页 共 4 页17.(15分)“氢能源”的开发利用意义重大。请回答下列问题: 18.(15分)度鲁特韦可以用于治疗HTV-1感染,M是合成度鲁特韦的一种中间体。合成M的路线如下:(部
分反应条件或试剂略去)
Ⅰ.镧镍合金(LaNi ,La-镧、Ni-镍)被称为会“呼吸”的金属,是解决氢储存问题的重要材料。储氢原
5
理为LaNi s3H g LaNi H s ΔH31.77kJmol1。恒压时,使镧镍合金“呼出”氢气的方法
5 2 5 6
是 。
Ⅱ.乙醇与水催化重整制“氢”发生如下反应。
反应Ⅰ:C H OH(g)H O(g)2CO(g)4H (g) ΔH
2 5 2 2 1
反应Ⅱ:CO(g)H O(g) CO (g)H (g) H 41.2kJmol1
2 2 2 2
反应Ⅲ:C H OH(g)3H O(g) 2CO (g)6H (g) H 173.3kJmol1
2 5 2 2 2 3
回答下列问题:
已知:I. 特殊溶剂
(1)反应Ⅰ的H ,该反应 (填“高温”或“低温”或“不能”)自发进行。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。 RuCl 3
II.RCHCHR RCOOHR COOH
1 2 1 2
NaIO
4
A.增大CO浓度,反应①、②的正反应速率都增加
III.
B.加入反应①的催化剂,可提高CHOH的平衡转化率
2 5
C.降低反应温度,反应①②③的正、逆反应速率都减小
(1)芳香族化合物A的名称是 。
(3)反应Ⅱ的速率v v
正
v
逆
k
正
c(CO)c H
2
O k
逆
c CO
2
c H
2
,其中k
正
、k
逆
分别为正、逆反应
(2)B→C的反应条件是 。
速率常数。降低温度时lgk lgk (填“增大”“减小”或“不变”)。
(3)F→G的反应类型是 。
正 逆
(4)E不能与金属Na反应生成氢气,麦芽酚生成E的化学方程式是 。
(4)压强为100kPa下,1molC H OH(g)和3molH O(g)发生上述反应,平衡时CO 和CO的选择性、乙醇
2 5 2 2
(5)X的分子式为C H O N,X中的官能团的名称是 。
3 9 2
的转化率随温度的变化曲线如图。
(6)有机物E的同分异构体中,遇Fe3+显紫色且核磁共振氢谱为4:4:2:1:1的芳香族化合物的结构简式
n CO
[已知:CO的选择性
n CO
生
成
n CO
]
为__________________(写出一种即可)
生成 生成 2
(7)K→M转化的一种路线如图,中间产物1、中间产物2的结构简式分别是 、
①表示CO 选择性的曲线是 (填标号);
2
②573K时,生成CO的物质的量为 ;
pCO pH K+Y -H 2 O 中间产物1 中间产物2 -H 2 O M
2 2
p p
③反应Ⅱ的标准平衡常数K ,其中 p为100kPa,
p(CO)
pH O
2
p p
pCO
2
、pH
2
、pCO和 pH
2
O为各组分的平衡分压,则反应Ⅲ的 K ___________(列出计算式即可)。
江西省十校协作体2025届高三第二次联考化学试卷 第 4 页 共 4 页