文档内容
河北省唐山市2025-2026学年高三上学期开学考试化学试题
本试卷共8页,18小题,满分100分。考试时长75分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 N-14 O-16 Mg-24 S-32 Mn-55 Bi-209
第I卷(选择题共42分)
一、选择题(共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一个选项符合题
意。)
1.评剧,又称“唐山落子”,是中国五大戏曲剧种之一。戏曲演员用“油彩”化妆,下列制作“油彩”的
原料中,主要成分属于无机物的是
A.植物油,如麻油、菜油、豆油,赋予油彩良好的流动性
B.颜料,如天然矿石粉、金属氧化物,为脸谱提供丰富的色彩
C.香料,如沉香、檀香、丁香,改善油彩气味,掩盖颜料的异味
D.添加剂,如牛胆汁、醋,调整油彩的酸碱度,确保油彩长时间使用
2.实验室中,下列试剂保存方法正确的是
A.新制氯水保存在棕色细口试剂瓶中 B.液溴加水封保存在广口试剂瓶中
C.高锰酸钾与乙醇存放在同一药品柜中 D.金属锂保存在盛有煤油的广口试剂瓶中
3.下列高分子材料由缩聚反应获得的是
A.聚乙烯保鲜膜 B.丁苯橡胶 C.尼龙-66 D.ABS工程塑料
4.下列化学用语表述正确的是
A.基态Si原子的价层电子轨道表示式: B.顺-2-丁烯的结构式:
C. 的电子式: D. 的价层电子对互斥模型:
5.镁及其化合物的转化关系如下图所示,设 为阿伏加德罗常数的值。下列说法正确的是
A. 含中子数B.标准状况下, 中 键数目为
C.反应①中,每生成 ,转移电子数
D.常温下 的 溶液中,由水电离的 数目为
6.茚三酮可作为分析反应探针检测氨基酸,由肉桂酸制备茚三酮的路线如下:
下列有关说法正确的是
A.茚三酮的分子式为 B.1mol肉桂酸分子最多能消耗
C.中间产物X可发生消去反应 D.中间产物Z中所有原子可能共平面
7.如图所示装置(加热、除杂和尾气处理装置任选),不能完成相应气体的制备和检验的是
A.电石与饱和食盐水 B.过氧化钠和水
C. 与浓盐酸 D. 固体和 的浓硫酸
8.物质结构决定性质,下列物质性质差异与解释不相符的是
选项 性质差异 解释
A 非金属性:
沸点:
B 键能:
热稳定性:
C 硬度:金刚石>晶体硅 原子半径:
D
在 中的溶解度: 分子极性:
9.下列实验操作及现象能得出相应结论的是
选项 实验操作及现象 结论
A 向盛有淀粉溶液的试管中加适量稀硫酸,加热,冷却后加NaOH溶液至 淀粉已经完全水解
䂸性,再加入少量碘水,溶液未变蓝
B
向盛有久置 溶液的试管中加入KSCN溶液,溶液变红 已经完全变质
C
向盛有 溶液的试管中滴加溶液,产生白色沉淀,振荡试管,再滴加
溶液,有黄色沉淀生成
D
向盛有 的恒压密闭容器中充入一定量的 化学平衡向 浓度
减小的方向移动
,最终颜色变浅
10.短周期非金属主族元素W、X、Y、Z原子序数依次增大,Y的s轨道电子数等于p轨道电子数,Z的第一
电离能小于其同周期相邻元素,且W、X、Y的未成对电子数之和等于Z的价电子数。下列说法正确的是
A.原子半径: B.电负性:
C.第一电离能: D.简单氢化物的键角:
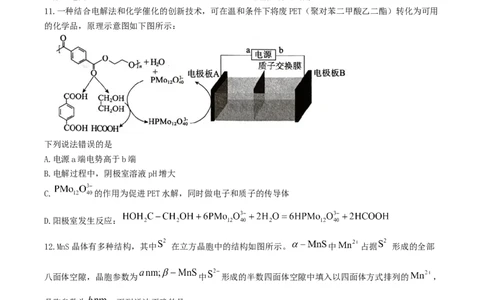
11.一种结合电解法和化学催化的创新技术,可在温和条件下将废PET(聚对苯二甲酸乙二酯)转化为可用
的化学品,原理示意图如下图所示:
下列说法错误的是
A.电源a端电势高于b端
B.电解过程中,阴极室溶液pH增大
C. 的作用为促进PET水解,同时做电子和质子的传导体
D.阳极室发生反应:
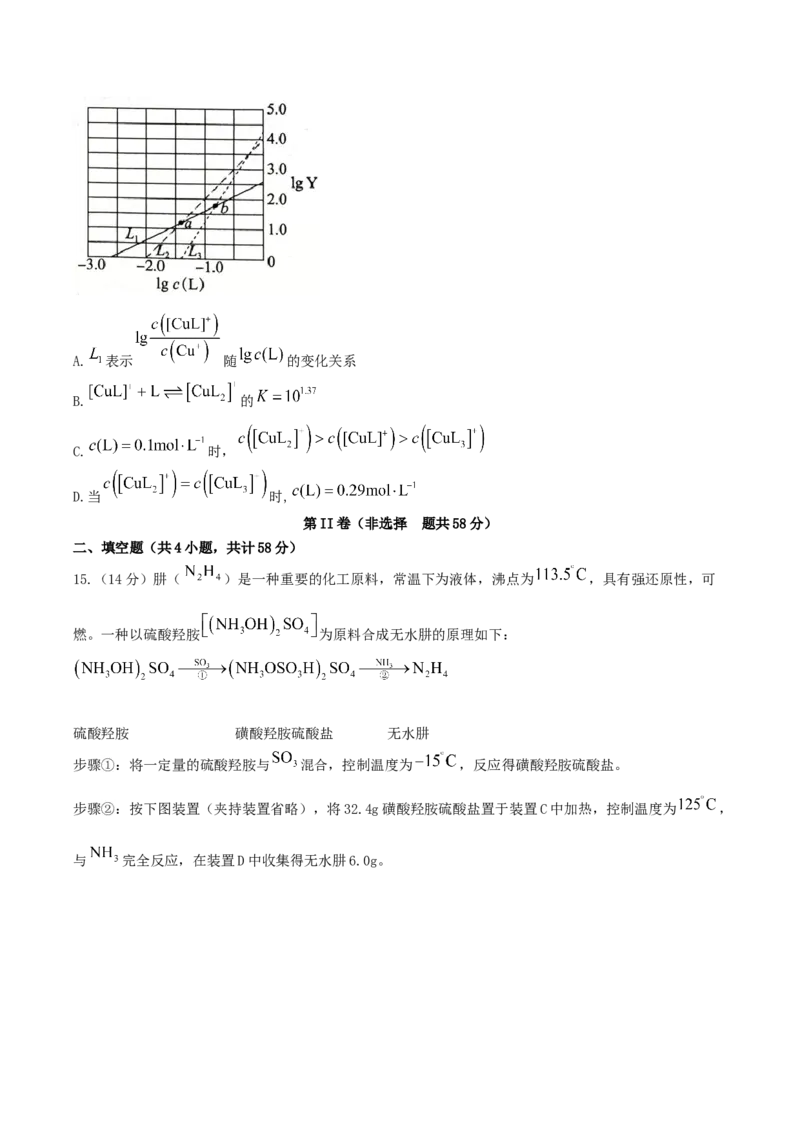
12.MnS晶体有多种结构,其中 在立方晶胞中的结构如图所示。 中 占据 形成的全部
八面体空隙,晶胞参数为 中 形成的半数四面体空隙中填入以四面体方式排列的 ,
晶胞参数为 。下列说法正确的是
A. 与 互为同素异形体B. 晶胞中,与 距离最近的 个数为12
C. 晶胞中, 之间的最短距离为
D. 晶体与 晶体的密度之比为
13.乙烯是一种重要的化工原料。乙炔电催化制乙烯的反应历程如图所示(*表示吸附态)。
下列说法错误的是
A.该反应的控速步骤为
B. 中 的作用是与 生成
C. 中断裂 键吸收的能量小于生成 键释放的能量
D.总反应方程式为:
14.已知 和L可形成三种配离子 和 ,常温下 表示
或 随 的变化关系如图所示,其中a、b两点坐标分别为
。下列说法错误的是A. 表示 随 的变化关系
B. 的
C. 时,
D.当 时,
第II卷(非选择 题共58分)
二、填空题(共4小题,共计58分)
15.(14分)肼( )是一种重要的化工原料,常温下为液体,沸点为 ,具有强还原性,可
燃。一种以硫酸羟胺 为原料合成无水肼的原理如下:
硫酸羟胺 磺酸羟胺硫酸盐 无水肼
步骤①:将一定量的硫酸羟胺与 混合,控制温度为 ,反应得磺酸羟胺硫酸盐。
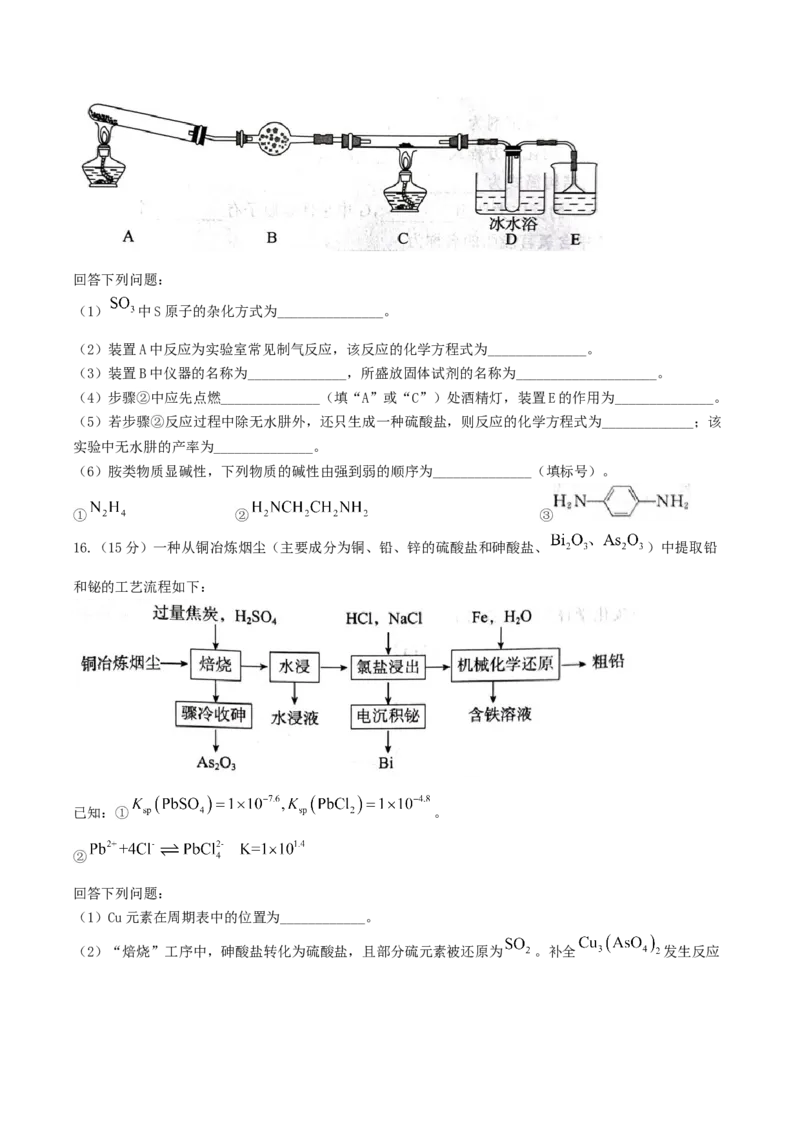
步骤②:按下图装置(夹持装置省略),将32.4g磺酸羟胺硫酸盐置于装置C中加热,控制温度为 ,
与 完全反应,在装置D中收集得无水肼6.0g。回答下列问题:
(1) 中S原子的杂化方式为_______________。
(2)装置A中反应为实验室常见制气反应,该反应的化学方程式为______________。
(3)装置B中仪器的名称为______________,所盛放固体试剂的名称为____________________。
(4)步骤②中应先点燃______________(填“A”或“C”)处酒精灯,装置E的作用为______________。
(5)若步骤②反应过程中除无水肼外,还只生成一种硫酸盐,则反应的化学方程式为_____________;该
实验中无水肼的产率为______________。
(6)胺类物质显碱性,下列物质的碱性由强到弱的顺序为______________(填标号)。
① ② ③
16.(15分)一种从铜冶炼烟尘(主要成分为铜、铅、锌的硫酸盐和砷酸盐、 )中提取铅
和铋的工艺流程如下:
已知:① 。
②
回答下列问题:
(1)Cu元素在周期表中的位置为____________。
(2)“焙烧”工序中,砷酸盐转化为硫酸盐,且部分硫元素被还原为 。补全 发生反应的化学方程式: ___________+____________
___________+____________+___________ ____________。
(3)对水浸液电解,可提取铜、锌,电解余液可在“__________________”工序循环利用。
(4)“氯盐浸出”序中, 生成 的离子方程式为_______________;反应
的化学平衡常数 _______________(填数值);NaCl浓度与铅、铋的浸出率关系如
下表所示:
Bi浸出率 Pb浸出率
NaCl浓度
50
150
250
实际生产中,常选择NaCl浓度______________ 为宜。
(5)“电沉积铋”工序中,若阴极生成Bi41.8g,则阳极理论上生成气体的体积为______________L(标
准状况下)。
(6)机械化学还原的主要机制是:机械力的引入可以实现颗粒细化和复杂结构的解离,改变了 和
的反应活性,实现增强还原反应的目的。与传统的焦炭还原相比,其优点是______________。
17.(14分)乙胺是一种重要的有机化工原料。乙腈催化加氢是工业上制备乙胺的重要方法:
。
(1)按化学计量系数比投料,固定平衡转化率 ,探究压强与温度的关系如图。
①转化率 由大到小的顺序为_____________;原因是_____________。
② _____________0(填“>”、“<”或“=”),该反应可在_____________(填“低温”、“高温”
或“任意温度”)下自发进行。(2) 时,该反应以物质的量分数表示的平衡常数 。维持压强 ,按化学计量系数比投料
和 ,发生反应。
①下列说法能说明反应达到平衡状态的是___________(填字母)。
a. 的物质的量分数不变
b.
c. 的物质的量之比为1:2:1
② 为以平衡分压表示的平衡常数(分压=总压 物质的量分数),则 ______________________
(用含 的代数式表示)。
③若 ,则 _________________MPa。
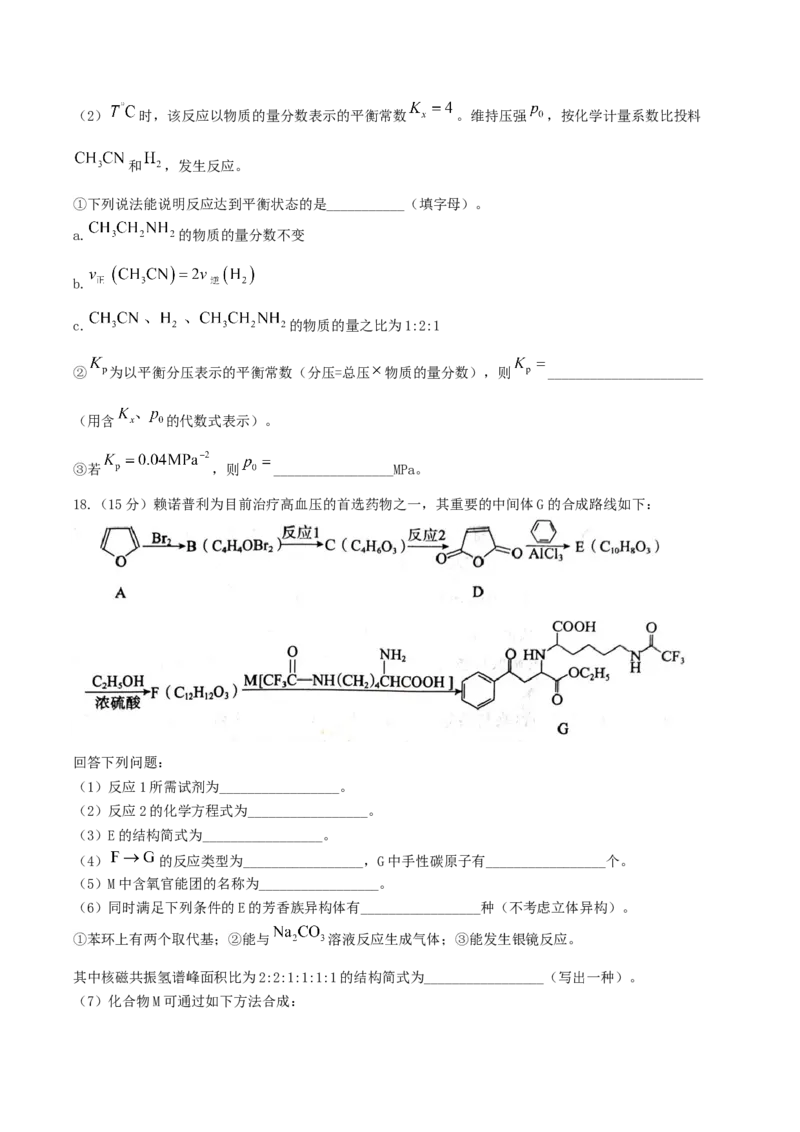
18.(15分)赖诺普利为目前治疗高血压的首选药物之一,其重要的中间体G的合成路线如下:
回答下列问题:
(1)反应1所需试剂为_________________。
(2)反应2的化学方程式为_________________。
(3)E的结构简式为_________________。
(4) 的反应类型为_________________,G中手性碳原子有_________________个。
(5)M中含氧官能团的名称为_________________。
(6)同时满足下列条件的E的芳香族异构体有_________________种(不考虑立体异构)。
①苯环上有两个取代基;②能与 溶液反应生成气体;③能发生银镜反应。
其中核磁共振氢谱峰面积比为2:2:1:1:1:1的结构简式为_________________(写出一种)。
(7)化合物M可通过如下方法合成:化合物L的结构简式为_________________唐山市2025—2026学年度高三年级摸底演练
化学评分细则
1 2 3 4 5 6 7 8 9 10 11 12 13 14
B A C B D C A A C D B B C D
15.(14分)(1) (1分)
(2) (2分)
无加热符号扣1分,气体符号可不做要求
(3)球形干燥管(1分)答案唯一 有错不得分
碱石灰(1分)其它合理答案(如氧化钙、氢氧化钠)给分,写化学式不得分
(4)A(2分)注意区分A和a 尾气处理,吸收 (1分)合理表述可给分
(5) (2分)无加热符号扣1分
(2分)准确数值,答案唯一
(6)②>①>③(2分)不写“>”但顺序正确给分
16.(15分)(1)第四周期IB族(1分)
(2) (2分)
本题物质及系数正确给分,出现错误0分。
(3)焙烧(2分)答案唯一 有错不得分
(4) (2分)答案唯一 有错不得分
(2分)数值正确即可给分 150(2分)数值正确即可给分
(5)6.72(2分)数值正确即可给分
(6)条件温和,能耗低;减少碳氧化物、硫氧化物的排放(2分)合理表述可给分
17.(14分)
(1)① (2分)由小到大不得分 该反应为气体体积减小的反应,温度相同时,增大压强,
平衡正向移动,平衡转化率增大(2分)合理表述可酌情给分
②<(2分)“小于”不给分 低温(2分)答案唯一有错不得分
(2)①ac(2分)漏选得1分,有错不得分,注意区分大小写
② (2分) ③10(2分)答案唯一18.(15分)(1)NaOH水溶液(1分)NaOH醇溶液不得分
(2) (2分)
不写条件或条件错误扣1分
(3) (2分)不写键线式,且书写正确也给分
(4)加成反应(1分) 2(1分)“两”等合理答案可给分
(5)酰胺基、羧基(2分)漏写得1分,有错不得分
(6)12(2分) 或 (2分,其他合理答案也给分)不写键线式,且书写正确也给分
(7) (2分)或 名称不得分