文档内容
2025届高三年级第三次质量检测
化学
注意事项:
1 .本试卷共两大题,18小题,考试时间75分钟,满分100分。
2 .答题前,考生先将条形码粘贴在“贴条形码区”并将本人学校、班级、姓名、考号、考场和
座号填写在相应位置。
3 .答题时,必须使用0. 5毫米的黑色墨水签字笔书写;作图时,可用2B铅笔,笔迹要清晰;
选择题填涂时,必须用2B铅笔按图示规范填涂。
4 .严格按题号所示的答题区域内作答,超出答题区域的答案无效;在草稿纸、试卷纸上答
题无效。
可能用到的相对原子质■:H-l C-12 N-14 0-16 S-32 Fe—56 Zn-65
一、选择题(共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1 .河南省作为文物大省,出土了大量珍贵文物。下列文物中,主要材质属于合金的是
2 .家务劳动中蕴含着丰富的化学知识。下列相关解释错误的是
A.用小苏打作膨松剂加工面包:碳酸钠可与酸反应
B.用白醋清洗水壶中的水垢:乙酸具有酸性
C.用纯碱清洗厨房油污:油脂在碱性环境下可水解
D.用84消毒液对桌椅消毒:含氯消毒剂具有氧化性
3.关于反应Cl2 + 2NaOH - NaCl+NaClO+H2。,下列图示或化学用语错误的是
a,基态Na原子轨道表示式:GEGELtlMfflEp
Is 2s 2p 3s
B.CI2中共价键的电子云轮廓图:
做凡0的空间填充模型:©
b.NaCl固体溶解形成的水合离子: 用整
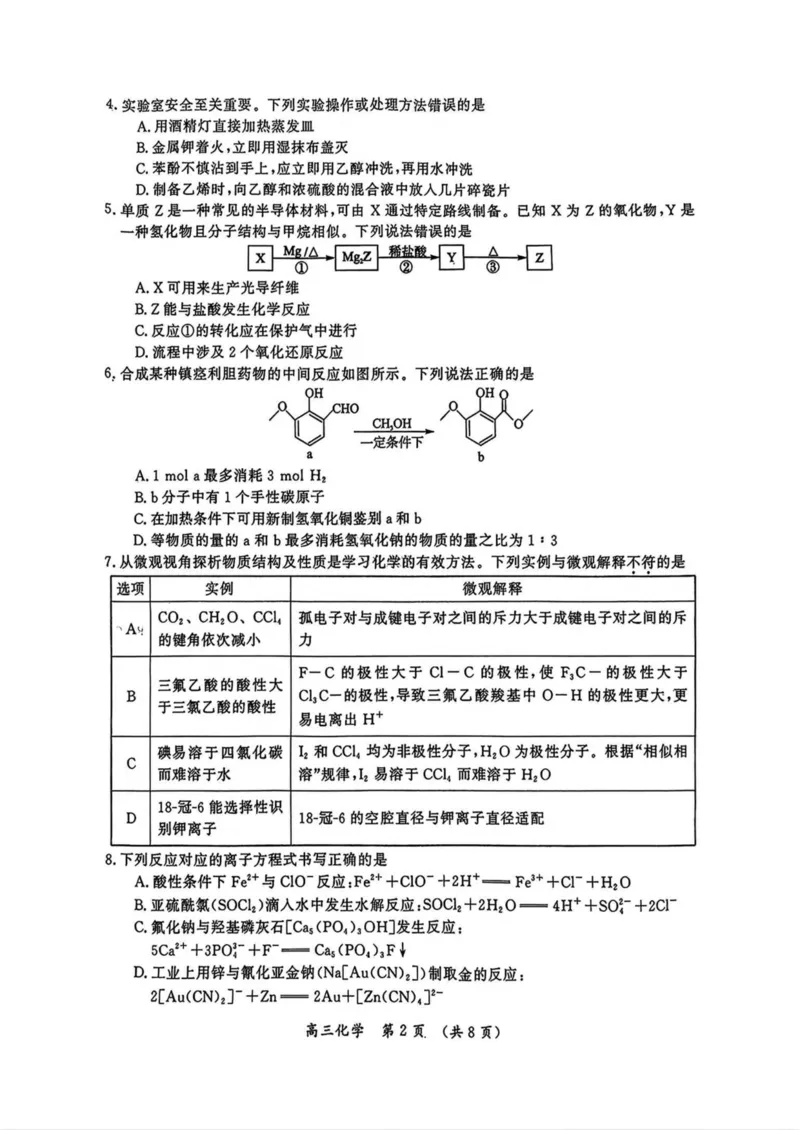
高三化学)第1页(共8页)4 .实验室安全至关重要。下列实验操作或处理方法错误的是
A.用酒精灯直接加热蒸发皿
B.金属钾着火,立即用湿抹布盖灭
C.苯酚不慎沾到手上,应立即用乙醇冲洗,再用水冲洗
D.制备乙烯时,向乙醇和浓硫酸的混合液中放入几片碎瓷片
5 .单质Z是一种常见的半导体材料,可由X通过特定路线制备。已知X为Z的氧化物,Y是
一种氢化物且分子结构与甲烷相似。下列说法错误的是
X Mg/a 稀卷酸 △ z
① ② ③
A.X可用来生产光导纤维
B.Z能与盐酸发生化学反应
C.反应①的转化应在保护气中进行
D.流程中涉及2个氧化还原反应
6,合成某种镇痉利胆药物的中间反应如图所示。下列说法正确的是
A.l mol a 最多消耗 3 mol H2
B.b分子中有1个手性碳原子
C.在加热条件下可用新制氢氧化铜鉴别a和b
D.等物质的量的a和b最多消耗氢氧化钠的物质的量之比为1 : 3
7.从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与微观解释不符的是
* ♦
选项 实例 微观解释
CO2,网0、CCI4 孤电子对与成键电子对之间的斥力大于成键电子对之间的斥
,、Au
的键角依次减小 力
F-C的极性大于C1-C的极性,使F3c一的极性大于
三氟乙酸的酸性大
B ChC—的极性,导致三氟乙酸竣基中O-H的极性更大,更
于三氯乙酸的酸性
易电离出H+
碘易溶于四氯化碳 12和CC14均为非极性分子,乩0为极性分子。根据“相似相
C
而难溶于水 溶”规律儿易溶于CC14而难溶于H2O
18-冠-6能选择性识
D 18-冠-6的空腔直径与钾离子直径适配
别钾离子
8.下列反应对应的离子方程式书写正确的是
A.酸性条件下 Fe?+与 C1CF 反应:Fe2++CKT+2H+- Fe3++Cr+H2O
B.亚硫酰氯(SOC。)滴入水中发生水解反应:SOC12+2H2O- 4H+ +SO「+2CP
C,氟化钠与羟基磷灰石KX (PO4 % OH1发生反应:
5Ca2+ +3PO: +F-— Ca5(PO4)3F I
D.工业上用锌与假化亚金钠(Na[Au(CN)21)制取金的反应:
2[Au(CN)2]-+Zn=_ 2Au+[Zn(CN) j-
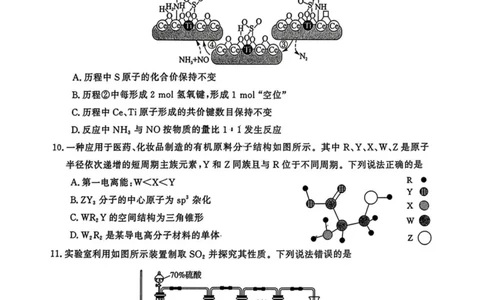
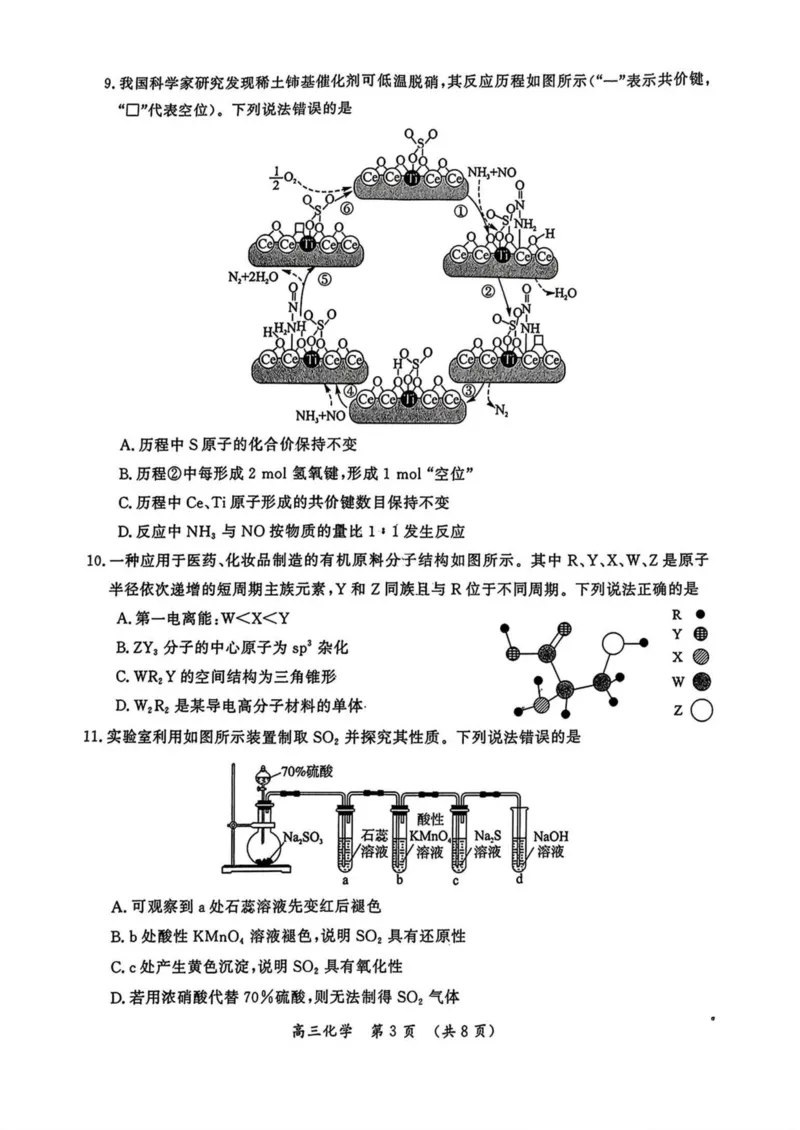
高三化学第2页,(共8页)9.我国科学家研究发现稀土锦基催化剂可低温脱硝,其反应历程如图所示(“一”表示共价犍,
“口”代表空位)。下列说法错误的是
A.历程中S原子的化合价保持不变
B.历程②中每形成2 mol氢氧键,形成1 mol “空位”
C历程中Ce、Ti原子形成的共价键数目保持不变
D.反应中NH3与NO按物质的量比1 : 1发生反应
10. 一种应用于医药、化妆品制造的有机原料分子结构如图所示。其中R、Y、X、W、Z是原子
半径依次递增的短周期主族元素,Y和Z同族且与R位于不同周期。下列说法正确的是
A.第一电离能:WVXVY
B.ZY3分子的中心原子为sp3杂化
C. WR? Y的空间结构为三角锥形
D. W2R2是某导电高分子材料的单体•
”.实验室利用如图所示装置制取SO2并探究其性质。下列说法错误的是
A.可观察到a处石蕊溶液先变红后褪色
B.b处酸性KMnO4溶液褪色,说明SO2具有还原性
C. c处产生黄色沉淀,说明SO2具有氧化性
D.若用浓硝酸代替70%硫酸,则无法制得SO2气体
9
高三化学第3页(共8页)12.摄取一定域的浪酸盐会使人出现恶心、腹泻等症状。某科研团队设计在RuCu/CNT上电
A.电子流向:M-Pf电解质溶液fR—N
B. P极上的电极反应式为BrO; +6e- +6H+— Br" +3H2O
C.若电源为铅蓄电池,则N极为Pb电极
D.每处理1 mol BrO;,理论上阳极区溶液质量减少48 g
13.利用测压法在刚性反应器中研究30C时N2O5S)分解反应:
2NA(g)——-4NO2(g) + 02(g)
11
2NA(g)
其中N02二聚为N2O4的反应可、以迅速达到平衡。体系的总压强p随时间t的变化如
下表所示0=8时,NzOKg)完全分解
i/min 0 30 60 120 - 200 1200 1500 00
//kPa 32.5 37,2 39.8 43.6 46.8 58.5 59.6 60.8
下列说法正确的是
A.。〜30 min 内,十(明()5)21. 6X10-3 kPa • min-1
B. 30℃ 时,反应4 0, (g) - 2NO2 (g)的平衡常数 K「= 10. 2 kPa
C.若提高反应温度至40℃,则NzOs(g)完全分解后体系压强/>oo(40℃)<60.8 kPa
D.研究表明,、。5兔)分解的反应速率。= 1.8X1O-3X />(N2O5) (kPa • min-1),
£ = 50 min 时,测得体系中 />(O2)=2,2 kPa,则此时 0506 kPa ・ min-1
14.常温下,用0.2 mol・L-1盐酸滴定25. 00 mL 0.2 mol・L-1NH3・H2。溶液,所得溶液
pH、NHj和N% -凡0的分布分数占[平衡时某含氮微粒的浓度占含氮微粒总浓度的分
黑 乩要
・
数,如NH'的分布分数孔NH[)= “N*% 与滴加盐酸体积的关系
如图所示。下列说法正确的是
A.曲线c代表三NH:)
B. M点加入盐酸体积为12. 5 mL
C. NH3 • H2O的电离常数的数量级为10-5
D.应选酚醐作为指示剂,滴定终点溶液由红色变为无色
高三化学第4页(共8页)二、非选择题(共4小题,58分)
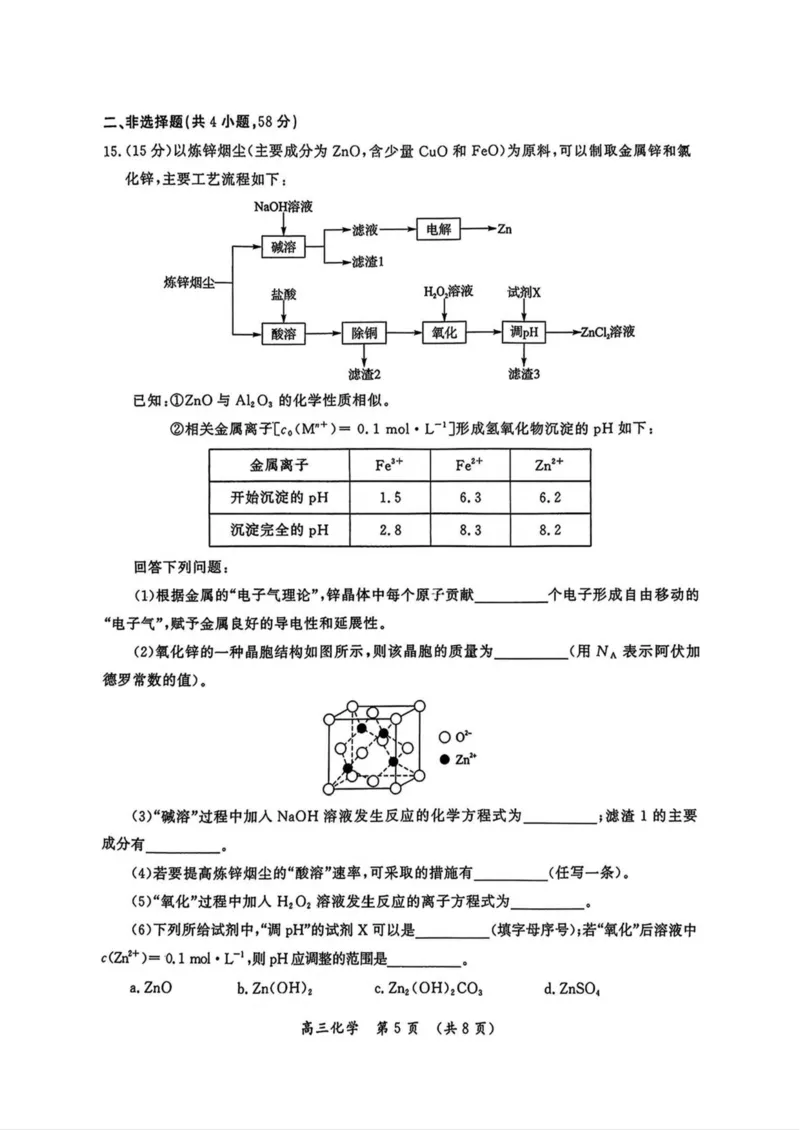
15.(15分)以炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,可以制取金属锌和氯
化锌,主要工艺流程如下:
滤渣2 滤渣3
已知:①ZnO与AI2O3的化学性质相似。
②相关金属离子[c0(M"+)= 0. 1 mol - L-叮形成氢氧化物沉淀的pH如下:
金属离子 Fe3+ Fe*+ Zn2+
开始沉淀的pH 1.5 6.3 6.2
沉淀完全的pH 2.8 8.3 8.2
回答下列问题:
(1)根据金属的“电子气理论”,锌晶体中每个原子•贡献 个电子形成自由移动的
“电子气”,赋予金属良好的导电性和延展性。
(2)氧化锌的一种晶胞结构如图所示,则该晶胞的质量为(用Na表示阿伏加
德罗常数的值)。
(3)“碱溶”过程中加入NaOH溶液发生反应的化学方程式为;滤渣1的主要
成分有 0
(4)若要提高炼锌烟尘的“酸溶”速率,可采取的措施有(任写一条)。
(5)“氧化”过程中加入H2O2溶液发生反应的离子方程式为。
(6)下列所给试剂中,“调pH”的试剂X可以是(填字母序号);若“氧化”后溶液中
c(Zn2+)= 0.1 mol • L_1,则pH应调整的范围是 o
a. ZnO b. Zn(OH)2 c. Zn2 (OH)2CO3 d. ZnSO4
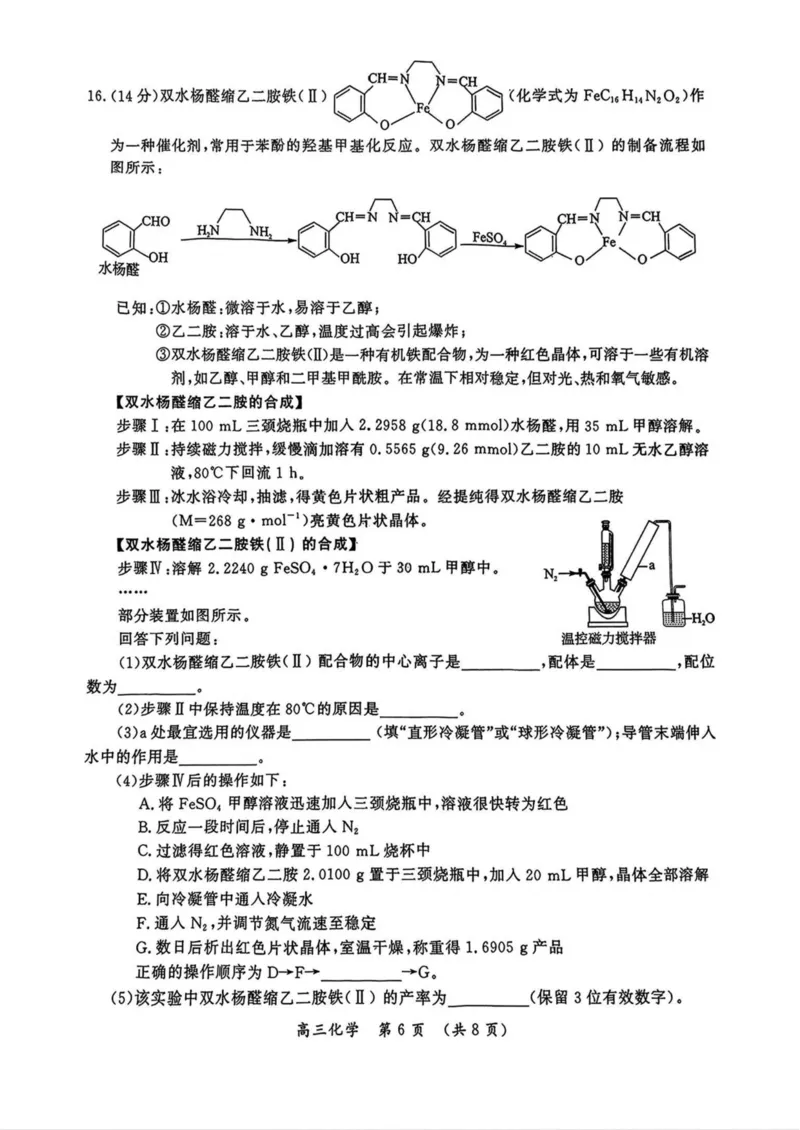
高三化学第5页(共8页)16.(14分)双水杨醛缩乙二胺铁(H ) •(化学式为FeGGH.NzOz)作
为一种催化剂,常用于苯酚的羟基甲基化反应。双水杨醛缩乙二胺铁(口)的制备流程如
图所示:
已知:①水杨醛:微溶于水,易溶于乙醇;
②乙二胺:溶于水、乙醇,温度过高会引起爆炸;
③双水杨醛缩乙二胺铁(口)是一种有机铁配合物,为一种红色晶体,可溶于一些有机溶
剂,如乙醇、甲醇和二甲基甲酰胺。在常温下相对稳定,但对光、热和氧气敏感。
【双水杨醛缩乙二胺的合成】
步骤I :在100 mL三颈烧瓶中加入2. 2958 g(18. 8 mmol)水杨醛,用35 mL甲醇溶解。
步骤D :持续磁力搅拌,缓慢滴加溶有0. 5565 g(9. 26 mmol)乙二胺的10 mL无水乙醇溶
液,80℃下回流1 h。
步骤m :冰水浴冷却,抽滤,得黄色片状粗产品。经提纯得双水杨醛缩乙二胺
(M=268 g - 亮黄色片状晶体。
【双水杨醛缩乙二胺铁(口)的合成】
步骤IV :溶解2. 2240 g FeSCh・7氏O于30 mL甲醇中。
部分装置如图所示。
回答下列问题:
(1)双水杨醛缩乙二胺铁(口)配合物的中心离子是,配体是,配位
数为 0
(2)步骤D中保持温度在80℃的原因是。
(3)a处最宜选用的仪器是(填“直形冷凝管”或“球形冷凝管”);导管末端伸入
水中的作用是 0
(4)步骤W后的操作如下:
A.将FeSO4甲醇溶液迅速加入三颈烧瓶中,溶液很快转为红色
B.反应一段时间后,停止通入N2
C.过滤得红色溶液,静置于100 mL烧杯中
D.将双水杨醛缩乙二胺2. 0100 g置于三颈烧瓶中,加入20 mL甲醇,晶体全部溶解
E.向冷凝管中通入冷凝水
F.通人N2,并调节氮气流速至稳定
G.数日后析出红色片状晶体,室温干燥,称重得1. 6905 g产品
正确的操作顺序为D->F->-G。
(5)该实验中双水杨醛缩乙二胺铁(口)的产率为(保留3位有效数字)。
高三化学第6页(共8页)17. (14分)氢能是理想清洁能源,其产业链由制氢和储氢组成。回答下列问题:
【制氢】
甲醇水蒸气重整制氢过程主要发生的反应有:
i. CH3OH(g) =F=^CO(g)+2H2(g) AH] =+90. 6 kJ ・ mo「
ii. CO(g) + H2O(g) CO2(g) + H2(g) △口2 = -41.2 kJ ・ mol-1
iii. CH3OH(g) + H20(g) CO2 (g)+3H2 (g) AH3
<1)AH3=kJ • mol-1 o
(2)恒温恒容的密闭容器中,假设只发生反应i,下列选项能表明反应i达到平衡状态的是
(填字母序号)。
a. 2v (CH3OH)— (H2)
b.容器内混合气体的平均相对分子质量不再变化
c.容器内混合气体的密度不再变化
d.单位时间内,断裂3 moi G-H键的同时生成2 moi H-H键
⑶实验室模拟甲醇水蒸气重整制氢,若只考虑反应iii,当合成气组成
n(CH3OH):n(H2O)=l: 1时,体系中CH3 0H的平衡转化率随温度和压强的变化如图所示。
100
90
80
70
60
50
40
30
20
100
2
①图中的压强由大到小的顺序是
②温度为250℃、压强为p2时,该反应的平衡常数K、=(Kx为用气体的物质
的量分数表示的平衡常数,物质的量分数x(B) = ^^,保留两位有效数字)。
【储氢】
(4)HCO7催化储氢:在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应
=萼
制得)中通人H2生成HCOO-,其离子方程式为HCOr +H2 hcoo- + H20o
工
①下列有关说法正确的是(填字母序号)。 100[ /O
a.这种储氢方式便于运输
b.储氢过程中HCO;被氧化
c.这种储氢方法有利于实现“碳中和”
d.释氢过程中,每消耗3.6 g氏0放出4.48 L的H? 20 40 SJ0 100120
②其他条件不变,HCOr转化为HCOO-的转化率随温度的变化如图所示。反应温度在
80℃〜120℃范围内,HCO「催化加氢的转化率下降的原因可能是(写出一条即可)0
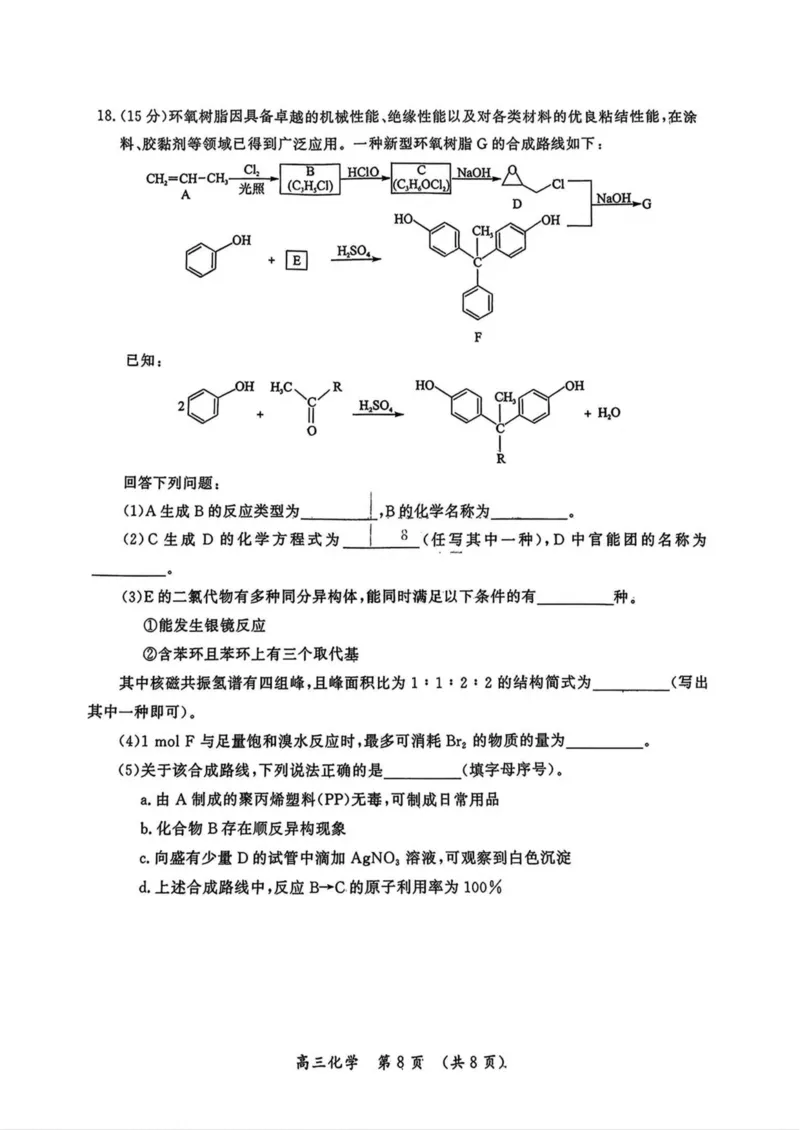
高三化学第7页(共8页)18. (15分)环氧树脂因具备卓越的机械性能、绝缘性能以及对各类材料的优良粘结性能,在涂
料、胶黏剂等领域已得到广泛应用。一种新型环氧树脂G的合成路线如下:
回答下列问题:
(DA生成B的反应类型为 |,B的化学名称为__________o
(2)C生成D的化学方程式为 I 8 (任、其中一种),D中官能团的名称为
(3)E的二氯代物有多种同分异构体,能同时满足以下条件的有 种。
①能发生银镜反应
②含苯环且苯环上有三个取代基
其中核磁共振氢谱有四组峰,且峰面积比为1 : 1 : 2 : 2的结构简式为 (写出
其中一种即可)。
(4)1 mol F与足量饱和滨水反应时,最多可消耗Br2的物质的量为。
(5)关于该合成路线,下列说法正确的是(填字母序号)。
a.由A制成的聚丙烯塑料(PP)无毒,可制成日常用品
b.化合物B存在顺反异构现象
c.向盛有少量D的试管中滴加AgNO3溶液,可观察到白色沉淀
d.上述合成路线中,反应B-C的原子利用率为100%
高三化学第8页(共8页).高三化学三模参考答案
一、选择题(共14小题,每题3分,共42分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B A D B B C A D C D A B D C
二、非选择题(共4小题,共58分)
说明:1.若考生给出其他答案,只要合理,可比照给分。
2 .题中没要求写出化学式、元素符号(或名称)的,考生给出名称(或化学式、元素符号)也给分。
3 .化学方程式未写反应条件或未标“个”、“(”符号的,可不扣分;未配平的,给一半分。
15. (15 分)
(1)2(1 分) (2)寸-8(2 分)
N A
(3)ZnO + 2NaOH + H2O--- Naz[Zn(OH).,] (2 分) CuO 和 FeO(2 分)
(4)适当增大盐酸浓度(或搅拌、适当升高温度等)(2分)
(5)2Fe2++H2()2 + 2H + == 2Fe3++2H2()(2 分)
(6)abc(2 分) 2. pH < 6. 2(2 分)
16. (14 分)
(l)Fe2+(l分) 双水杨醛缩乙二胺(1分) 4 (2分)
(2)温度过低反应速率慢,温度过高乙二胺会引起爆炸(2分)
(3)球形冷凝管(2分)液封,防止空气中的氧气进入三颈烧瓶中(2分)
(4) E-*, A->, B-*0( 2 分)
(5)70. 0%(2 分)
17. (14 分)
(1) + 49. 4(2 分) (2)b (2 分)
(3)①色>色>/八(2分) 该反应为气体体积增大的反应,在相同温度下,增大压强,平衡逆
向移动,CH30H的平衡转化率减小(2分)
②21(2分)
(4)①ac(2 分)
②储氢过程放热,80℃〜120℃范围内升温平衡逆向移动;升温催化剂活性降低(2分,一条即可)
18. (15 分)
(1)取代反应(1分) 3 一氯丙烯(2分)
0H
(2)CICH,CH—CH,CI + NaOH ----------►及、+ NaCI + %0
Cl
(或 HOCH2cH—CH© + NaOH ----------+ NaCl + H20) (2 分)
酸键 碳氯键(共2分)
(3)16(2 分)
CH2cH0 fH2cH0
守或A "讣
Cl Cl
(4) 4 mol (2 分)
(5) ad(2 分)