文档内容
2025年湖北云学名校联盟高三年级2月联考
化学试卷
命题学校:夷陵中学 命题人:高三化学组 审题人:黄石市教科院 杨彩云
考试时间:2025年2月18日14:30-17:05 时长:75分钟 试卷满分:100分
可能用到的相对原子质量:H1 O16 S32 Cr52
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.化学与社会生活及生产实践联系紧密,下列说法错误的是
A.在工业上,石膏被用来调节水泥的硬化速率
B.浓硝酸和浓盐酸按体积比3:1构成的混合物叫王水,能使金属铂溶解
C.脲醛塑料俗称电玉,绝缘性好,可制成电器开关、插座
D.橡胶消声瓦可有效降低潜艇航行时的噪声,提高其隐蔽性
2.下列化学用语表达正确的是
A.BCl 的电子式为: B.联氨(N H )分子的结构式为:
3 2 4
C.PCl 的共价键类型:sp3-pσ键 D.激发态H原子的轨道表示式:
3
3.过二硫酸( )是一种强氧化剂,用K S O 制备高锰酸钾的方程式如下:
2 2 8
K S O MnSO H OKMnO K SO Y(未配平)。设N 表示阿伏加德罗常数的值,下列
2 2 8 4 2 4 2 4 A
说法错误的是
A.194g过二硫酸中过氧键数目为N B.当生成1molKMnO 时,转移电子数为5N
A 4 A
C.1mol 中硫原子的价层电子对数为4N D.1molMn2+中M层电子数为11N
A A
2−
4.下列反应
S
的
O4
离子方程式正确的是
A.Na S O 溶液中加入稀硫酸: − +2 −+6H+=4 ↑+3
2 2 3
2 2
B.NaHCO 3 溶液中通入足量的Cl 2S :2O23 −+SCOl42 =Cl-+ClSOO -2+2COH2 2+OH 2 O
C.含氟牙膏防治龋齿:Ca
5
(PO
4
)
3
OHH(sC)+OF3 -(aq) Ca
5
(PO
4
)
3
F(s)+OH-(aq)
D.阿司匹林与足量NaOH溶液共热: +2OH- Δ +CH COO-+H O
3 2
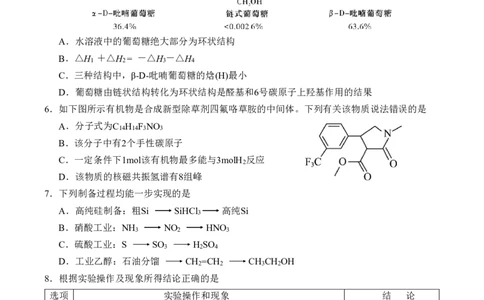
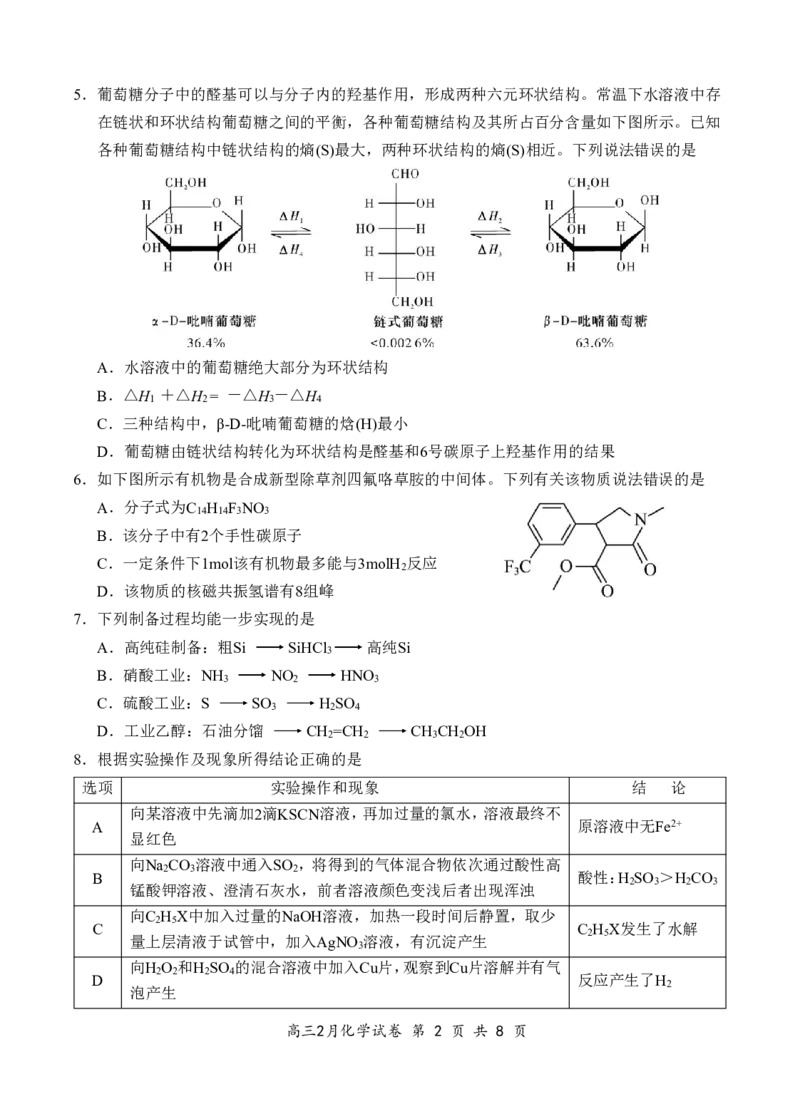
高三2月化学试卷 第 1 页 共 8 页5.葡萄糖分子中的醛基可以与分子内的羟基作用,形成两种六元环状结构。常温下水溶液中存
在链状和环状结构葡萄糖之间的平衡,各种葡萄糖结构及其所占百分含量如下图所示。已知
各种葡萄糖结构中链状结构的熵(S)最大,两种环状结构的熵(S)相近。下列说法错误的是
A.水溶液中的葡萄糖绝大部分为环状结构
B.△H +△H = -△H -△H
1 2 3 4
C.三种结构中,β-D-吡喃葡萄糖的焓(H)最小
D.葡萄糖由链状结构转化为环状结构是醛基和6号碳原子上羟基作用的结果
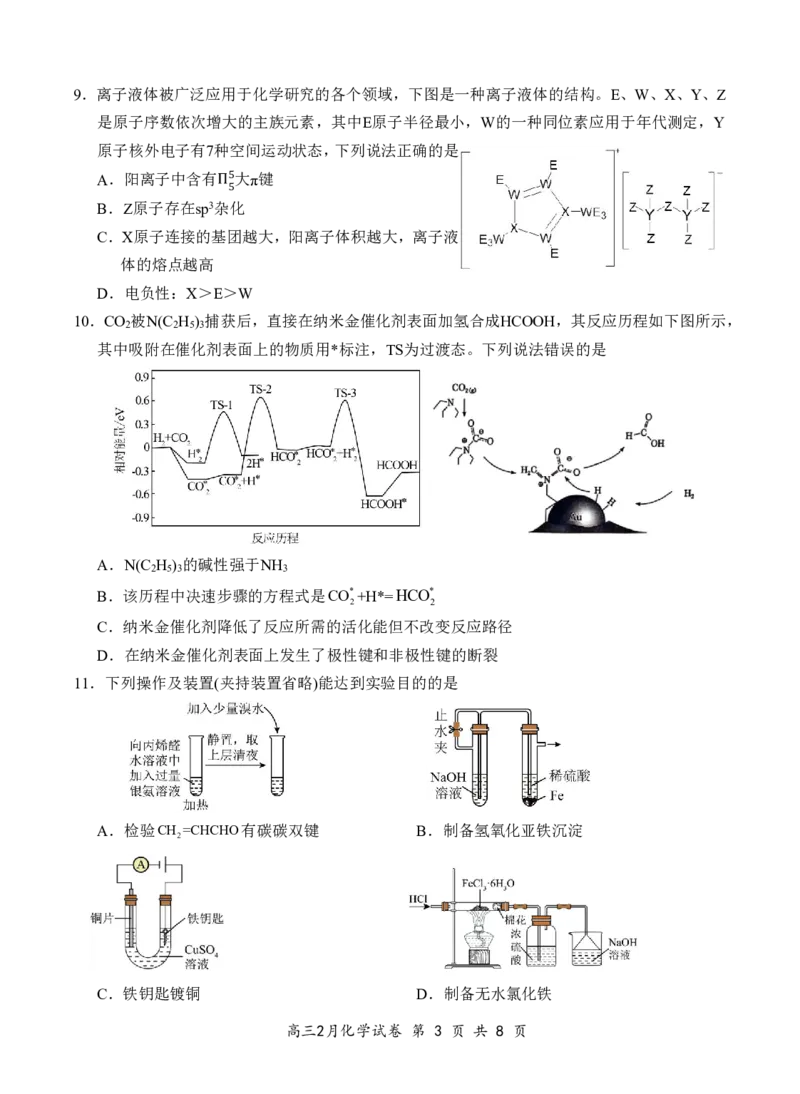
6.如下图所示有机物是合成新型除草剂四氟咯草胺的中间体。下列有关该物质说法错误的是
A.分子式为C H F NO
14 14 3 3
B.该分子中有2个手性碳原子
C.一定条件下1mol该有机物最多能与3molH 反应
2
D.该物质的核磁共振氢谱有8组峰
7.下列制备过程均能一步实现的是
A.高纯硅制备:粗Si SiHCl 高纯Si
3
B.硝酸工业:NH NO HNO
3 2 3
C.硫酸工业:S SO H SO
3 2 4
D.工业乙醇:石油分馏 CH =CH CH CH OH
2 2 3 2
8.根据实验操作及现象所得结论正确的是
选项 实验操作和现象 结 论
向某溶液中先滴加2滴KSCN溶液,再加过量的氯水,溶液最终不
A 原溶液中无Fe2+
显红色
向Na CO 溶液中通入SO ,将得到的气体混合物依次通过酸性高
2 3 2
B 酸性:H SO >H CO
2 3 2 3
锰酸钾溶液、澄清石灰水,前者溶液颜色变浅后者出现浑浊
向C H X中加入过量的NaOH溶液,加热一段时间后静置,取少
2 5
C C H X发生了水解
2 5
量上层清液于试管中,加入AgNO 溶液,有沉淀产生
3
向H O 和H SO 的混合溶液中加入Cu片,观察到Cu片溶解并有气
2 2 2 4
D 反应产生了H
2
泡产生
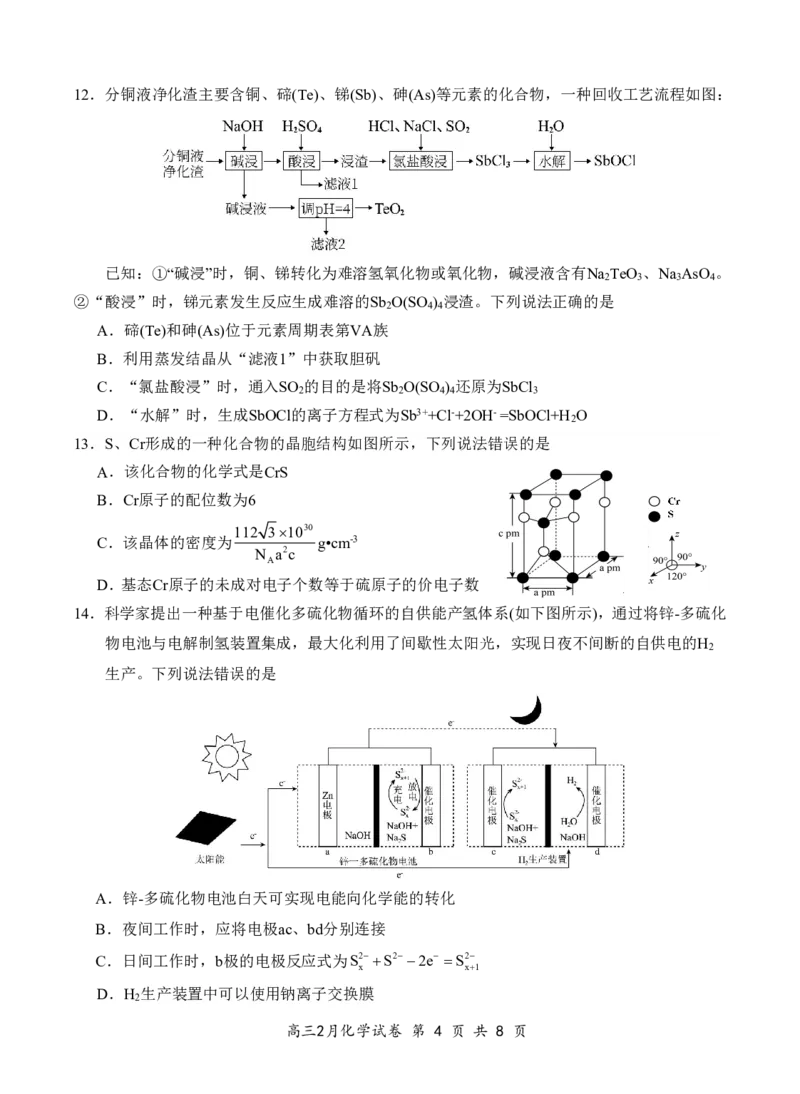
高三2月化学试卷 第 2 页 共 8 页9.离子液体被广泛应用于化学研究的各个领域,下图是一种离子液体的结构。E、W、X、Y、Z
是原子序数依次增大的主族元素,其中E原子半径最小,W的一种同位素应用于年代测定,Y
原子核外电子有7种空间运动状态,下列说法正确的是
A.阳离子中含有 大π键
�
B.Z原子存在sp3杂
��
化
C.X原子连接的基团越大,阳离子体积越大,离子液
体的熔点越高
D.电负性:X>E>W
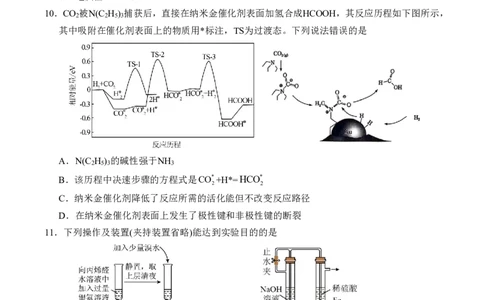
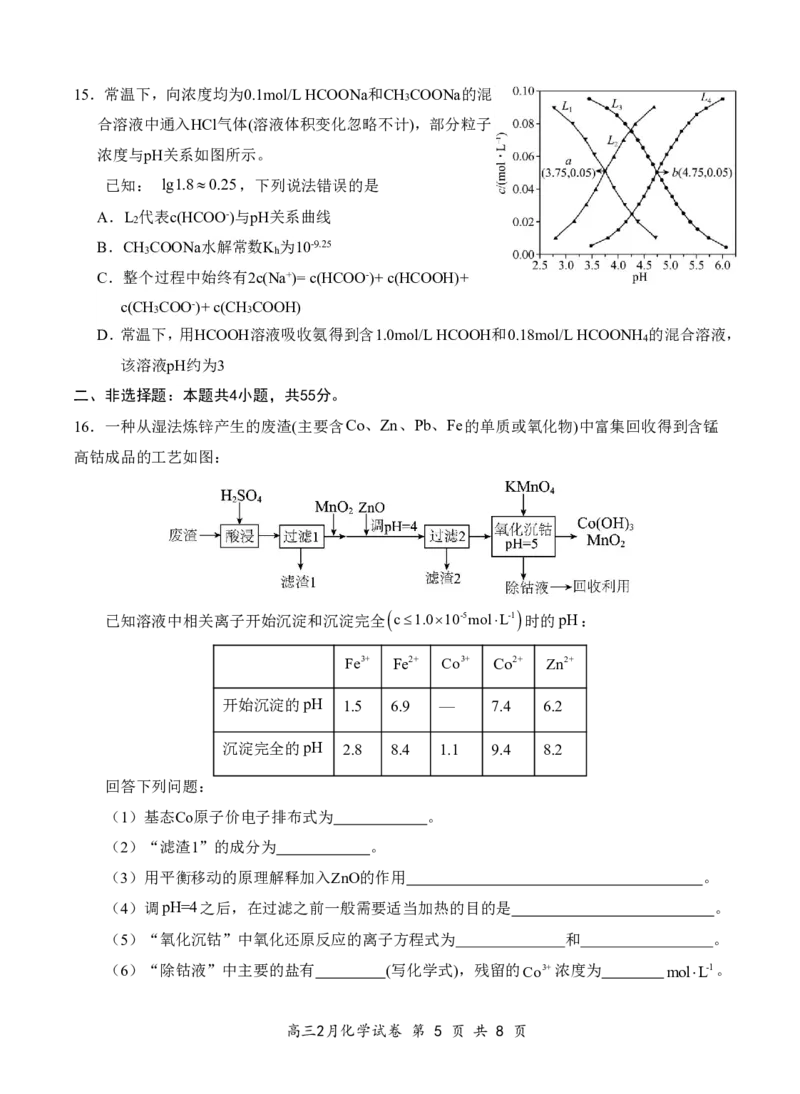
10.CO 被N(C H ) 捕获后,直接在纳米金催化剂表面加氢合成HCOOH,其反应历程如下图所示,
2 2 5 3
其中吸附在催化剂表面上的物质用*标注,TS为过渡态。下列说法错误的是
A.N(C H ) 的碱性强于NH
2 5 3 3
B.该历程中决速步骤的方程式是CO*+H*=HCO*
2 2
C.纳米金催化剂降低了反应所需的活化能但不改变反应路径
D.在纳米金催化剂表面上发生了极性键和非极性键的断裂
11.下列操作及装置(夹持装置省略)能达到实验目的的是
A.检验CH =CHCHO有碳碳双键 B.制备氢氧化亚铁沉淀
2
C.铁钥匙镀铜 D.制备无水氯化铁
高三2月化学试卷 第 3 页 共 8 页12.分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图:
已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na TeO 、Na AsO 。
2 3 3 4
②“酸浸”时,锑元素发生反应生成难溶的Sb O(SO ) 浸渣。下列说法正确的是
2 4 4
A.碲(Te)和砷(As)位于元素周期表第VA族
B.利用蒸发结晶从“滤液1”中获取胆矾
C.“氯盐酸浸”时,通入SO 的目的是将Sb O(SO ) 还原为SbCl
2 2 4 4 3
D.“水解”时,生成SbOCl的离子方程式为Sb3++Cl-+2OH-=SbOCl+H O
2
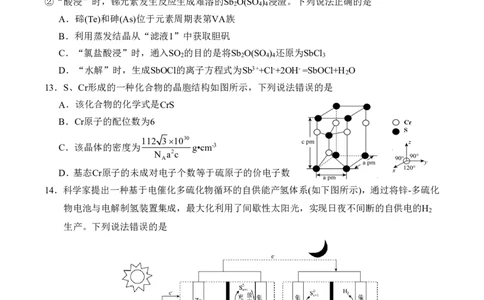
13.S、Cr形成的一种化合物的晶胞结构如图所示,下列说法错误的是
A.该化合物的化学式是CrS
B.Cr原子的配位数为6
112 31030
C.该晶体的密度为 g•cm-3
N a2c
A
D.基态Cr原子的未成对电子个数等于硫原子的价电子数
14.科学家提出一种基于电催化多硫化物循环的自供能产氢体系(如下图所示),通过将锌-多硫化
物电池与电解制氢装置集成,最大化利用了间歇性太阳光,实现日夜不间断的自供电的H
2
生产。下列说法错误的是
A.锌-多硫化物电池白天可实现电能向化学能的转化
B.夜间工作时,应将电极ac、bd分别连接
C.日间工作时,b极的电极反应式为S2 S2 2e S2
x x1
D.H 生产装置中可以使用钠离子交换膜
2
高三2月化学试卷 第 4 页 共 8 页15.常温下,向浓度均为0.1mol/LHCOONa和CH COONa的混
3
合溶液中通入HCl气体(溶液体积变化忽略不计),部分粒子
浓度与pH关系如图所示。
已知: lg1.80.25,下列说法错误的是
A.L 代表c(HCOO-)与pH关系曲线
2
B.CH COONa水解常数K 为10-9.25
3 h
C.整个过程中始终有2c(Na+)=c(HCOO-)+c(HCOOH)+
c(CH COO-)+c(CH COOH)
3 3
D.常温下,用HCOOH溶液吸收氨得到含1.0mol/LHCOOH和0.18mol/LHCOONH 的混合溶液,
4
该溶液pH约为3
二、非选择题:本题共4小题,共55分。
16.一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰
高钴成品的工艺如图:
已知溶液中相关离子开始沉淀和沉淀完全
c1.010-5molL-1
时的pH:
Fe3+ Fe2+ Co3+ Co2+ Zn2+
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)基态Co原子价电子排布式为 。
(2)“滤渣1”的成分为 。
(3)用平衡移动的原理解释加入ZnO的作用 。
(4)调pH=4之后,在过滤之前一般需要适当加热的目的是 。
(5)“氧化沉钴”中氧化还原反应的离子方程式为 和 。
(6)“除钴液”中主要的盐有 (写化学式),残留的Co3+浓度为 molL-1。
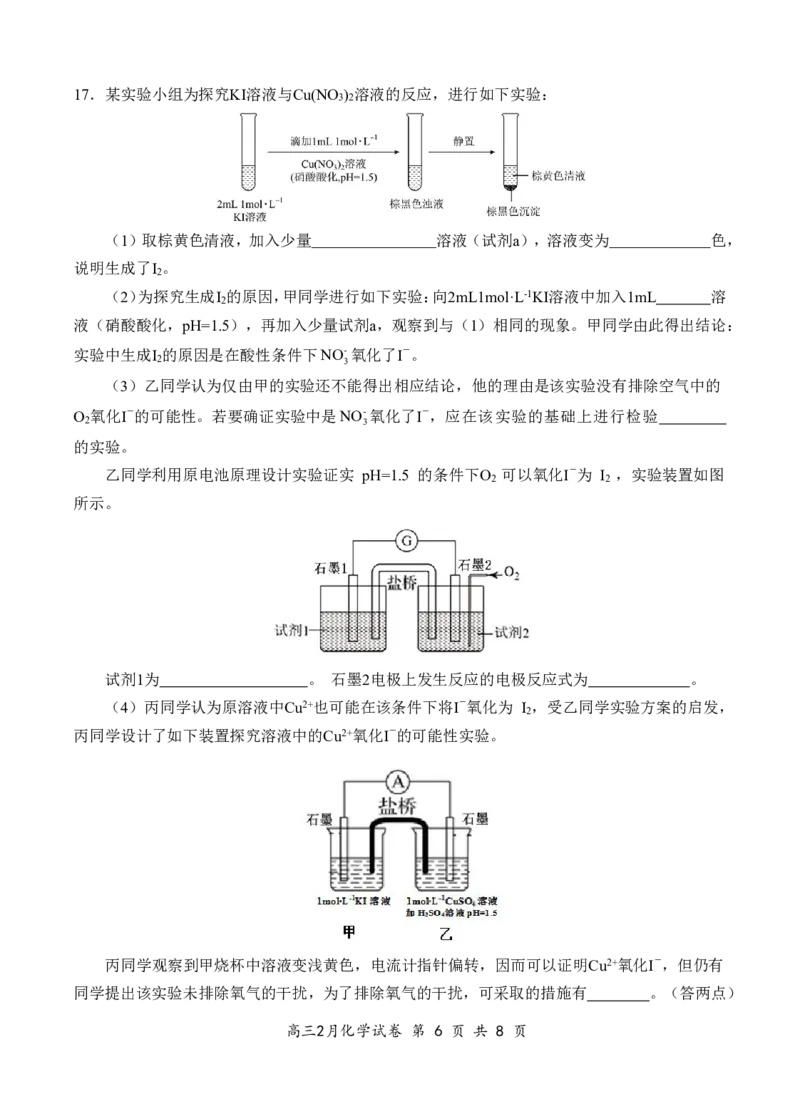
高三2月化学试卷 第 5 页 共 8 页17.某实验小组为探究KI溶液与Cu(NO ) 溶液的反应,进行如下实验:
3 2
(1)取棕黄色清液,加入少量 溶液(试剂a),溶液变为 色,
说明生成了I 。
2
(2)为探究生成I 的原因,甲同学进行如下实验:向2mL1mol·L-1KI溶液中加入1mL 溶
2
液(硝酸酸化,pH=1.5),再加入少量试剂a,观察到与(1)相同的现象。甲同学由此得出结论:
实验中生成I 的原因是在酸性条件下NO-氧化了I-。
2 3
(3)乙同学认为仅由甲的实验还不能得出相应结论,他的理由是该实验没有排除空气中的
O 氧化I-的可能性。若要确证实验中是NO-氧化了I-,应在该实验的基础上进行检验
2 3
的实验。
乙同学利用原电池原理设计实验证实 pH=1.5 的条件下O 可以氧化I-为 I ,实验装置如图
2 2
所示。
试剂1为 。 石墨2电极上发生反应的电极反应式为 。
(4)丙同学认为原溶液中Cu2+也可能在该条件下将I-氧化为 I ,受乙同学实验方案的启发,
2
丙同学设计了如下装置探究溶液中的Cu2+氧化I-的可能性实验。
丙同学观察到甲烧杯中溶液变浅黄色,电流计指针偏转,因而可以证明Cu2+氧化I-,但仍有
同学提出该实验未排除氧气的干扰,为了排除氧气的干扰,可采取的措施有 。(答两点)
高三2月化学试卷 第 6 页 共 8 页18.随着工业化加速,氮氧化物(NO )与碳氧化物(CO )排放量激增,对环境和气候构成严
x x
峻挑战。科研人员正积极探索高效转化技术及减排策略,以实现环境友好型可持续发展。
Ⅰ.NO和CO主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:
−1
N2(g)+O2(g)⇌ 2NO(g) △�=+180kJ�mol
−1
2CO(g)+O2(g)⇌ 2CO2(g) △�=−� △ 64kHJ=�m __ o _l___。
(1)2NO时(g,)+将2等C物O(质g)的量的N2COO和2(CgO)+充N入2容(g)积为2L的密闭容器中,保持温度和体积不变,反应过
(
程
2)T
~
℃
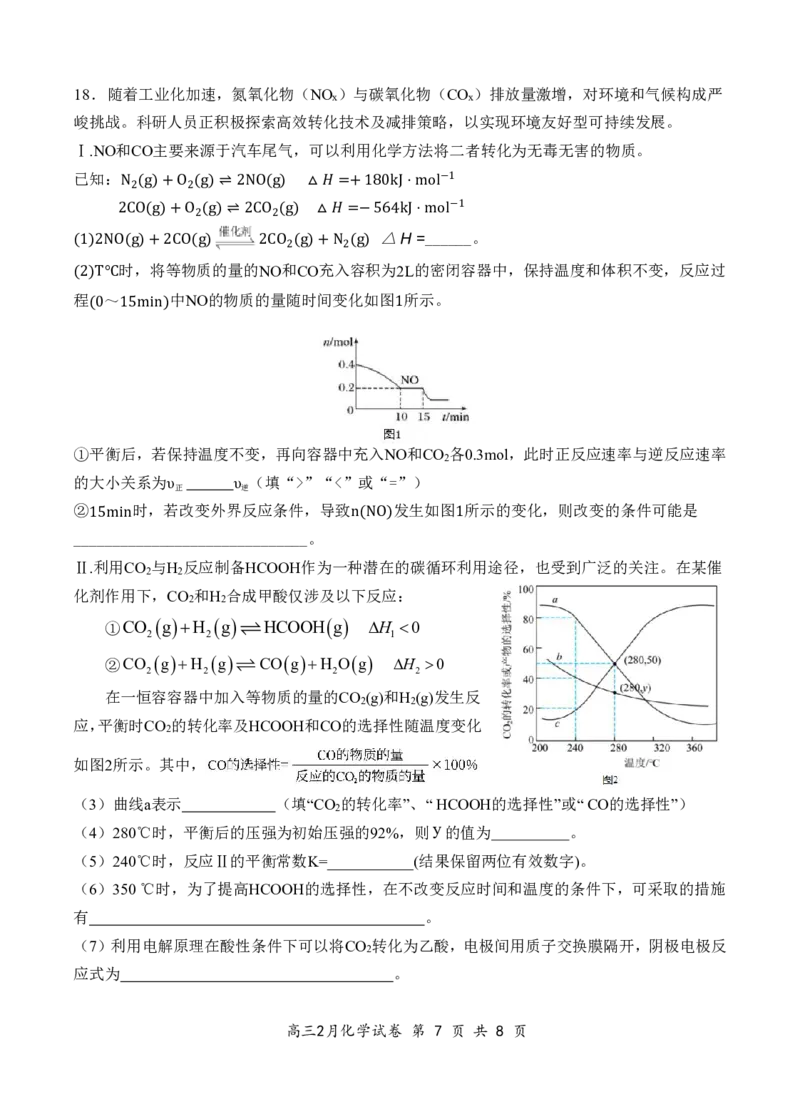
中NO的物质的量随时间变化如图 所示。
(0 1�min) 1
①平衡后,若保持温度不变,再向容器中充入NO和CO 各0.3mol,此时正反应速率与逆反应速率
2
的大小关系为υ υ (填“>”“<”或“=”)
正 逆
② 时,若改变外界反应条件,导致 发生如图 所示的变化,则改变的条件可能是
______________________________。
1�min n(NO) 1
Ⅱ.利用CO 与H 反应制备HCOOH作为一种潜在的碳循环利用途径,也受到广泛的关注。在某催
2 2
化剂作用下,CO 和H 合成甲酸仅涉及以下反应:
2 2
①CO g H g HCOOH g H 0
2 2 1
②CO gH g COgH Og H 0
2 2 2 2
在一恒容容器中加入等物质的量的CO (g)和H (g)发生反
2 2
应,平衡时CO 的转化率及HCOOH和CO的选择性随温度变化
2
如图2所示。其中,
(3)曲线a表示 (填“CO 的转化率”、“HCOOH的选择性”或“CO的选择性”)
2
(4)280℃时,平衡后的压强为初始压强的92%,则y的值为 。
(5)240℃时,反应Ⅱ的平衡常数K=___________(结果保留两位有效数字)。
(6)350℃时,为了提高HCOOH的选择性,在不改变反应时间和温度的条件下,可采取的措施
有 。
(7)利用电解原理在酸性条件下可以将CO 转化为乙酸,电极间用质子交换膜隔开,阴极电极反
2
应式为 。
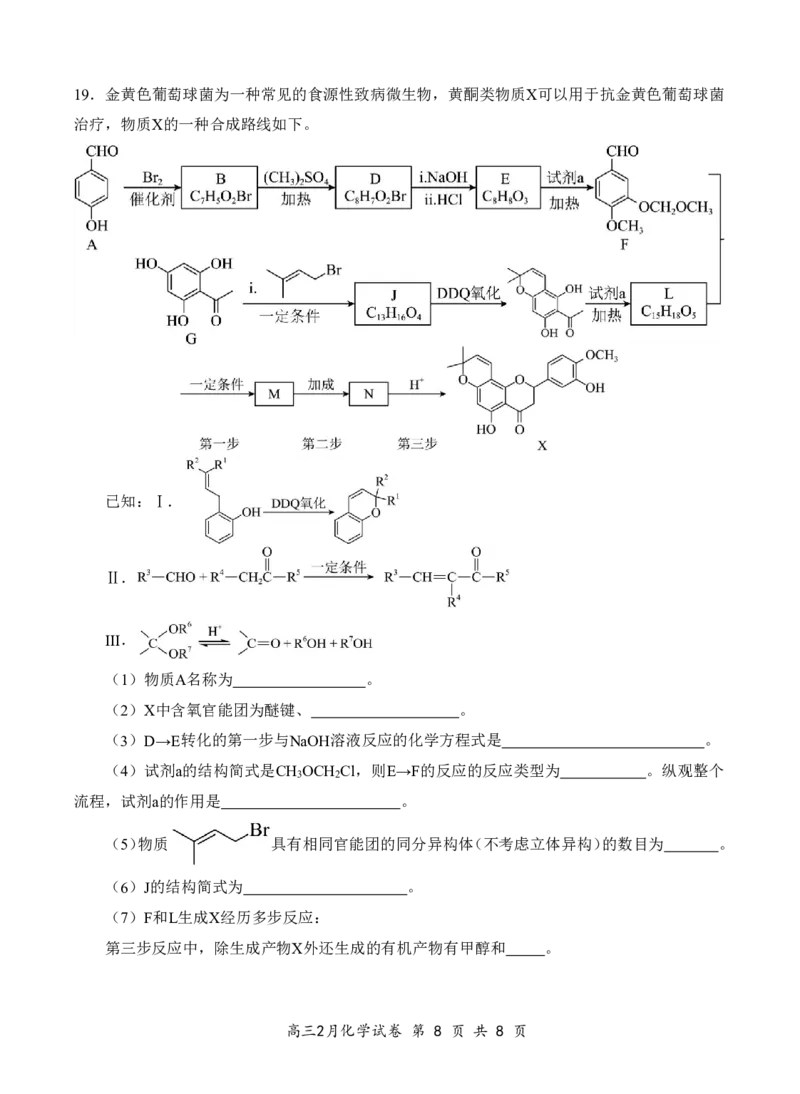
高三2月化学试卷 第 7 页 共 8 页19.金黄色葡萄球菌为一种常见的食源性致病微生物,黄酮类物质X可以用于抗金黄色葡萄球菌
治疗,物质X的一种合成路线如下。
已知:Ⅰ.
Ⅱ.
III.
(1)物质A名称为 。
(2)X中含氧官能团为醚键、 。
(3)D→E转化的第一步与NaOH溶液反应的化学方程式是 。
(4)试剂a的结构简式是CH OCH Cl,则E→F的反应的反应类型为 。纵观整个
3 2
流程,试剂a的作用是 。
(5)物质 具有相同官能团的同分异构体(不考虑立体异构)的数目为 。
(6)J的结构简式为 。
(7)F和L生成X经历多步反应:
第三步反应中,除生成产物X外还生成的有机产物有甲醇和 。
高三2月化学试卷 第 8 页 共 8 页