文档内容
绝密★考试结束前
Z20 名校联盟(浙江省名校新高考研究联盟)2025 届高三第三次联考
化学试题
命题:宁海中学 胡惠芳、潘爱娅
磨题:嘉善高级中学 张海雨 鲁迅中学 任 静 海宁高级中学 李 艳 校稿:苏艳丽、魏丽娜
本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
可能用到的相对原子质量:C:12 H:1 O:16 N:14
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
1.下列只含极性键的极性分子是
A.BF B.H O C. C H D.O
3 2 2 2 6 3
2.下列表示正确的是
A.异丙基的结构简式:
B.激发态H原子的轨道表示式:
C.N-甲基乙酰胺的键线式为:
D.32S 与34S 互为同位素
2 4
3.化学与生产、生活、科技密切相关。下列说法不
.
正
.
确
.
的是
A.生活中常用聚乙烯制成的薄膜来包装水果、蔬菜等食物
B.等离子体具有良好的导电性和流动性,可以用于制造等离子体显示器等
C.用热的纯碱溶液可清洗衣物上的汽油污渍
D.电热水器用镁棒防止内胆腐蚀,原理是电化学保护法的牺牲阳极法
4.物质的结构决定物质的性质,下列说法正确的是
A.相同浓度的Cu2+和Cu(NH ) 2+氧化性:前者>后者
3 4
B.金刚石中碳碳键键长较短,键能和硬度很大,不容易因锤击而破碎
C.由于水分子间存在氢键,所以稳定性:H O>H S
2 2
D.甘油是粘稠液体是因为甘油分子间存在较强的范德华力
5.关于实验室安全,下列说法不
.
正
.
确
.
的是
A.轻微烫伤或烧伤时,可用冷水处理,然后涂上烫伤膏即可
B.苯酚不慎沾到皮肤上,先用抹布擦拭,再用650C以上的水冲洗
C.探究钠与水的反应时需要注意:
D.镁燃烧起火不可用泡沫灭火器灭火
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 1 页 共 8 页6.设N
A
是阿伏加德罗常数的值,下列说法不
.
正
.
确
.
的是
A.0.1mol羟胺(NH OH)中氧的价层电子对数为0.4N
2 A
B.NaCl和NH 4 Cl的固体混合物中含1 mol Cl-,则混合物中质子数为28N A
C.0.1molCaH 中含阴离子个数为0.1N
2 A
D.由甘氨酸形成的18.9g三肽C H N O (相对分子质量:189)中的肽键数目为0.2N
6 11 3 4 A
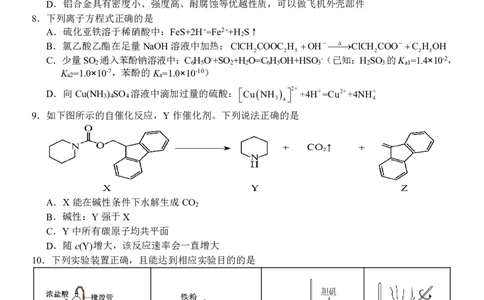
7.下列有关物质的性质和用途不具有对应关系的是
A.纤维素主链上的羟基可与硝酸发生反应,故可制备“无烟火药”硝化纤维
B.乙醇受热易挥发,故酿米酒需晾凉米饭后加酒曲
C.过氧碳酸钠(Na CO )具有较强氧化性,故可用Na CO 漂白衣物
2 4 2 4
D.铝合金具有密度小、强度高、耐腐蚀等优越性质,可以做飞机外壳部件
8.下列离子方程式正确的是
A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H S↑
2
B.氯乙酸乙酯在足量NaOH溶液中加热:ClCH COOC H OH ClCH COO C H OH
2 2 5 2 2 5
C.少量SO 通入苯酚钠溶液中:C H O-+SO +H O=C H OH+HSO -(已知:H SO 的K =1.4×10-2,
2 6 5 2 2 6 5 3 2 3 a1
K =1.0×10-7,苯酚的K =1.0×10-10)
a2 a
D.向Cu(NH ) SO 溶液中滴加过量的硫酸:CuNH 2+ +4H+=Cu2++4NH+
3 4 4 3 4 4
9.如下图所示的自催化反应,Y作催化剂。下列说法正确的是
A.X能在碱性条件下水解生成CO
2
B.碱性:Y强于X
C.Y中所有碳原子均共平面
D.随c(Y)增大,该反应速率会一直增大
10.下列实验装置正确,且能达到相应实验目的的是
D.除去 Na CO
B.验证铁粉与水蒸气 2 3
A.验证反应有Cl 生成 C.制备无水CuSO 固体中少量的
2 反应有H 产生 4
2
NaHCO
3
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 2 页 共 8 页11.下列说法不
.
正
.
确
.
的是
A.依据相同温度下可逆反应的浓度商Q与平衡常数K大小的比较,可推断反应进行的方向
B.平衡:2NO (g) N O (g) H<0中,断裂2 molNO (g)中的共价键所需能量小于断裂1 mol
2 2 4 2
N O (g)中的共价键所需能量
2 4
⇌ △
C.依据第二周期主族元素电负性依次增大,可推断它们的第一电离能也依次增大
D.在合成氨反应中:N (g)+3H (g) 2NH (g),一定条件下,将n(N ):n(H )=1:1通入恒容的容
2 2 3 2 2
器中反应,当N 物质的量分数不变时不能判断可逆反应是否达平衡状态
2
⇌
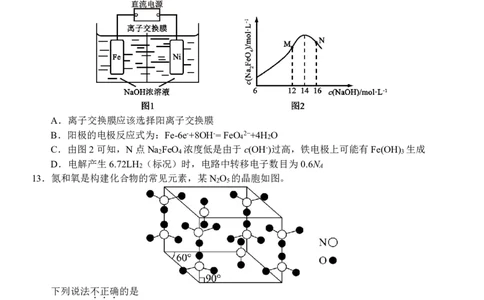
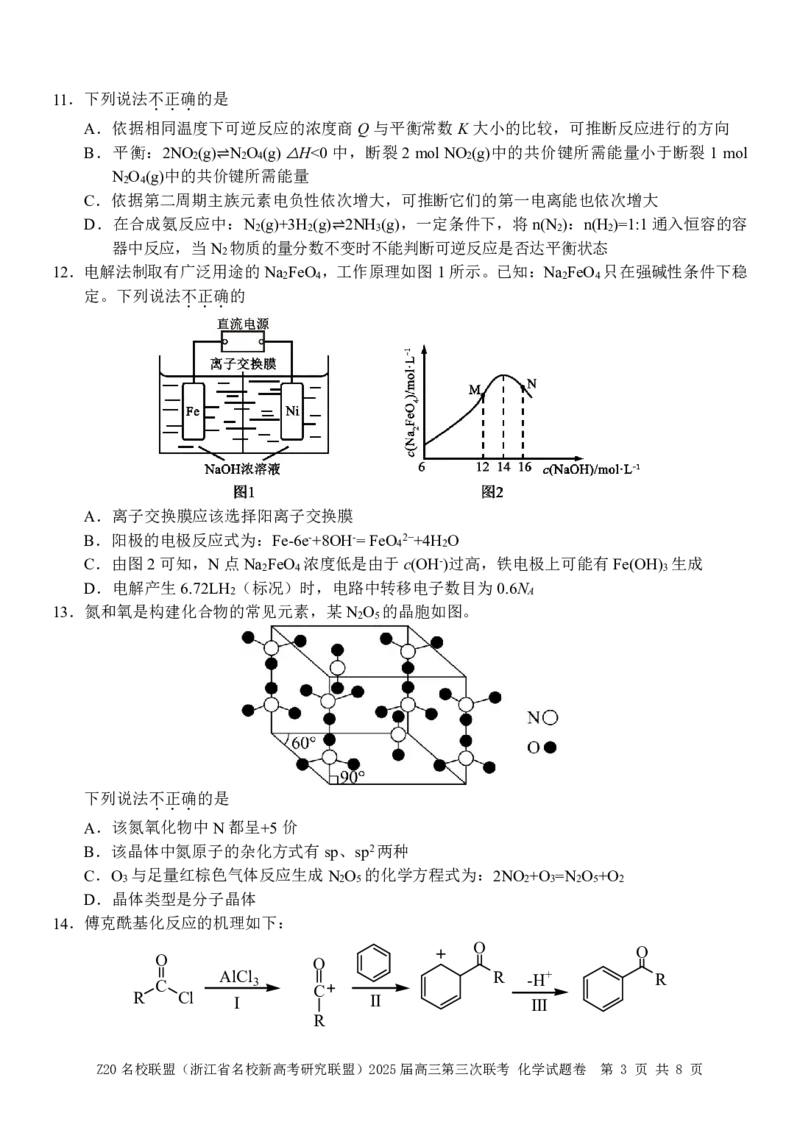
12.电解法制取有广泛用途的Na FeO ,工作原理如图1所示。已知:Na FeO 只在强碱性条件下稳
2 4 2 4
定。下列说法不正确的
...
A.离子交换膜应该选择阳离子交换膜
B.阳极的电极反应式为:Fe-6e-+8OH-=FeO 2−+4H O
4 2
C.由图2可知,N点Na FeO 浓度低是由于c(OH-)过高,铁电极上可能有Fe(OH) 生成
2 4 3
D.电解产生6.72LH (标况)时,电路中转移电子数目为0.6N
2 A
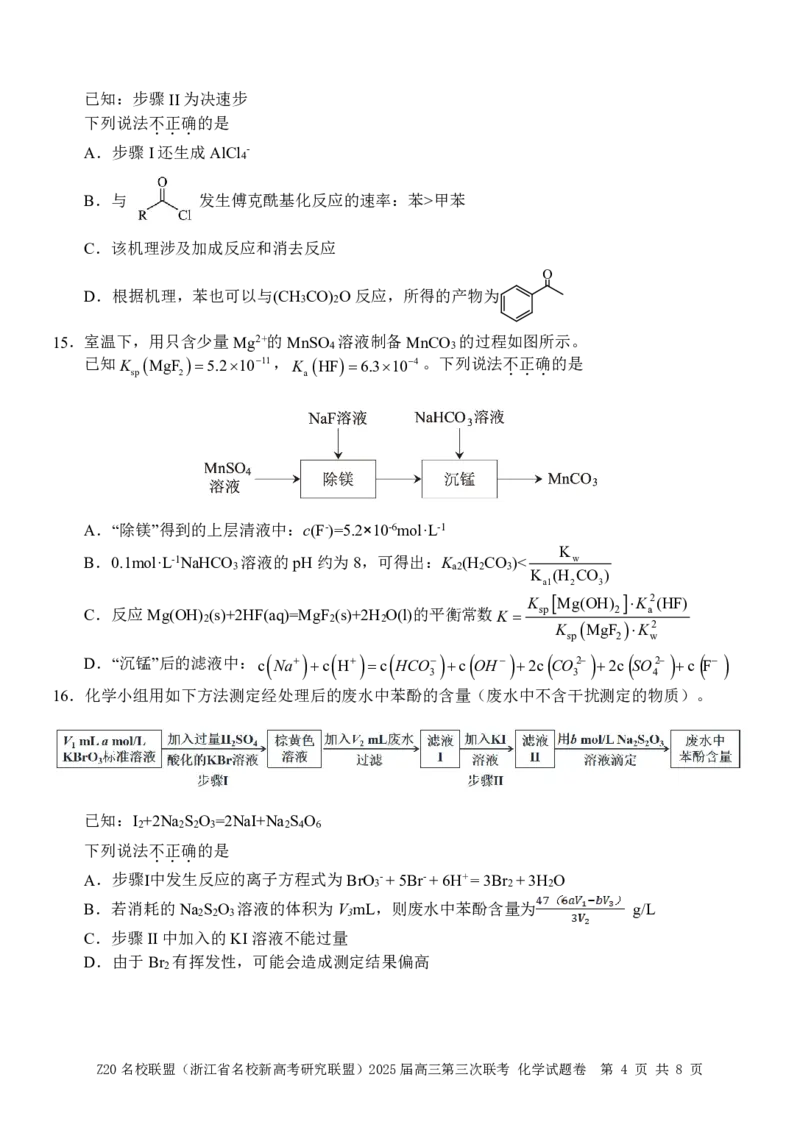
13.氮和氧是构建化合物的常见元素,某N O 的晶胞如图。
2 5
下列说法不正确的是
...
A.该氮氧化物中N都呈+5价
B.该晶体中氮原子的杂化方式有sp、sp2两种
C.O 与足量红棕色气体反应生成N O 的化学方程式为:2NO +O =N O +O
3 2 5 2 3 2 5 2
D.晶体类型是分子晶体
14.傅克酰基化反应的机理如下:
O O
O O
C AlCl 3 R -H+ R
C
R Cl Ⅰ Ⅱ Ⅲ
R
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 3 页 共 8 页已知:步骤II为决速步
下列说法不正确的是
...
A.步骤I还生成AlCl -
4
B.与 发生傅克酰基化反应的速率:苯>甲苯
C.该机理涉及加成反应和消去反应
O
D.根据机理,苯也可以与(CH CO) O反应,所得的产物为
3 2
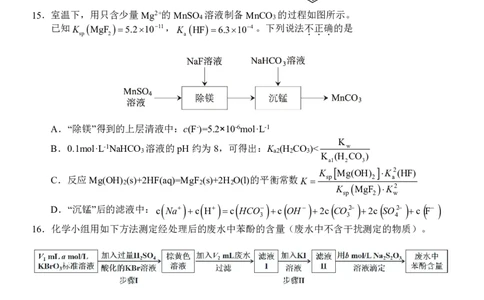
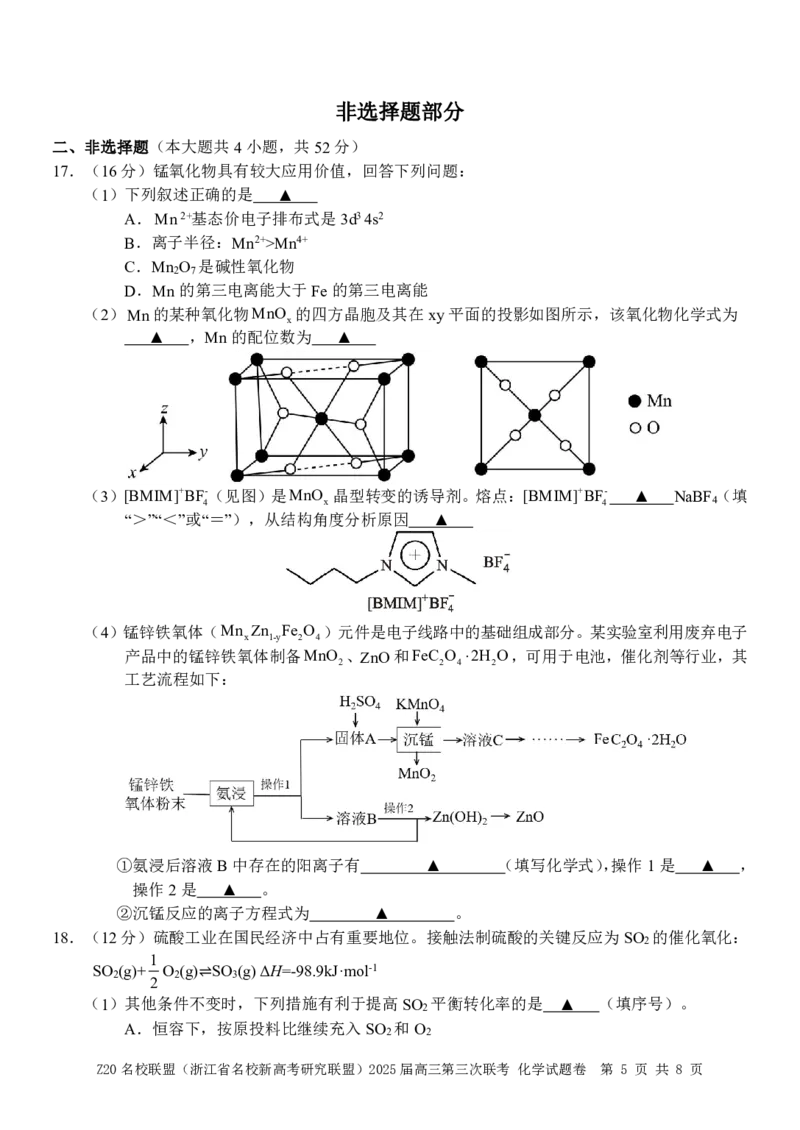
15.室温下,用只含少量Mg2+的MnSO 溶液制备MnCO 的过程如图所示。
4 3
已知K MgF 5.21011,
K
HF6.3104。下列说法不
.
正
.
确
.
的是
sp 2 a
A.“除镁”得到的上层清液中:c(F-)=5.2×10-6mol·L-1
K
B.0.1mol·L-1NaHCO 溶液的pH约为8,可得出:K (H CO )< w
3 a2 2 3
K (H CO )
a1 2 3
K
Mg(OH)
K2(HF)
C.反应Mg(OH)
2
(s)+2HF(aq)=MgF
2
(s)+2H
2
O(l)的平衡常数K sp 2 a
K MgF K2
sp 2 w
D.“沉锰”后的滤液中:c Na c H c HCO c OH 2c CO2 2c SO2 c F
3 3 4
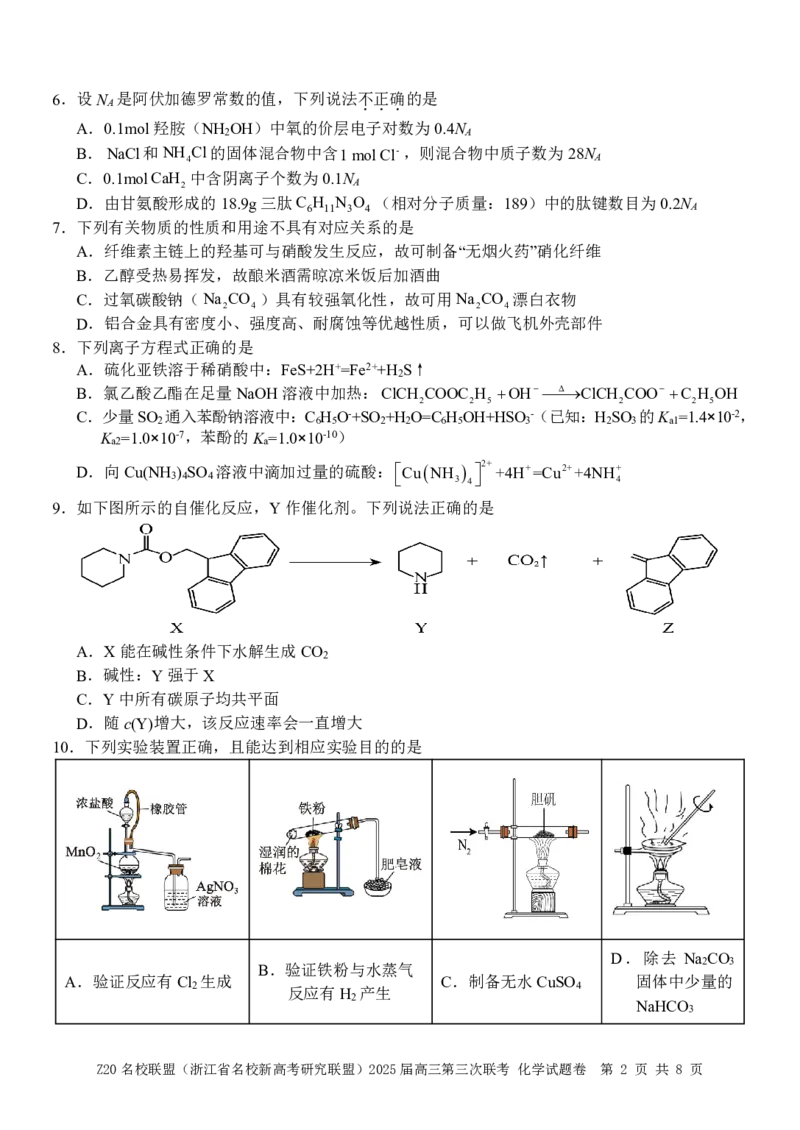
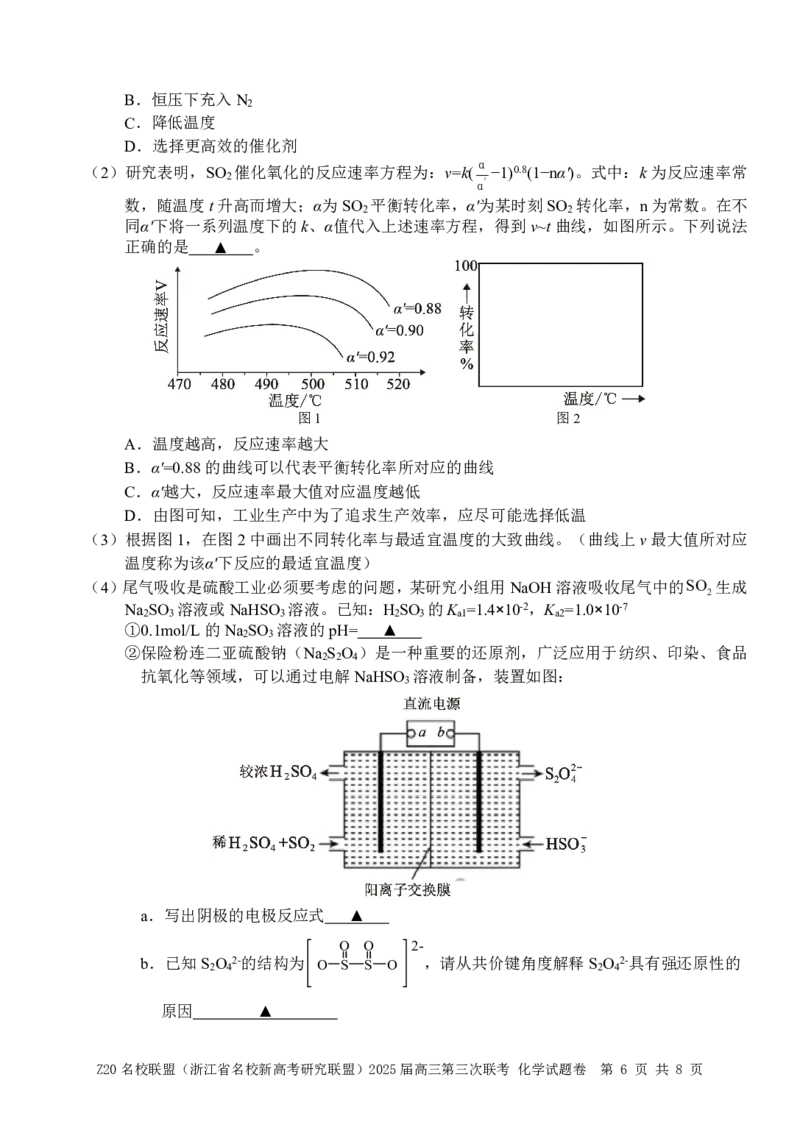
16.化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
已知:I +2Na S O =2NaI+Na S O
2 2 2 3 2 4 6
下列说法不正确的是
...
A.步骤Ⅰ中发生反应的离子方程式为BrO -+5Br-+6H+=3Br +3H O
3 2 2
B.若消耗的Na S O 溶液的体积为V mL,则废水中苯酚含量为 g/L
2 2 3 3
C.步骤II中加入的KI溶液不能过量
D.由于Br 有挥发性,可能会造成测定结果偏高
2
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 4 页 共 8 页非选择题部分
二、非选择题(本大题共4小题,共52分)
17.(16分)锰氧化物具有较大应用价值,回答下列问题:
(1)下列叙述正确的是 ▲
A.Mn2+基态价电子排布式是3d34s2
B.离子半径:Mn2+>Mn4+
C.Mn O 是碱性氧化物
2 7
D.Mn的第三电离能大于Fe的第三电离能
(2)Mn的某种氧化物MnO 的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为
x
▲ ,Mn的配位数为 ▲
(3)[BMIM]+BF-(见图)是MnO 晶型转变的诱导剂。熔点:[BMIM]+BF- ▲ NaBF(填
4 x 4 4
“>”“<”或“=”),从结构角度分析原因 ▲
(4)锰锌铁氧体(Mn Zn Fe O )元件是电子线路中的基础组成部分。某实验室利用废弃电子
x 1-y 2 4
产品中的锰锌铁氧体制备MnO 、ZnO和FeC O 2H O,可用于电池,催化剂等行业,其
2 2 4 2
工艺流程如下:
①氨浸后溶液B中存在的阳离子有 ▲ (填写化学式),操作1是 ▲ ,
操作2是 ▲ 。
②沉锰反应的离子方程式为 ▲ 。
18.(12分)硫酸工业在国民经济中占有重要地位。接触法制硫酸的关键反应为SO 的催化氧化:
2
1
SO (g)+ O (g) SO (g)ΔH=-98.9kJ·mol-1
2 2 3
2
(1)其他条件不⇌变时,下列措施有利于提高SO
2
平衡转化率的是 ▲ (填序号)。
A.恒容下,按原投料比继续充入SO 和O
2 2
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 5 页 共 8 页B.恒压下充入N
2
C.降低温度
D.选择更高效的催化剂
α
(2)研究表明,SO 催化氧化的反应速率方程为:v=k( −1)0.8(1−nα')。式中:k为反应速率常
2
α′
数,随温度t升高而增大;α为SO 平衡转化率,α'为某时刻SO 转化率,n为常数。在不
2 2
同α'下将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。下列说法
正确的是 ▲ 。
图1 图2
A.温度越高,反应速率越大
B.α'=0.88的曲线可以代表平衡转化率所对应的曲线
C.α'越大,反应速率最大值对应温度越低
D.由图可知,工业生产中为了追求生产效率,应尽可能选择低温
(3)根据图1,在图2中画出不同转化率与最适宜温度的大致曲线。(曲线上v最大值所对应
温度称为该α'下反应的最适宜温度)
(4)尾气吸收是硫酸工业必须要考虑的问题,某研究小组用NaOH溶液吸收尾气中的SO 生成
2
Na SO 溶液或NaHSO 溶液。已知:H SO 的K =1.4×10-2,K =1.0×10-7
2 3 3 2 3 a1 a2
①0.1mol/L的Na SO 溶液的pH= ▲
2 3
②保险粉连二亚硫酸钠(Na S O )是一种重要的还原剂,广泛应用于纺织、印染、食品
2 2 4
抗氧化等领域,可以通过电解NaHSO 溶液制备,装置如图:
3
a.写出阴极的电极反应式 ▲
O O 2-
b.已知S 2 O 4 2-的结构为 O S S O ,请从共价键角度解释S 2 O 4 2-具有强还原性的
原因 ▲
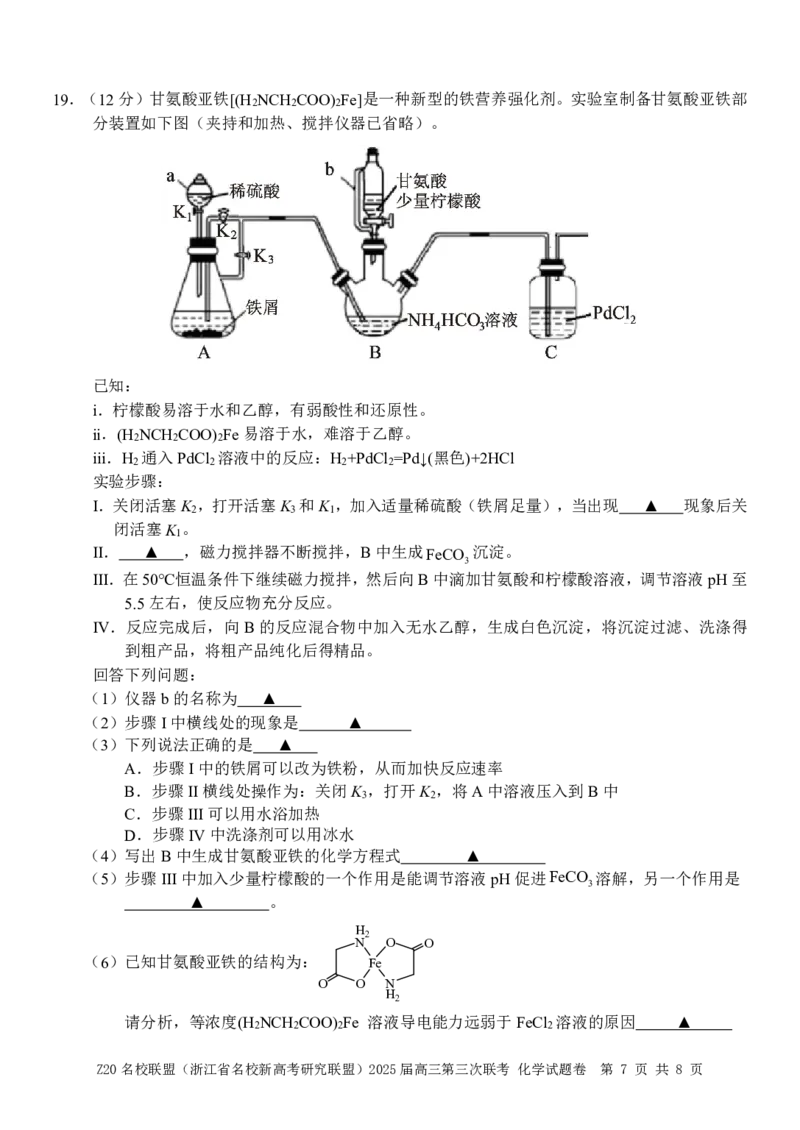
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 6 页 共 8 页19.(12分)甘氨酸亚铁[(H NCH COO) Fe]是一种新型的铁营养强化剂。实验室制备甘氨酸亚铁部
2 2 2
分装置如下图(夹持和加热、搅拌仪器已省略)。
已知:
ⅰ.柠檬酸易溶于水和乙醇,有弱酸性和还原性。
ⅱ.(H NCH COO) Fe易溶于水,难溶于乙醇。
2 2 2
iii.H 通入PdCl 溶液中的反应:H +PdCl =Pd↓(黑色)+2HCl
2 2 2 2
实验步骤:
I.关闭活塞K ,打开活塞K 和K ,加入适量稀硫酸(铁屑足量),当出现 ▲ 现象后关
2 3 1
闭活塞K 。
1
II. ▲ ,磁力搅拌器不断搅拌,B中生成 FeCO 沉淀。
3
III.在50℃恒温条件下继续磁力搅拌,然后向B中滴加甘氨酸和柠檬酸溶液,调节溶液pH至
5.5左右,使反应物充分反应。
IV.反应完成后,向B的反应混合物中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得
到粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称为 ▲
(2)步骤I中横线处的现象是 ▲
(3)下列说法正确的是 ▲
A.步骤I中的铁屑可以改为铁粉,从而加快反应速率
B.步骤II横线处操作为:关闭K ,打开K ,将A中溶液压入到B中
3 2
C.步骤III可以用水浴加热
D.步骤IV中洗涤剂可以用冰水
(4)写出B中生成甘氨酸亚铁的化学方程式 ▲
(5)步骤III中加入少量柠檬酸的一个作用是能调节溶液pH促进FeCO 溶解,另一个作用是
3
▲ 。
H
2
N O O
(6)已知甘氨酸亚铁的结构为: Fe
O O N
H
2
请分析,等浓度(H NCH COO) Fe 溶液导电能力远弱于FeCl 溶液的原因 ▲
2 2 2 2
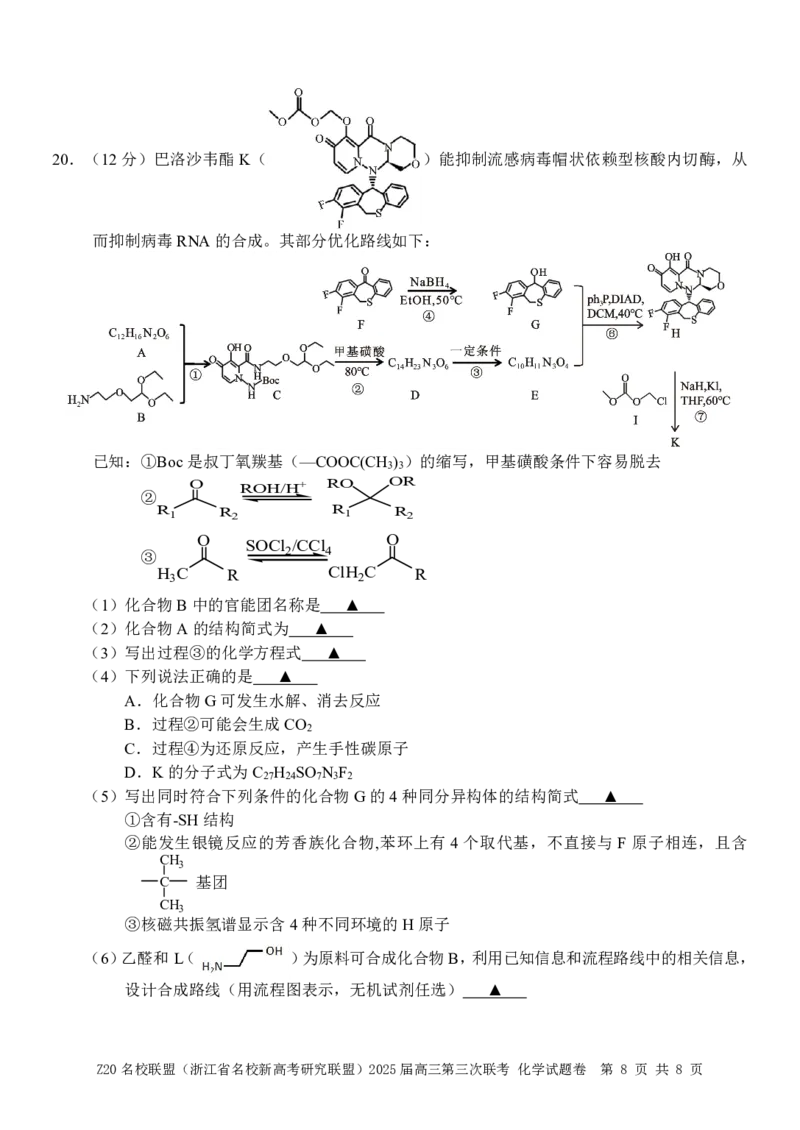
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 7 页 共 8 页20.(12分)巴洛沙韦酯K( )能抑制流感病毒帽状依赖型核酸内切酶,从
而抑制病毒RNA的合成。其部分优化路线如下:
已知:①Boc是叔丁氧羰基(—COOC(CH ) )的缩写,甲基磺酸条件下容易脱去
3 3
O ROH/H+ RO OR
②
R 1 R 2 R 1 R 2
O O
SOCl /CCl
③ 2 4
H 3 C R ClH 2 C R
(1)化合物B中的官能团名称是 ▲
(2)化合物A的结构简式为 ▲
(3)写出过程③的化学方程式 ▲
(4)下列说法正确的是 ▲
A.化合物G可发生水解、消去反应
B.过程②可能会生成CO
2
C.过程④为还原反应,产生手性碳原子
D.K的分子式为C H SO N F
27 24 7 3 2
(5)写出同时符合下列条件的化合物G的4种同分异构体的结构简式 ▲
①含有-SH结构
②能发生银镜反应的芳香族化合物,苯环上有 4 个取代基,不直接与 F 原子相连,且含
CH
3
C 基团
CH
3
③核磁共振氢谱显示含4种不同环境的H原子
(6)乙醛和L( )为原料可合成化合物B,利用已知信息和流程路线中的相关信息,
设计合成路线(用流程图表示,无机试剂任选) ▲
Z20名校联盟(浙江省名校新高考研究联盟)2025届高三第三次联考 化学试题卷 第 8 页 共 8 页