文档内容
湖南师范大学附属中学2025届高三下学期模拟试卷(一)化学试题
一、单选题
1.科技是国家强盛之基,创新是民族进步之魂。下列说法正确的是
A.“天目一号”气象卫星的光伏发电系统,可将化学能转化成电能
B.C919飞机上使用了芳纶纤维,芳纶属于天然纤维
C.一种高性能涂料的主要成分石墨烯属于不饱和有机物
D.“天和核心舱”电推进系统中的腔体采用氮化硼陶瓷,其属于新型无机非金属材料
2.下列化学用语或表述正确的是
A.HS的电子式:
2
B.基态氧原子的核外电子排布图:
C.气态二聚氟化氢[(HF) ]分子结构:
2
D.《易经》中“泽中有火”描述了沼气燃烧,沼气的危险品标识:
3.实验室进行下列实验时,所选玻璃仪器(其他材质仪器任选)均正确的是
A.用含水酒精制备无水乙醇:①⑧⑨
B.除去苯中的二甲苯:②④⑥⑦
C.除去 KNO 中少量NaCl:②⑤⑧⑨
3
D.配制质量分数约为20%的 NaCl溶液:⑧⑨⑩
4.从微观视角探析物质结构及性质是学习化学的有效方法。下列说法正确的是
A.环己烷中的碳原子为sp3杂化,苯中的碳原子为sp2杂化,因此苯的C—H键能大于环己烷的C—H
键能
B.C H₈分子中的碳碳单键可以围绕键轴旋转,旋转时键的强度会发生改变
3C.-CF₃是吸电子基团。-CCl 是推电子基团,因此FCCOOH的酸性强于
3 3
D.O-H…O氢键的作用力大于F—H…F氢键的作用力,因此HO的沸点比HF高
2
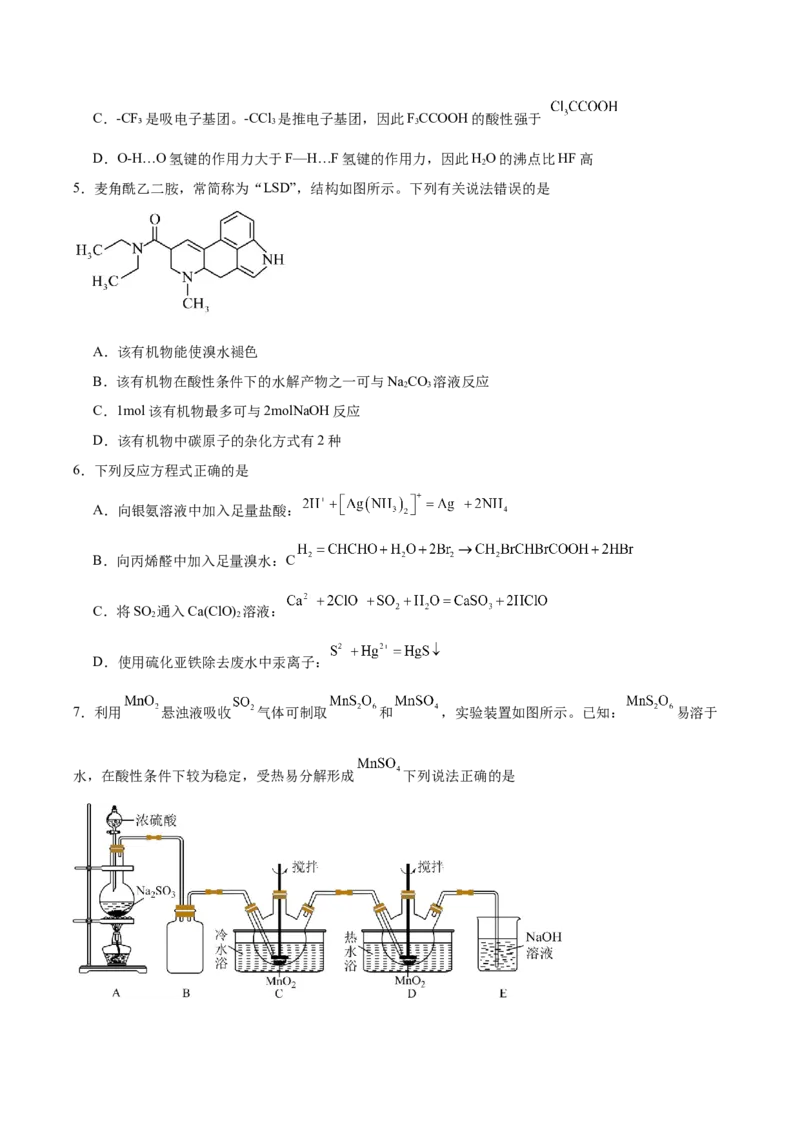
5.麦角酰乙二胺,常简称为“LSD”,结构如图所示。下列有关说法错误的是
A.该有机物能使溴水褪色
B.该有机物在酸性条件下的水解产物之一可与NaCO 溶液反应
2 3
C.1mol该有机物最多可与2molNaOH反应
D.该有机物中碳原子的杂化方式有2种
6.下列反应方程式正确的是
A.向银氨溶液中加入足量盐酸:
B.向丙烯醛中加入足量溴水:C
C.将SO 通入Ca(ClO) 溶液:
2 2
D.使用硫化亚铁除去废水中汞离子:
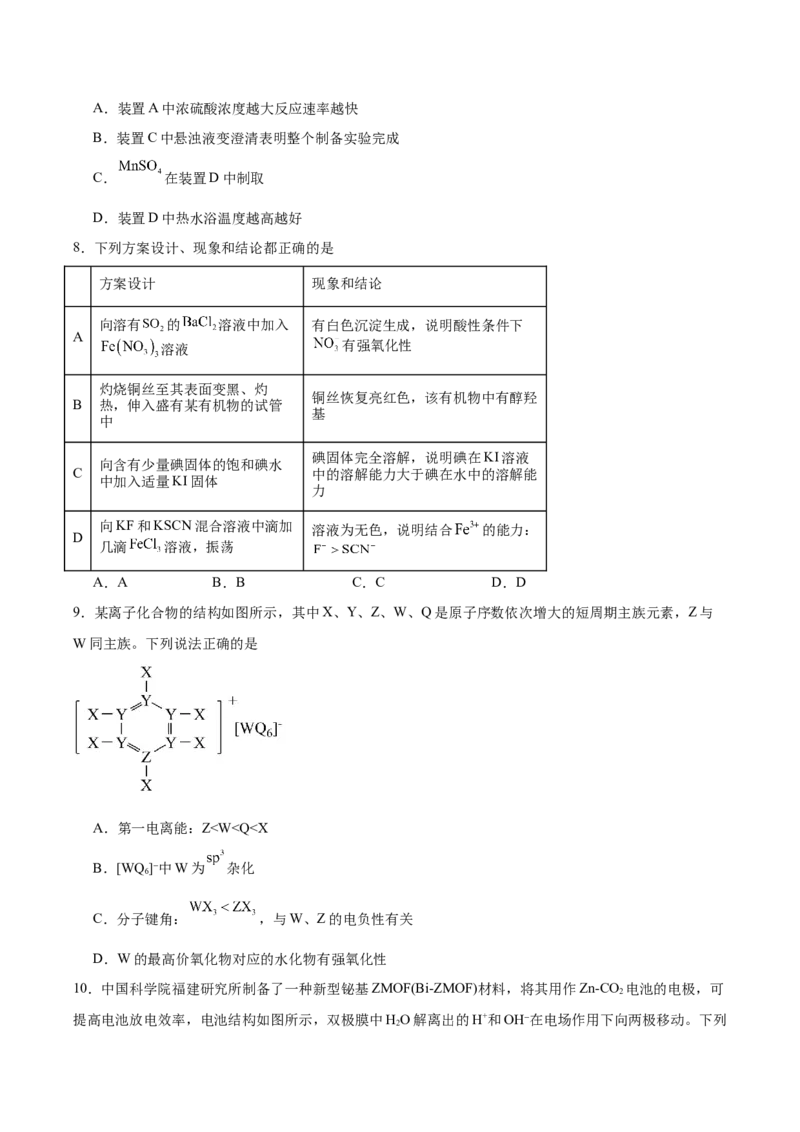
7.利用 悬浊液吸收 气体可制取 和 ,实验装置如图所示。已知: 易溶于
水,在酸性条件下较为稳定,受热易分解形成 下列说法正确的是A.装置A中浓硫酸浓度越大反应速率越快
B.装置C中悬浊液变澄清表明整个制备实验完成
C. 在装置D中制取
D.装置D中热水浴温度越高越好
8.下列方案设计、现象和结论都正确的是
方案设计 现象和结论
向溶有 的 溶液中加入 有白色沉淀生成,说明酸性条件下
A
溶液 有强氧化性
灼烧铜丝至其表面变黑、灼
铜丝恢复亮红色,该有机物中有醇羟
B 热,伸入盛有某有机物的试管
基
中
碘固体完全溶解,说明碘在KI溶液
向含有少量碘固体的饱和碘水
C 中的溶解能力大于碘在水中的溶解能
中加入适量KI固体
力
向KF和KSCN混合溶液中滴加 溶液为无色,说明结合 的能力:
D
几滴 溶液,振荡
A.A B.B C.C D.D
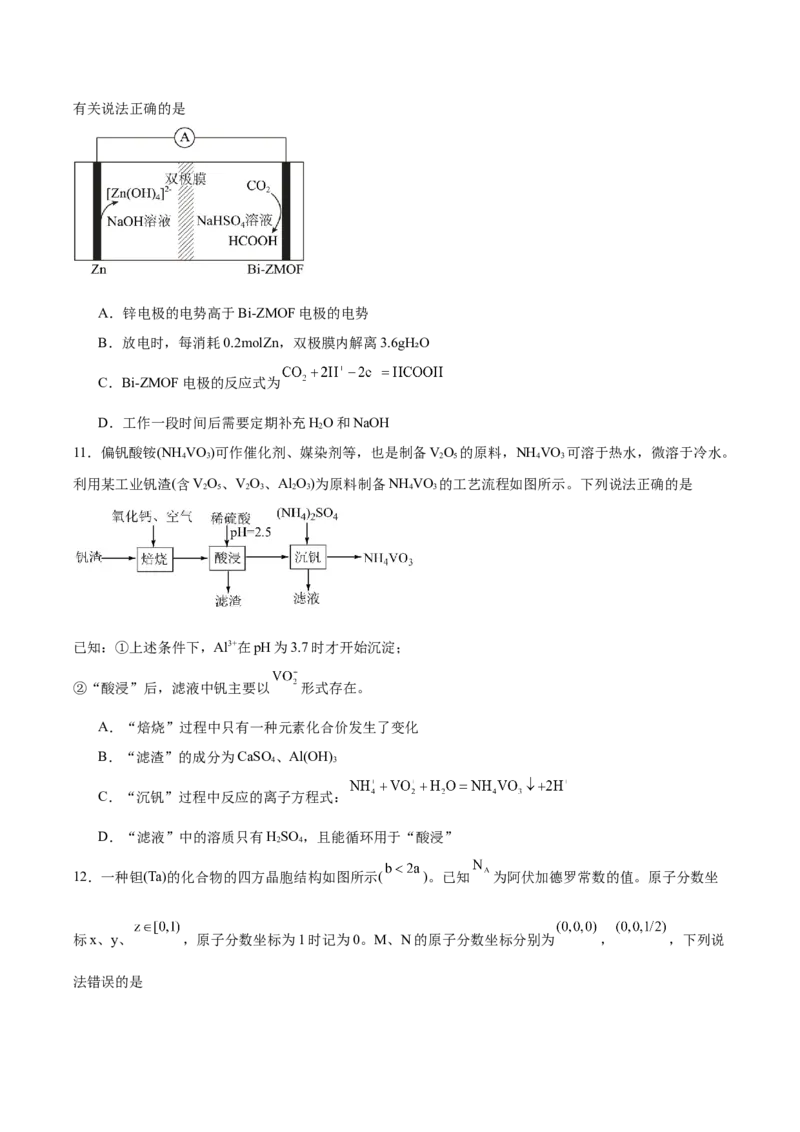
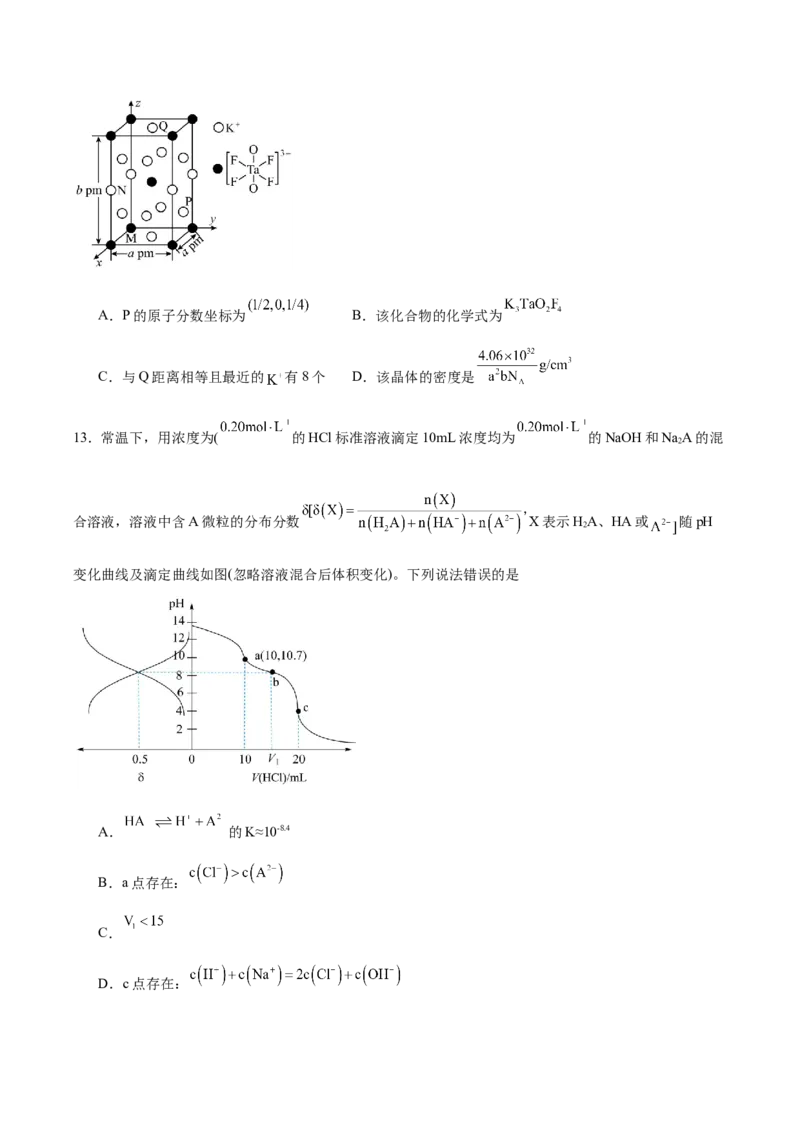
9.某离子化合物的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与
W同主族。下列说法正确的是
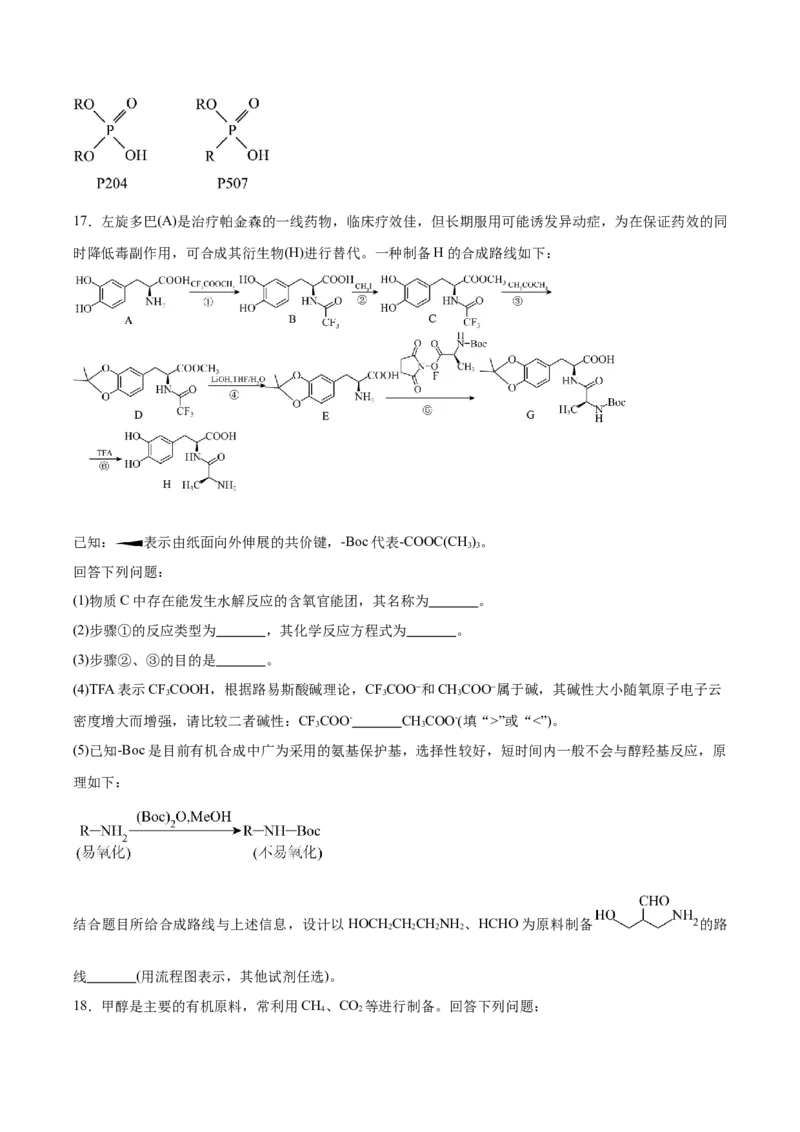
A.第一电离能:Z”或“<”)。
3 3
(5)已知-Boc是目前有机合成中广为采用的氨基保护基,选择性较好,短时间内一般不会与醇羟基反应,原
理如下:
结合题目所给合成路线与上述信息,设计以HOCH CHCHNH 、HCHO为原料制备 的路
2 2 2 2
线 (用流程图表示,其他试剂任选)。
18.甲醇是主要的有机原料,常利用CH、CO 等进行制备。回答下列问题:
4 2Ⅰ.甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
(1)2CH (g)+O(g)=2CH OH(l) ∆H=-329kJ/mol,该反应的正反应方向在 (填“高温”或“低温”)条件
4 2 3
下更有利于其自发进行。
(2)已知大多数气体分子在催化剂表面的吸附过程是放热的。从反应速率的角度分析,通入CH 后将体系温
4
度维持在200℃的原因是 (不考虑催化剂活性变化)。
Ⅱ.利用合成气CO、H₂制备甲醇,涉及的反应如下:
反应①:CO(g)+3H(g)=CH OH(g) +HO(g) ∆H<0
2 2 3 2 1
反应②:CO(g)+H(g)=CO(g)+HO(g) ∆H>0
2 2 2 2
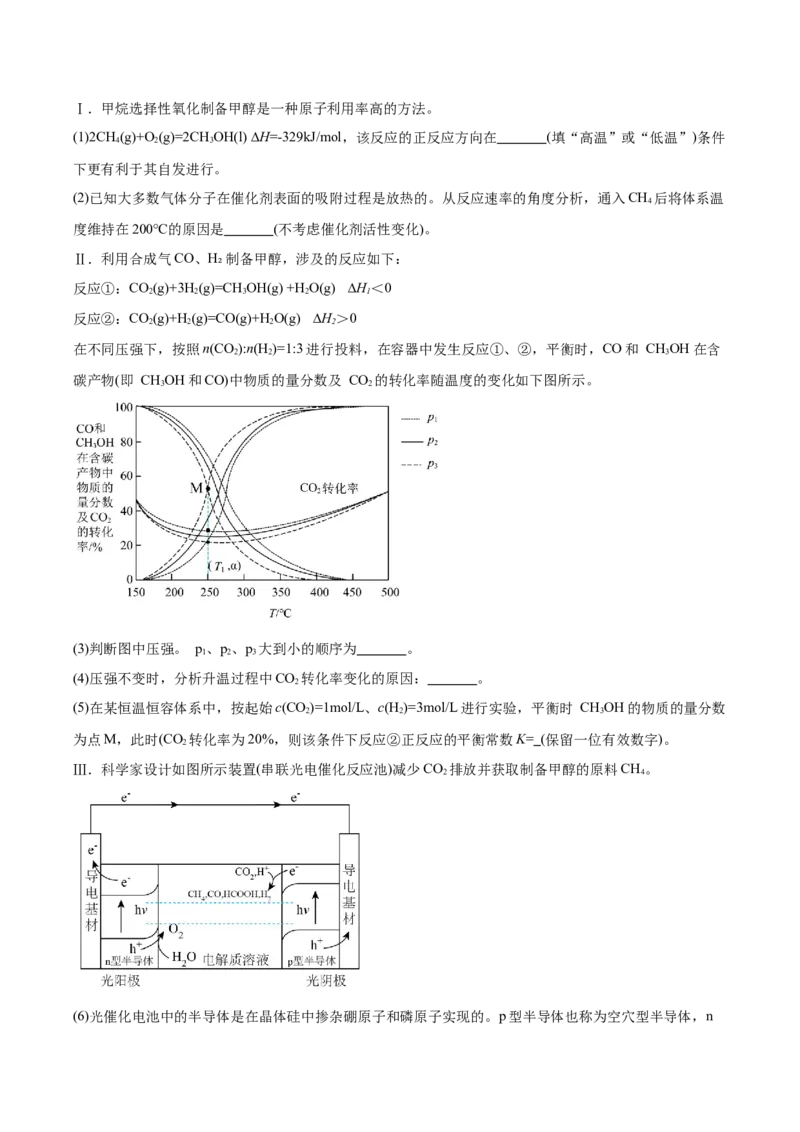
在不同压强下,按照n(CO):n(H )=1:3进行投料,在容器中发生反应①、②,平衡时,CO和 CHOH在含
2 2 3
碳产物(即 CHOH和CO)中物质的量分数及 CO 的转化率随温度的变化如下图所示。
3 2
(3)判断图中压强。 p、p、p 大到小的顺序为 。
1 2 3
(4)压强不变时,分析升温过程中CO 转化率变化的原因: 。
2
(5)在某恒温恒容体系中,按起始c(CO)=1mol/L、c(H )=3mol/L进行实验,平衡时 CHOH的物质的量分数
2 2 3
为点M,此时(CO 转化率为20%,则该条件下反应②正反应的平衡常数K= (保留一位有效数字)。
2
Ⅲ.科学家设计如图所示装置(串联光电催化反应池)减少CO 排放并获取制备甲醇的原料CH。
2 4
(6)光催化电池中的半导体是在晶体硅中掺杂硼原子和磷原子实现的。p型半导体也称为空穴型半导体,n型半导体也称为电子型半导体。据此,推测 n型半导体掺杂的是 (填元素符号)。
(7)产生 CH 的电极反应式为 。
4参考答案
1.D
2.C
3.D
4.C
5.C
6.B
7.C
8.C
9.C
10.D
11.C
12.D
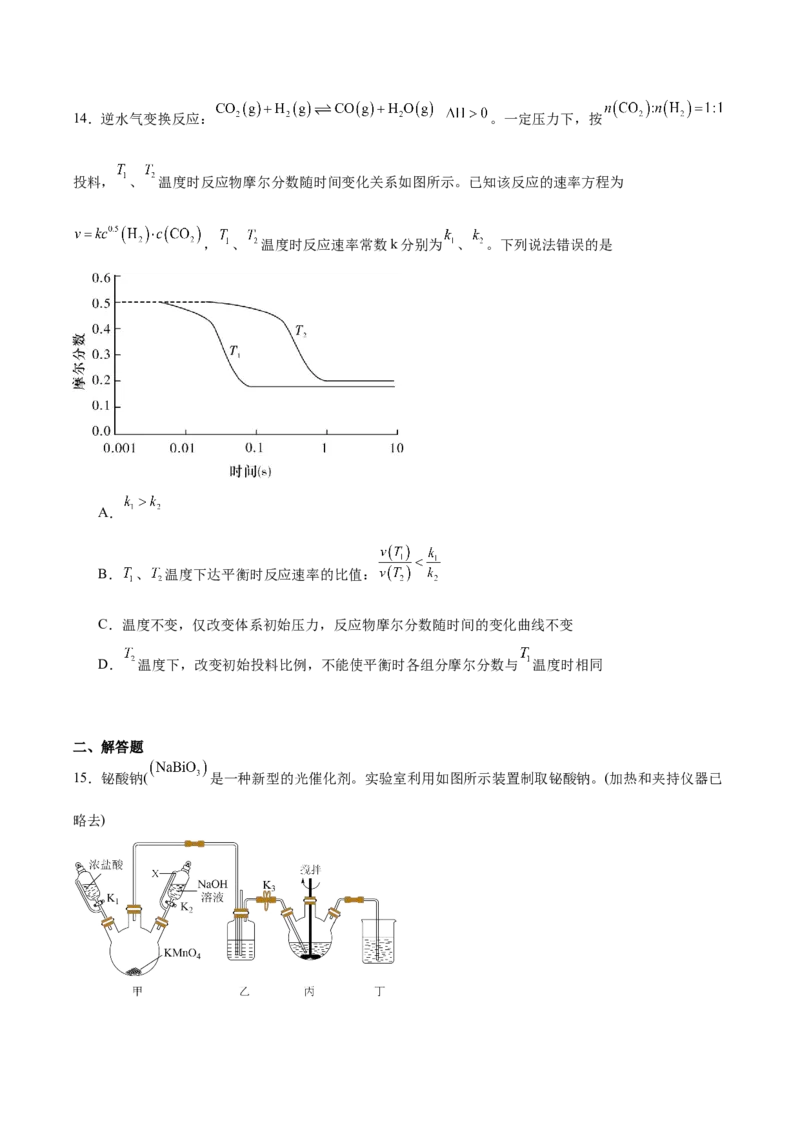
13.D
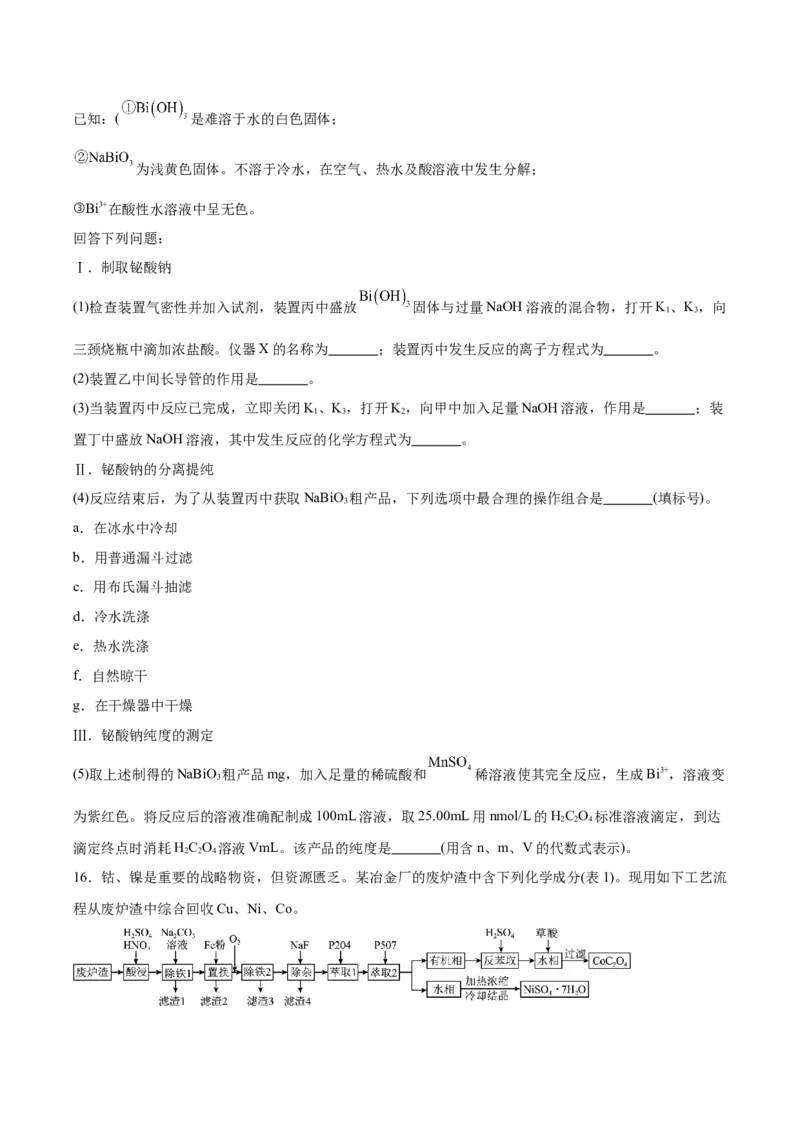
14.C
15.(1) 恒压滴液漏斗
(2)平衡装置内外气压
(3) 可防止 分解,还能吸收多余氯气
(4)acdg
(5)
16.(1)控制反应速率,防止反应过于剧烈,避免液体飞溅或气体产生过快;
(2) ; 用铁粉置换铜步骤会消耗更
多的铁粉 ;
(3)铜和铁
(4) Fe (SO )+NaSO +12HO Na Fe (SO )(OH) ↓+5H SO 与溶液中的
2 4 3 2 4 2 2 6 4 4 12 2 4
H+反应,降低H+浓度,促使Fe3+水解平衡Fe3++ 3H O Fe(OH) + 3H+向右移动,更多
2 3
Fe3+转化为黄钠铁矾晶体,提高除铁效率;
(5)20(6)小于
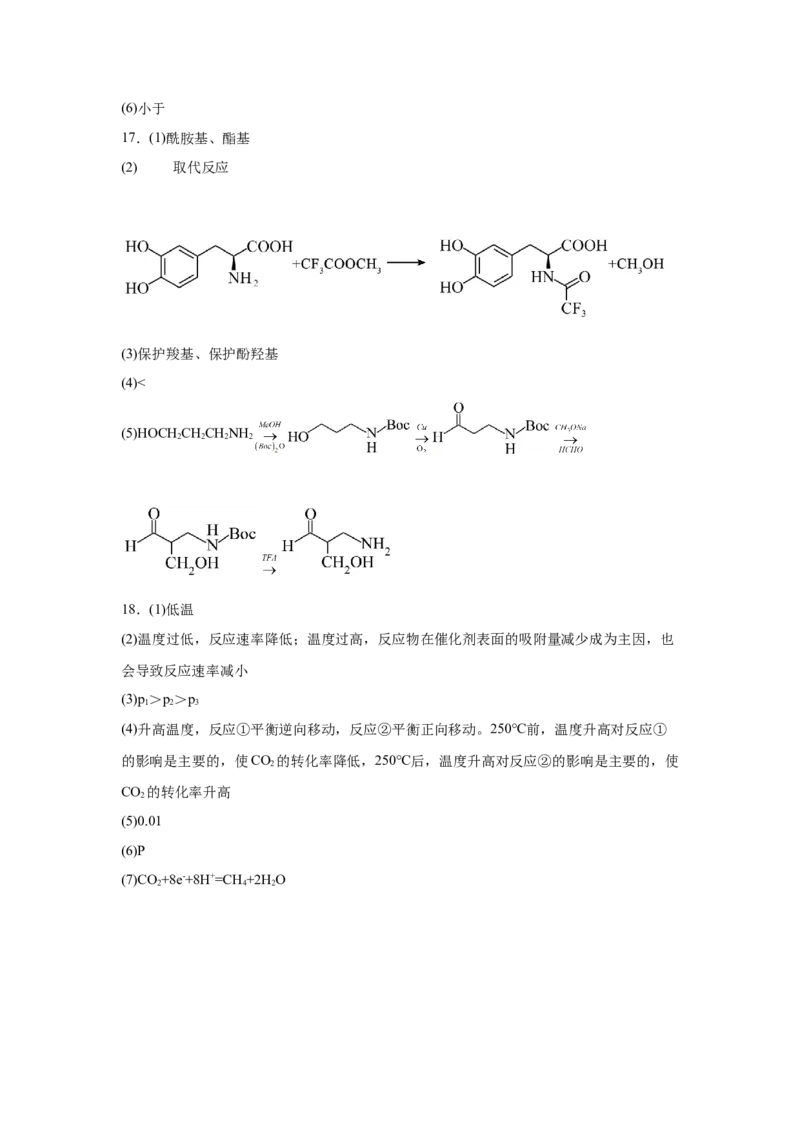
17.(1)酰胺基、酯基
(2) 取代反应
(3)保护羧基、保护酚羟基
(4)<
(5)HOCHCHCHNH
2 2 2 2
18.(1)低温
(2)温度过低,反应速率降低;温度过高,反应物在催化剂表面的吸附量减少成为主因,也
会导致反应速率减小
(3)p>p>p
1 2 3
(4)升高温度,反应①平衡逆向移动,反应②平衡正向移动。250℃前,温度升高对反应①
的影响是主要的,使CO 的转化率降低,250℃后,温度升高对反应②的影响是主要的,使
2
CO 的转化率升高
2
(5)0.01
(6)P
(7)CO +8e-+8H+=CH +2H O
2 4 2