文档内容
2025—2026 学年度第一学期高三第一次月考试题
化 学
(考试时间:90分钟;满分:100分)
可能用到的相对原子质量:H—1 N—14 O—16 Al—27 S—32 Cl—35.5 Ba—
137
第Ⅰ卷 选择题(共40分)
一、单项选择题(本题包括8小题,每小题只有一个选项符合题意。每小题2分,共16
分)
1.化学应用体现在生活的方方面面,下列用法不合理的是
A.用明矾净化文昌河水 B.用漂白粉漂白蚕丝制品
C.用食醋去除水壶中水垢 D.用小苏打作烘焙糕点膨松剂
2.下列离子组因发生氧化还原反应而不能大量共存的是
A.CO、Cl-、K+、H+ B.NH、Na+、OH-、HCO
C.Cu2+、Cl-、K+、SO D.ClO-、I-、K+、Na+
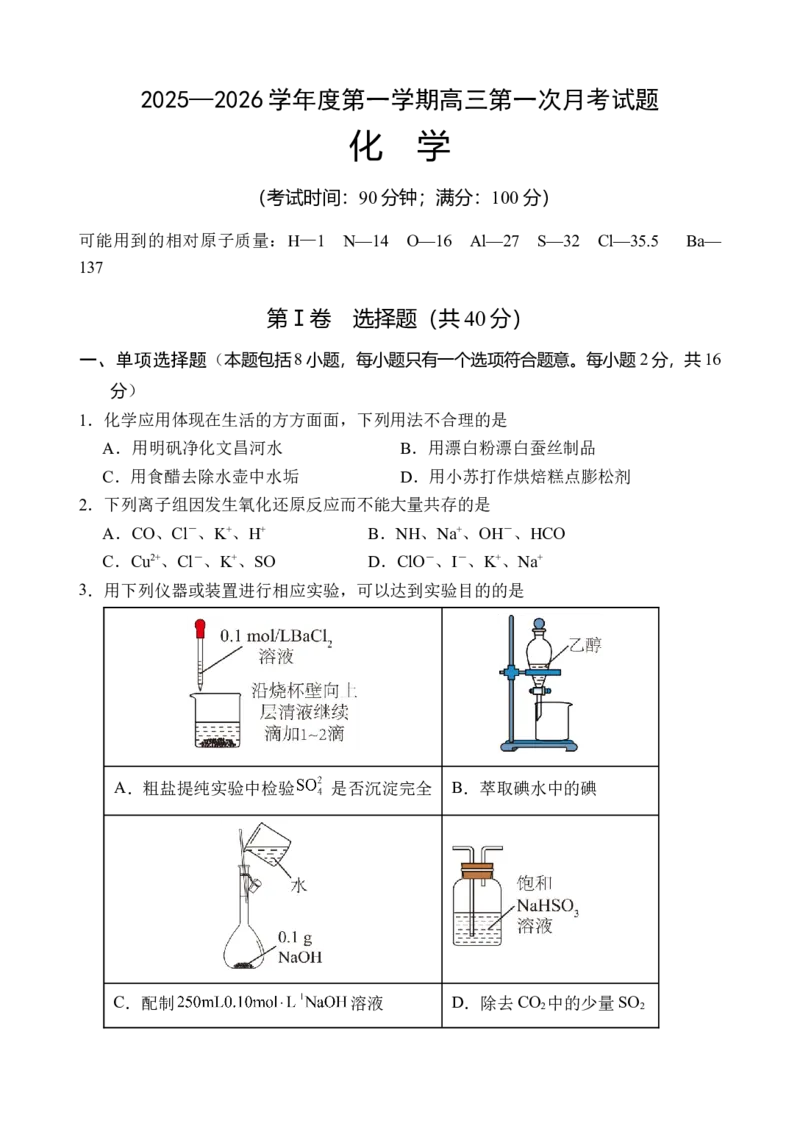
3.用下列仪器或装置进行相应实验,可以达到实验目的的是
A.粗盐提纯实验中检验 是否沉淀完全 B.萃取碘水中的碘
C.配制 溶液 D.除去CO 中的少量SO
2 24.下列在化学史上产生重要影响的成果中,不涉及氧化还原反应的是
A.拉瓦锡基于金属和O 的反应提出了燃烧的氧化学说
2
B.戴维电解盐酸得到H 和Cl ,从而提出了酸的含氢学说
2 2
C.侯德榜发明了以NH 、CO 和NaCl为原料的联合制碱法
3 2
D.哈伯发明了以N 和H 为原料合成氨的方法
2 2
5.设N 为阿伏加德罗常数值。下列说法正确的是
A
A.26g乙炔中含有σ键的数目为3N
A
B.1L1mol·L-1 NH NO 溶液中含NH +的数目为N
4 3 4 A
C.1mol CO和H 的混合气体含有的分子数目为3N
2 A
D.Na与H O反应生成11.2L H ,转移电子数目为N
2 2 A
6.用硫酸和NaN 可制备一元弱酸HN 。下列说法错误的是
3 3
A.NaN 的水溶液显碱性
3
B.N的空间构型为V形
C.NaN 为含有共价键的离子化合物
3
D.N的中心N原子所有价电子均参与成键
7.下列物质分类正确的是
A.SO 、SiO 、CO均为酸性氧化物
2 2
B.稀豆浆、鸡蛋清、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、盐酸、氨水均为混合物
8.24 mL 浓度为 0.05 mol/L 的 Na SO 溶液恰好与 20 mL 浓度为 0.02 mol/L 的
2 3
K M O 溶液完全反应。已知Na SO 被K M O 氧化为Na SO ,则元素M在还原产物
2 2 7 2 3 2 2 7 2 4
中的化合价为
A.+2 B.+3 C.+4 D.+5
二、不定项选择题(本题包括6小题,每小题有1-2个选项符合题意。每小题4分,
共24分。若该小题有两个正确选项,只选一个且正确得2分,多选错选不得分。)
9.利用软锰矿(主要成分为MnO )吸收SO₂,并制备高纯度Mn O (Mn元素显+2、
2 3 4
+3价),其原理为①MnO +SO =MnSO ;②Mn2++O +H O→Mn O ↓+H+(未
2 2 4 2 2 3 4
配平)。下列说法正确的是
A.反应①中SO 得到电子
2
B.反应①中MnO 发生氧化反应
2
C.反应②中Mn O 既是氧化产物又是还原产物
3 4
D.利用软锰矿,每制得1 mol Mn O 共转移4 mol电子
3 4
10.汽车尾气的排放会对环境造成污染,利用催化剂处理汽车尾气中的 NO与CO,反
应为2NO(g)+2CO(g) N (g)+2CO (g) △H<0。一定温度下,在1L恒容密闭容器
2 2中加入2mol NO和1 mol CO发生上述反应,3min时达到平衡,测得 c(N )=0.30
2
mol/L,下列说法正确的是
A.v(CO )=0.2mol/(L·min)
2
B.反应达到平衡时,CO 的体积分数为
2
C.催化剂加快反应速率,从而提高NO的平衡转化率
D.汽车尾气中的CO、NO是因汽油不充分燃烧产生的
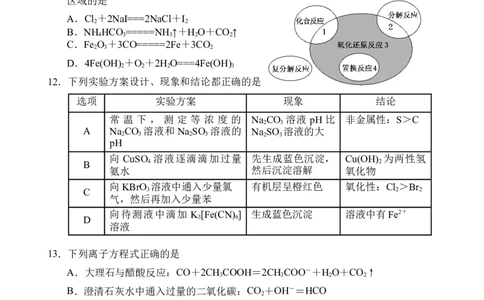
11.氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于阴影3
区域的是
A.Cl +2NaI===2NaCl+I
2 2
B.NH HCO =====NH ↑+H O+CO ↑
4 3 3 2 2
C.Fe O +3CO=====2Fe+3CO
2 3 2
D.4Fe(OH) +O +2H O===4Fe(OH)
2 2 2 3
12.下列实验方案设计、现象和结论都正确的是
选项 实验方案 现象 结论
常 温 下 , 测 定 等 浓 度 的 Na CO 溶液 pH 比 非金属性:S>C
2 3
A Na CO 溶液和Na SO 溶液的 Na SO 溶液的大
2 3 2 3 2 3
pH
向 CuSO 溶液逐滴滴加过量 先生成蓝色沉淀, Cu(OH) 为两性氢
B 4 2
氨水 然后沉淀溶解 氧化物
向KBrO 溶液中通入少量氯 有机层呈橙红色 氧化性:Cl >Br
C 3 2 2
气,然后再加入少量苯
向待测液中滴加 K [Fe(CN) ] 生成蓝色沉淀 溶液中有Fe2+
D 3 6
溶液
13.下列离子方程式正确的是
A.大理石与醋酸反应:CO+2CH COOH=2CH COO-+H O+CO ↑
3 3 2 2
B.澄清石灰水中通入过量的二氧化碳:CO +OH-=HCO
2
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO=BaSO ↓+H O
4 2
D.氢氧化钠溶液与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO=CaCO ↓+H O
3 2
14.向 500 mL FeBr 溶液中,通入适量的 Cl ,测得溶液中 c(Br-)=c(Cl-)=0.12
2 2
mol/L。反应过程中溶液的体积变化不计,则下列说法中正确的是
A.过程中只发生了2Fe2++Cl =2Fe3++2Cl-
2
B.反应后溶液中c(Fe3+)=1.5c(Cl-)
C.原溶液中c(Br-)=0.08 mol/LD.通入Cl 的体积为0.67 L(标准状况)
2第Ⅱ卷 非选择题(共60分)
三、填空题
15.(14分)
(1)0.3 mol NH 分子中所含质子数与______个H O分子中所含质子数相等。
3 2
(2)含0.4 mol Al3+的Al (SO ) 中所含的SO的物质的量是________。
2 4 3
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔
质量为________。
(4)2.3 g Na中含________ mol e-,在跟足量水反应中失去________ mol e-。
(5)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设
N 为阿伏加德罗常数)________。
A
(6)实验室需200 mL 4.6 mol/L的稀硫酸,现用98%(密度为1.84g/cm3)的浓硫酸
配置,需浓硫酸的体积 。
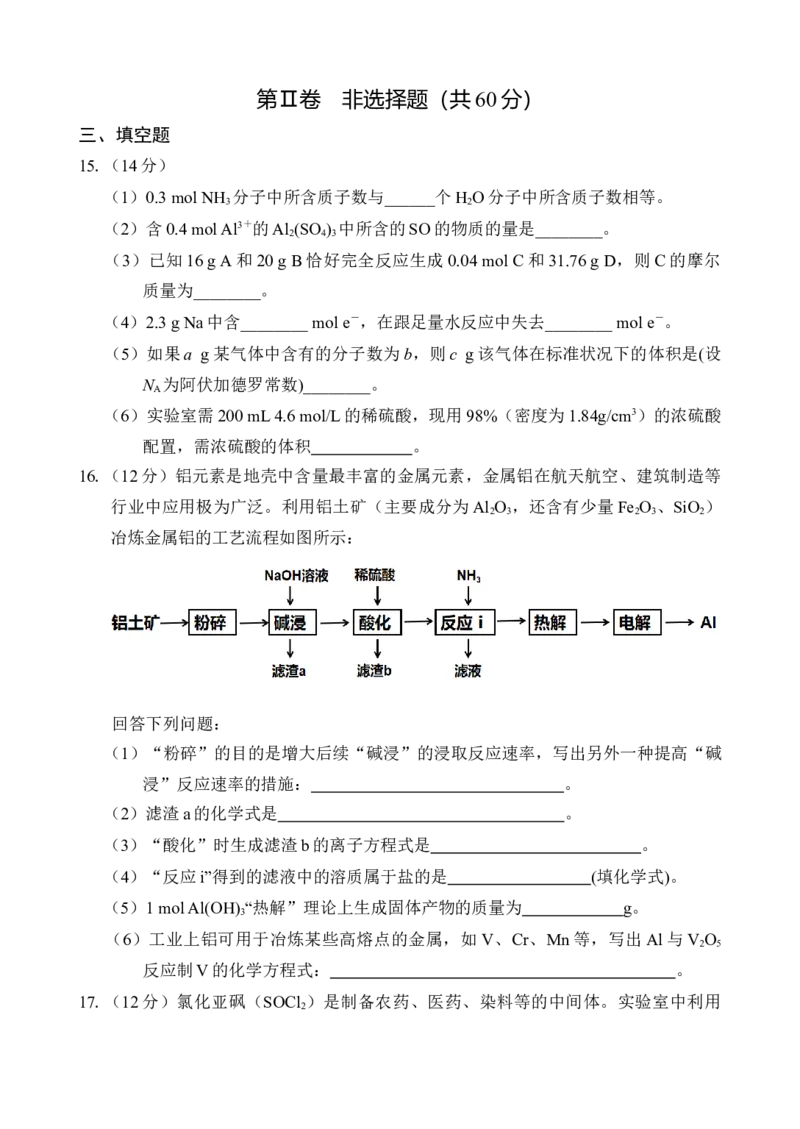
16.(12分)铝元素是地壳中含量最丰富的金属元素,金属铝在航天航空、建筑制造等
行业中应用极为广泛。利用铝土矿(主要成分为Al O ,还含有少量Fe O 、SiO )
2 3 2 3 2
冶炼金属铝的工艺流程如图所示:
回答下列问题:
(1)“粉碎”的目的是增大后续“碱浸”的浸取反应速率,写出另外一种提高“碱
浸”反应速率的措施: 。
(2)滤渣a的化学式是 。
(3)“酸化”时生成滤渣b的离子方程式是 。
(4)“反应i”得到的滤液中的溶质属于盐的是 (填化学式)。
(5)1 mol Al(OH) “热解”理论上生成固体产物的质量为 g。
3
(6)工业上铝可用于冶炼某些高熔点的金属,如V、Cr、Mn等,写出Al与V O
2 5
反应制V的化学方程式: 。
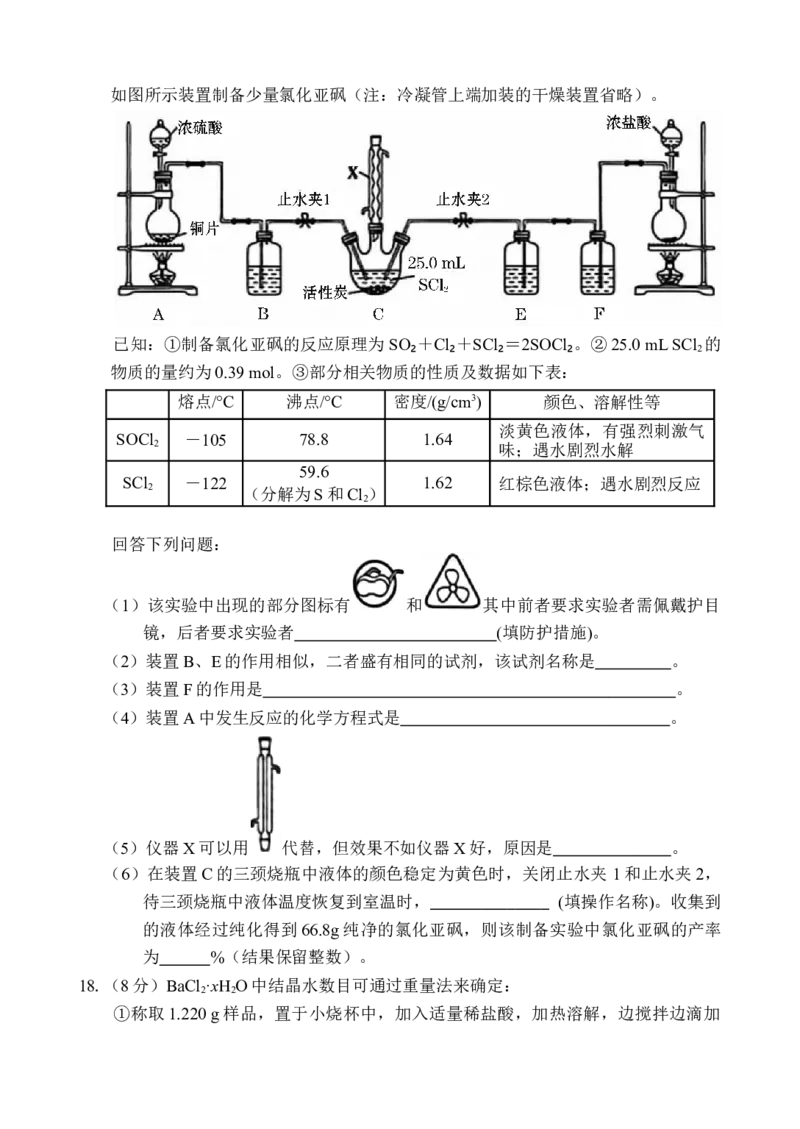
17.(12分)氯化亚砜(SOCl )是制备农药、医药、染料等的中间体。实验室中利用
2如图所示装置制备少量氯化亚砜(注:冷凝管上端加装的干燥装置省略)。
已知:①制备氯化亚砜的反应原理为SO₂+Cl₂+SCl₂=2SOCl₂。②25.0 mL SCl 的
2
物质的量约为0.39 mol。③部分相关物质的性质及数据如下表:
熔点/°C 沸点/°C 密度/(g/cm3) 颜色、溶解性等
淡黄色液体,有强烈刺激气
SOCl -105 78.8 1.64
2 味;遇水剧烈水解
59.6
SCl -122 1.62 红棕色液体;遇水剧烈反应
2 (分解为S和Cl )
2
回答下列问题:
(1)该实验中出现的部分图标有 和 其中前者要求实验者需佩戴护目
镜,后者要求实验者 (填防护措施)。
(2)装置B、E的作用相似,二者盛有相同的试剂,该试剂名称是 。
(3)装置F的作用是 。
(4)装置A中发生反应的化学方程式是 。
(5)仪器X可以用 代替,但效果不如仪器X好,原因是 。
(6)在装置C的三颈烧瓶中液体的颜色稳定为黄色时,关闭止水夹 1和止水夹2,
待三颈烧瓶中液体温度恢复到室温时, (填操作名称)。收集到
的液体经过纯化得到66.8g纯净的氯化亚砜,则该制备实验中氯化亚砜的产率
为 %(结果保留整数)。
18.(8分)BaCl ·xH O中结晶水数目可通过重量法来确定:
2 2
①称取1.220 g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉
淀质量为1.165 g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和________洗涤沉淀;检验沉淀中氯离子是否
洗净的方法是________________________________________________。
(2)计算BaCl ·xH O中的x=________。
2 2
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原
为BaS,这使x的测定结果________(填“偏低”、“偏高”或“不变”)。
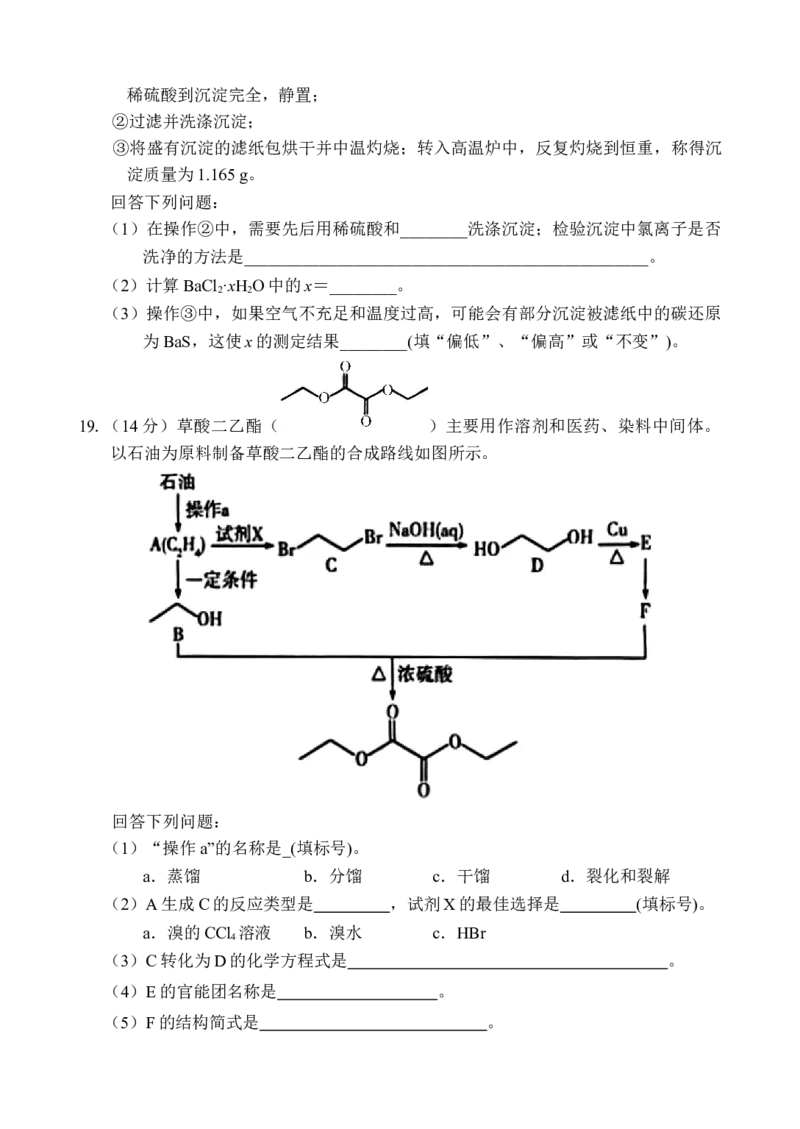
19.(14分)草酸二乙酯( )主要用作溶剂和医药、染料中间体。
以石油为原料制备草酸二乙酯的合成路线如图所示。
回答下列问题:
(1)“操作a”的名称是_(填标号)。
a.蒸馏 b.分馏 c.干馏 d.裂化和裂解
(2)A生成C的反应类型是 ,试剂X的最佳选择是 (填标号)。
a.溴的CCl 溶液 b.溴水 c.HBr
4
(3)C转化为D的化学方程式是 。
(4)E的官能团名称是 。
(5)F的结构简式是 。(6)Y为草酸二乙酯的同分异构体,1 molY与足量NaHCO 溶液反应生成2mol CO ,
3 2
则Y的结构有 种(不考虑立体异构),其中,核磁共振氢谱有3组峰的
Y的结构简式是 (填一种)。