文档内容
福建省厦门第一中学 2025-2026 学年上学期 10 月月考
高三年化学学科试卷
命题教师: 审核教师: 2025.10
说明:1. 完成时间75分钟
2. 可能用到的相对原子质量:H—1 B—11 C—12 N—14 O—16 S—32 Fe—56 Mo—96
一.单项选择题(共12题,1-5题每题3分,6-12题每题4分,共43分。每题只有一个选项符合题意)
1.化学与生产、生活密切相关。下列有关说法错误的是
A.晋朝傅玄“近朱者赤,近墨者黑”中的“朱”的主要成分为HgS
B.合成纤维、人造纤维及碳纤维都属于有机高分子材料
C.长期服用阿司匹林(乙酰水杨酸)因其水解产物水杨酸具有酸性导致胃部不适
D.大桥路面使用的沥青是可以通过石油分馏这一物理变化过程得到
2.下列离子方程式正确的是
A.向FeBr 溶液通入等物质的量的Cl :2Fe2++2Br- +2Cl =2Fe3++Br +4Cl-
2 2 2 2
B.向NH Al(SO ) 溶液中滴加Ba(OH) 使SO 2-恰好完全反应:
4 4 2 2 4
2Ba2++4OH- +Al3++2SO 2- =2BaSO ↓+[Al(OH) ]-
4 4 4
C.向CuSO 溶液通入H S:Cu2++S2- =CuS↓
4 2
D.用氨水清洗附着在试管内壁的AgCl:Ag++2NH ·H O=[Ag(NH ) ]++2H O
3 2 3 2 2
3.在下列条件下,一定能大量共存的离子组是
A.无色澄清透明溶液:[Fe(CN) ]3-、NO -、K+、Br-
6 3
B.0.1mol·L-1的Na CO 溶液中:Na+、K+、I-、[Al(OH) ]-
2 3 4
C.加入锌粉后只有红色金属单质析出现象的溶液中:Fe3+、H+、NO -、Cl-
3
D.与单质Al反应生成氢气溶液:Na+、Mg2+、NO -、SO 2-
3 4
4.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.273K、101kPa下,22.4L的 和11.2L的 混合反应,则反应后气体分子数为
B.加热条件下, 和 充分反应,转移的电子数目为
C. 分子中:含σ键的数目为5 ,含 键的数目为2
D.已知NaH PO 为正盐,则1molH PO 含羟基数为2N
2 2 3 2 A
高二化学 第 1 页 共8页5.某矿物因有良好的抗紫外线功能而被作为防晒霜的重要成分,该矿物主要成分的化学式为
AB (BX Y )(YZ) 。Z、Y、B、X、A的原子序数依次增大且均为前四周期主族元素,这五种元素原
2 3 10 2
子序数之和为55。其中,Z无中子数,Y的最外层电子数是最内层电子数的3倍,X的最高价氧化物
对应的水化物难溶于水,B是地壳中含量最多的金属元素。下列说法正确的是
A.简单离子半径:A>B>Y
B.B的氧化物可以和A的最高价氧化物对应的水化物发生反应
C.X与Y元素组成物质XY ,其空间构型为直线形
2
D.元素的电负性:Y>A>Z
阅读下列材料,完成6~7题:
二氧化氯(ClO )是国际上公认的安全、无毒的绿色消毒剂。对酸性污水中的Mn2+也有明显的去除效
2
果,其反应原理为:ClO +Mn2+→MnO ↓+Cl-(部分反应物和产物省略、未配平),工业上可用NaClO
2 2 3
制取ClO ,化学方程式如下:2NaClO +SO +H SO =2ClO +2NaHSO 。
2 3 2 2 4 2 4
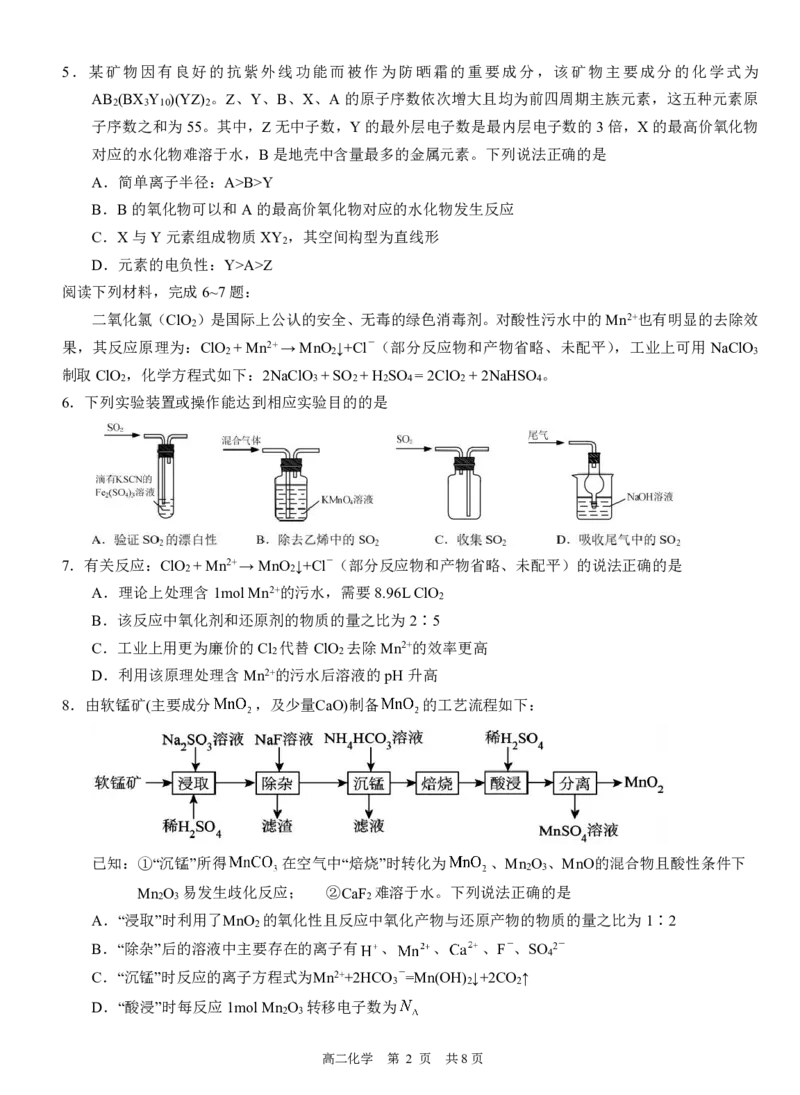
6.下列实验装置或操作能达到相应实验目的的是
7.有关反应:ClO +Mn2+→MnO ↓+Cl-(部分反应物和产物省略、未配平)的说法正确的是
2 2
A.理论上处理含1molMn2+的污水,需要8.96LClO
2
B.该反应中氧化剂和还原剂的物质的量之比为2∶5
C.工业上用更为廉价的Cl 代替ClO 去除Mn2+的效率更高
2 2
D.利用该原理处理含Mn2+的污水后溶液的pH升高
8.由软锰矿(主要成分 ,及少量CaO)制备 的工艺流程如下:
已知:①“沉锰”所得 在空气中“焙烧”时转化为 、Mn O 、MnO的混合物且酸性条件下
2 3
Mn O 易发生歧化反应; ②CaF 难溶于水。下列说法正确的是
2 3 2
A.“浸取”时利用了MnO 的氧化性且反应中氧化产物与还原产物的物质的量之比为1∶2
2
B.“除杂”后的溶液中主要存在的离子有 、 、 、F-、SO 2-
4
C.“沉锰”时反应的离子方程式为Mn2++2HCO -=Mn(OH) ↓+2CO ↑
3 2 2
D.“酸浸”时每反应1molMn O 转移电子数为
2 3
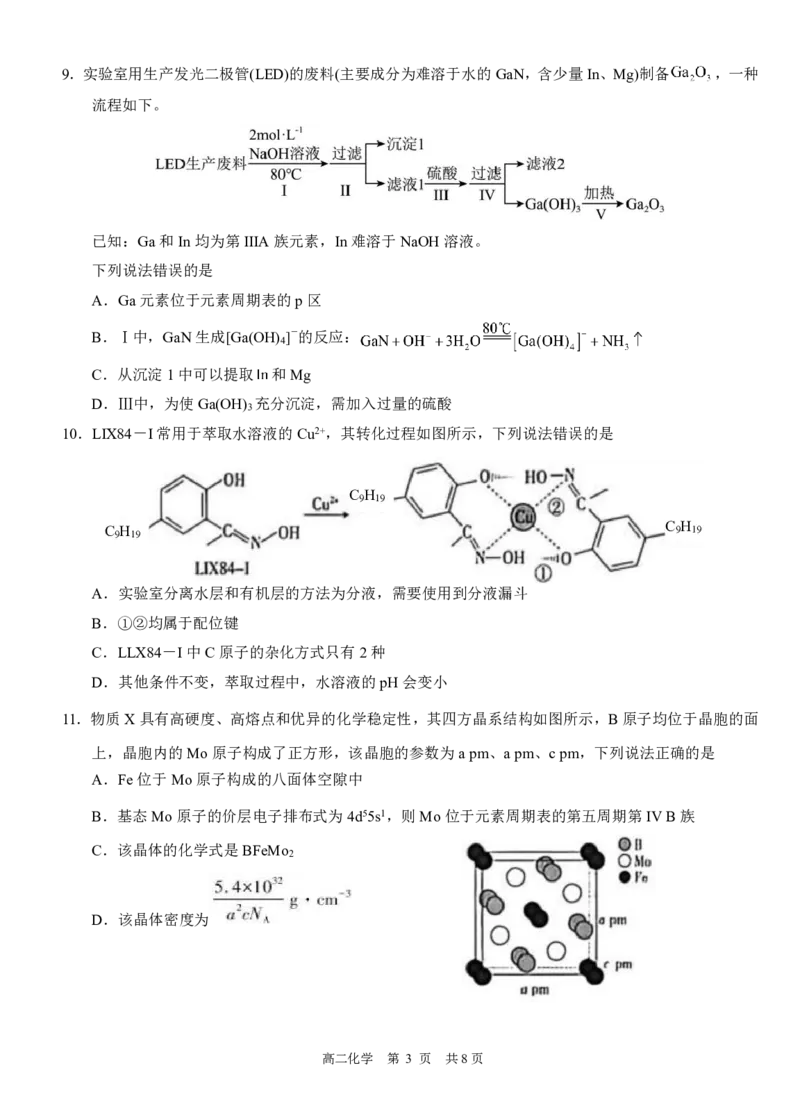
高二化学 第 2 页 共8页9.实验室用生产发光二极管(LED)的废料(主要成分为难溶于水的GaN,含少量In、Mg)制备 ,一种
流程如下。
已知:Ga和In均为第IIIA族元素,In难溶于NaOH溶液。
下列说法错误的是
A.Ga元素位于元素周期表的p区
B.Ⅰ中,GaN生成[Ga(OH) ]-的反应:
4
C.从沉淀1中可以提取 和Mg
D.Ⅲ中,为使Ga(OH) 充分沉淀,需加入过量的硫酸
3
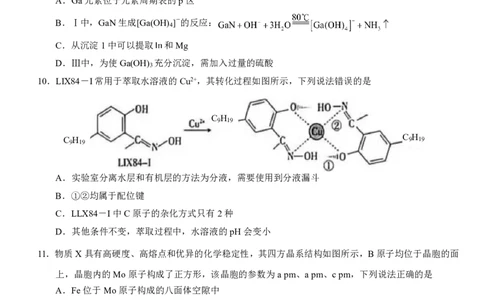
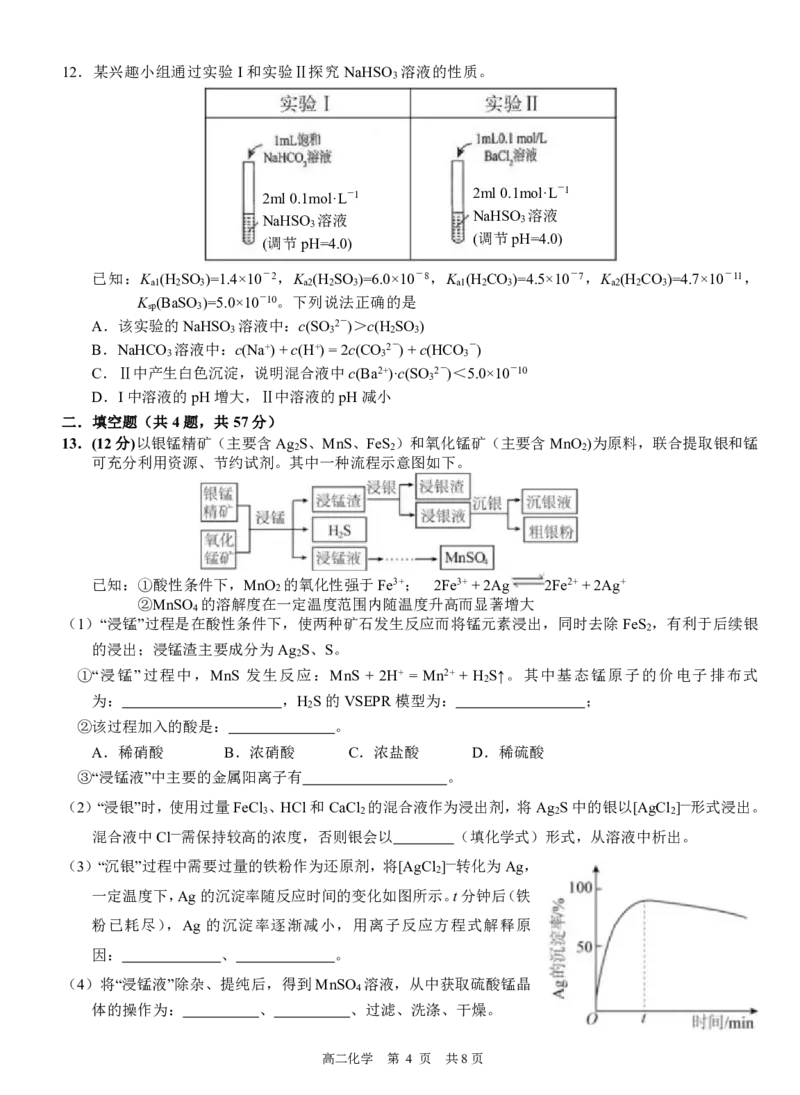
10.LIX84-I常用于萃取水溶液的Cu2+,其转化过程如图所示,下列说法错误的是
C H
9 19
C H
C H 9 19
9 19
A.实验室分离水层和有机层的方法为分液,需要使用到分液漏斗
B.①②均属于配位键
C.LLX84-I中C原子的杂化方式只有2种
D.其他条件不变,萃取过程中,水溶液的pH会变小
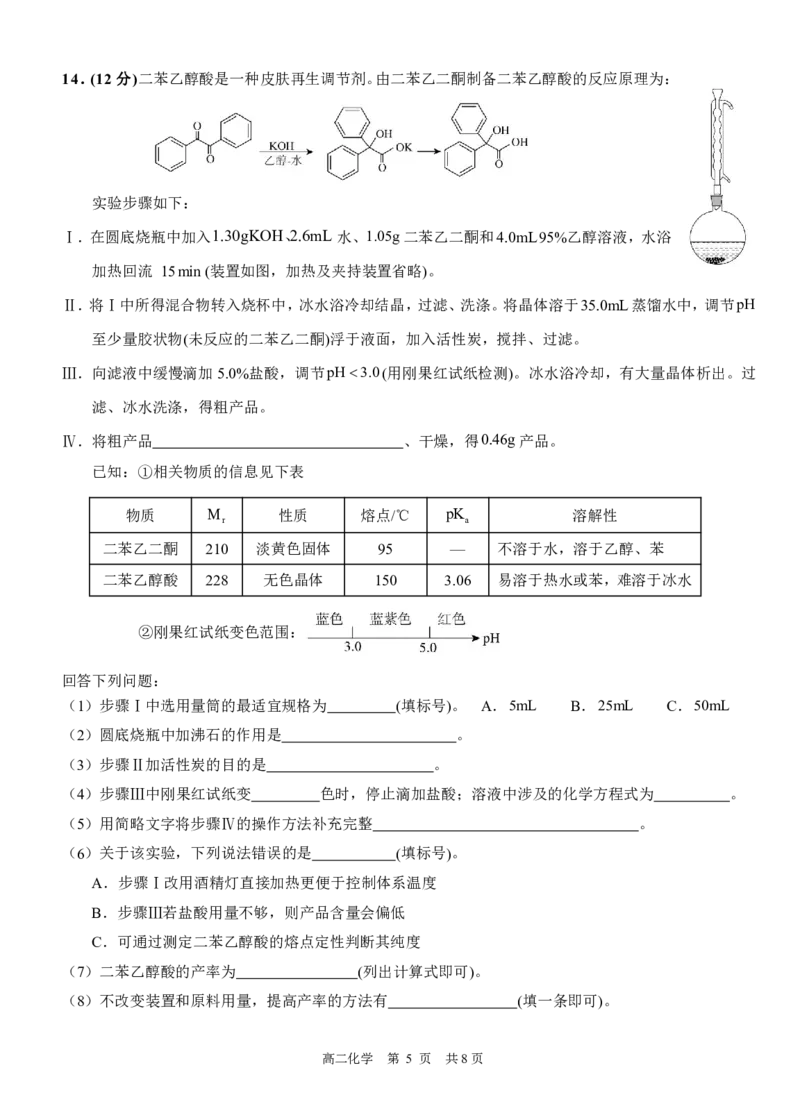
11.物质X具有高硬度、高熔点和优异的化学稳定性,其四方晶系结构如图所示,B原子均位于晶胞的面
上,晶胞内的Mo原子构成了正方形,该晶胞的参数为apm、apm、cpm,下列说法正确的是
A.Fe位于Mo原子构成的八面体空隙中
B.基态Mo原子的价层电子排布式为4d55s1,则Mo位于元素周期表的第五周期第IVB族
C.该晶体的化学式是BFeMo
2
D.该晶体密度为
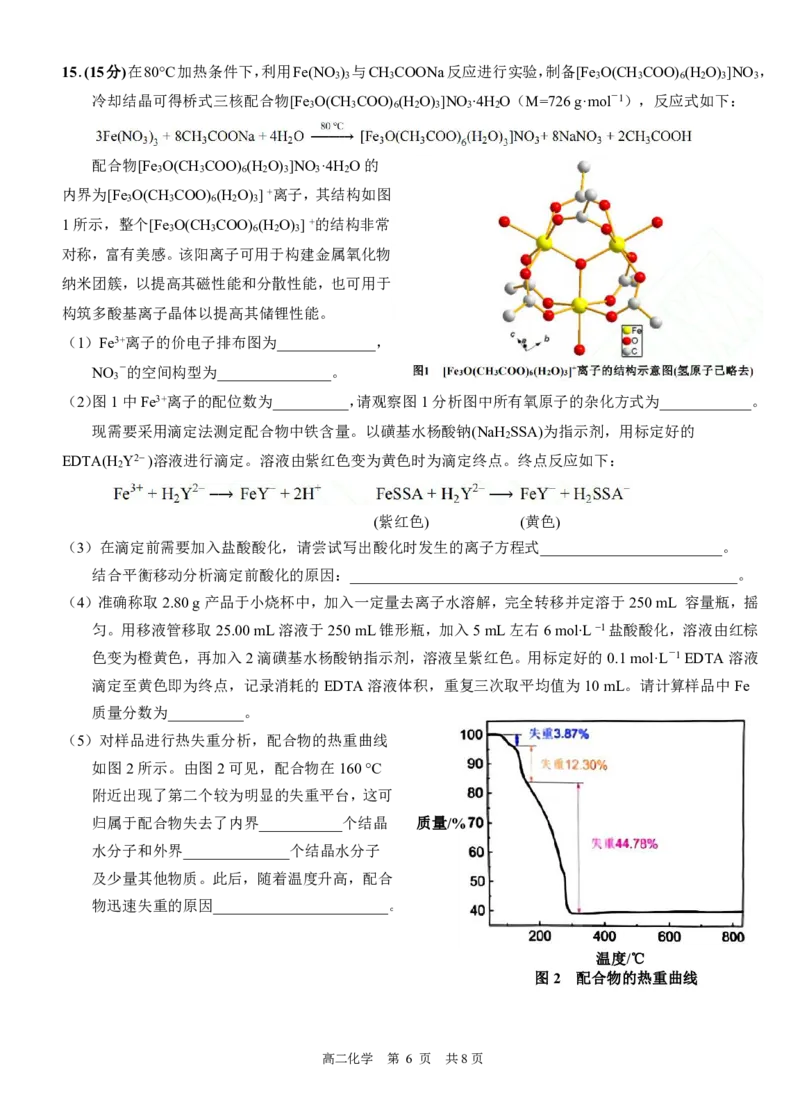
高二化学 第 3 页 共8页12.某兴趣小组通过实验 I和实验Ⅱ探究NaHSO 溶液的性质。
3
2ml0.1mol·L-1
2ml0.1mol·L-1
NaHSO 溶液 NaHSO 3 溶液
3
(调节pH=4.0)
(调节pH=4.0)
已知:K (H SO )=1.4×10-2,K (H SO )=6.0×10-8,K (H CO )=4.5×10-7,K (H CO )=4.7×10-11,
a1 2 3 a2 2 3 a1 2 3 a2 2 3
K (BaSO )=5.0×10-10。下列说法正确的是
sp 3
A.该实验的NaHSO 溶液中:c(SO 2-)>c(H SO )
3 3 2 3
B.NaHCO 溶液中:c(Na+)+c(H+)=2c(CO 2-)+c(HCO -)
3 3 3
C.Ⅱ中产生白色沉淀,说明混合液中c(Ba2+)·c(SO 2-)<5.0×10-10
3
D.I中溶液的pH增大,Ⅱ中溶液的pH减小
二.填空题(共4题,共57分)
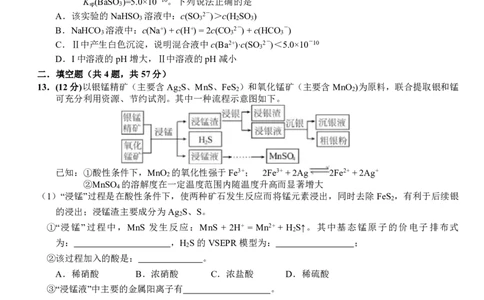
13.(12分)以银锰精矿(主要含Ag S、MnS、FeS )和氧化锰矿(主要含MnO )为原料,联合提取银和锰
2 2 2
可充分利用资源、节约试剂。其中一种流程示意图如下。
已知:①酸性条件下,MnO 的氧化性强于Fe3+; 2Fe3++2Ag 2Fe2++2Ag+
2
②MnSO 的溶解度在一定温度范围内随温度升高而显著增大
4
(1)“浸锰”过程是在酸性条件下,使两种矿石发生反应而将锰元素浸出,同时去除FeS ,有利于后续银
2
的浸出;浸锰渣主要成分为Ag S、S。
2
①“浸锰”过程中,MnS 发生反应:MnS + 2H+ = Mn2++ H S↑。其中基态锰原子的价电子排布式
2
为: ,H S的VSEPR模型为: ;
2
②该过程加入的酸是: 。
A.稀硝酸 B.浓硝酸 C.浓盐酸 D.稀硫酸
③“浸锰液”中主要的金属阳离子有 。
(2)“浸银”时,使用过量FeCl 、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以[AgCl ]—形式浸出。
3 2 2 2
混合液中Cl—需保持较高的浓度,否则银会以 (填化学式)形式,从溶液中析出。
(3)“沉银”过程中需要过量的铁粉作为还原剂,将[AgCl ]—转化为Ag,
2
一定温度下,Ag的沉淀率随反应时间的变化如图所示。t分钟后(铁
粉已耗尽),Ag 的沉淀率逐渐减小,用离子反应方程式解释原
因: 、 。
(4)将“浸锰液”除杂、提纯后,得到MnSO 溶液,从中获取硫酸锰晶
4
体的操作为: 、 、过滤、洗涤、干燥。
高二化学 第 4 页 共8页14.(12 分)二苯乙醇酸是一种皮肤再生调节剂。由二苯乙二酮制备二苯乙醇酸的反应原理为:
实验步骤如下:
Ⅰ.在圆底烧瓶中加入1.30gKOH、2.6mL 水、1.05g二苯乙二酮和4.0mL95%乙醇溶液,水浴
加热回流 15min(装置如图,加热及夹持装置省略)。
Ⅱ.将Ⅰ中所得混合物转入烧杯中,冰水浴冷却结晶,过滤、洗涤。将晶体溶于35.0mL蒸馏水中,调节pH
至少量胶状物(未反应的二苯乙二酮)浮于液面,加入活性炭,搅拌、过滤。
Ⅲ.向滤液中缓慢滴加5.0%盐酸,调节pH3.0(用刚果红试纸检测)。冰水浴冷却,有大量晶体析出。过
滤、冰水洗涤,得粗产品。
Ⅳ.将粗产品 、干燥,得0.46g产品。
已知:①相关物质的信息见下表
物质 M 性质 熔点/℃ pK 溶解性
r a
二苯乙二酮 210 淡黄色固体 95 — 不溶于水,溶于乙醇、苯
二苯乙醇酸 228 无色晶体 150 3.06 易溶于热水或苯,难溶于冰水
②刚果红试纸变色范围:
回答下列问题:
(1)步骤Ⅰ中选用量筒的最适宜规格为 (填标号)。 A.5mL B.25mL C.50mL
(2)圆底烧瓶中加沸石的作用是 。
(3)步骤Ⅱ加活性炭的目的是 。
(4)步骤Ⅲ中刚果红试纸变 色时,停止滴加盐酸;溶液中涉及的化学方程式为 。
(5)用简略文字将步骤Ⅳ的操作方法补充完整 。
(6)关于该实验,下列说法错误的是 (填标号)。
A.步骤Ⅰ改用酒精灯直接加热更便于控制体系温度
B.步骤Ⅲ若盐酸用量不够,则产品含量会偏低
C.可通过测定二苯乙醇酸的熔点定性判断其纯度
(7)二苯乙醇酸的产率为 (列出计算式即可)。
(8)不改变装置和原料用量,提高产率的方法有 (填一条即可)。
高二化学 第 5 页 共8页15.(15分)在80°C加热条件下,利用Fe(NO ) 与CH COONa反应进行实验,制备[Fe O(CH COO) (H O) ]NO ,
3 3 3 3 3 6 2 3 3
冷却结晶可得桥式三核配合物[Fe O(CH COO) (H O) ]NO ∙4H O(M=726g·mol-1),反应式如下:
3 3 6 2 3 3 2
配合物[Fe O(CH COO) (H O) ]NO ·4H O的
3 3 6 2 3 3 2
内界为[Fe O(CH COO) (H O) ]+离子,其结构如图
3 3 6 2 3
1所示,整个[Fe O(CH COO) (H O) ]+的结构非常
3 3 6 2 3
对称,富有美感。该阳离子可用于构建金属氧化物
纳米团簇,以提高其磁性能和分散性能,也可用于
构筑多酸基离子晶体以提高其储锂性能。
(1)Fe3+离子的价电子排布图为_____________,
NO -的空间构型为_______________。
3
(2)图1中Fe3+离子的配位数为__________,请观察图1分析图中所有氧原子的杂化方式为____________。
现需要采用滴定法测定配合物中铁含量。以磺基水杨酸钠(NaH SSA)为指示剂,用标定好的
2
EDTA(H Y2−)溶液进行滴定。溶液由紫红色变为黄色时为滴定终点。终点反应如下:
2
(紫红色) (黄色)
(3)在滴定前需要加入盐酸酸化,请尝试写出酸化时发生的离子方程式________________________。
结合平衡移动分析滴定前酸化的原因:___________________________________________________。
(4)准确称取2.80g产品于小烧杯中,加入一定量去离子水溶解,完全转移并定溶于250mL 容量瓶,摇
匀。用移液管移取25.00mL溶液于250mL锥形瓶,加入5mL左右6mol∙L−1盐酸酸化,溶液由红棕
色变为橙黄色,再加入2滴磺基水杨酸钠指示剂,溶液呈紫红色。用标定好的0.1mol·L-1EDTA溶液
滴定至黄色即为终点,记录消耗的EDTA溶液体积,重复三次取平均值为10mL。请计算样品中Fe
质量分数为__________。
(5)对样品进行热失重分析,配合物的热重曲线
如图2所示。由图2可见,配合物在160°C
附近出现了第二个较为明显的失重平台,这可
归属于配合物失去了内界___________个结晶 质量/%
水分子和外界______________个结晶水分子
及少量其他物质。此后,随着温度升高,配合
物迅速失重的原因_______________________。
温度/℃
图2 配合物的热重曲线
高二化学 第 6 页 共8页16.(18分)rGO(还原氧化石墨烯)表面负载二维晶体,具有室温铁磁性和压电行为共存等反常的物理性
质,有望用于制作新型电子器件。
I.制备GO(氧化石墨烯)
(1)制备GO的过程可能会生成 、 ,需要在通风橱中进行。
(2)不同反应阶段所需温度不同,其中“<20℃”可用 的方法来控制温度范围。
(3)反应结束后,向容器内加入30%H O 溶液除去未反应完的KMnO ,紫红色悬浊液的颜色褪去。
2 2 4
①H O 的电子式是
2 2
②除去KMnO 的离子方程式为 。
4
(4)将(3)所得的悬浊液经离心、蒸馏水洗涤、干燥后,得到土黄色的GO。通过检验SO 2-的存在可判
4
断洗涤是否完全,具体检验方法为 。
Ⅱ.制备rGO(还原氧化石墨烯)
i.称取0.50gGO粉末于烧杯,加入100mL水,用超声震荡形成分散液;
ii.向分散液中加入维生素C,继续超声震荡,从所得悬浊液分离出rGO并制成薄膜。
(5)GO还原为rGO后,在水中溶解度会下降的原因是 。
(6)下列有关制备rGO的说法中,正确的是 。(填标号)
a.维生素C的实际用量应比理论值大 b.H 可以代替维生素C,还原GO
2
c.超声震荡的效果相当于搅拌 d.分离rGO最好用蒸发结晶
高二化学 第 7 页 共8页iii..rGO表面负载二维晶体
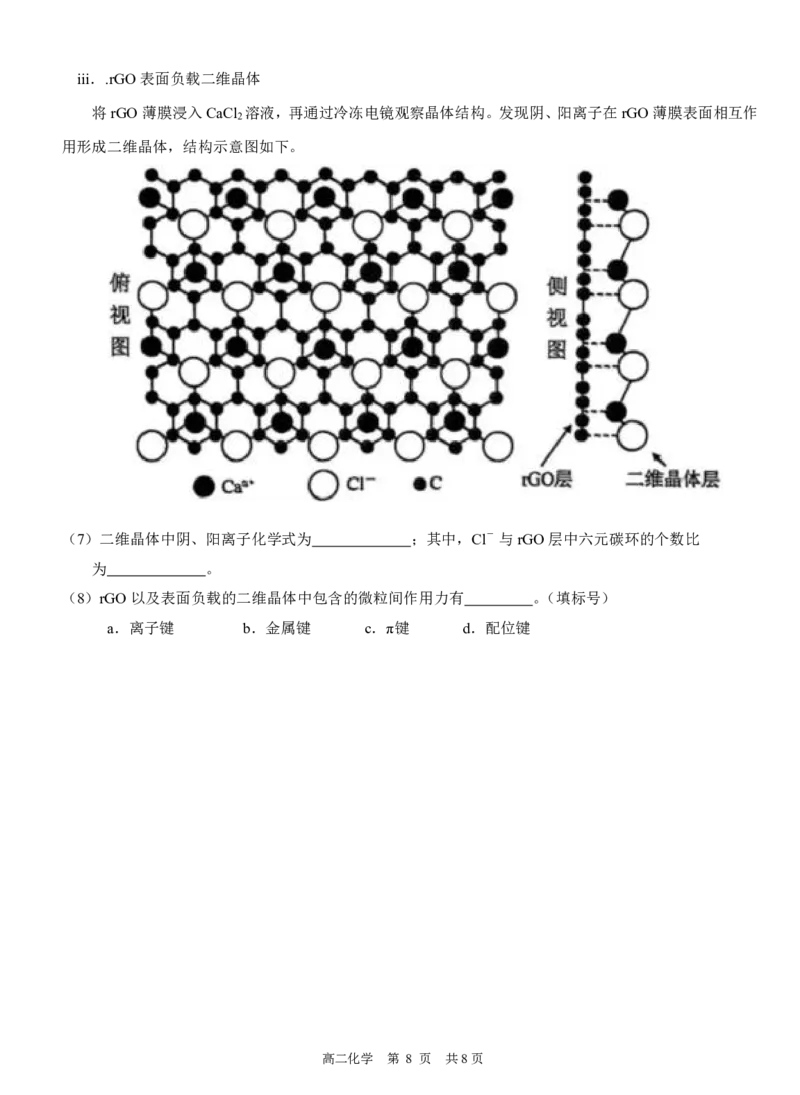
将rGO薄膜浸入CaCl 溶液,再通过冷冻电镜观察晶体结构。发现阴、阳离子在rGO薄膜表面相互作
2
用形成二维晶体,结构示意图如下。
(7)二维晶体中阴、阳离子化学式为 ;其中,Cl- 与rGO层中六元碳环的个数比
为 。
(8)rGO以及表面负载的二维晶体中包含的微粒间作用力有 。(填标号)
a.离子键 b.金属键 c.π键 d.配位键
高二化学 第 8 页 共8页高三上化学月考 1参考答案
一.单项选择题(共15题,1-5题每题3分,6-12题每题4分,共43分。每题只有一个选项符合
题意)
1 2 3 4 5 6
B A B B B D
7 8 9 10 11 12
B D D B D D
二.填空题(共4题,共57分)
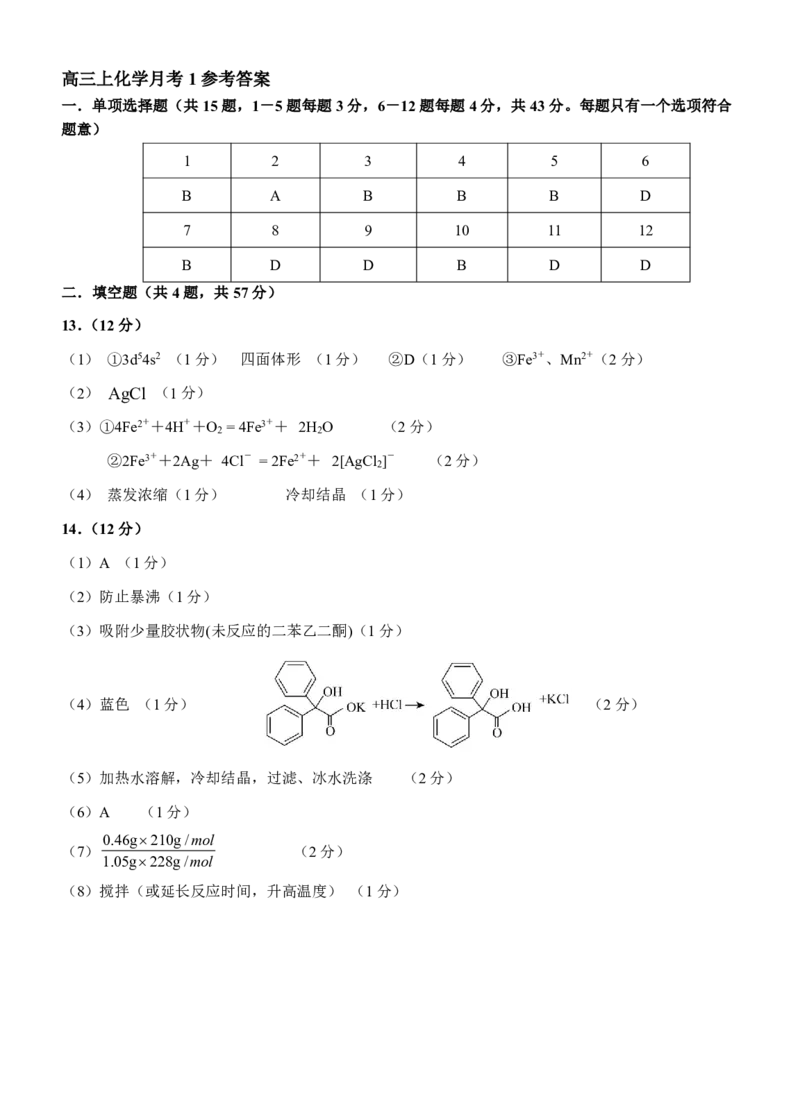
13.(12分)
(1) ①3d54s2 (1分) 四面体形 (1分) ②D(1分) ③Fe3+、Mn2+(2分)
(2) AgCl (1分)
(3)①4Fe2++4H++O =4Fe3++ 2H O (2分)
2 2
②2Fe3++2Ag+ 4Cl- =2Fe2++ 2[AgCl ]- (2分)
2
(4) 蒸发浓缩(1分) 冷却结晶 (1分)
14.(12分)
(1)A (1分)
(2)防止暴沸(1分)
(3)吸附少量胶状物(未反应的二苯乙二酮)(1分)
(4)蓝色 (1分) (2分)
(5)加热水溶解,冷却结晶,过滤、冰水洗涤 (2分)
(6)A (1分)
0.46g210g/mol
(7) (2分)
1.05g228g/mol
(8)搅拌(或延长反应时间,升高温度) (1分)15.(15分)
(1) (1分), 平面三角形 (1分)
(2)6 (1分), sp2,sp3杂化 (2分)
(3)[Fe O(CH COO) (H O) ]++8H+=3Fe3++6CH COOH+4H O (2分)
3 3 6 2 3 3 2
向配合物溶液中加入盐酸酸化,使乙酸根离子结合质子变为乙酸,降低其作为桥式配体的配位能力,
从而使游离态Fe3+被释放到溶液中 (2分)
(4)20.00% (2分)
(5)3(1分) 2 (1分) 由于失水导致配合物结构坍塌或破坏配合物空间结构 (2分)
16.(18分)
(1)SO 、NO 或SO 、NO 或SO 、NO (2分)
2 x 2 2 2
(2)冰(冷)水浴(1分)
(3)① (1分)
②2MnO - +5H O +6H+=2Mn2++8H O+5O ↑(2分)
4 2 2 2 2
(4)取最后一次洗涤液于试管,滴加BaCl 溶液,若没有白色沉淀生成,则说明已经洗涤完全(2分)
2
(5)rGo的亲水基团减少(或羟基数减少或氢键数减少)(2分)
(6)ac(2分)
(7)CaCl(2分) 1:3(2分)
(8)acd (2分)