文档内容
绵阳南山中学实验学校高 2023 级高三(上)10 月月考
化 学
命题人:董海英 审题人:杨梦姣 完成时间:75 分钟 满分:100 分
可能用到的相对原子质量:H 1 C12 N 14 O 16 Ti 48 Co 59
第 I 卷(选择题,共45分)
一、选择题(包括15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.中秋节是我国民间传统节日之一,自古便有祭月、赏月、吃月饼、燃灯、饮桂花酒等民俗,流传至
今,经久不息。下列有关说法错误的是( )
A. 若人体内缺少乙醛脱氢酶,饮桂花酒会产生醉酒症状
B. 月饼保存时常放入装有铁粉的透气袋保持月饼干燥
C. “万里婵娟,几许雾屏云幔”中“云”和“雾”均为胶体
D. “燃灯”“酿桂花酒”过程中均涉及化学变化
2.下列有关物质的分类正确的是( )
A. 混合物:氢硫酸、碱石灰、胆矾
B. 强电解质:稀硫酸、硫酸钡、硫酸氢钠
C. 酸性氧化物:SO 、CO 、SiO
2 2 2
D. 碱性氧化物: CaO 、Na O 、K O
2 2 2
3.化学用语是学习化学的重要工具,下列化学用语表述正确的是( )
A. H 2 S的电离方程式:H 2 S 2H++S2-
B. 有机物 不存在顺反异构
C. 环己醇( )中没有手性碳原子
D. SO 分子的空间填充模型:
2
4.下列说法不正确的是( )
A. 核苷酸、硬脂酸甘油酯、人工结晶牛胰岛素、聚乳酸都是生物大分子
B. 在淀粉、纤维素的主链上再接上含强亲水基团的支链,可提高它们的吸水能力
C. 医用高分子材料、高分子催化剂、磁性高分子材料等属于功能高分子材料
D. 是由三种单体加聚得到的
第 1 页 共 9 页
学科网(北京)股份有限公司5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 澄清透明的溶液中:K+、Mg2+、 、
MnO− SO2−
4 4
B.
的溶液中:K+、NO−-、CO2−-、ClO-
3 3
C. 饱和氯水中:Cl-、Na+、Fe2+、Cu2+
D. 能使甲基橙变红的溶液中: NH+、Br—、I—、 NO−
4 3
6.氯及其化合物部分转化关系如图所示,设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 反应①中1mol Fe与1mol Cl 反应转移电子数目为3N
2 A
B. 100 mL 0.1 mol/L NaClO溶液中含有ClO— 离子数目为0.01N
A
C. 1mol H37Cl分子中含有中子数目为20N
A
D. 反应④生成标准状况下2.24L CHCl需要Cl 数目为0.05N
3 2 A
7.下列离子方程式不符合反应事实的是( )
A. 硝酸银溶液中滴入过量氨水:Ag+ + 2NH ∙H O == [Ag(NH )]+ + 2HO
3 2 3 2 2
B. 磁性氧化铁溶于HI溶液:Fe O + 8H+ == 2Fe3+ + Fe2+ + 4HO
3 4 2
C. 澄清石灰水与过量碳酸氢钠溶液混合:2HCO−+Ca2++2OH−=CaCO ↓+2H O+CO2−
3 3 2 3
D. 已知:酸性 H CO >HCN>HCO−,向 NaCN溶液中通入少量CO 的离子方程式:
2 3 3 2
CN−+CO +H O=HCN+HCO−
2 2 3
8.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: 低于 晶体类型
酸性: 远强于
C 羟基极性
D 溶解性:HS在水中的溶解度大于CH 在水中的溶解度 分子的极性
2 4
第 2 页 共 9 页
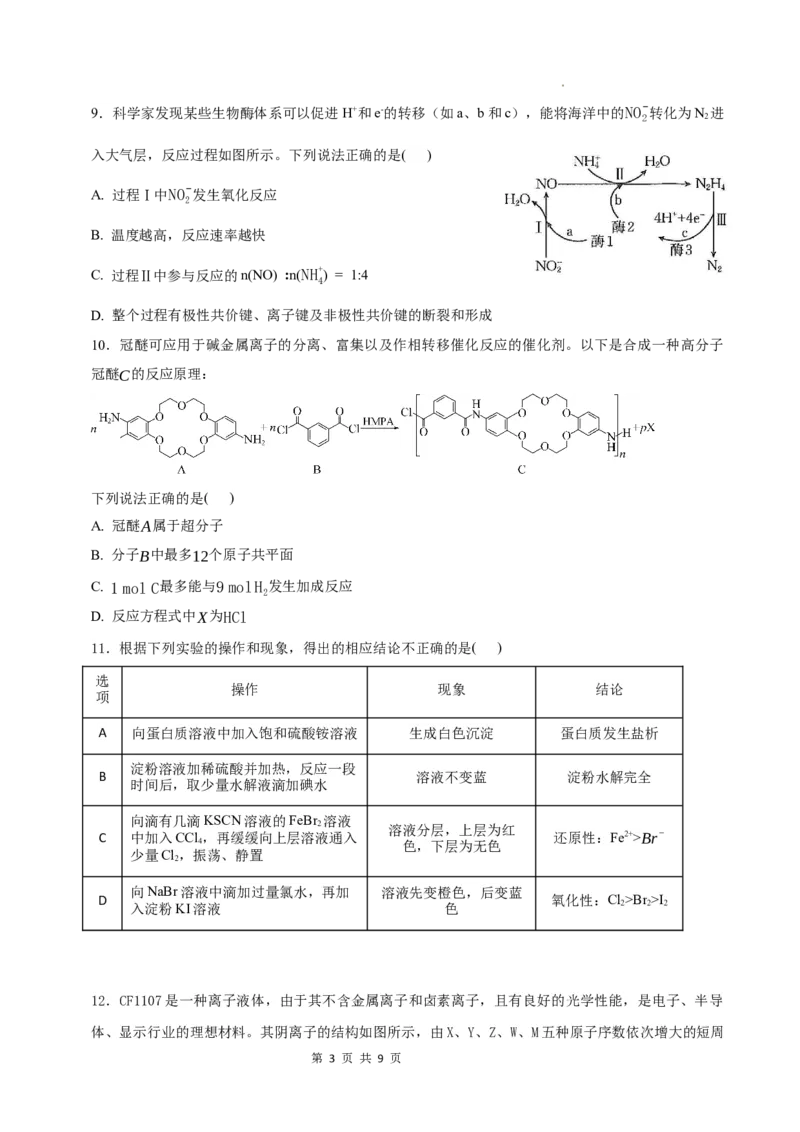
学科网(北京)股份有限公司9.科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO−转化为N 进
2 2
入大气层,反应过程如图所示。下列说法正确的是( )
A. 过程Ⅰ中NO−发生氧化反应
2
B. 温度越高,反应速率越快
C. 过程Ⅱ中参与反应的n(NO)
:n(NH+
) = 1:4
4
D. 整个过程有极性共价键、离子键及非极性共价键的断裂和形成
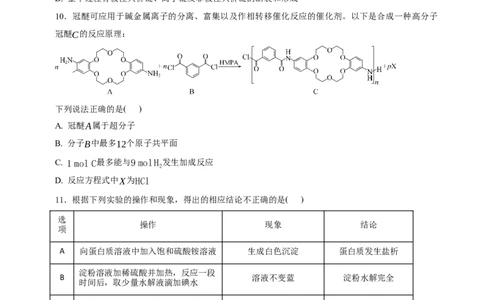
10.冠醚可应用于碱金属离子的分离、富集以及作相转移催化反应的催化剂。以下是合成一种高分子
冠醚C的反应原理:
下列说法正确的是( )
A. 冠醚A属于超分子
B. 分子B中最多12个原子共平面
C. 1 mol C最多能与9 molH 发生加成反应
2
D. 反应方程式中X为HCl
11.根据下列实验的操作和现象,得出的相应结论不正确的是( )
选
操作 现象 结论
项
A 向蛋白质溶液中加入饱和硫酸铵溶液 生成白色沉淀 蛋白质发生盐析
淀粉溶液加稀硫酸并加热,反应一段
B 溶液不变蓝 淀粉水解完全
时间后,取少量水解液滴加碘水
向滴有几滴KSCN溶液的FeBr 溶液
2 溶液分层,上层为红
C 中加入CCl ,再缓缓向上层溶液通入 还原性:Fe2+>Br−
4 色,下层为无色
少量Cl,振荡、静置
2
向NaBr溶液中滴加过量氯水,再加 溶液先变橙色,后变蓝
D 氧化性:Cl>Br >I
入淀粉KI溶液 色 2 2 2
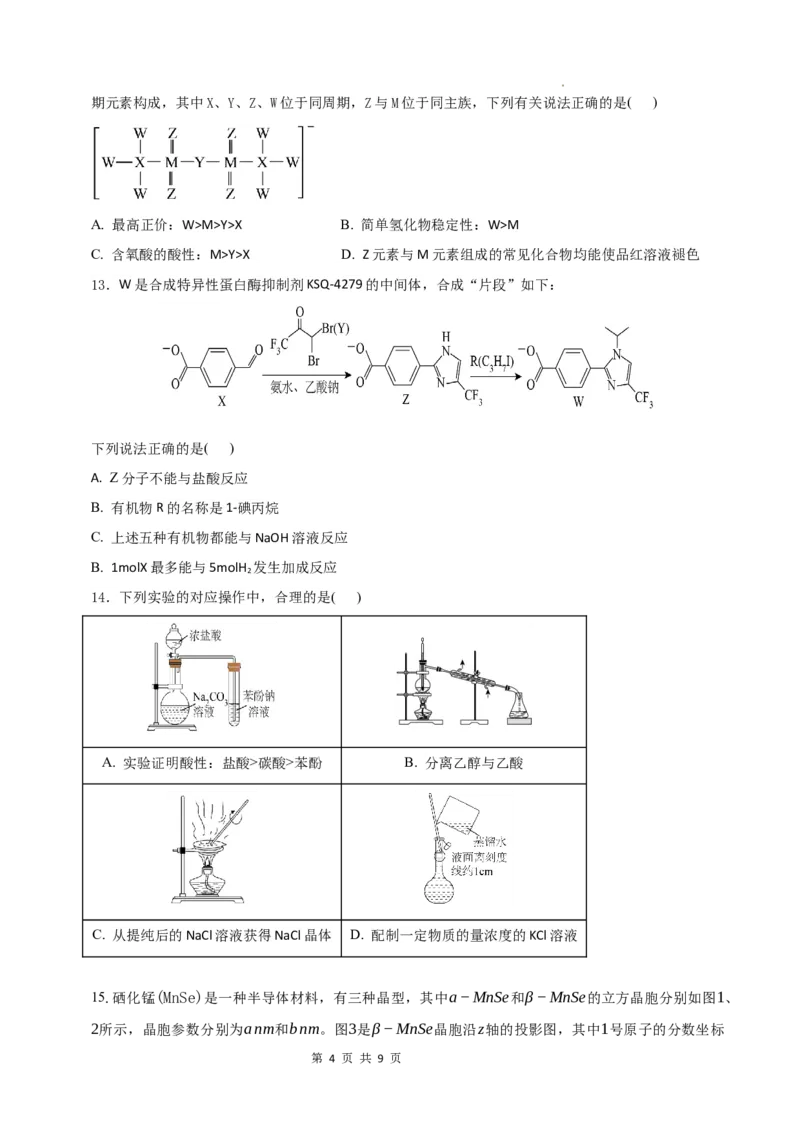
12.CF1107是一种离子液体,由于其不含金属离子和卤素离子,且有良好的光学性能,是电子、半导
体、显示行业的理想材料。其阴离子的结构如图所示,由X、Y、Z、W、M五种原子序数依次增大的短周
第 3 页 共 9 页
学科网(北京)股份有限公司期元素构成,其中X、Y、Z、W位于同周期,Z与M位于同主族,下列有关说法正确的是( )
A. 最高正价:W>M>Y>X B. 简单氢化物稳定性:W>M
C. 含氧酸的酸性:M>Y>X D. Z元素与M元素组成的常见化合物均能使品红溶液褪色
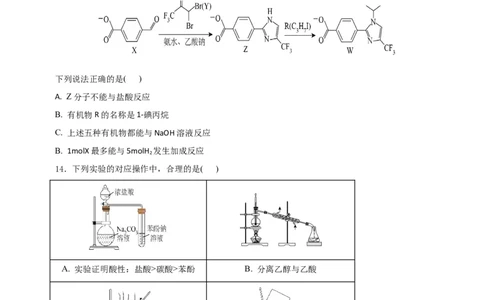
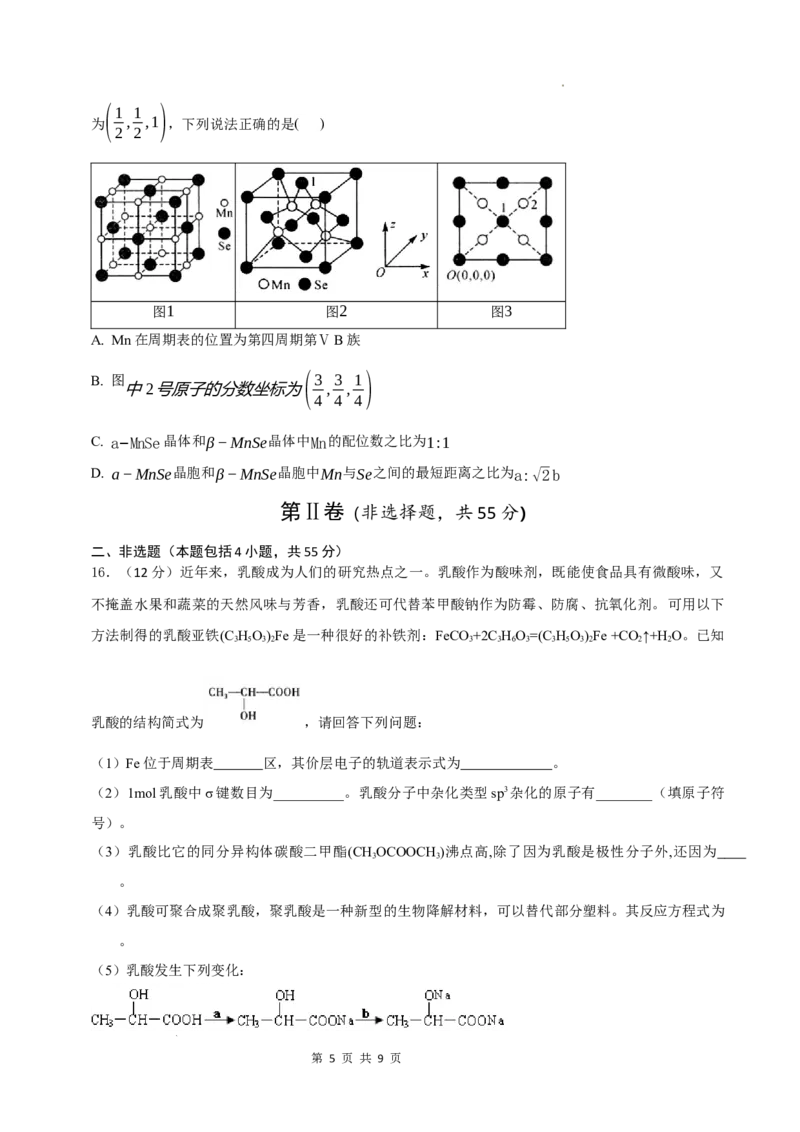
13.W是合成特异性蛋白酶抑制剂KSQ-4279的中间体,合成“片段”如下:
下列说法正确的是( )
A. Z分子不能与盐酸反应
B. 有机物R的名称是1-碘丙烷
C. 上述五种有机物都能与NaOH溶液反应
B. 1molX最多能与5molH 发生加成反应
2
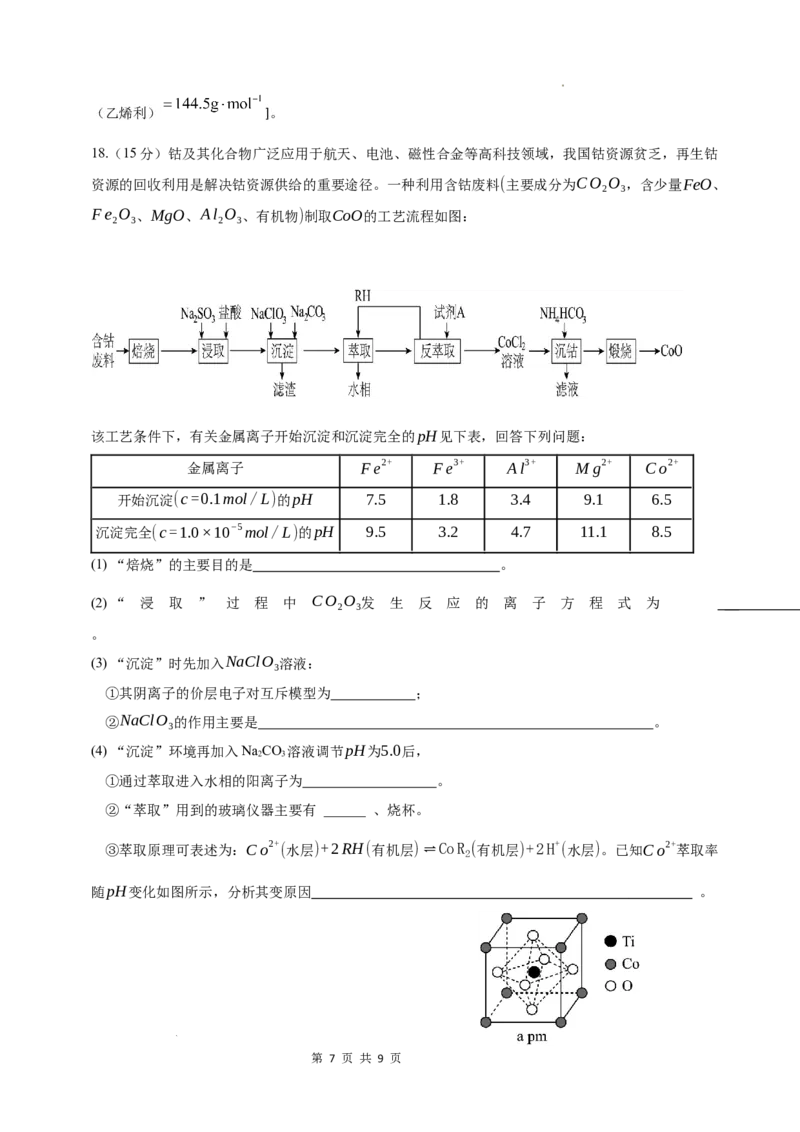
14.下列实验的对应操作中,合理的是( )
A. 实验证明酸性:盐酸>碳酸>苯酚 B. 分离乙醇与乙酸
C. 从提纯后的NaCl溶液获得NaCl晶体 D. 配制一定物质的量浓度的KCl溶液
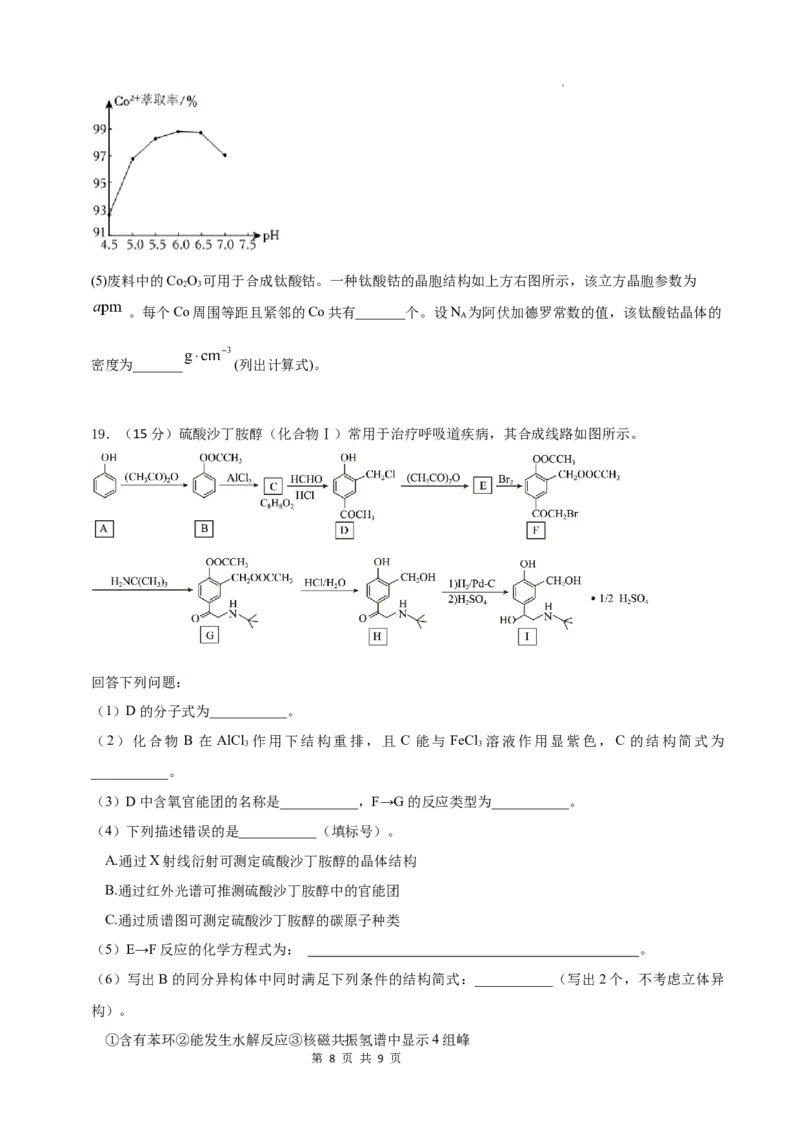
15.硒化锰(MnSe)是一种半导体材料,有三种晶型,其中a−MnSe和β−MnSe的立方晶胞分别如图1、
2所示,晶胞参数分别为anm和bnm。图3是β−MnSe晶胞沿z轴的投影图,其中1号原子的分数坐标
第 4 页 共 9 页
学科网(北京)股份有限公司(1 1 )
为 , ,1 ,下列说法正确的是( )
2 2
图1 图2 图3
A. Mn在周期表的位置为第四周期第ⅤB族
B. 图 (3 3 1)
中2号原子的分数坐标为 , ,
4 4 4
C. a−MnSe晶体和β−MnSe晶体中Mn的配位数之比为1:1
D. a−MnSe晶胞和β−MnSe晶胞中Mn与Se之间的最短距离之比为a:√ 2b
第Ⅱ卷
(
非选择题,共55分
)
二、非选题(本题包括4小题,共55分)
16.(12分)近年来,乳酸成为人们的研究热点之一。乳酸作为酸味剂,既能使食品具有微酸味,又
不掩盖水果和蔬菜的天然风味与芳香,乳酸还可代替苯甲酸钠作为防霉、防腐、抗氧化剂。可用以下
方法制得的乳酸亚铁(C HO)Fe是一种很好的补铁剂:FeCO+2C HO=(C HO)Fe +CO ↑+H O。已知
3 5 3 2 3 3 6 3 3 5 3 2 2 2
乳酸的结构简式为 ,请回答下列问题:
(1)Fe位于周期表 区,其价层电子的轨道表示式为 。
(2)1mol乳酸中σ键数目为__________。乳酸分子中杂化类型sp3杂化的原子有________(填原子符
号)。
(3)乳酸比它的同分异构体碳酸二甲酯(CHOCOOCH )沸点高,除了因为乳酸是极性分子外,还因为
3 3
。
(4)乳酸可聚合成聚乳酸,聚乳酸是一种新型的生物降解材料,可以替代部分塑料。其反应方程式为
。
(5)乳酸发生下列变化:
第 5 页 共 9 页
学科网(北京)股份有限公司所用的试剂是a__________________,b_______________(写化学式)
17.(13分)乙烯利( )是一种农用植物生长调节剂,广泛应用于农作物增产和储存。
常温下,乙烯利为固体,具有一定的腐蚀性,易溶于水,所得溶液显酸性。某实验小组同学用40%乙
烯利溶液和稍过量的NaOH固体为原料制备乙烯。回答下列问题:
(1)关于实验仪器的选择和使用:
①配制100g40%乙烯利溶液时,下图所示仪器不需要的是_______(填仪器名称)。
②装瓶时,不小心将乙烯利溶液滴到手上,应先用大量水冲洗,再涂抹 (填序号)。
A.生理盐水 B.医用酒精 C.烧碱溶液 D.3%~5%的小苏打溶液
(2)根据反应原理设计下图所示的装置制备乙烯气体。
①写出乙烯的电子式 。
②已知电负性C>P,乙烯利中P的化合价为 。
用40%乙烯利溶液与NaOH固体反应(磷转化为NaPO )生成乙烯的化学方程式为 。
3 4
③当观察到 时,即可关闭活塞1,打开活塞2,用气囊收集乙烯气体。
(3)实验室也可以使用乙烯利固体与强碱溶液混合制备乙烯。分别使用KOH溶液、NaOH溶液与乙烯
利固体混合制备乙烯气体,现象如下:
试剂 现象
30%KOH溶液 产气速率快,气流平稳,无盐析现象
30%NaOH溶液 产气速率快,气流平稳,有盐析现象
①通过上述现象分析可知,应选用30% (填“KOH”或“NaOH”)溶液与乙烯利固体混合制
备乙烯气体,原因是 。
②在实验中,乙烯利固体的质量为10.0g(强碱溶液足量),制得的乙烯气体恰好能使含0.12 mol
KMnO 的酸性高锰酸钾溶液完全褪色,则产品的产率为 (保留小数点后两位)[已知M
4
第 6 页 共 9 页
学科网(北京)股份有限公司(乙烯利) ]。
18.(15分)钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴
资源的回收利用是解决钴资源供给的重要途径。一种利用含钴废料(主要成分为CO O ,含少量FeO、
2 3
Fe O 、MgO、Al O 、有机物)制取CoO的工艺流程如图:
2 3 2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表,回答下列问题:
金属离子 Fe2+ Fe3+ Al3+ M g2+ Co2+
开始沉淀(c=0.1mol/L)的pH 7.5 1.8 3.4 9.1 6.5
沉淀完全(c=1.0×10−5mol/L)的pH 9.5 3.2 4.7 11.1 8.5
(1) “焙烧”的主要目的是 。
(2) “ 浸 取 ” 过 程 中 CO O 发 生 反 应 的 离 子 方 程 式 为
2 3
。
(3) “沉淀”时先加入NaClO 溶液:
3
①其阴离子的价层电子对互斥模型为 ;
②NaClO 的作用主要是 。
3
(4) “沉淀”环境再加入NaCO 溶液调节pH为5.0后,
2 3
①通过萃取进入水相的阳离子为 。
②“萃取”用到的玻璃仪器主要有 ______ 、烧杯。
③萃取原理可表述为:Co2+ (水层)+2RH(有机层)⇌ CoR (有机层)+2H+ (水层)。已知Co2+萃取率
2
随pH变化如图所示,分析其变原因 。
第 7 页 共 9 页
学科网(北京)股份有限公司(5)废料中的Co O 可用于合成钛酸钴。一种钛酸钴的晶胞结构如上方右图所示,该立方晶胞参数为
2 3
。每个Co周围等距且紧邻的Co共有_______个。设N 为阿伏加德罗常数的值,该钛酸钴晶体的
A
密度为_______ (列出计算式)。
19.(15分)硫酸沙丁胺醇(化合物Ⅰ)常用于治疗呼吸道疾病,其合成线路如图所示。
回答下列问题:
(1)D的分子式为___________。
(2)化合物 B 在 AlCl 作用下结构重排,且 C 能与 FeCl 溶液作用显紫色,C 的结构简式为
3 3
___________。
(3)D中含氧官能团的名称是___________,F→G的反应类型为___________。
(4)下列描述错误的是___________(填标号)。
A.通过X射线衍射可测定硫酸沙丁胺醇的晶体结构
B.通过红外光谱可推测硫酸沙丁胺醇中的官能团
C.通过质谱图可测定硫酸沙丁胺醇的碳原子种类
(5)E→F反应的化学方程式为: 。
(6)写出B的同分异构体中同时满足下列条件的结构简式:___________(写出2个,不考虑立体异
构)。
①含有苯环②能发生水解反应③核磁共振氢谱中显示4组峰
第 8 页 共 9 页
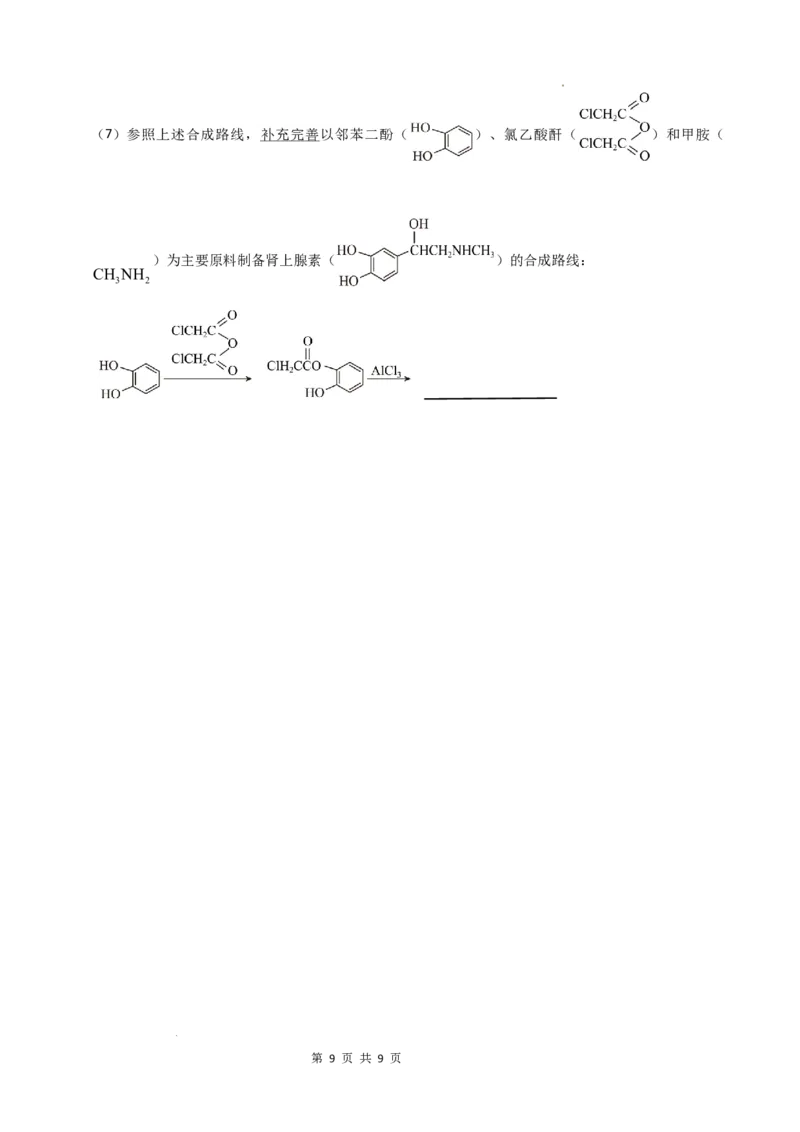
学科网(北京)股份有限公司(7)参照上述合成路线,补充完善以邻苯二酚( )、氯乙酸酐( )和甲胺(
)为主要原料制备肾上腺素( )的合成路线:
CH NH
3 2
第 9 页 共 9 页
学科网(北京)股份有限公司