2025-2026 学年度(上)七校协作体期初高三联考化学试题
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Mg-24 S-32 Fe-56
第I卷 (选择题,共45分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)。
1. 科技发展与化学密切相关。下列说法正确的是
A.“天宫二号”空间站使用了石墨烯存储器,石墨烯属于新型烯烃
B.“水立方”场馆顶部覆盖聚四氟乙烯(PTFE)膜,PTFE分子中有碳碳双键
C.“深海一号”母船海水浸泡区镶上铝基是利用牺牲阳极的金属防腐原理
D.长征运载火箭以液氧和煤油为推进剂,液氧分子间靠共价键凝聚在一起
2. 宏观辨识与微观探析是化学学科核心素养之一,下列化学用语正确的是
A.基态Cr3+的结构示意图: B.SO 的VSEPR模型:
3
C.丙炔的键线式: D.CH 的共价键类型:s-p σ键
4
3. NH ClO 是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,如:
4 4
NH ClO +2C=NH ↑+2CO ↑+HCl↑。下列说法正确的是
4 4 3 2
A.在石墨和金刚石中,碳原子均为sp2杂化
B.上述气态产物都是含有极性键的极性分子
C.NH ClO 中的阴、阳离子有相同的VSEPR模型和空间结构
4 4
D.NH 和CO 都能作制冷剂是因为它们有相同类型的分子间作用力
3 2
4. Na O 可 用 作 潜 水 或 宇 航 装 置 的 CO 吸 收 剂 和 供 氧 剂 , 反 应 方 程 式 为
2 2 2
2Na O +2CO =2Na CO +O 。N 为阿伏加德罗常数的值。下列说法正确的是
2 2 2 2 3 2 A
A.11.2L CO 中π键的数目为N
2 A
B.1mol Na O 晶体中离子数目为4N
2 2 A
C.该反应生成1mol O 转移的电子数目为2N
2 A
D.0.1mol/L Na CO 溶液中含有的CO 2-数目小于0.1N
2 3 3 A
5. 光刻胶是芯片制造的关键材料。以下是一种光刻胶的酸解过程,下列说法正确的是
A.X在水中的溶解度大于Y B.X通过缩聚制备
C.该酸解过程不含消去反应 D.1mol X消耗NaOH溶液3n mol6. 下列过程中,对应的反应方程式正确的是
《天工开物》记载用炉甘石(ZnCO )火 2ZnCO +C 2Zn+3CO ↑
A 3 3 2
法炼锌
B NaH用作野外生氢剂 NaH+H O=NaOH+H ↑
2 2
C 用Na S作沉淀剂除废水中的Cu2+ Na S+Cu2+=CuS↓+2Na+
2 2
海上油气加工平台“海葵一号”的钢
D Zn2+(aq)+2e-=Zn(s)
壳外壁铺装锌锭减缓腐蚀
7. P、Q、X、Y、Z是原子序数依次增大的短周期主族元素。基态 P原子核外电子有3种空
间运动状态;Q与Y含有2个单电子;Z与P同主族。下列说法正确的是
A.化合物Q H 中,σ键与π键的数目之比为2:3
2 2
B.P元素形成的单质在常温下为固态,属于共价晶体
C.与Y同周期的元素中,第一电离能大于Y的有2种
D.X、Y与氢原子形成的简单化合物的键角大小:Y>X
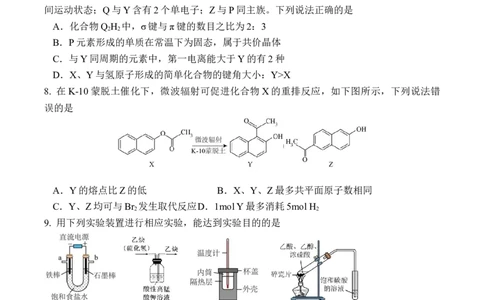
8. 在K-10蒙脱土催化下,微波辐射可促进化合物X的重排反应,如下图所示,下列说法错
误的是
A.Y的熔点比Z的低 B.X、Y、Z最多共平面原子数相同
C.Y、Z均可与Br 发生取代反应D.1mol Y最多消耗5mol H
2 2
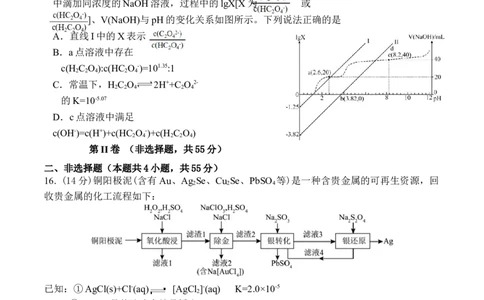
9. 用下列实验装置进行相应实验,能达到实验目的的是
图1 图2 图3 图4
A.图1电解法制氯气 B.图2除去乙炔气体中的杂质
C.图3测定中和热 D.图4制备乙酸乙酯
10. 铁镁合金是一种新型储氢材料,立方晶胞类似于CaF ,结构如图所示。该合金储氢后H
2 2
位于晶胞的体心和棱心位置(晶胞图中未画出),晶胞参数为apm,N 为阿伏加德罗常数的值。
A
下列说法错误的是
A.该合金的化学式为FeMg
2B.1cm3该合金的质量为
C.熔融该合金的过程中需要破坏金属键
D.储氢后晶体中的原子个数之比Fe:Mg:H=1:2:1
11. 无水FeCl 常用作芳烃氯代反应的催化剂。以废铁屑(主要成分Fe,还有少量Fe O 、C和
3 2 3
SiO )制取无水FeCl 的流程如下,下列说法正确的是
2 3
A.“过滤”所得滤液中大量存在的离子有:Fe2+、H+、Cl-
B.“氧化”时可使用H O 作氧化剂,离子方程式是
2 2
Fe2++2H++H O =Fe3++2H O
2 2 2
C.将“氧化”后的溶液蒸干可获得FeCl ·6H O
3 2
D.“脱水”时加入SOCl 能抑制FeCl 的水解,原因是SOCl 与水反应生成H SO 和HCl
2 3 2 2 4
12. 依据下列实验现象,判断所得相应结论错误的是
实验现象 结论
CuCl 浓溶液呈黄绿色,加水稀释后溶液呈 配体 H O、Cl-与 Cu2+间
A 2 2
蓝色 存在配位平衡移动
用0.1mol/L NaOH 溶液分别中和等体积的
B 0.1mol/L H SO 溶液和 0.1mol/L CH COOH 酸性:H SO >CH COOH
2 4 3 2 4 3
溶液,H SO 消耗的NaOH溶液多
2 4
C 将SO 通入溴水至过量,溶液的橙色褪去 SO 有还原性
2 2
将蛋清溶液滴入饱和NaCl溶液中,溶液变 蛋白质的盐析是可逆的
D
浑浊,继续加入蒸馏水,溶液变澄清
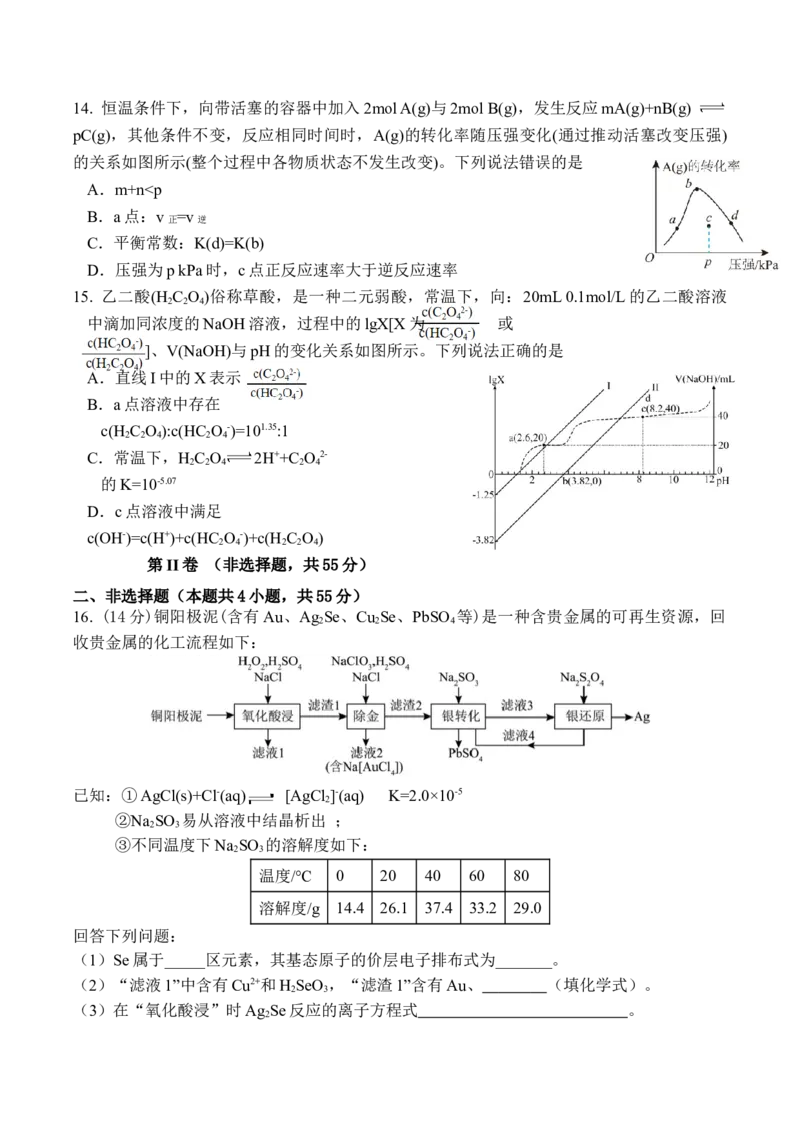
13. 一种高容量水系电池示意图如图。已知:放电时,电极Ⅱ上MnO 减少;电极材料每转移
2
1mol电子,对应的理论容量为26.8A·h。下列说法正确的是
A.电极电势:I>II
B.放电时Ⅱ极室中溶液的pH降低
C.充电时阳极反应为:MnS-2e-=S+Mn2+
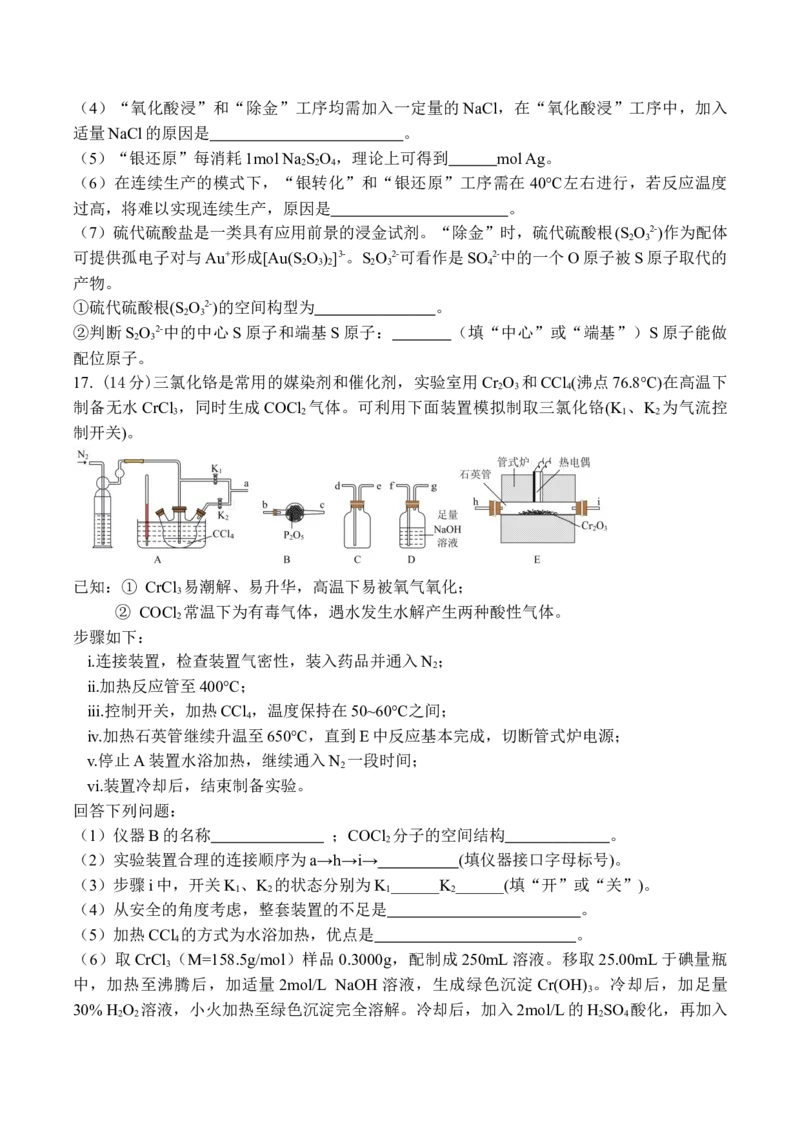
D.充电时24g S能提供的理论容量为40.2A·h14. 恒温条件下,向带活塞的容器中加入2mol A(g)与2mol B(g),发生反应mA(g)+nB(g)
pC(g),其他条件不变,反应相同时间时,A(g)的转化率随压强变化(通过推动活塞改变压强)
的关系如图所示(整个过程中各物质状态不发生改变)。下列说法错误的是
A.m+n
Ea
(正) (逆)
B.向容器中充入He,使体系压强增大,可增大反应速率
C.平衡后,压缩容器体积,反应i平衡正向移动,反应ii平衡不移动
D.选择合适的催化剂,不但可以加快反应速率,还可提高甲醇的平衡产率
II. CH -CO 重整反应:CO (g)+CH (g) 2CO(g)+2H (g),易发生副反应:CO (g)+H (g)
4 2 2 4 2 2 2
CO(g)+H O(g) 。某温度下将等物质的量的CH (g)和CO (g)充入起始压强为 P kPa的恒容密
2 4 2 0
闭容器中发生反应,达平衡时,测得某种反应物的转化率为20%,另一种为40%。
(4)平衡时总压为 kPa。
(5)该温度下平衡时 n(CO):n(H )= ,CH -CO 重整反应的分压平衡常数 K =
2 4 2 p
(用含“P ”的式子表示)。
0
(已知:气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常
数K )
p
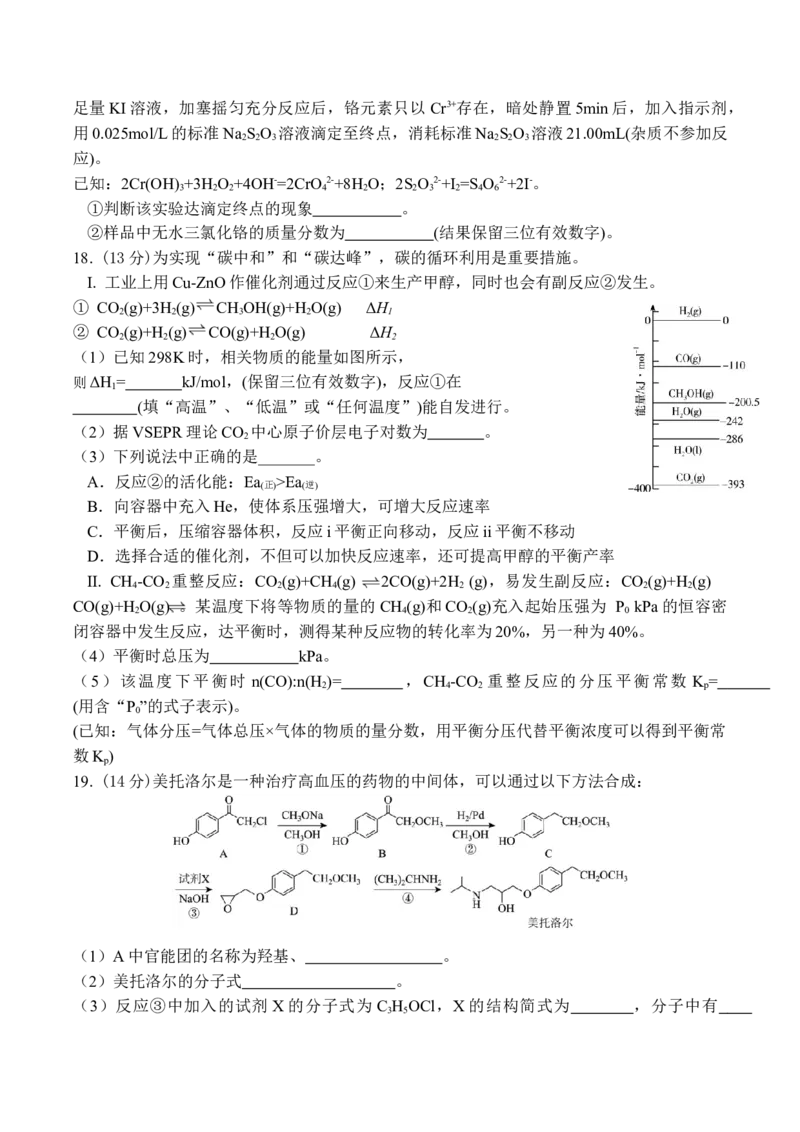
19. (14分)美托洛尔是一种治疗高血压的药物的中间体,可以通过以下方法合成:
(1)A中官能团的名称为羟基、 。
(2)美托洛尔的分子式 。
(3)反应③中加入的试剂 X 的分子式为 C H OCl,X 的结构简式为 ,分子中有
3 5个手性碳原子。
(4)反应②的反应类型为 。
(5)写出A与足量NaOH水溶液(加热)反应的化学方程式: 。
(6)B的同分异构体满足下列条件:
i.能发生银镜反应;
ii.能与FeCl 溶液发生显色反应;
3
iii.分子中有4种不同化学环境的氢,且1 mol该物质与足量金属钠反应产生1 mol H
2
写出其中一种满足上述条件的同分异构体的结构简式: 。
(7)根据已有知识并结合题目所给相关信息,写出以 CH OH和 为有机原料
3
及必要的无机试剂制备 的合成路线所示,其中物
质X与Z的结构简式分别为 和 。一、选择题(本题共15小题,每小题3分,共45分)
1 2 3 4 5 6 7 8
C A C C D B B D
9 10 11 12 13 14 15
A D A B D B C
二、非选择题(共55分)
16. (14分)
(1)p (1分) 4s24p4 (1分)
(2)AgCl、PbSO (2分,各1分)
4
(3)Ag Se+3H O +2Cl-+2H+=2AgCl+H SeO +3H O (2分)
2 2 2 2 3 2
(4)使硒化银完全转化为AgCl,防止氯化钠过少导致转化不完全,并且防止氯化钠过量导
致AgCl转化为[AgCl ]- (2分)
2
(5)2 (2分)
(6)高于40℃后,Na SO 的溶解度下降,“银转化”和“银还原”的效率降低,难以实现
2 3
连续生产 (2分)
(7) ①.四面体(1分) ②.端基(1分)
17. (14分)
(1)(球形)干燥管(1分) 平面三角形(1分)
(2)debcfg (2分)
(3)开(1分) 关(1分)
(4)升华的三氯化铬易凝华,堵塞导管 (2分)
(5)受热更均匀,便于控制反应温度 (2分)
(6)①当滴入最后半滴Na S O 溶液,溶液蓝色刚好褪去,且半分钟内不恢复(2分)
2 2 3
②92.5%(2分)
18. (13分)
(1)-49.5 (2分) 低温 (2分) (2) 2 (1分)
3P2
(3) A (2分) (4)1.2P (2分) (5)3:1 (2分) 0 (2分)
0
400
19. (14分)
(1)(酮)羰基、碳氯键(或氯原子) (2分,各1个)
(2)C H O N (1分)
15 25 3
(3) (2分) 1 (1分)
(4)还原反应 (2分)(5) + 2NaOH + NaCl + H O (2分)
2
(6) 或 (2分)
(7) (1分) (1分)