文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(黑龙江、甘肃、吉林、
安徽、江西、贵州、广西)
黄金卷 02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Si 28 Cl 35.5 Na 23 Ti 48 Cu 64
第Ⅰ卷
一、单项选择题:共15题,每题3分,共45分。每题只有一个选项最符合题意。
1.神舟十六号载人飞船顺利发射,我国航天航空事业再次迎来飞速发展。下列有关说法错误的是
A.飞船采用的太阳能刚性电池阵:将太阳能转化为电能
B.航天员的航天服使用的多种合成纤维:有机高分子材料
C.飞船返回舱使用的高温结构陶瓷:新型无机非金属材料
D.火箭燃料偏二甲肼(CH ) N-NH :属于烃类
3 2 2
【答案】D
【解析】A.载人飞船采用了太阳能刚性电池阵,是将太阳能转化为电能供飞船使用,A正确;
B.航天员穿的航天服使用的多种合成纤维为有机合成高分子材料,B正确;
C.高温结构陶瓷属于新型无机非金属材料,其性能优良,C正确;
D.分子中含N元素,不属于烃类化合物,D错误;
故选D。
2.ClO 在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备ClO 的一种方法为:5NaClO 4HCl
2 2 2
5NaCl4ClO 2H O,下列有关化学用语表达正确的是
2 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.中子数为8的氧原子:16O B.Na的结构示意图:
8
C.HCl的电子式: D.ClO 的空间填充模型:
2
【答案】A
【解析】A.O原子的质子数为8,中子数为8的氧原子质量数为16,核素表示为:16O,故A正确;
8
B.Na的结构示意图: ,故B错误;
C.HCl为共价分子,电子式为: ,故C错误;
D.ClO 的价层电子对数为4,含孤对电子,不是直线形,故D错误;
2
故选:A。
3.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.1mol金属钠生成Na O ,转移的电子数为2N
2 2 A
B.60g二氧化硅晶体中含有N 个SiO 分子
A 2
C.乙烯和丙烯的混合物共28g,含有的氢原子数为4N
A
D.由1molCH COONa和少量CH COOH形成的中性溶液中,CH COO-数目小于N
3 3 3 A
【答案】C
【解析】A.1molNa完全反应失去1mol电子,无论产物为氧化钠还是过氧化钠,转移的电子数都为1mol,
转移电子总数N 个,A错误;
A
B.二氧化硅为共价晶体,不存在二氧化硅分子,B错误;
C.乙烯和丙烯的最简式均为CH ,混合物共28g可以认为有2molCH ,含有的氢原子数为4N ,C正确;
2 2 A
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002D.由1mol CH COONa和少量CH COOH形成的中性溶液中,含有1mol钠离子;溶液为中性,氢离子与
3 3
氢氧根离子物质的量相等,根据电荷守恒,则钠离子与CH COO-的物质的量相等,所以溶液中含有CH COO-
3 3
的物质的量为1mol,含有的CH COO-数目为N 个,D错误;
3 A
故选C。
4.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 配制FeCl 溶液 将FeCl 固体溶于浓盐酸后再稀释
3 3
B 提纯含有少量乙酸的乙酸乙酯 加NaOH溶液后分液
C 实验室制NH 加热使氯化铵固体分解
3
D 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
A.A B.B C.C D.D
【答案】A
【解析】A.浓盐酸可抑制铁离子水解,则将FeCl 于少量浓盐酸中,再加水稀释可配制溶液,A符合题意;
3
B.氢氧化钠促进乙酸乙酯水解,饱和碳酸钠溶液能和乙酸反应生成可溶性的乙酸钠,且能降低乙酸乙酯的
溶解性,所以应该用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,B不符合题意;
C.验室制氨气利用用氯化铵与氢氧化钙作用生成氯化钙、水、氨气,C不符合题意;
D.加热促进镁离子水解,且生成盐酸易挥发,应在HCl气流中加热制备无水MgCl ,D不符合题意;
2
故选A。
5.下列有关物质的性质和用途说法不正确的是
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.利用高纯单质硅的半导体性能,可以制成光电池
B.石灰石在高温下的分解产物可与SO 反应,可用于减少燃煤烟气中的SO
2 2
C.Na O 与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
D.二氧化硅导电能力强,可用于制造光导纤维
【答案】D
【解析】A.高纯单质硅具有半导体性能,可以利用其光电效应制成光电池,故A正确;
B.石灰石高温下分解生成氧化钙,氧化钙与二氧化硫、氧气反应生成硫酸钙,可以减小二氧化硫的排放,
故B正确;
C.过氧化钠与二氧化碳反应生成碳酸钠和氧气,可以用于制作呼吸面具中氧气的来源,故C正确;
D.二氧化硅不导电,制造光导纤维是利用二氧化硅对光的全反射性能,故D错误;
故选D。
6.W、X、Y、Z、M五种短周期主族元素,原子序数依次增大。W的核外电子数等于其周期数,XW 分
3
子呈三角锥形,Y的核外电子数等于W、X核外电子数之和,在同周期元素中M的第一电离能最小。下列
说法正确的是
A.M Y与M Y 含有的化学键类型完全相同
2 2 2
B.X、Y、Z三种元素的电负性顺序为:XZ>M,故C错误;
D.W与Y分别是H和O,形成的10电子微粒有H O、OH和H O+等,不只两种,故D错误;
2 3
故选B。
7.2022年3月15日,新发布的《新型冠状病毒肺炎诊疗方案(试行第九版)》明确,处于医学观察期或临
床治疗期(确诊病例)的轻型和普通型病人,推荐服用连花清瘟胶囊(颗粒)作为治疗药物。“连翘酯苷A”是“连
花清瘟胶囊”的有效成分之一,其结构如图所示。下列有关该有机物的说法错误的是
A.有机物的官能团有苯环、羟基、醚键和酯基
B.有机物能使酸性高锰酸钾溶液褪色
C.1mol分子最多能与9molNa发生反应
D.在酸性条件下可发生水解反应,其最简单产物的化学式为C H O
9 8 4
【答案】A
【解析】A.该有机物的官能团有羟基、醚键、碳碳双键和酯基,A错误;
B.该物质中含双键,能使酸性高锰酸钾溶液褪色,B正确;
C.1mol分子含9mol羟基,最多能与9molNa发生反应,C正确;
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002D.该物质含酯基,在酸性条件下可发生水解反应,其最简单产物的结构简式为: ,
化学式为C H O ,D正确;
9 8 4
故选A。
8.工业上以黄铁矿(主要成分为FeS )为原料,采用接触法制备浓硫酸的原理如下:
2
下列说法不正确的是
A.用盐酸和烧碱可从烧渣中提取铁红
B.净化SO 的目的是防催化剂中毒降低活性
2
C.用水替代98.3%浓硫酸能提高吸收效率
D.制备硫酸的3个反应中2个是氧化还原反应
【答案】C
【解析】A.用盐酸溶解烧渣,可除去二氧化硅;再用氢氧化钠可分离铝元素和铁元素,灼烧氢氧化铁制铁
红,故A正确;
B.二氧化硫中有砷等杂质会使催化剂中毒(降低活性),净化SO 的目的是防催化剂中毒降低活性,故B正
2
确;
C.三氧化硫与水反应放出大量热量,用水直接吸收三氧化硫会形成“酸雾”,污染环境且吸收率低,故C错
误;
D.黄铁矿(FeS )与O 反应,SO 和O 反应2个是氧化还原反应,故D正确;
2 2 2 2
故答案为C
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx0029.下列相关反应的离子方程式书写正确的是
A.氢氧化铁溶于氢碘酸:Fe(OH) +3H+ =Fe3++3H O
3 2
B.氯化铝溶液中滴加过量的氨水:Al3++4 NH ·H O=AlO -+4NH ++2H O
3 2 2 4 2
C.NH Al(SO ) 溶液中加入Ba(OH) 溶液使SO 2-完全沉淀:NH +
4 4 2 2 4 4
+Al3++2SO 2-+2Ba2++4OH-=Al(OH) ↓+2BaSO ↓+ NH ·H O
4 3 4 3 2
D.NaHCO 溶液中加入过量的Ba(OH) 溶液:2HCO -+Ba2++2OH- =BaCO ↓+2H O+ CO 2-
3 2 3 3 2 3
【答案】C
【解析】A项、氢氧化铁溶于氢碘酸,发生氧化还原反应生成碘化亚铁、单质碘和水,反应的离子方程式
为2Fe(OH) +3H++2I-═2Fe2++3H O+I ,故A错误;
3 2 2
B项、氨水是弱碱,不能溶解氢氧化铝,反应的离子方程式为Al3++3NH •H O═Al(OH) -↓+3NH+ ,故B
3 2 3 4
错误;
C项、向NH Al(SO ) 溶液中滴入Ba(OH) 溶液使SO 2-沉淀完全,二者物质的量之比为1:2,反应
4 4 2 2 4
生成硫酸钡沉淀、氢氧化铝沉淀和一水合氨,反应的离子方程式为:2Ba2++NH ++Al3++2SO 2-+4OH-═Al(OH)
4 4
↓+2BaSO ↓++NH .H O,故C正确;
3 4 3 2
D项、NaHCO 溶液中加入过量的Ba(OH) 溶液,反应生成碳酸钡沉淀、氢氧化钠和水,反应的离子方
3 2
程式为:HCO -+Ba2++OH-═BaCO ↓+H O,故D错误。
3 3 2
故选C。
10.下列说法正确的是
A.基态 Cr 原子有 6 个未成对电子
B.元素 Ga 的核外电子排布式为 [Ar]4s24p1,位于元素周期表中 p 区
C.NH 中 N—H 间的键角比 CH 中 C—H 间的键角大
3 4
D.XY 分子为 V 形,则 X 原子一定为 sp2 杂化
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002【答案】A
【解析】A.铬为24号元素,基态Cr原子价电子排布为3d54s1,基态 Cr 原子有 6 个未成对电子,A正
确;
B..元素Ga为31号元素,位于元素周期表中p区,其核外电子排布式为[Ar]3d104s24p1,B错误;
C.NH 是三角锥形含有1对孤电子对,CH 是正四面体形无孤电子对,因此NH 中N-H间的键角比CH
3 4 3 4
中C-H间的键角小,C错误;
D.XY 分子中原子个数比为1:2,XY 分子为 V 形,则X原子不一定为sp2杂化,也可能含有2对孤
2 2
电子对为sp3杂化,D错误;
故选A。
11.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是
A.转化过程中所涉及的元素均呈现了两种价态
B.假设每一步均完全转化,每生成2 mol NH ,同时生成1.5 mol O
3 2
C.反应①②③均为氧化还原反应
D.参与反应的物质均只含离子键
【答案】B
【解析】A.根据转化关系可知:在转化过程中H始终呈+1价,A错误;
B.假设每一步均完全转化,生成O 转移4 mol电子,每生成1 mol NH 转移了3 mol电子,则当生成2
2 3
6
mol NH 时转移6 mol电子,则反应生成O 的物质的量为n(O )= mol =1.5 mol,B正确;
3 2 2
4
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C.反应②为Li N+3H O=NH ↑+3LiOH,该反应过程中元素化合价不变,因此反应属于非氧化还原反应,C
3 2 3
错误;
D.根据反应转化关系可知:反应过程中参与反应的物质含有离子键、共价键,D错误;
故合理选项是B。
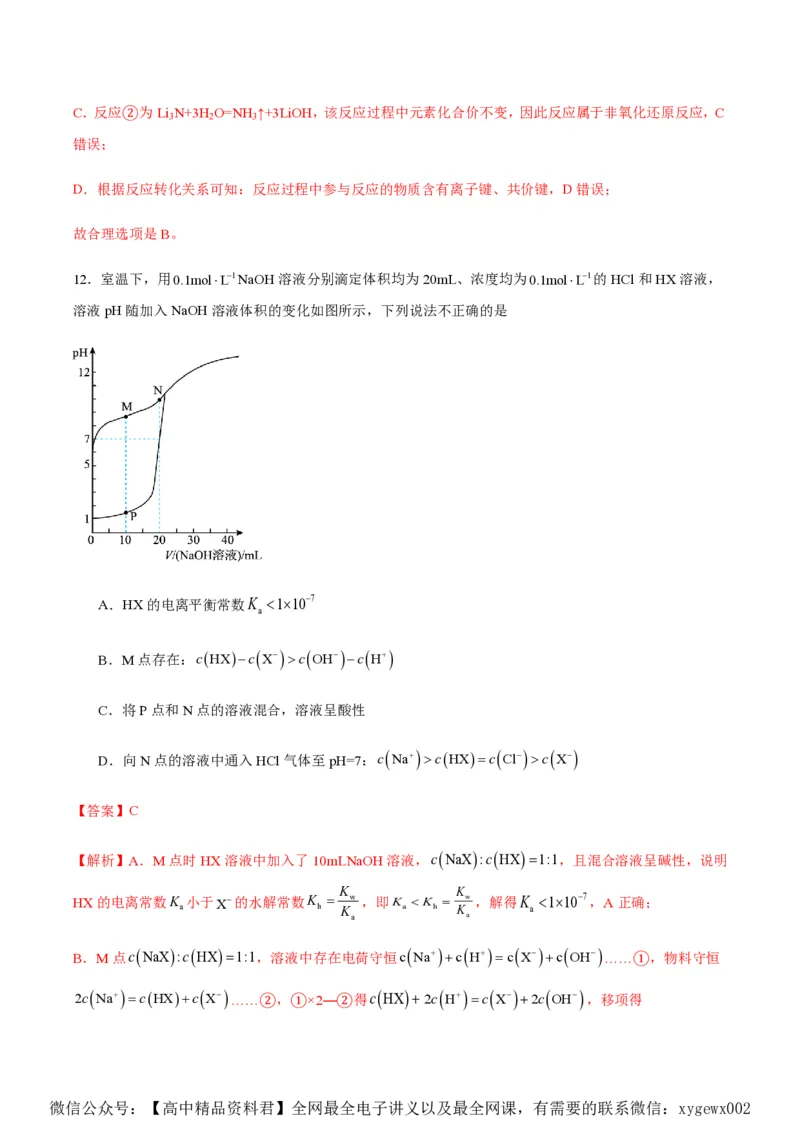
12.室温下,用0.1molL1NaOH溶液分别滴定体积均为20mL、浓度均为0.1molL1的HCl和HX溶液,
溶液pH随加入NaOH溶液体积的变化如图所示,下列说法不正确的是
A.HX的电离平衡常数K 1107
a
B.M点存在:cHXc X c OH c H
C.将P点和N点的溶液混合,溶液呈酸性
D.向N点的溶液中通入HCl气体至pH=7:c Na cHXc Cl c X
【答案】C
【解析】A.M点时HX溶液中加入了10mLNaOH溶液,cNaX:cHX1:1,且混合溶液呈碱性,说明
K K
HX的电离常数K 小于X的水解常数K w ,即K K w ,解得K 1107,A正确;
a h K a h K a
a a
B.M点cNaX:cHX1:1,溶液中存在电荷守恒c Na c H c X c OH ……①,物料守恒
2c Na cHXc X ……②,①×2―②得cHX 2c H c X 2c OH ,移项得
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002cHXc X 2c OH c H,且M点:c OH c H ,所以cHX c X c OH c H ,B
正确;
C.P点nNaClnHCl1103mol,N点nNaX2103mol,二者混合后HCl和NaX发生反应得到
NaCl和HX,此时溶液中nNaCl:nHX :nNaX2:1:1,由A选项可知,溶液呈碱性,C错误;
D.N点溶质为NaX,通入HCl气体至pH=7,由电荷守恒推知c
Na
c
X
c
Cl
……①,物料守恒
为c Na cHXc X ……②,所以c Na cHXc Cl ,又由A选项知K
a
c
H
c
X
1107,c H 1107molL1时cHX c X ,即c Na cHXc Cl c X ,D
cHX
正确;
故选C。
13.银锌电池的总反应式:Zn+Ag O+H O=Zn(OH) +2Ag。某学习小组以该电池为电源电解处理含Ba(OH)
2 2 2 2
的废水和含Ni2+、Cl-的酸性废水,并分别获得BaCl 溶液和单质镍。电解处理的工作原理如图所示。下列
2
说法正确的是
A.X电极与银锌电池的Zn电极相连
B.若去掉离子膜M,则X电极的反应式不变
C.离子膜M为阳离子交换膜,离子膜N为阴离子交换膜
D.电解过程中b室BaCl 浓度不变
2
【答案】C
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002【解析】A.电解结果是获得BaCl 溶液和单质镍,所以Y极发生的电极反应为Ni2 2e=Ni,即Y极为阴
2
极,则X极为阳极,与银锌电池的正极相连,而根据电池总反应可知,Zn极为负极,A项错误;
B.去掉离子膜M,X极上发生的反应为氯离子失去电子生成氯气,而之前为OH失电子生成氧气,B项错
误;
C.为了得到氯化钡溶液,a区的Ba2透过离子膜M进入b区,c区的氯离子透过离子膜N进入b区,所以
离子膜M为阳离子交换膜,离子膜N为阴离子交换膜,C项正确;
D.电解过程中b室BaCl 浓度不断增大,D项错误;
2
故选C。
14.已知反应①CO(g)+CuO(s)⇌CO (g)+Cu(s)和反应②H (g)+CuO(s)⇌Cu(s)+H O(g)在相同温度下的平
2 2 2
衡常数分别为K 和K ,该温度下反应③CO(g)+H O(g)⇌CO (g)+H (g)的平衡常数为K 。则下列说法中正
1 2 2 2 2 3
确的是
cCO cCu
A.反应①的平衡常数K = 2
1 cCO cCuO
K
B.反应③的平衡常数K = 1
3 K
2
C.对于反应③,恒容时,温度升高,氢气的浓度减小,则该反应的ΔH > 0
D.对于反应②,增加CuO的量,平衡正移
【答案】B
【解析】A、由化学平衡常数定义:可逆化学反应达到平衡状态时生成物与反应物的浓度(方程式系数幂次
方)乘积比或反应产物与反应底物的浓度(方程式系数幂次方)乘积比可知,反应①的平衡常数K =
1
cCO
2 ,故A错误;
cCO
K
B、反应①-反应②可得反应③,因此K = 1 ,故B正确;
3 K
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C、对于反应③,升高温度时,若氢气的浓度减小,说明平衡逆向移动,由此可知逆向为吸热反应,则该反
应的ΔH<0,故C错误;
D、增加固体的量,不会影响化学平衡,故D错误;
故答案为B。
15.为研究用AgNO 溶液将混合溶液中的Cl和CrO2沉淀分离,绘制了25℃时AgCl和Ag CrO 两种难溶
3 4 2 4
化合物的溶解平衡曲线。其中,pAg lgc Ag ,其余离子类推。两条相交的溶解平衡曲线把图像分成
了X、Y、Z、M四个区域。下列说法中不正确的是
A.K Ag CrO 约为11012,K AgCl的数量级为1010
sp 2 4 sp
B.M区域内可析出Ag CrO 沉淀,而不析出AgCl沉淀
2 4
C.向Cl、CrO2均为0.1mol/L的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀
4
c
CrO2
4
D.向Ag CrO 、AgCl混合固体和水的溶解平衡体系中加少量水, 增大
2 4 c2 Cl
【答案】D
【解析】A.根据图像,对于Ag CrO ,K (Ag CrO )=c2(Ag+)·c(CrO2)=(10-4)2×10-4=10-12,对于AgCl,
2 4 sp 2 4 4
K (AgCl)=c(Ag+)·c(Cl-)=10-8×10-2=10-10,A正确;
sp
B.曲线上的点达到沉淀溶解平衡,在M区域,相对于Ag CrO 来说,相当于在沉淀溶解平衡的基础上增
2 4
大Ag+浓度,则Q >K (Ag CrO ),不利于Ag CrO 沉淀溶解,从而析出Ag CrO 沉淀,而相对于AgCl来
c sp 2 4 2 4 2 4
说,相当于在沉淀溶解平衡的基础上减少Ag+浓度,则Q ”、“<”、“=”或“不确定”);B点时N 的转化率= (保
B C 2
留2位有效数字)。
(3)从图乙中获知反应Ⅰ存在着高温降低平衡产率与低温降低反应速率等调控矛盾。在提高合成氨的产率的
工业生产中,通常从以下多个视角来综合考虑合理的工业生产条件:
反应速率的视角:①加入催化剂;②提高温度(控制在催化剂的活性温度内)
平衡移动和原料的转化率的视角:③ ,④ 。
(4)科学家为避免直接破坏NN键而消耗大量热能,通过新型催化剂降低了反应路径中决速步的能垒,
使该反应在常温、常压下采用电化学方法也能实现,反应装置如图所示,阴极上的电极反应式
为 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002【答案】(1)+571.6
(2)0.075 = 82%
(3)增大压强 增大N 的浓度
2
(4)N 6H 6e=2NH
2 3
【解析】(1)依据盖斯定律可知Ⅰ×2+Ⅱ×3即得到反应2N (g)+6H O(l)=4NH (g)+3O (g),则
2 2 3 2
153092.42
H 571.6kJ /mol;
3 3
故答案为:+571.6;
(2) ①反应前氮气浓度是mol/L,氢气浓度是1mol/L,0~10min内消耗氢气是浓度是1mol/L-0.25mol/L=
c 0.75mol/L
0.75mol/L,则v 0.075mol/L·min;
t 10min
故答案为:0.075;
②平衡常数只与温度有关系,则B、C两点的平衡常数K =K ,设B点时消耗氮气的物质的量是xmol,
B C
N g 3H g 2NH g
2 2 3
起始mol 1 3 0
,此时氨气的体积分数是0.7,
转化mol x 3x 2x
平衡mol 1x 33x 2x
14
2x 14
0.7,x ,所以的转化率17 ;
1x33x2x 17 100%82%
1
故答案为:=;82%;
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(3)由于正反应是体积减小的放热反应,则从平衡移动和原料的转化率的视角应该是增大压强或增大的浓
度有利于平衡正向移动,可以提高氢气转化率;
故答案为:增大压强;增大 N 的浓度;
2
(4)阴极上氮气得到电子结合氢离子转化为氨气,电极反应式为N 6H 6e 2NH ;
2 3
故答案为:N 6H 6e 2NH 。
2 3
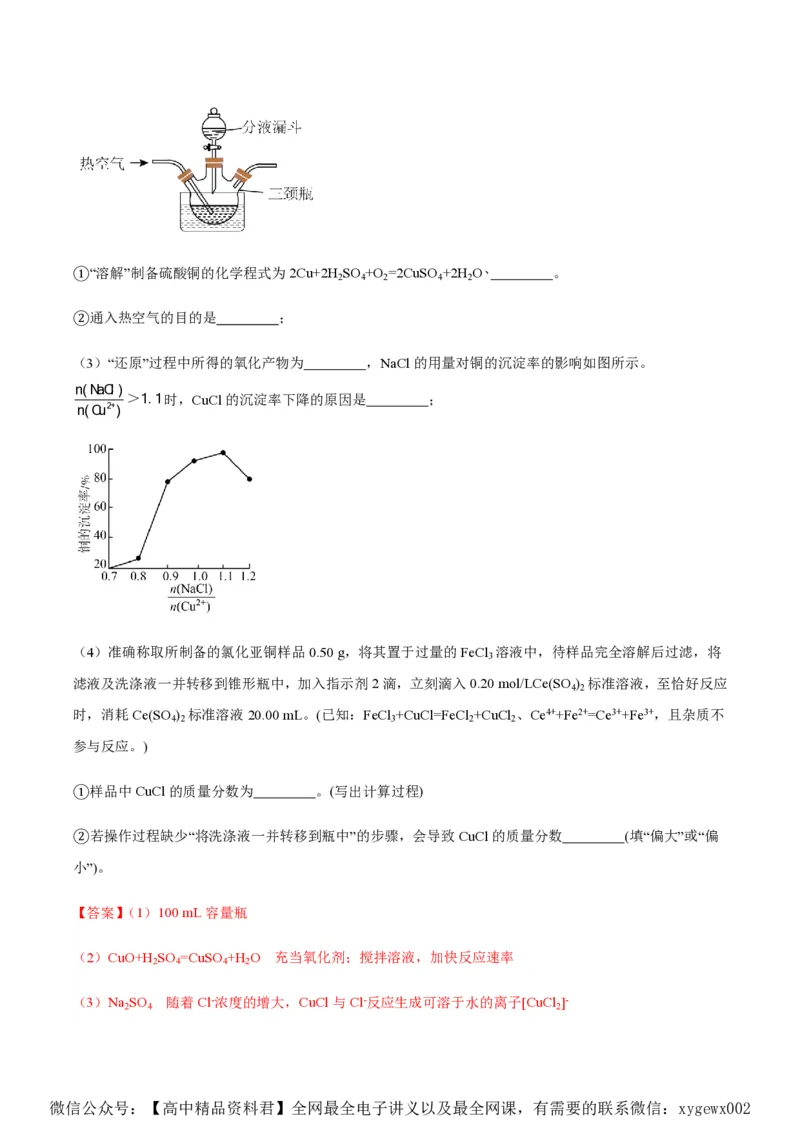
18.(14分)金属钛有“生物金属、海洋金属、太空金属”的美称。有些含钛的化合物在耐高温、环保或者抑
菌方面有着重要的应用,钛元素也被称为“健康钛”。
(1)Ti元素位于元素周期表的 区,基态原子电子排布式为 。
(2)TiCl 与SiCl 互为等电子体。SiCl 可以与N-甲基咪唑 发生反应。
4 4 4
①TiCl 分子的空间构型为 。
4
②N-甲基咪唑分子中碳原子的杂化轨道类型为 ,C、N、Si的电负性由大到小的顺序为 ,1个
含有 个π键。
(3)TiCl 可以与胺形成配合物,如TiCl (CH NH ) 、TiCl (H NCH CH NH )。
4 4 3 2 2 4 2 2 2 2
① TiCl (H NCH CH NH )中提供电子对形成配位键的原子是 。
4 2 2 2 2
②乙二胺(H NCH CH NH )能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳
2 2 2 2
定性较差的是 (填“Mg2+”或“Cu2+”)。
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-
射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则r(N3-)为 pm。该氮化钛的密度为
g·cm-3(N 为阿伏加德罗常数的值,只列计算式)。
A
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002【答案】(1)d 1s22s22p63s2 3p63d2 4s2
(2)正四面体 sp2 sp3 N>C>Si 2
(3)N、Cl Mg2+
2 462
(4) a
4 N a310-30
A
【解析】(1)钛是22号元素,位于元素周期表的d区;其中每一个电子是运动状态都不同,钛是22号元
素,电子数也是22,基态原子电子排布式为1s22s22p63s2 3p63d2 4s2,故答案为:d;1s22s22p63s2 3p63d2 4s2;
(2)①TiCl 分子中Ti原子价层电子对数为4,没有孤对电子,因此分子的空间构型是正四面体,故答案
4
为:正四面体;
②甲基的C原子形成4个σ键,无孤电子对,C原子价层电子对个数是4,为sp3杂化,环上C原子形成3
个σ键,无孤电子对,价层电子对个数是3,为sp2杂化;元素非金属性越强,其电负性越大,元素的非金
属性大小:N>C>Si,则电负性大小顺序:N>C>Si;共价单键为σ键、共价双键中含有1个σ键、1个π键,
则 中含有2个π键,故答案为:sp2 sp3;N>C>Si;2;
(3)①在TiCl (H NCH CH NH )中Ti原子与4个Cl原子及H NCH CH NH 的2个N原子形成配位键,
4 2 2 2 2 2 2 2 2
即提供电子对形成配位键的原子是N、Cl,故答案为:N、Cl;
②根据形成配位键的条件,可以得出乙二胺的两个N提供孤电子对给金属离子,从而形成稳定的环状离子,
由于Cu2+半径大,更容易提供空轨道,Mg2+与乙二胺形成的化合物稳定性相对较差,故答案为:Mg2+;
2
(4)紧邻的N原子所在的位置为晶胞面对角线的一半,所以r(N3-)= a pm;该该晶胞中含有Ti原子数
4
1 1 1
为:12 1=4,含有的N原子数为:8 6 =4,晶胞边长为apm,则该晶胞的密度
4 8 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002ρ= m = 4(4814) g/cm3= 462 g/cm3,故答案为: 2 a; 462 。
V N (a10-10)3 N a310-30 4 N a310-30
A A A
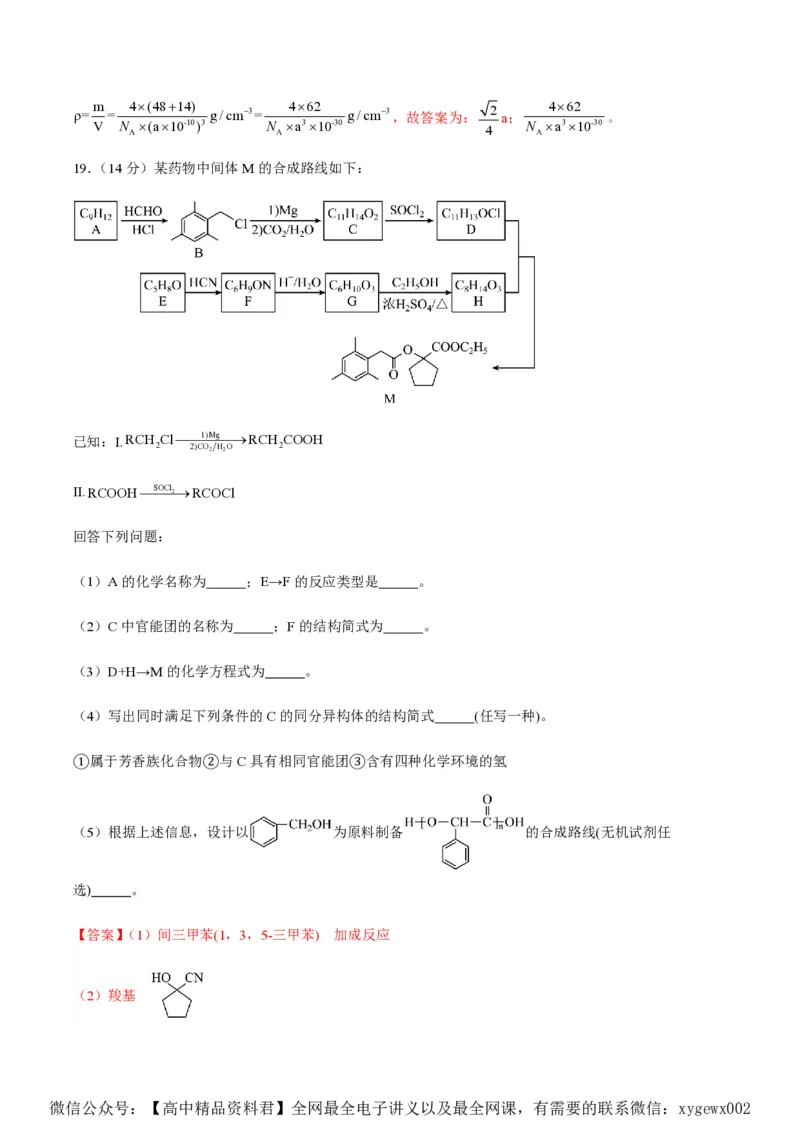
19.(14分)某药物中间体M的合成路线如下:
已知:I.RCH Cl1)MgRCH COOH
2 2)CO2 H2O 2
II.RCOOHSOCl2RCOCl
回答下列问题:
(1)A的化学名称为 ;E→F的反应类型是 。
(2)C中官能团的名称为 ;F的结构简式为 。
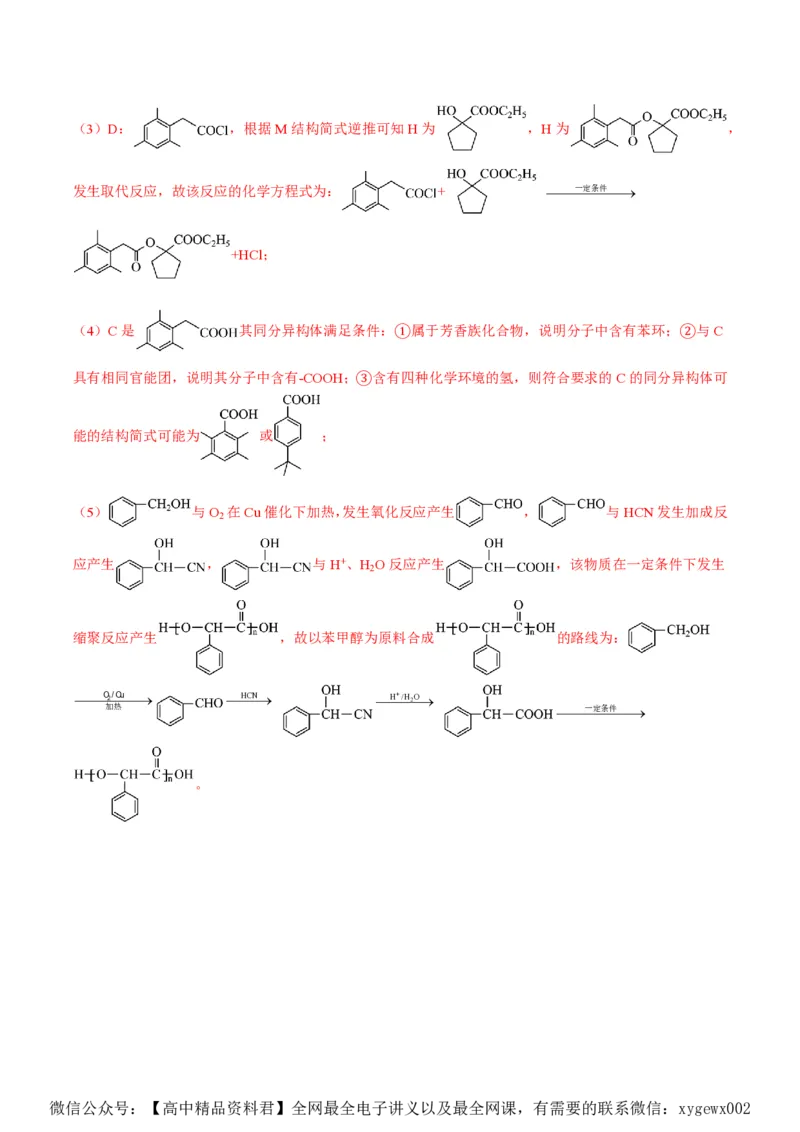
(3)D+H→M的化学方程式为 。
(4)写出同时满足下列条件的C的同分异构体的结构简式 (任写一种)。
①属于芳香族化合物②与C具有相同官能团③含有四种化学环境的氢
(5)根据上述信息,设计以 为原料制备 的合成路线(无机试剂任
选) 。
【答案】(1)间三甲苯(1,3,5-三甲苯) 加成反应
(2)羧基
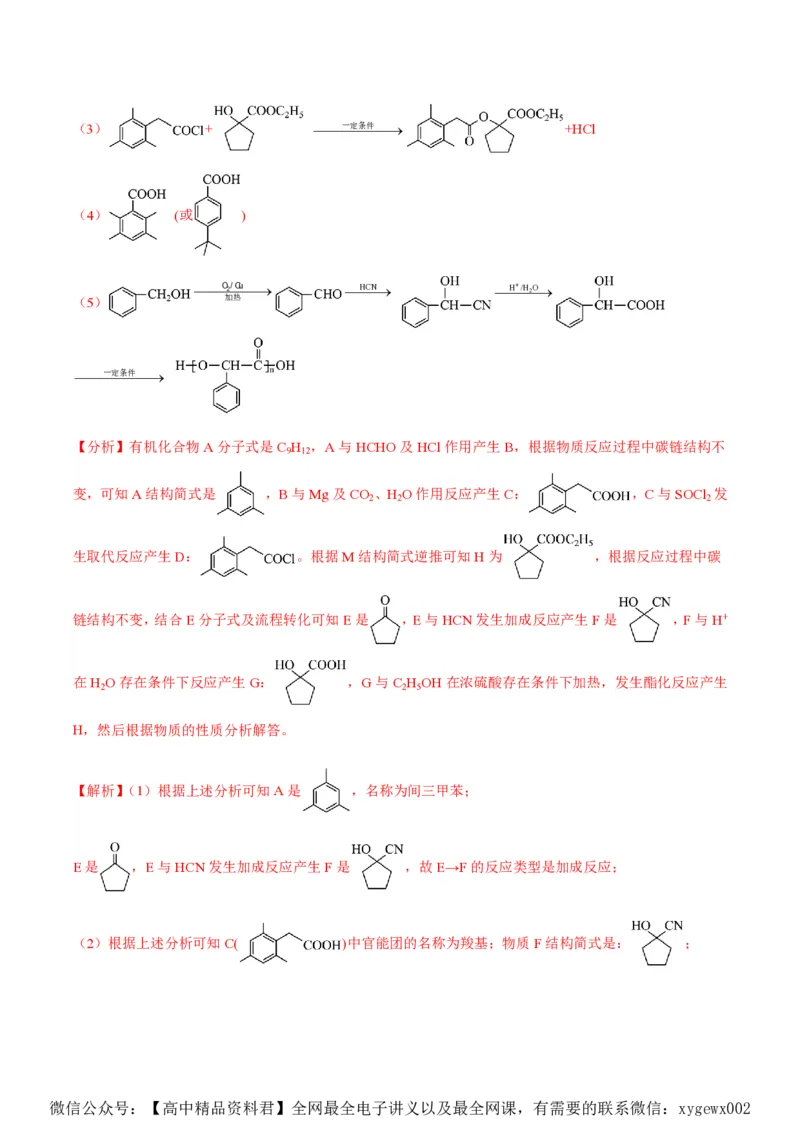
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(3) + 一定条件 +HCl
(4) (或 )
O2 /Cu HCN H+/H2O
(5) 加热
一定条件
【分析】有机化合物A分子式是C H ,A与HCHO及HCl作用产生B,根据物质反应过程中碳链结构不
9 12
变,可知A结构简式是 ,B与Mg及CO 、H O作用反应产生C: ,C与SOCl 发
2 2 2
生取代反应产生D: 。根据M结构简式逆推可知H为 ,根据反应过程中碳
链结构不变,结合E分子式及流程转化可知E是 ,E与HCN发生加成反应产生F是 ,F与H+
在H O存在条件下反应产生G: ,G与C H OH在浓硫酸存在条件下加热,发生酯化反应产生
2 2 5
H,然后根据物质的性质分析解答。
【解析】(1)根据上述分析可知A是 ,名称为间三甲苯;
E是 ,E与HCN发生加成反应产生F是 ,故E→F的反应类型是加成反应;
(2)根据上述分析可知C( )中官能团的名称为羧基;物质F结构简式是: ;
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(3)D: ,根据M结构简式逆推可知H为 ,H为 ,
发生取代反应,故该反应的化学方程式为: + 一定条件
+HCl;
(4)C是 其同分异构体满足条件:①属于芳香族化合物,说明分子中含有苯环;②与C
具有相同官能团,说明其分子中含有-COOH;③含有四种化学环境的氢,则符合要求的C的同分异构体可
能的结构简式可能为 或 ;
(5) 与O 在Cu催化下加热,发生氧化反应产生 , 与HCN发生加成反
2
应产生 , 与H+、H O反应产生 ,该物质在一定条件下发生
2
缩聚反应产生 ,故以苯甲醇为原料合成 的路线为:
O2 /Cu HCN H+/H2O
加热 一定条件
。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002