文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(黑龙江、甘肃、吉林、
安徽、江西、贵州、广西)
黄金卷 04
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Co 59 Cu 64
第Ⅰ卷
一、单项选择题:共15题,每题3分,共45分。每题只有一个选项最符合题意。
1.化学和生活、科技、社会发展息息相关,下列说法正确的是
A.华为新上市的mate60 pro手机引发关注,其CPU基础材料是SiO
2
B.三星堆黄金面具出土时光亮且薄如纸,说明金不活泼和有很好的延展性
C.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO
D.医用外科口罩使用的材料聚丙烯,能使酸性高锰酸钾溶液褪色
2.下列叙述正确的是
A.HBrO的结构式为:H-Br-O
B.醋酸的电离方程式为:CH
3
COOH+H
2
O‡ˆ ˆˆ†ˆ CH
3
COO-+H
3
O+
C.基态Si原子的价层电子的轨道表示式:
D.NH 的VSEPR模型:
3
3.设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.10g46%乙醇水溶液中含有氧原子的数目为0.4N
A
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.1mol 中含有σ键的数目为5N
A
C.0.2molNO和0.1molO 混合得到NO 分子数目为0.2N
2 2 A
D.在电解精炼铜中,阳极质量减少32g时理论上转移电子数目为N
A
D.在电解精炼铜中,阳极质量减少32g时理论上转移电子数目为N
A
4.能正确表示下列反应的离子方程式为
A.向CuSO 溶液中滴加少量稀氨水:Cu2++2OH-=Cu(OH) ↓
4 2
B.足量NaOH溶液与H C O 溶液反应:H C O +2OH-=C O2+2H O
2 2 4 2 2 4 2 4 2
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO2=BaSO ↓+H O
4 4 2
D.铝粉与过量NaOH溶液反应:Al+4OH-=AlO+2H O
2 2
5.下列说法错误的是
A.油脂碱性条件下的水解反应可用于生产肥皂
B.CuSO 会使体内的蛋白质变性从而失去生理活性
4
C.纤维素在人体内可水解成葡萄糖,供人体组织的营养需要
D.葡萄糖能发生银镜反应
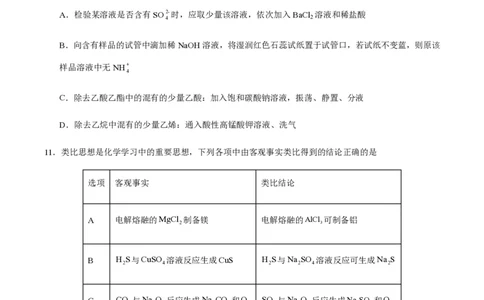
6.下列实验操作能达到实验目的的是
选项 A B C D
实验 证明K (AgI)< 探究化学反应速率的影响
sp
除去乙烯中少量的SO 增大HClO的浓度
2
目的 K (AgCl) 因素
sp
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002实验
操作
7.物质的性质决定用途,下列两者对应关系不正确的是
A.生铁的硬度大,可以用于制造钢轨、车轮、建材
B.SO 具有漂白、防腐和抗氧化等作用,可用作食品添加剂
2
C.常温下铁制容器遇浓硝酸钝化,可用铁制容器来盛装浓硝酸
D.SiC硬度很大,可用作砂轮的磨料
8.X、Y、Z、W是原子半径依次增大的短周期主族元素,X与其他元素不在同一周期,Y元素的电负性仅
次于氟元素,Z的基态原子中单电子与成对电子个数比为3∶4,W原子电子总数与Y原子的最外层电子数相
同。下列说法正确的是
A.第一电离能:Z>Y>W B.基态Z原子核外电子有7种空间运动状态
C.由四种元素组成的化合物仅含共价键 D.X、Y形成的化合物都是由极性键构成的极性分子
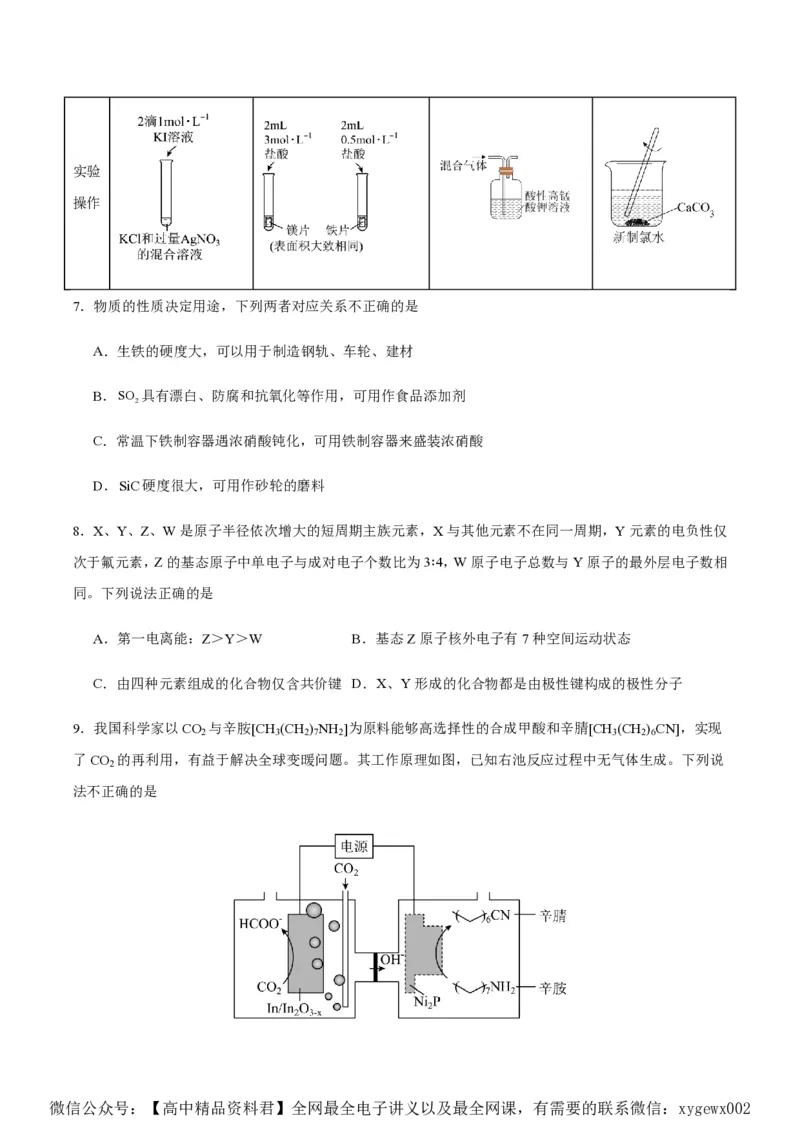
9.我国科学家以CO 与辛胺[CH (CH ) NH ]为原料能够高选择性的合成甲酸和辛腈[CH (CH ) CN],实现
2 3 2 7 2 3 2 6
了CO 的再利用,有益于解决全球变暖问题。其工作原理如图,已知右池反应过程中无气体生成。下列说
2
法不正确的是
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.Ni P电极的电势高于In/In O 电极
2 2 3-x
B.In/In O 电极上可能有副产物H 生成
2 3-x 2
C.阴极上的电极反应:CO + H O +2e-=HCOO+OH-
2 2
D.标准状况下,33.6L CO 参与反应时,Ni P电极有1.5 mol辛腈生成
2 2
10.下列关于物质的鉴别与除杂的说法正确的是
A.检验某溶液是否含有SO2-时,应取少量该溶液,依次加入BaCl 溶液和稀盐酸
4 2
B.向含有样品的试管中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,若试纸不变蓝,则原该
样品溶液中无NH+
4
C.除去乙酸乙酯中的混有的少量乙酸:加入饱和碳酸钠溶液,振荡、静置、分液
D.除去乙烷中混有的少量乙烯:通入酸性高锰酸钾溶液、洗气
11.类比思想是化学学习中的重要思想,下列各项中由客观事实类比得到的结论正确的是
选项 客观事实 类比结论
A 电解熔融的MgCl 制备镁 电解熔融的AlCl 可制备铝
2 3
B H S与CuSO 溶液反应生成CuS H S与Na SO 溶液反应可生成Na S
2 4 2 2 4 2
C CO 与Na O 反应生成Na CO 和O SO 与Na O 反应生成Na SO 和O
2 2 2 2 3 2 2 2 2 2 3 2
D Al SO 可作净水剂 Fe SO 也可作净水剂
2 4 3 2 4 3
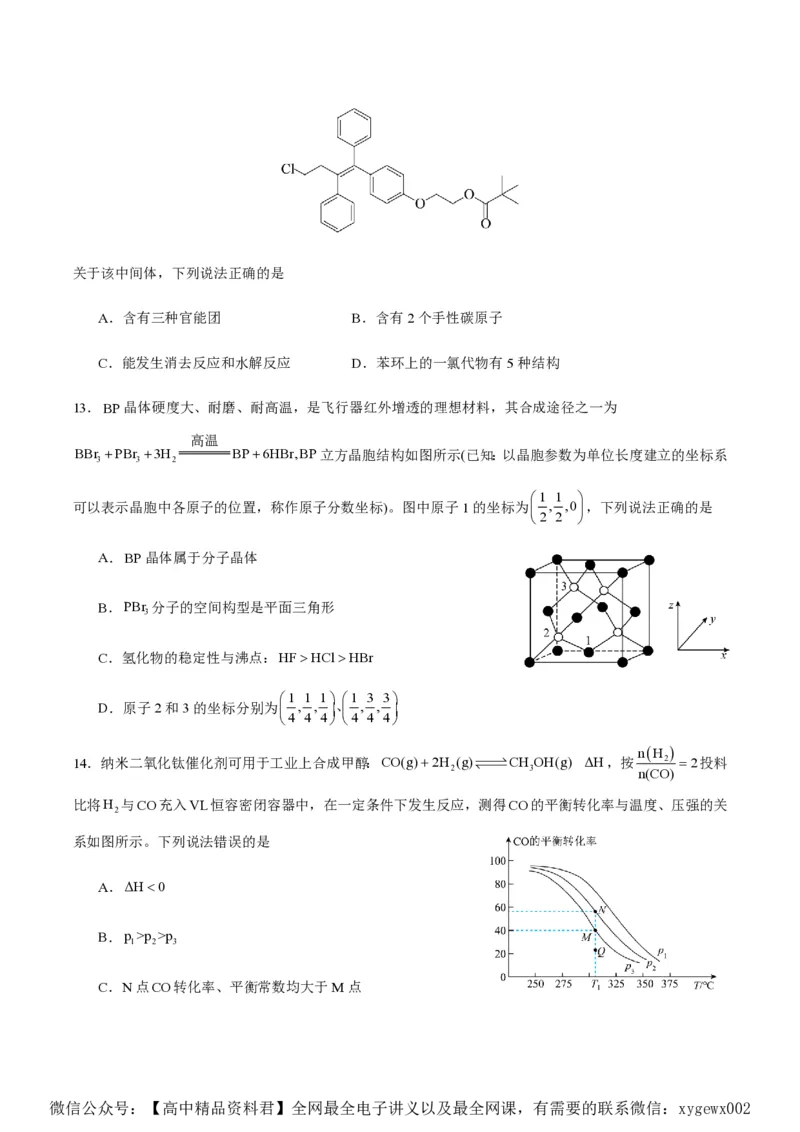
12.奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002关于该中间体,下列说法正确的是
A.含有三种官能团 B.含有2个手性碳原子
C.能发生消去反应和水解反应 D.苯环上的一氯代物有5种结构
13.BP晶体硬度大、耐磨、耐高温,是飞行器红外增透的理想材料,其合成途径之一为
高温
BBr PBr 3H BP6HBr,BP立方晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系
3 3 2
1 1
可以表示晶胞中各原子的位置,称作原子分数坐标)。图中原子1的坐标为 , ,0,下列说法正确的是
2 2
A.BP晶体属于分子晶体
B.PBr 分子的空间构型是平面三角形
3
C.氢化物的稳定性与沸点:HFHClHBr
1 1 1 1 3 3
D.原子2和3的坐标分别为 , , 、 , ,
4 4 4 4 4 4
nH
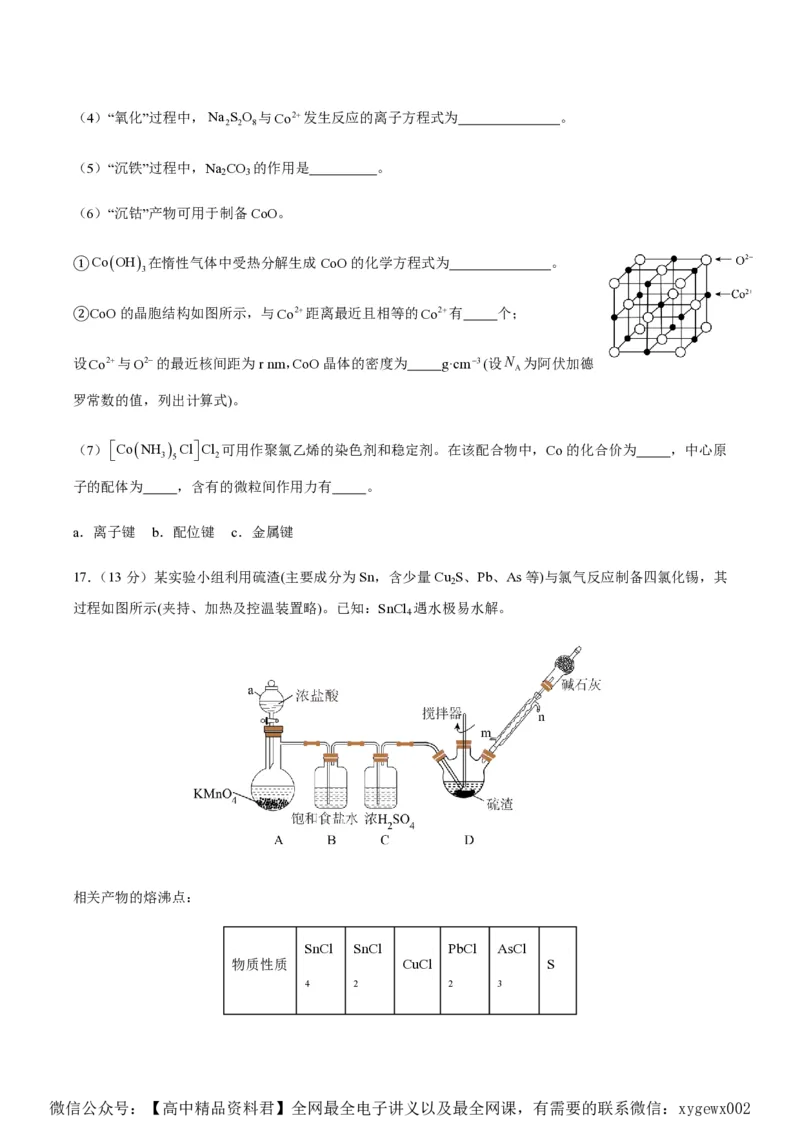
14.纳米二氧化钛催化剂可用于工业上合成甲醇:CO(g)2H
2
(g) CH
3
OH(g) ΔH,按
n(CO
2
)
2投料
比将H 与CO充入VL恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关
2
系如图所示。下列说法错误的是
A.ΔH0
B.p >p >p
1 2 3
C.N点CO转化率、平衡常数均大于M点
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002D.T℃、p 压强下,Q点对应的v v
1 3 正 逆
15.已知:硫氰酸(HSCN)是强酸,丙酮酸(CH COCOOH)是弱酸。在体积均为20 mL,浓度均为0.1 mol·L-1
3
的HSCN溶液和CH COCOOH溶液中分别滴加0.1 mol·L-1 NaOH溶液,溶液导电率与滴加NaOH溶液体积
3
的关系如图所示。下列叙述正确的是
A.曲线2代表CH COCOOH溶液的导电率变化
3
B.c点溶液中,c(Na+ )=c(SCN-)>c(H+ )=c(OH- )
C.HSCN和CH COCOOH中C的杂化方式完全相同
3
D.加水稀释b点溶液,各离子浓度都减小
第Ⅱ卷
二、非选择题:共4题,共55分。
16.(14分)钴是生产电池材料、高温合金、磁性材料及染色剂的重要原料。一种以湿法炼锌净化渣(主要
含有Co、Fe、Cu、Pb、ZnO、Fe O 等)为原料提取钴的工艺流程如下:
2 3
已知:常温下,K CuS8.91036,K CoS4.01021。
sp sp
回答下列问题:
(1)基态Co原子的价电子排布式为 。
(2)“浸出”过程中,为提高浸出率可采取的措施有 (写2种),浸出渣的成分为 。
(3)“除铜”后溶液中Co2浓度为0.4 mol·L1,为防止除铜时产生CoS沉淀,应控制溶液的pH不超过
[已知:常温下,饱和H S水溶液中存在关系式:c2 H c S2 1.01022( molL13 ]。
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(4)“氧化”过程中,Na S O 与Co2发生反应的离子方程式为 。
2 2 8
(5)“沉铁”过程中,Na CO 的作用是 。
2 3
(6)“沉钴”产物可用于制备CoO。
①CoOH 在惰性气体中受热分解生成CoO的化学方程式为 。
3
②CoO的晶胞结构如图所示,与Co2距离最近且相等的Co2有 个;
设Co2与O2的最近核间距为r nm,CoO晶体的密度为 g·cm3(设N 为阿伏加德
A
罗常数的值,列出计算式)。
(7)
CoNH
3
5
Cl
Cl
2
可用作聚氯乙烯的染色剂和稳定剂。在该配合物中,Co的化合价为 ,中心原
子的配体为 ,含有的微粒间作用力有 。
a.离子键 b.配位键 c.金属键
17.(13分)某实验小组利用硫渣(主要成分为Sn,含少量Cu S、Pb、As等)与氯气反应制备四氯化锡,其
2
过程如图所示(夹持、加热及控温装置略)。已知:SnCl 遇水极易水解。
4
相关产物的熔沸点:
SnCl SnCl PbCl AsCl
物质性质 CuCl S
4 2 2 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002熔点/℃ -33 246 426 501 -18 112
沸点/℃ 114 652 1490 951 130 444
(1)仪器a的名称 ,A中发生反应的化学方程式 。
(2)冷凝管的进水口为 (填“m”或“n”),碱石灰的作用为 。
(3)如果缺少B装置,可能造成的影响为 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温, (填操作名称,下同),得到粗产品,粗
产品再 可得到纯净的SnCl 。
4
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I 溶液20.00mL,并加
2
入少量的淀粉溶液:用1.0010-3molL1的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫
代硫酸钠标准溶液。测定过程中发生的相关反应:
①AsCl +3H O=H AsO +3HCl
3 2 3 3
②H AsO +I +H O=H AsO +2HI
3 3 2 2 3 4
③2S O2+I =2I-+S O2
2 3 2 4 6
则产品中SnCl 的质量分数 (保留三位有效数字)。某同学认为粗产品中会溶有少量氯气,导致测量
4
结果 (填“偏高”“偏低”或“无影响”)。
18.(14分)氮及其化合物在人们的日常生活、生产工业中和环保事中属于“明星物质”,目前最成功的应用
就是“人工固氮”,在某特殊催化剂和光照条件下,N 与水反应可生成NH 。
2 3
(1)已知:
①4NH (g) + 3O (g) 2N (g) + 6H O(g) ΔH =-1260 kJ/mol;
3 2 2 2 1
②H O(l)= H O(g) ΔH =+44.0 kJ/mol。
2 2 2
则 2N (g) + 6H O(1) 4NH (g)+ 3O (g) ΔH = kJ / mol
2 2 3 2 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(2)N (g) + 3H (g) 2NH (g) ΔH=-92.4 kJ/mol。将1. 00 mol N 和3. 00 mol H 充入容积为3 L的恒容密
2 2 3 2 2
闭容器中,发生上述反应。
①图甲是测得X、Y的浓度随时间变化的曲线,反应达到平衡时的平均反应速率v(H )= 。
2
②在不同温度和压强下,平衡体系中NH 的体积分数与温度、压强关系如图乙,则压强P P (填“大
3 2 1
于”“小于”或“不确定”,下同),B、D两点的平衡常数K(D) K(B),B点N 的转化率= (保留4
2
位有效数字)。
(3)在恒容密闭容器中充入NH 和NO ,在一定温度下发生反应:8NH (g) + 6NO (g) 7N (g) +
3 2 3 2 2
12H O(g)。下列表明该反应能达到平衡状态的是 (填字母)
2
a. 混合气体压强保持不变 b. 混合气体密度保持不变
c. NO 和NH 的消耗速率之比为3 : 4 d. 混合气体颜色不变
2 3
(4)“绿水青山就是金山银山”,利用原电池原理(6NO + 8NH =7N + 12H O),可以处理氮的氧化物和NH
2 3 2 2 3
尾气,装置原理图如图丙,正极反应式为 ,当有标准状况下44.8 L NO 被处理时,转移电子的物
2
质的量为 mol。
19.(14分)布洛芬具有退热、镇痛的疗效,是缓解新冠病毒病症的有效药物。布洛芬的传统合成路线如图。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002已知:RCHONR2OHRCH=NOH(R为烃基)
回答下列问题:
(1)A→B的反应类型为 。
(2)ClCH COOC H 的官能团名称为 。
2 2 5
(3)写出D与银氨溶液反应的化学方程式 。
(4)布洛芬的同系物M分子式为C H O ,其可能结构有 种(不考虑立体异构),其中核磁共振氢谱
9 10 2
有四组峰且峰面积之比为1∶2∶6∶1的结构简式为 (写出一种即可)。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002