文档内容
西南大学附属中学高2026届10月月考
4.下列有关离子方程式错误的是( )。
化学试题
A.CuCl₂ 浓溶液稀释,绿色溶液变蓝:[CaCLP+4H₂O=[Cu(H₂O)4]²++4CT
B. 铅酸蓄电池充电时的阳极反应:Pb²++2H₂O-2e⁻=PbO₂+4H+
注意事项: C. 少量氢氧化钡溶液与硫酸氢铵溶液反应:Ba²+20H⁻+2H⁴+SO?=BaSO₄↓+2H₂O
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。 D.AlCl₃ 溶液和NaHCO₃溶液混合:AP++3HCO₃=AI(OH)₃↓+3CO₂↑
2. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用 5.W、X、Y、Z 是原子序数依次增大的短周期主族元素,其中基态Z原子s轨道电子数与p
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
轨道电子数之比为3:4,由上述四种元素形成的一种化合物M的结构如图所示。下列说
3. 试卷由…… … 一… 整理排版。考试结束后,将本试卷和答题卡一并交回。 法正确的是( )。
4. 可能用到的相对原子质量:H—1 B—11 C—12 N—14 O—16 Na—23 Ce—140 A.W、X、Y 的简单离子的半径:YHCO;
D 向苯酚浓溶液中滴加少量溴水、振荡 无白色沉淀产生 该条件下两者不反应
2. 下列化学用语或图示表达正确的是( )。
7.Cl₂O可用于水的杀菌消毒,遇水发生反应: Cl₂O+H₂O=2HCIO。下列说法正确的是( )。
A.H₂O 和OF₂ 的键角大小关系为: H₂O C.N 点:c(HX-)约为4×10-7
分离铁粉和I
受热分解的产物 Zn>Fe>Cu Kp(Ag₂S) D.K(BaX) 约为1.2×10-21
11.硼及其化合物在材料制造、有机合成等方面应用广泛。图(a)为一种无限长单链状结构的多 二 、解答题:本题包括4小题,共58分。
硼酸根,图(b)为硼氢化钠晶胞结构。(Na 为阿伏伽德罗常数值),下列说法正确的是( )。 15.(14分)稀土元素Ce 是重要的战略资源,其氧化物CeO₂ 是一种重要的催化剂。一种沉淀
法制备CeO₂的过程如下:
氨水、NH₄HCO₃溶液
●BH
ONa Ce(NO₃)₃溶液— 沉淀 过滤 Ce₂(CO₃)₃·8H₂O灼烧CeO₂
滤液
(a) (b)
(1)制备Ce₂(CO₃)₃·8H₂O 沉淀
A. 图(a)中多硼酸根的化学式为[BO₃] B. 图(a)中和BH 中的B的杂化方式不同 ①配制Ce(NO₃)₃溶液时,需滴加适量稀硝酸调节酸度,其原因为 9
C. 硼氢化钠晶体中Na 配位数为4 D. 硼氢化钠晶体的密度为 ②生成Ce₂(CO₃)₃·8H₂O 沉淀的化学方程式为_
第4页共8页(2)灼烧Ce₂(CO₃)₃·8H₂O 制备CeO₂ Ⅱ.待回流中无色油状液体变为乳白色油珠,将混合物转入水蒸气蒸馏装置.进行蒸馏。
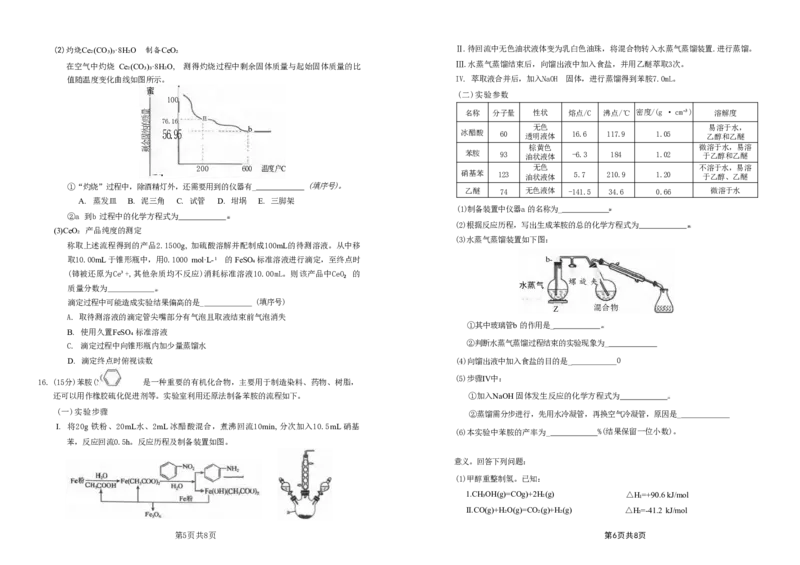
在空气中灼烧 Ce₂(CO₃)₃·8H₂O, 测得灼烧过程中剩余固体质量与起始固体质量的比 Ⅲ.水蒸气蒸馏结束后,向馏出液中加入食盐,并用乙醚萃取3次。
值随温度变化曲线如图所示。 IV. 萃取液合并后,加入NaOH 固体,进行蒸馏得到苯胺7.0mL。
蜜
(二)实验参数
100
名称 分子量 性状 熔点/C 沸点/℃ 密度/(g ·cm⁻³) 溶解度
76.16 旦
56.95 b 冰醋酸 60 透明 无 液 色 体 16.6 117.9 1.05 乙 易 醇 溶 和 于 乙 水 醚 ,
棕黄色 微溶于水,易溶
苯胺 93 油状液体 -6.3 184 1.02 于乙醇和乙醚
200 600 温度户C 无色 不溶于水,易溶
硝基苯 123 油状液体 5.7 210.9 1.20 于乙醇、乙醚
①“灼烧”过程中,除酒精灯外,还需要用到的仪器有_ (填序号)。
乙醚 74 无色液体 -141.5 34.6 0.66 微溶于水
A. 蒸发皿 B. 泥三角 C. 试管 D. 坩埚 E. 三脚架
(1)制备装置中仪器a的名称为_
②a 到b过程中的化学方程式为
(2)根据反应历程,写出生成苯胺的总的化学方程式为
(3)CeO₂ 产品纯度的测定
(3)水蒸气蒸馏装置如下图:
称取上述流程得到的产品2.1500g, 加硫酸溶解并配制成100mL的待测溶液。从中移
取10.00mL于锥形瓶中,用0.1000 mol·L-¹ 的FeSO₄标准溶液进行滴定,至终点时 b-
(铈被还原为Ce³+,其他杂质均不反应)消耗标准溶液10.00mL。则该产品中CeO₂ 的
螺旋夹
质量分数为 水蒸气
滴定过程中可能造成实验结果偏高的是_ (填序号)
Z 混合物
A. 取待测溶液的滴定管尖嘴部分有气泡且取液结束前气泡消失
①其中玻璃管b的作用是_
B. 使用久置FeSO₄标准溶液
C. 滴定过程中向锥形瓶内加少量蒸馏水 ②判断水蒸气蒸馏过程结束的实验现象为_
D. 滴定终点时俯视读数 (4)向馏出液中加入食盐的目的是_ 0
16.(15分)苯胺(NH₂) 是一种重要的有机化合物,主要用于制造染料、药物、树脂,
(5)步骤IV中:
还可以用作橡胶硫化促进剂等。实验室利用还原法制备苯胺的流程如下。 ①加入NaOH固体发生反应的化学方程式为
(一)实验步骤 ②蒸馏需分步进行,先用水冷凝管,再换空气冷凝管,原因是_
I. 将20g铁粉、20mL水、2mL冰醋酸混合,煮沸回流10min,分次加入10.5mL硝基
(6)本实验中苯胺的产率为_ %(结果保留一位小数)。
苯,反应回流0.5h。反应历程及制备装置如图。
意义。回答下列问题:
(1)甲醇重整制氢。已知:
1.CH₃OH(g)=COg)+2H₂(g) △H₁=+90.6kJ/mol
II.CO(g)+H₂O(g)=CO₂(g)+H₂(g) △H₂=-41.2 kJ/mol
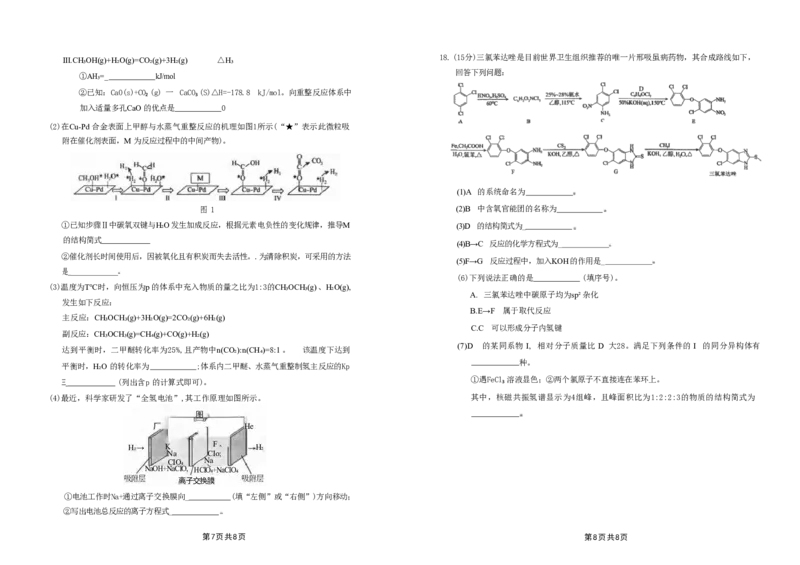
第5页共8页 第6页共8页Ⅲ.CH₃OH(g)+H₂O(g)=CO₂(g)+3H₂(g) △H₃ 18.(15分)三氯苯达唑是目前世界卫生组织推荐的唯一片邢吸虽病药物,其合成路线如下,
回答下列问题:
①AH₃=_ kJ/mol
②已知:CaO(s)+CO₂(g) 一 CaCO₃(S)△H=-178.8 kJ/mol。向重整反应体系中
加入适量多孔CaO的优点是 0
(2)在Cu-Pd合金表面上甲醇与水蒸气重整反应的机理如图1所示(“★”表示此微粒吸
附在催化剂表面,M为反应过程中的中间产物)。
(1)A 的系统命名为
图 1 (2)B 中含氧官能团的名称为
①已知步骤Ⅱ中碳氧双键与H₂O发生加成反应,根据元素电负性的变化规律,推导M (3)D 的结构简式为_
的结构简式
(4)B→C 反应的化学方程式为_
②催化剂长时间使用后,因被氧化且有积炭而失去活性。.为清除积炭,可采用的方法
(5)F→G 反应过程中,加入KOH的作用是_
是_
(6)下列说法正确的是 (填序号)。
(3)温度为T℃时,向恒压为p的体系中充入物质的量之比为1:3的CH₃OCH₃(g)、H₂O(g),
A. 三氯苯达唑中碳原子均为sp²杂化
发生如下反应:
B.E→F 属于取代反应
主反应:CH₃OCH₃(g)+3H₂O(g)=2CO₂(g)+6H₂(g)
C.C 可以形成分子内氢键
副反应:CH₃OCH₃(g)=CH₄(g)+CO(g)+H₂(g)
(7)D 的某同系物I, 相对分子质量比 D 大28。满足下列条件的I 的同分异构体有
达到平衡时,二甲醚转化率为25%,且产物中n(CO₂):n(CH₄)=8:1。 该温度下达到
种。
平衡时,H₂O 的转化率为 ;体系内二甲醚、水蒸气重整制氢主反应的Kp
三_ (列出含p的计算式即可)。
①遇FeCl₃溶液显色;②两个氯原子不直接连在苯环上。
(4)最近,科学家研发了“全氢电池”,其工作原理如图所示。 其中,核磁共振氢谱显示为4组峰,且峰面积比为1:2:2:3的物质的结构简式为
图
厂 He
H₂→ K
F、
H₂
Na CIo;
CIO₄ Na
NaOH+NaCIO, HCIO₄+NaCIO₄
吸附层 离子交换膜 吸附层
①电池工作时Na+通过离子交换膜向_ (填“左侧”或“右侧”)方向移动;
②写出电池总反应的离子方程式_
第7页共8页 第8页共8页(4)①右侧 ②H⁴+OH-=H₂O
18.
(1)1,2,4 一三氯苯
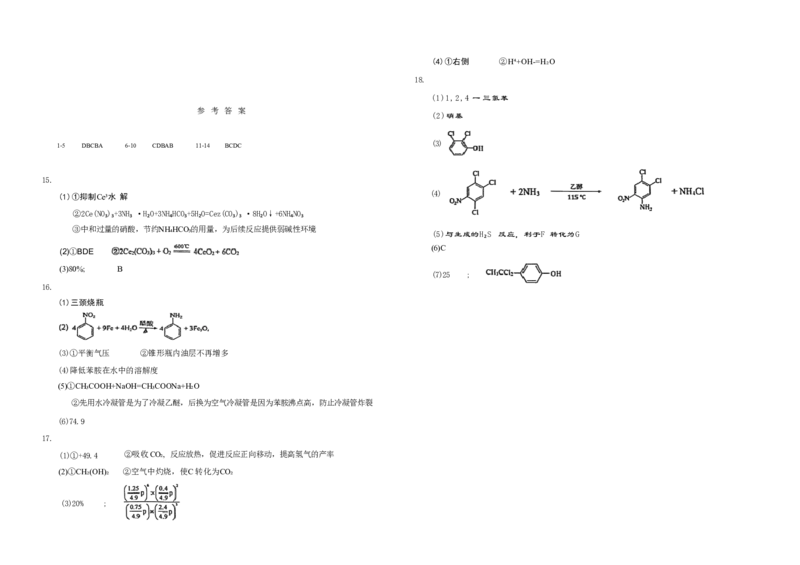
参 考 答 案
(2)硝基
(3)
1-5 DBCBA 6-10 CDBAB 11-14 BCDC
15.
(4)
(1)①抑制Ce³水 解
②2Ce(NO₃)₃+3NH₃ ·H₂O+3NH₄HCO₃+5H₂O=Cez(CO₃)₃ ·8H₂O↓+6NH₄NO₃
③中和过量的硝酸,节约NH₄HCO₃的用量,为后续反应提供弱碱性环境
(5)与生成的H₂S 反应,利于F 转化为G
(2)①BDE (6)C
(3)80%; B
(7)25 ;
16.
(1)三颈烧瓶
(3)①平衡气压 ②锥形瓶内油层不再增多
(4)降低苯胺在水中的溶解度
(5)①CH₃COOH+NaOH=CH₃COONa+H₂O
②先用水冷凝管是为了冷凝乙醚,后换为空气冷凝管是因为苯胺沸点高,防止冷凝管炸裂
(6)74.9
17.
(1)①+49.4 ②吸收CO₂, 反应放热,促进反应正向移动,提高氢气的产率
(2)①CH₂(OH)₂ ②空气中灼烧,使C转化为CO₂
(3)20% ;