文档内容
湖北省部分高中协作体2025—2026学年上学期9月联考
高三化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并
将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在试卷、草稿
纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符合题意。
1.“乌铜走银”是我国传统铜制工艺品。它以铜为胎,在胎上雕刻各种花纹图案,然
后将熔化的银水填入花纹图案中,冷却后打磨光滑处理,时间久了底铜自然变为乌黑,透
出银纹图案,呈现出黑白分明的装饰效果,古香古色,典雅别致。下列叙述正确的是(
)
A.“乌铜走银”发生的是物理变化
B.铜和银在任何条件下都不能形成原电池
C.铜表面变黑是由于生成了Cu (OH) CO
2 2 3
D.铜和银在元素周期表中均位于长周期
2.氯化铁是一种重要的盐,下列说法不正确的是( )
A.氯化铁属于弱电解质
B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得
D.氯化铁溶液可制备氢氧化铁胶体
3.磷有多种同素异形体,其中白磷和黑磷(每一个层由曲折的磷原子链组成)的结构如
图所示,设N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.3.1 g 31P中含有的中子数为1.6N
AB.31 g白磷与31 g黑磷中含有的P—P键数目均为1.5N
A
C.12.4 g白磷与0.6 mol H 在密闭容器中充分反应,生成的PH 分子数为0.4N
2 3 A
D.6.82 g白磷发生反应:11P +60CuSO +96HO===20Cu P+24HPO +60HSO ,
4 4 2 3 3 4 2 4
转移的电子数为0.6N
A
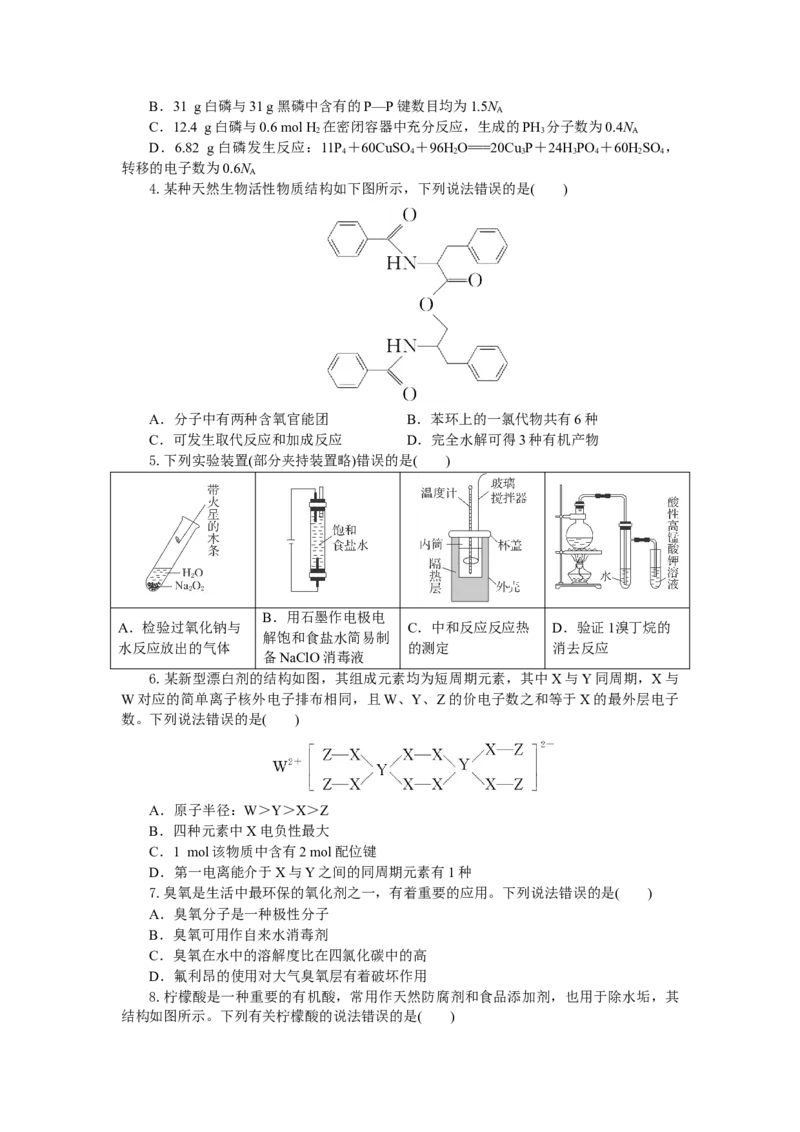
4.某种天然生物活性物质结构如下图所示,下列说法错误的是( )
A.分子中有两种含氧官能团 B.苯环上的一氯代物共有6种
C.可发生取代反应和加成反应 D.完全水解可得3种有机产物
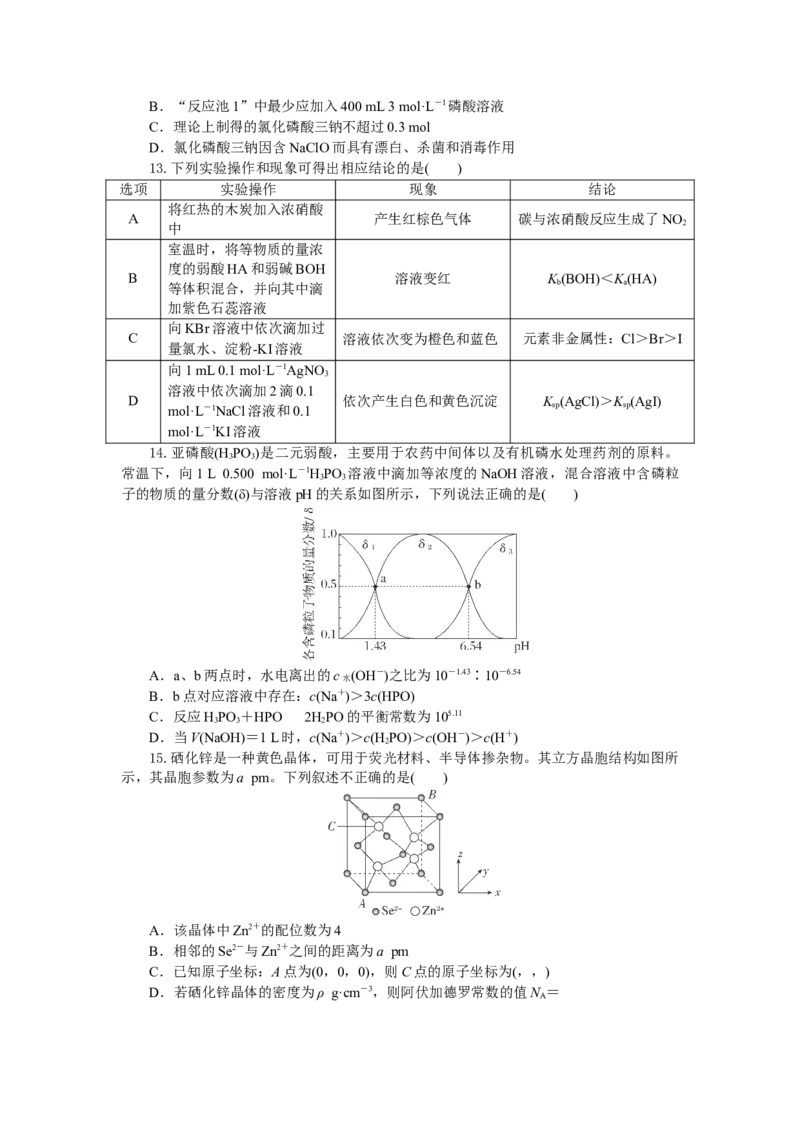
5.下列实验装置(部分夹持装置略)错误的是( )
B.用石墨作电极电
A.检验过氧化钠与 C.中和反应反应热 D.验证1溴丁烷的
解饱和食盐水简易制
水反应放出的气体 的测定 消去反应
备NaClO消毒液
6.某新型漂白剂的结构如图,其组成元素均为短周期元素,其中X与Y同周期,X与
W对应的简单离子核外电子排布相同,且W、Y、Z的价电子数之和等于X的最外层电子
数。下列说法错误的是( )
A.原子半径:W>Y>X>Z
B.四种元素中X电负性最大
C.1 mol该物质中含有2 mol配位键
D.第一电离能介于X与Y之间的同周期元素有1种
7.臭氧是生活中最环保的氧化剂之一,有着重要的应用。下列说法错误的是( )
A.臭氧分子是一种极性分子
B.臭氧可用作自来水消毒剂
C.臭氧在水中的溶解度比在四氯化碳中的高
D.氟利昂的使用对大气臭氧层有着破坏作用
8.柠檬酸是一种重要的有机酸,常用作天然防腐剂和食品添加剂,也用于除水垢,其
结构如图所示。下列有关柠檬酸的说法错误的是( )A.酸性强于碳酸
B.元素电负性:O>C>H
C.1 mol柠檬酸可与3 mol NaOH反应
D.分子中碳原子均为sp2杂化
9.研究表明,结构中含有N、N的含氮含能材料如Pb(N ) 、NAsF均可以用于炸药。
3 2
下列说法正确的是( )
A.Pb属于副族元素
B.N的空间结构为直线形
C.基态As原子核外最高能级电子云形状为球形
D.基态F原子中,电子运动状态有7种
10.科学家设计了一种以镍基普鲁士蓝为电极材料的“热再生电化学循环”转化电池
(如图所示),用于收集废热,提高能源利用率。该电池以KCl溶液和Ni(NO ) 溶液作电解
3 2
质溶液,电极之间用多孔隔膜分隔,工作时发生反应:
KNi[Fe(CN) ]+AgClKNi[Fe(CN) ]+K++Ag+Cl-。下列说法不正确的是( )
2 6 6
A.低温工作时,K+通过多孔隔膜移向Ag电极
B.收集废热时,阳极发生的反应为KNi[Fe(CN) ]-e-===KNi[Fe(CN) ]+ K+
2 6 6
C.收集废热时,阴极上附着的AgCl减少
D.低温工作时,Ag电极增重7.1 g,理论上外电路转移电子0.2 mol
11.NF 与汞共热得到NF 和一种汞盐,下列有关说法错误的是( )
3 2 2
A.NF 的空间构型为三角锥形
3
B.NF 的结构式为F-N===N-F
2 2
C.NF 沸点一定高于NH
3 3
D.NF 分子存在顺反异构
2 2
12.氯化磷酸三钠[(Na PO ·12H O)·NaClO]具有良好的灭菌、消毒、漂白作用,亦能除
3 4 2 4
去墨迹、血迹、油迹和茶迹等多种污垢,广泛地用于医院、餐馆、食品加工行业。氯化磷
酸三钠的熔点为67 ℃,常温下较稳定,受热易分解。在水溶液中可直接与钙、镁及重金
属离子形成不溶性磷酸盐。某小组设计如图流程制备氯化磷酸三钠。下列叙述错误的是(
)
A.“系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤和高温烘干B.“反应池1”中最少应加入400 mL 3 mol·L-1磷酸溶液
C.理论上制得的氯化磷酸三钠不超过0.3 mol
D.氯化磷酸三钠因含NaClO而具有漂白、杀菌和消毒作用
13.下列实验操作和现象可得出相应结论的是( )
选项 实验操作 现象 结论
将红热的木炭加入浓硝酸
A 产生红棕色气体 碳与浓硝酸反应生成了NO
中 2
室温时,将等物质的量浓
度的弱酸HA和弱碱BOH
B 溶液变红 K (BOH)<K(HA)
等体积混合,并向其中滴 b a
加紫色石蕊溶液
向KBr溶液中依次滴加过
C 溶液依次变为橙色和蓝色 元素非金属性:Cl>Br>I
量氯水、淀粉-KI溶液
向1 mL 0.1 mol·L-1AgNO
3
溶液中依次滴加2滴0.1
D 依次产生白色和黄色沉淀 K (AgCl)>K (AgI)
mol·L-1NaCl溶液和0.1 sp sp
mol·L-1KI溶液
14.亚磷酸(H PO )是二元弱酸,主要用于农药中间体以及有机磷水处理药剂的原料。
3 3
常温下,向1 L 0.500 mol·L-1HPO 溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒
3 3
子的物质的量分数(δ)与溶液pH的关系如图所示,下列说法正确的是( )
A.a、b两点时,水电离出的c (OH-)之比为10-1.43∶10-6.54
水
B.b点对应溶液中存在:c(Na+)>3c(HPO)
C.反应HPO +HPO2HPO的平衡常数为105.11
3 3 2
D.当V(NaOH)=1 L时,c(Na+)>c(H PO)>c(OH-)>c(H+)
2
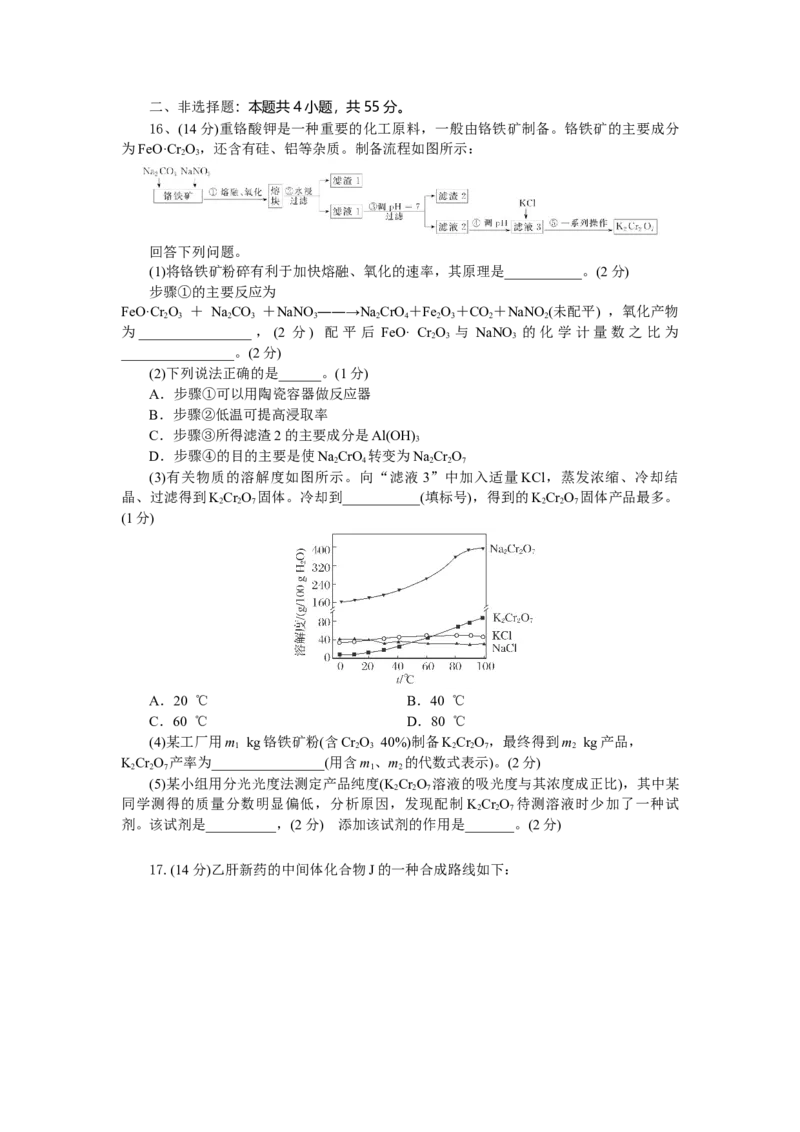
15.硒化锌是一种黄色晶体,可用于荧光材料、半导体掺杂物。其立方晶胞结构如图所
示,其晶胞参数为a pm。下列叙述不正确的是( )
A.该晶体中Zn2+的配位数为4
B.相邻的Se2-与Zn2+之间的距离为a pm
C.已知原子坐标:A点为(0,0,0),则C点的原子坐标为(,,)
D.若硒化锌晶体的密度为ρ g·cm-3,则阿伏加德罗常数的值N =
A二、非选择题:本题共4小题,共55分。
16、(14分)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分
为FeO·Cr O,还含有硅、铝等杂质。制备流程如图所示:
2 3
回答下列问题。
(1)将铬铁矿粉碎有利于加快熔融、氧化的速率,其原理是___________。(2分)
步骤①的主要反应为
FeO·Cr O + NaCO +NaNO ――→NaCrO +Fe O +CO +NaNO (未配平) ,氧化产物
2 3 2 3 3 2 4 2 3 2 2
为________________,(2 分) 配平后 FeO· Cr O 与 NaNO 的化学计量数之比为
2 3 3
________________。(2分)
(2)下列说法正确的是______。(1分)
A.步骤①可以用陶瓷容器做反应器
B.步骤②低温可提高浸取率
C.步骤③所得滤渣2的主要成分是Al(OH)
3
D.步骤④的目的主要是使NaCrO 转变为NaCr O
2 4 2 2 7
(3)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩、冷却结
晶、过滤得到KCr O 固体。冷却到___________(填标号),得到的KCr O 固体产品最多。
2 2 7 2 2 7
(1分)
A.20 ℃ B.40 ℃
C.60 ℃ D.80 ℃
(4)某工厂用m kg铬铁矿粉(含Cr O 40%)制备KCr O,最终得到m kg产品,
1 2 3 2 2 7 2
KCr O 产率为________________(用含m、m 的代数式表示)。(2分)
2 2 7 1 2
(5)某小组用分光光度法测定产品纯度(K Cr O 溶液的吸光度与其浓度成正比),其中某
2 2 7
同学测得的质量分数明显偏低,分析原因,发现配制KCr O 待测溶液时少加了一种试
2 2 7
剂。该试剂是__________,(2分) 添加该试剂的作用是_______。(2分)
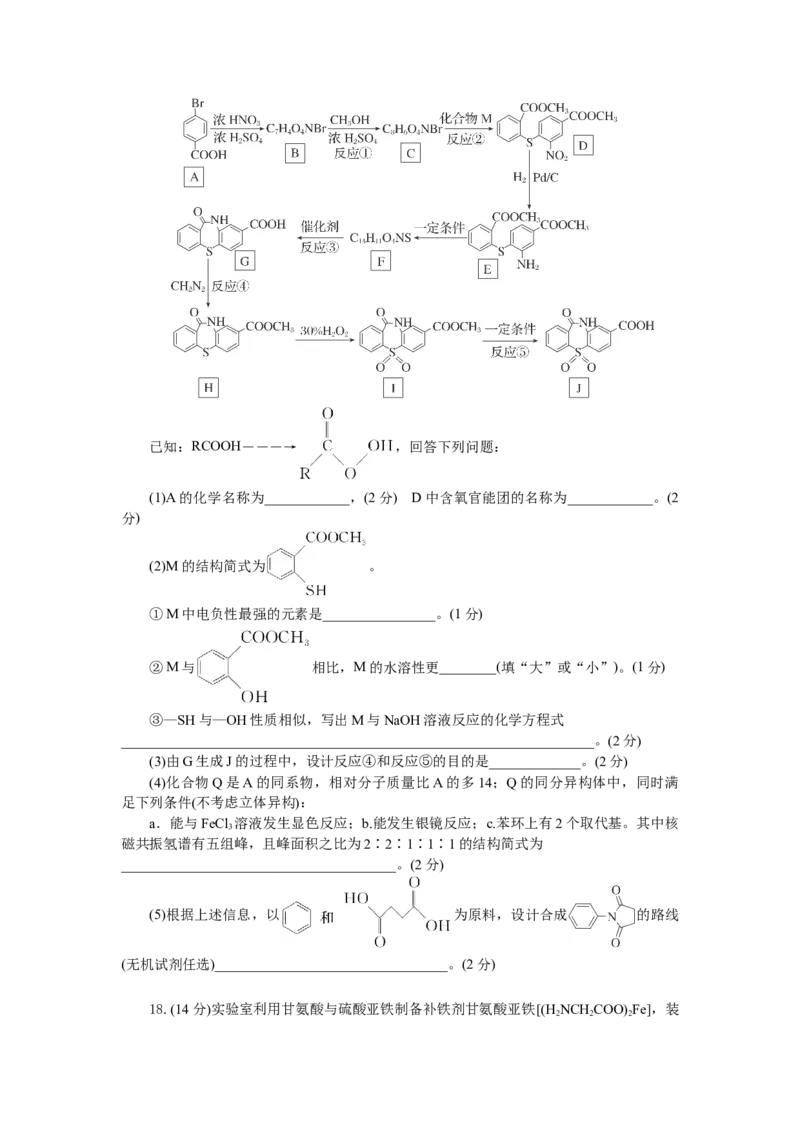
17.(14分)乙肝新药的中间体化合物J的一种合成路线如下:已知:RCOOH―――→ ,回答下列问题:
(1)A的化学名称为____________,(2分) D中含氧官能团的名称为____________。(2
分)
(2)M的结构简式为 。
①M中电负性最强的元素是________________。(1分)
②M与 相比,M的水溶性更________(填“大”或“小”)。(1分)
③—SH与—OH性质相似,写出M与NaOH溶液反应的化学方程式
___________________________________________________________________。(2分)
(3)由G生成J的过程中,设计反应④和反应⑤的目的是_____________。(2分)
(4)化合物Q是A的同系物,相对分子质量比A的多14;Q的同分异构体中,同时满
足下列条件(不考虑立体异构):
a.能与FeCl 溶液发生显色反应;b.能发生银镜反应;c.苯环上有2个取代基。其中核
3
磁共振氢谱有五组峰,且峰面积之比为2∶2∶1∶1∶1的结构简式为
_______________________________________。(2分)
(5)根据上述信息,以 为原料,设计合成 的路线
(无机试剂任选)_________________________________。(2分)
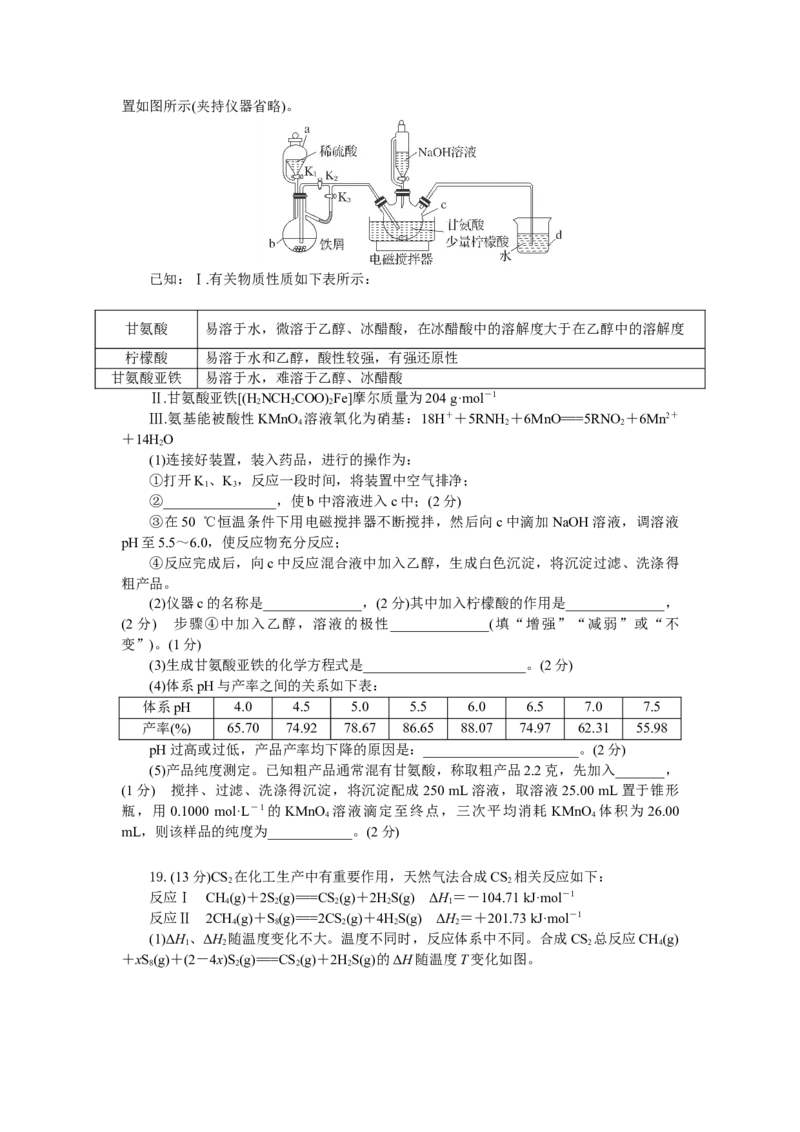
18.(14分)实验室利用甘氨酸与硫酸亚铁制备补铁剂甘氨酸亚铁[(H NCH COO)Fe],装
2 2 2置如图所示(夹持仪器省略)。
已知:Ⅰ.有关物质性质如下表所示:
甘氨酸 易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中的溶解度大于在乙醇中的溶解度
柠檬酸 易溶于水和乙醇,酸性较强,有强还原性
甘氨酸亚铁 易溶于水,难溶于乙醇、冰醋酸
Ⅱ.甘氨酸亚铁[(H NCH COO)Fe]摩尔质量为204 g·mol-1
2 2 2
Ⅲ.氨基能被酸性KMnO 溶液氧化为硝基:18H++5RNH +6MnO===5RNO +6Mn2+
4 2 2
+14HO
2
(1)连接好装置,装入药品,进行的操作为:
①打开K、K,反应一段时间,将装置中空气排净;
1 3
②________________,使b中溶液进入c中;(2分)
③在50 ℃恒温条件下用电磁搅拌器不断搅拌,然后向c中滴加NaOH溶液,调溶液
pH至5.5~6.0,使反应物充分反应;
④反应完成后,向c中反应混合液中加入乙醇,生成白色沉淀,将沉淀过滤、洗涤得
粗产品。
(2)仪器c的名称是______________,(2分)其中加入柠檬酸的作用是______________,
(2 分) 步骤④中加入乙醇,溶液的极性______________(填“增强”“减弱”或“不
变”)。(1分)
(3)生成甘氨酸亚铁的化学方程式是_______________________。(2分)
(4)体系pH与产率之间的关系如下表:
体系pH 4.0 4.5 5.0 5.5 6.0 6.5 7.0 7.5
产率(%) 65.70 74.92 78.67 86.65 88.07 74.97 62.31 55.98
pH过高或过低,产品产率均下降的原因是:______________________。(2分)
(5)产品纯度测定。已知粗产品通常混有甘氨酸,称取粗产品2.2克,先加入_______,
(1分) 搅拌、过滤、洗涤得沉淀,将沉淀配成250 mL溶液,取溶液25.00 mL置于锥形
瓶,用 0.1000 mol·L-1的 KMnO 溶液滴定至终点,三次平均消耗 KMnO 体积为 26.00
4 4
mL,则该样品的纯度为____________。(2分)
19.(13分)CS 在化工生产中有重要作用,天然气法合成CS 相关反应如下:
2 2
反应Ⅰ CH(g)+2S(g)===CS (g)+2HS(g) ΔH=-104.71 kJ·mol-1
4 2 2 2 1
反应Ⅱ 2CH(g)+S(g)===2CS (g)+4HS(g) ΔH=+201.73 kJ·mol-1
4 8 2 2 2
(1)ΔH、ΔH 随温度变化不大。温度不同时,反应体系中不同。合成CS 总反应CH(g)
1 2 2 4
+xS(g)+(2-4x)S (g)===CS (g)+2HS(g)的ΔH随温度T变化如图。
8 2 2 2①S(g)===4S (g) ΔH=__________kJ·mol-1。(2分)
8 2
②为提高 CH 平衡转化率,控制温度范围在__________(填标号),(1 分)理由是
4
______________________________________________________________。(2分)
A.400~450 ℃ B.650~700 ℃
C.750~800 ℃ D.800 ℃以上
(2)合成CS 总反应中硫蒸气达到饱和时,反应时间t与CH 初始浓度c 和CH 转化率α
2 4 0 4
满足关系t=(),式中k为速率常数。
①T ℃、c =1.0 mol·L-1时,测得t=9.5 s、α=95%,则k=________________ L·mol
0
-1·s-1。(1分)
②T ℃时,计划在5 s内转化率达90%,应控制初始浓度c 大于__________L·mol-1。
0
(1分)
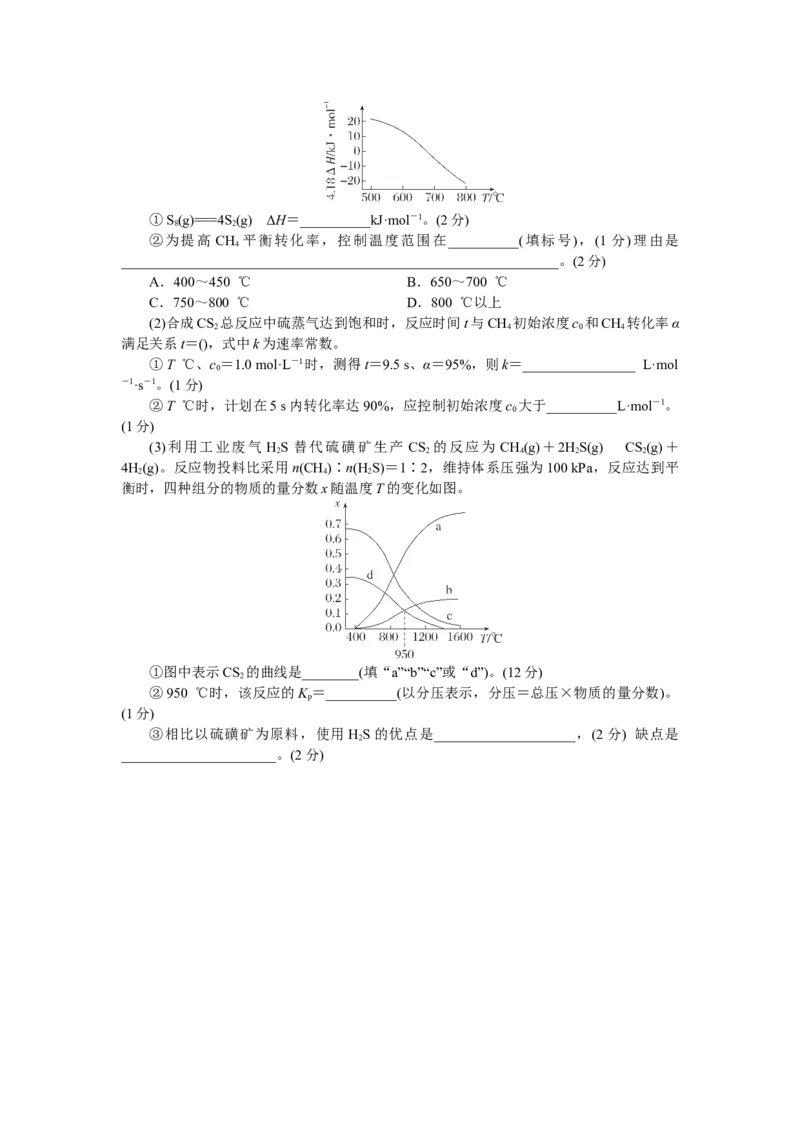
(3)利用工业废气 HS 替代硫磺矿生产 CS 的反应为 CH(g)+2HS(g)CS(g)+
2 2 4 2 2
4H(g)。反应物投料比采用n(CH)∶n(H S)=1∶2,维持体系压强为100 kPa,反应达到平
2 4 2
衡时,四种组分的物质的量分数x随温度T的变化如图。
①图中表示CS 的曲线是________(填“a”“b”“c”或“d”)。(12分)
2
②950 ℃时,该反应的K =__________(以分压表示,分压=总压×物质的量分数)。
p
(1分)
③相比以硫磺矿为原料,使用HS的优点是____________________,(2分) 缺点是
2
______________________。(2分)