文档内容
专题17 氧化还原反应相关计算
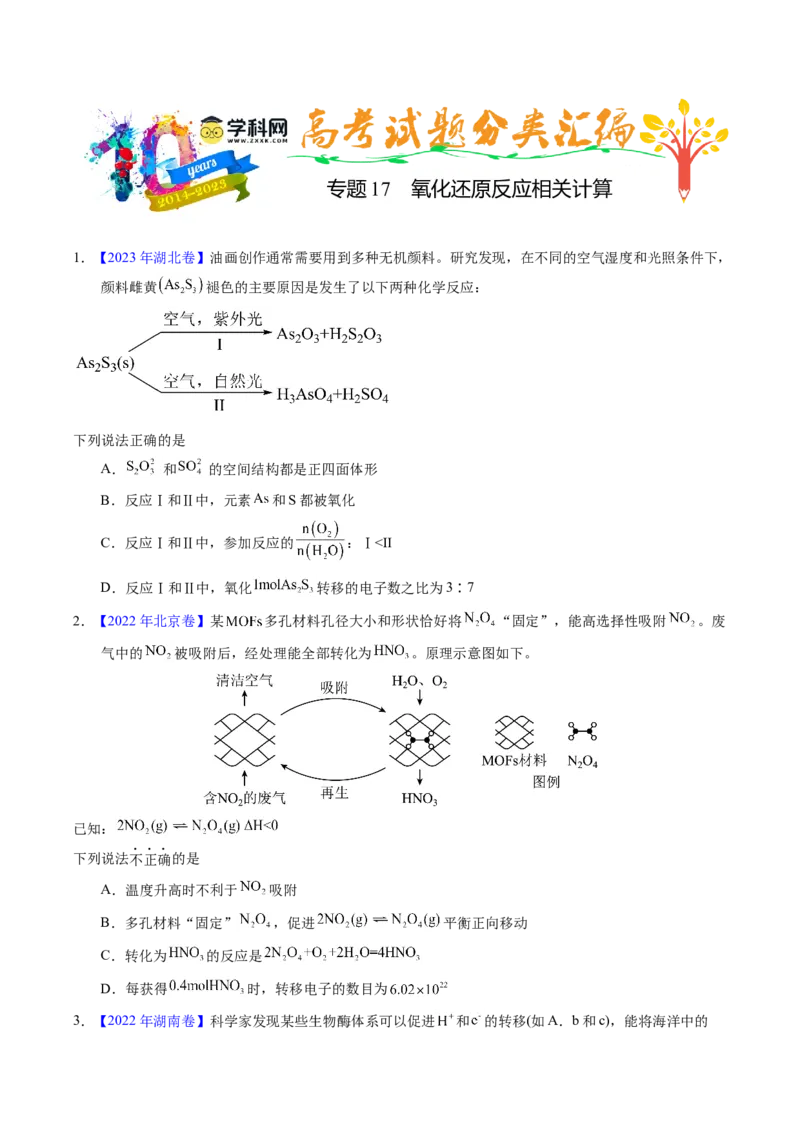
1.【2023年湖北卷】油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,
颜料雌黄 褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A. 和 的空间结构都是正四面体形
B.反应Ⅰ和Ⅱ中,元素 和S都被氧化
C.反应Ⅰ和Ⅱ中,参加反应的 :Ⅰ<Ⅱ
D.反应Ⅰ和Ⅱ中,氧化 转移的电子数之比为3∶7
2.【2022年北京卷】某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附 。废
气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
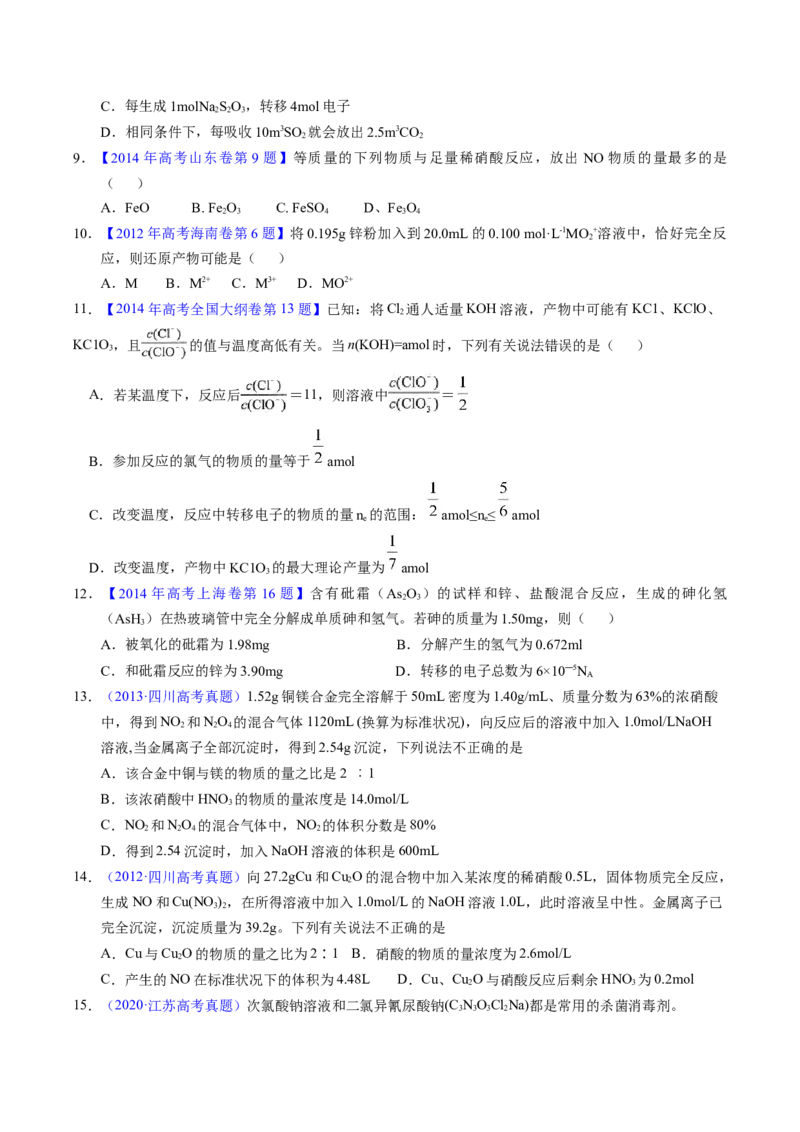
3.【2022年湖南卷】科学家发现某些生物酶体系可以促进 和 的转移(如A.b和c),能将海洋中的转化为 进入大气层,反应过程如图所示。
下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
4.(2016·浙江高考真题)已知氧化性 ,向含溶质 的 溶液中通入 ,充分反
应.下列说法不正确的是
A.离子的还原性强弱:
B.当 时,发生的离子反应:
C.当 时,反应后的离子浓度: ∶ ∶ ∶2∶2
D.当 时,发生的离子反应:
5.(2017·海南高考真题)在酸性条件下,可发生如下反应: +2M3++4H O= +Cl-+8H+,
2
中M的化合价是 ( )
A.+4 B.+5 C.+6 D.+7
6.(2016·上海高考真题)某铁的氧化物(Fe O)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下
x
112mlCl ,恰好将Fe2+完全氧化。x值为( )
2
A.0.80 B.0.85 C.0.90 D.0.93
7.(2014·山东高考真题)等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是
A.FeO B.Fe O C.FeSO D.Fe O
2 3 4 3 4
8、【2015上海化学】工业上将NaCO 和NaS以1:2的物质的量之比配成溶液,再通入SO ,可制取
2 3 2 2
NaSO,同时放出CO。在该反应中( )
2 2 3 2
A.硫元素既被氧化又被还原
B.氧化剂与还原剂的物质的量之比为1:2C.每生成1molNa SO,转移4mol电子
2 2 3
D.相同条件下,每吸收10m3SO 就会放出2.5m3CO
2 2
9.【2014年高考山东卷第9题】等质量的下列物质与足量稀硝酸反应,放出 NO物质的量最多的是
( )
A.FeO B. Fe O C. FeSO D、Fe O
2 3 4 3 4
10.【2012年高考海南卷第6题】将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO +溶液中,恰好完全反
2
应,则还原产物可能是( )
A.M B.M2+ C.M3+ D.MO2+
11.【2014年高考全国大纲卷第13题】已知:将Cl 通人适量KOH溶液,产物中可能有KC1、KClO、
2
KC1O ,且 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
3
A.若某温度下,反应后 =11,则溶液中 =
B.参加反应的氯气的物质的量等于 amol
C.改变温度,反应中转移电子的物质的量n 的范围: amol≤n≤ amol
e e
D.改变温度,产物中KC1O 的最大理论产量为 amol
3
12.【2014年高考上海卷第 16题】含有砒霜(As O )的试样和锌、盐酸混合反应,生成的砷化氢
2 3
(AsH )在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50mg,则( )
3
A.被氧化的砒霜为1.98mg B.分解产生的氢气为0.672ml
C.和砒霜反应的锌为3.90mg D.转移的电子总数为6×10―5N
A
13.(2013·四川高考真题)1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸
中,得到NO 和NO 的混合气体1120mL (换算为标准状况),向反应后的溶液中加入1.0mol/LNaOH
2 2 4
溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO 的物质的量浓度是14.0mol/L
3
C.NO 和NO 的混合气体中,NO 的体积分数是80%
2 2 4 2
D.得到2.54沉淀时,加入NaOH溶液的体积是600mL
14.(2012·四川高考真题)向27.2gCu和Cu O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,
2
生成NO和Cu(NO ),在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已
3 2
完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A.Cu与Cu O的物质的量之比为2∶1 B.硝酸的物质的量浓度为2.6mol/L
2
C.产生的NO在标准状况下的体积为4.48L D.Cu、Cu O与硝酸反应后剩余HNO 为0.2mol
2 3
15.(2020·江苏高考真题)次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。
3 3 3 2NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为
2
__________;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,
将会导致消毒作用减弱,其原因是__________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质
品标准。实验检测原理为
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸
和过量KI溶液,密封在暗处静置5min;用 NaSO 标准溶液滴定至溶液呈微黄色,加
2 2 3
入淀粉指示剂继续滴定至终点,消耗NaSO 溶液20.00mL。
2 2 3
①通过计算判断该样品是否为优质品_______。(写出计算过程,
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________(填“偏高”或“偏低”)。
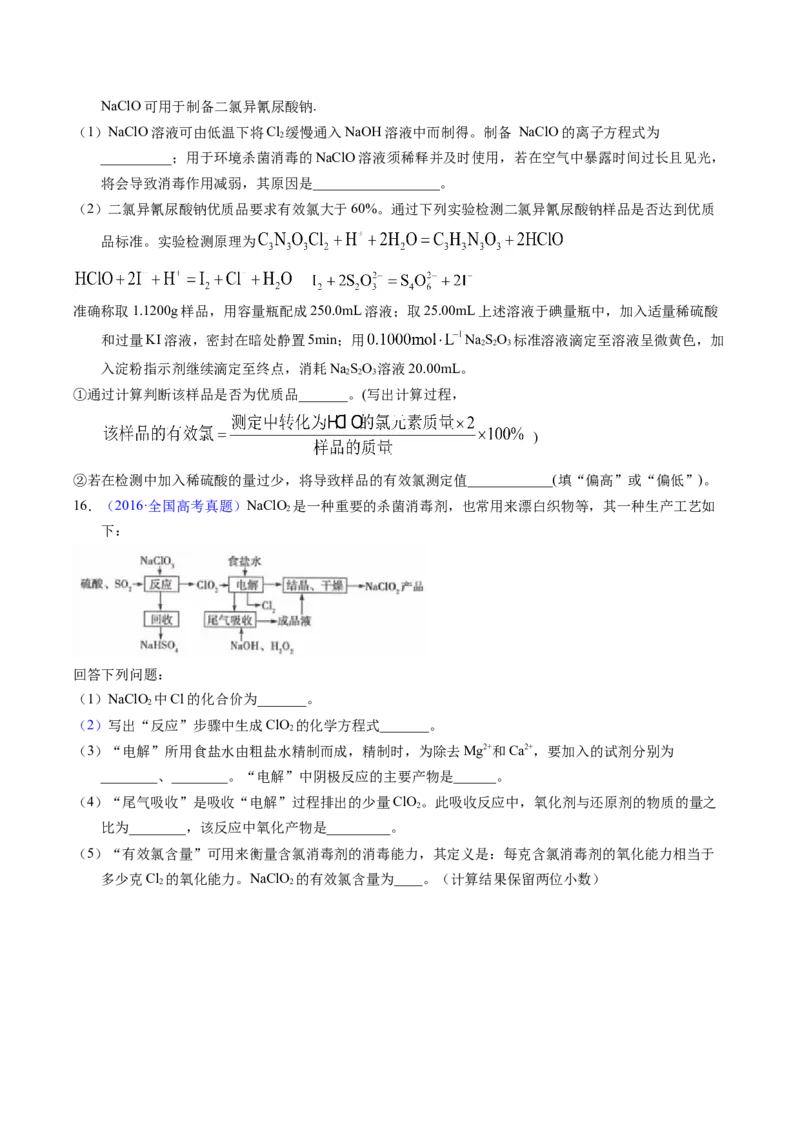
16.(2016·全国高考真题)NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如
2
下:
回答下列问题:
(1)NaClO 中Cl的化合价为_______。
2
(2)写出“反应”步骤中生成ClO 的化学方程式_______。
2
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为
________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO 。此吸收反应中,氧化剂与还原剂的物质的量之
2
比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于
多少克Cl 的氧化能力。NaClO 的有效氯含量为____。(计算结果保留两位小数)
2 2