文档内容
高三开学考化学试题
可能用到的相对原子质量:H:1 C:12 N:14 O:16 F:19 S:32 Cl:35.5 Ca:40 P:
31 I:127 Na:23 Fe:56 Cu:64 K:39 Mn:55 Cr:52 Co:59
第Ⅰ卷 选择题部分
一、每小题只有一个选项正确,每小题3分,共54分。
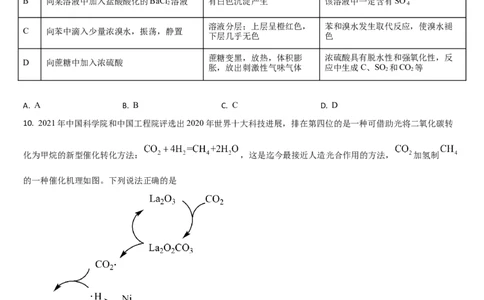
1. 2022年春晚,舞蹈节目《只此青绿》惊艳众人,再度将深藏博物馆的艺术史名作《千里江山图》推向了全民关注
的文化热点中心。下列关于成画工序涉及化学知识的描述错误的是
选项 成画工序 化学知识
A 以绢为画布 蚕丝是绢的主要成分,属于蛋白质
B 以水墨描底,画出粉本 炭黑是墨的主要成分,炭黑和石墨互为同素异形体
C 以孔雀石上绿色 碱式碳酸铜是孔雀石的主要成分,常温易分解
D 以赭石 ( )上红色 性质稳定不易被空气氧化
A. A B. B C. C D. D
2. 正确使用化学用语是学习化学必需的基本技能。下列化学用语表达正确的是
A. 中子数为8的碳核素:
B. 过氧化氢的电子式:
C. 葡萄糖的分子式:
D. 聚丙烯的键线式
3. 下列物质性质与用途具有对应关系的是
A. 浓硫酸具有脱水性,可用于干燥 、 气体
B. 密度比空气大,可用作镁着火时的灭火剂
C. 溶液能与Cu反应,可用作铜制线路板的蚀刻剂
D. 易溶于水,可用作木材防火剂
学科网(北京)股份有限公司4. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 在标准状况下, 分子中含氯原子数目为
B. 1LpH均为2的硫酸和醋酸溶液,氢离子数均为
为
C. 64g铜与足量硫粉加热充分反应,转移电子数
D. 30g由乙酸和葡萄糖组成的混合物中含氢原子个数为
5. 常温下,下列各组离子在指定溶液中不能大量共存的是
A. 透明澄清的溶液中: 、 、 、
B. 氨水溶液中: 、 、 、
的
C. 溶液中: 、 , 、
D. 无色溶液中: 、 、 、
6. 下列根据反应原理设计的应用,不正确的是
A. CO +H O HCO +OH- 热的纯碱溶液清洗油污
2
⇌
B. Al3++3H O Al(OH) (胶体)+3H+ 明矾净水
2 3
C. TiCl
4
+(x+2⇌)H
2
O(过量)=TiO
2
·xH
2
O↓+4HCl 用TiCl
4
制备TiO
2
D. SnCl +H O Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入NaOH固体
2 2
7. 设N
A
为阿伏⇌加德罗常数的值。下列叙述正确的是
A. 标准状况下,2.24 L 二氯甲烷中含有的碳氯共价键数目为0.2N
A
B. 50 mL 12 mol/L盐酸与足量MnO 加热反应,转移的电子数目为0.3N
2 A
C. 向含0.1 molNH Al(SO ) 的溶液中滴加NaOH溶液至沉淀恰好完全溶解,消耗OH-数目为0.5N
4 4 2 A
D. 电解精炼铜时,若阴极得电子数为2N ,则阳极质量减少64克
A
8. W、X、Y、Z为原子序数依次减小的短周期主族元素,且只有X、Y位于同一周期。这四种元素形成的某种化合物
的结构如图所示。下列叙述错误的是
A. 简单离子半径:X>W
学科网(北京)股份有限公司B. 简单气态氢化物的稳定性:X>Y
C. Y的氟化物所有原子最外层均达到8电子稳定结构
D. 该物质具有强氧化性,可能用于漂白
9. 下列对实验现象的解释与结论正确的是
选
实验操作 实验现象 解释与结论
项
向浓度均为0.1 mol·L-1NaS和NaI混合溶
A 2 出现黑色沉淀 K ( (AgI)<K (Ag S)
液中滴加少量AgNO 溶液 sp sp 2
3
B 向某溶液中加入盐酸酸化的BaCl 溶液 有白色沉淀产生 该溶液中一定含有SO
2
溶液分层;上层呈橙红色, 苯和溴水发生取代反应,使溴水褪
C 向苯中滴入少量浓溴水,振荡,静置
下层几乎无色 色
蔗糖变黑,放热,体积膨 浓硫酸具有脱水性和强氧化性,反
D 向蔗糖中加入浓硫酸
胀,放出刺激性气味气体 应中生成C、SO 和CO 等
2 2
A. A B. B C. C D. D
10. 2021年中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转
化为甲烷的新型催化转化方法: ,这是迄今最接近人造光合作用的方法, 加氢制
的一种催化机理如图。下列说法正确的是
A. 反应中 是中间产物
B. 转化为 利用了 的氧化性
C. 经过 活性中心裂解产生带负电荷的H
D. 使用催化剂可以降低反应的焓变,从而提高化学反应速率
学科网(北京)股份有限公司11.下列物质的转化在给定条件下能实现的是( )
A.H SO (稀) SO NH HSO (NH ) SO
2 4 2 4 3 4 2 3
B.NH NO NO HNO
3 2 3
C.Fe FeCl Fe(OH) Fe(OH)
2 2 3
D.Al NaAlO AlCl 溶液 无水AlCl
2 3 3
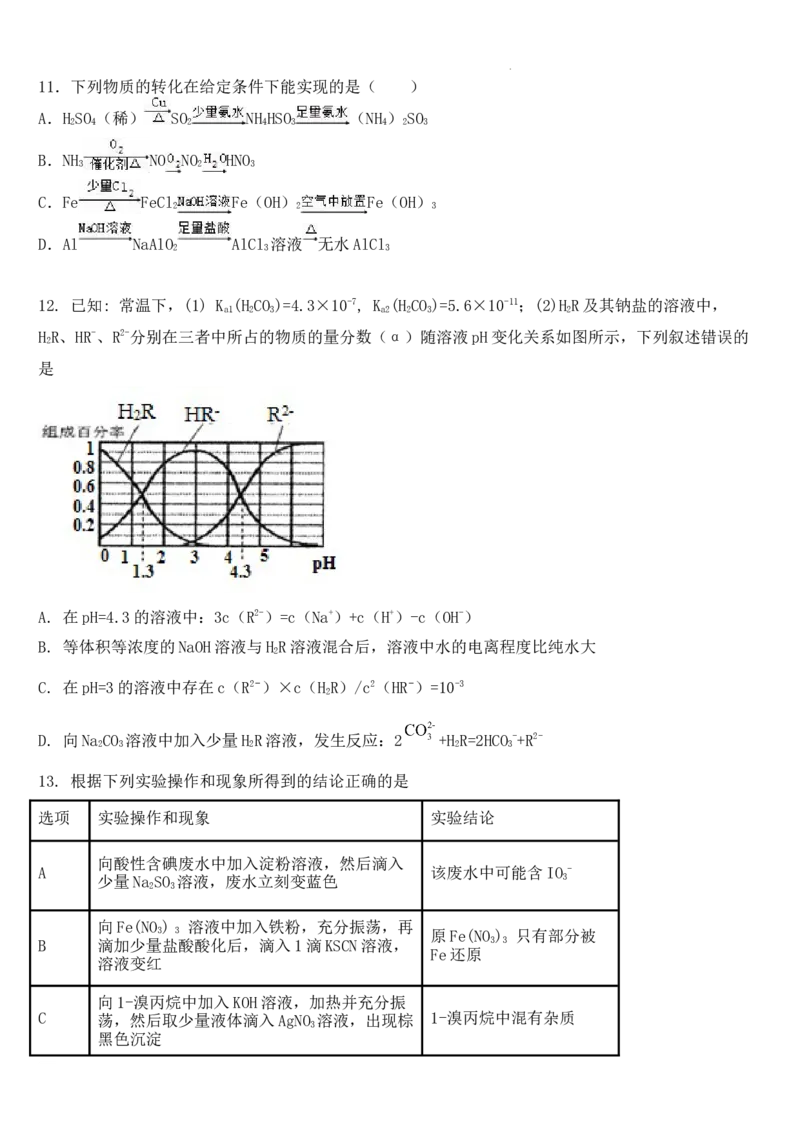
12. 已知: 常温下,(1) K (H CO )=4.3×10-7, K (H CO )=5.6×10-11;(2)H R及其钠盐的溶液中,
a1 2 3 a2 2 3 2
H R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的
2
是
A. 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)
B. 等体积等浓度的NaOH溶液与H R溶液混合后,溶液中水的电离程度比纯水大
2
C. 在pH=3的溶液中存在c(R2−)×c(H R)/c2(HR−)=10-3
2
D. 向Na CO 溶液中加入少量H R溶液,发生反应:2 +H R=2HCO -+R2-
2 3 2 2 3
13. 根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 实验结论
向酸性含碘废水中加入淀粉溶液,然后滴入
A 该废水中可能含IO -
少量Na SO 溶液,废水立刻变蓝色 3
2 3
向Fe(NO ) 溶液中加入铁粉,充分振荡,再
3 3 原Fe(NO ) 只有部分被
B 滴加少量盐酸酸化后,滴入1滴KSCN溶液, 3 3
Fe还原
溶液变红
向1-溴丙烷中加入KOH溶液,加热并充分振
C 荡,然后取少量液体滴入AgNO 溶液,出现棕 1-溴丙烷中混有杂质
3
黑色沉淀
学科网(北京)股份有限公司将乙醇与浓硫酸混合溶液加热,产生的气体
D 产生的气体一定是乙烯
直接通入酸性KMnO 溶液,溶液紫色逐渐褪去
4
A. A B. B C. C D. D
14. 根据下列实验,不能证明一元酸HR为弱酸的是( )
A. 室温下,NaR溶液的pH大于7
B. 25℃时,0.01mol/L的HR溶液pH=2.8
C. 加热NaR溶液时,溶液的pH变小
D. HR溶液加入少量NaR固体,溶解后溶液的pH变大
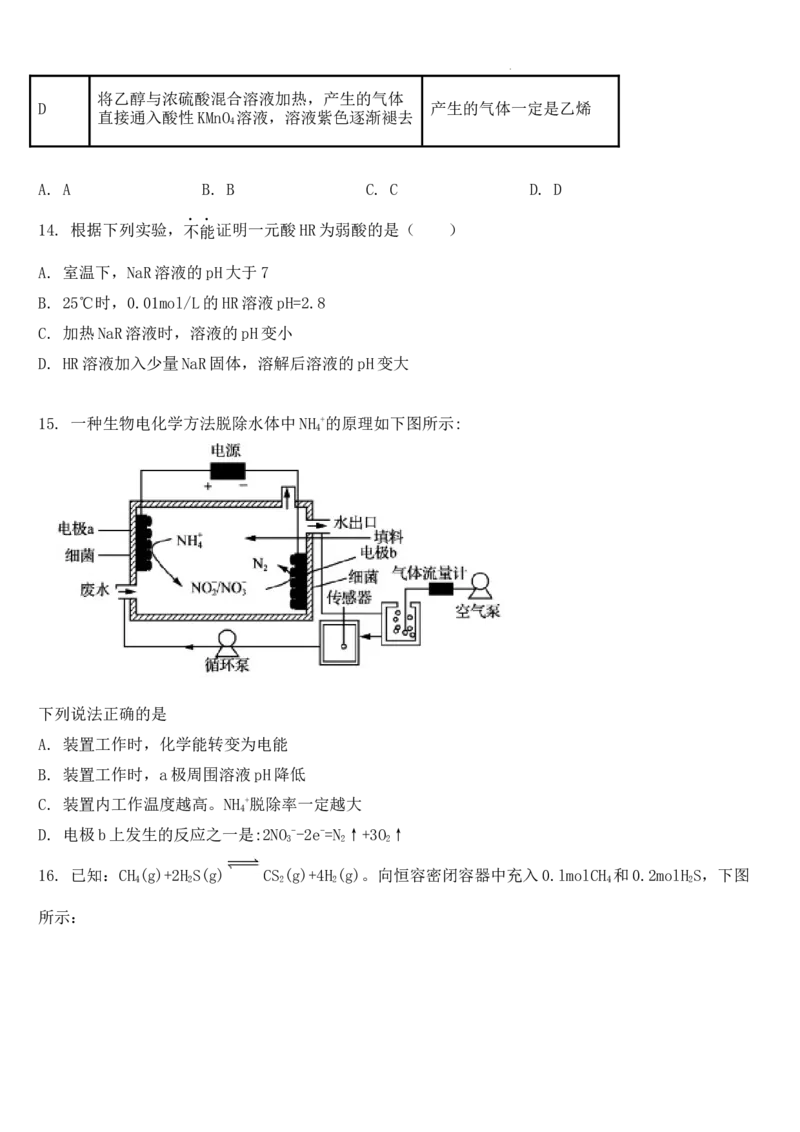
15. 一种生物电化学方法脱除水体中NH +的原理如下图所示:
4
下列说法正确的是
A. 装置工作时,化学能转变为电能
B. 装置工作时,a极周围溶液pH降低
C. 装置内工作温度越高。NH +脱除率一定越大
4
D. 电极b上发生的反应之一是:2NO --2e-=N ↑+3O ↑
3 2 2
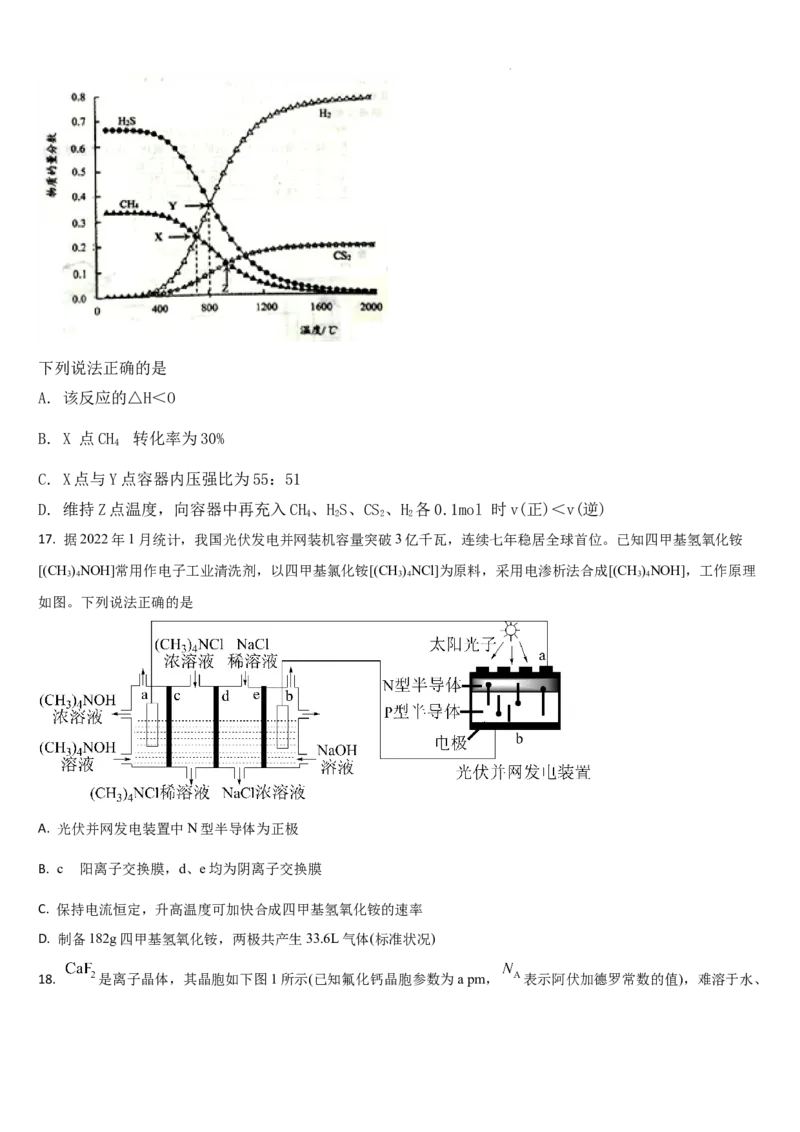
16. 已知:CH (g)+2H S(g) CS (g)+4H (g)。向恒容密闭容器中充入0.lmolCH 和0.2molH S,下图
4 2 2 2 4 2
所示:
学科网(北京)股份有限公司下列说法正确的是
A. 该反应的△H<O
的
B. X 点CH 转化率为30%
4
C. X点与Y点容器内压强比为55:51
D. 维持Z点温度,向容器中再充入CH 、H S、CS 、H 各0.1mol 时v(正)<v(逆)
4 2 2 2
17. 据2022年1月统计,我国光伏发电并网装机容量突破3亿千瓦,连续七年稳居全球首位。已知四甲基氢氧化铵
[(CH )NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成[(CH )NOH],工作原理
3 4 3 4 3 4
如图。下列说法正确的是
A. 光伏并网发电装置中N型半导体为正极
为
B. c 阳离子交换膜,d、e均为阴离子交换膜
C. 保持电流恒定,升高温度可加快合成四甲基氢氧化铵的速率
D. 制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况)
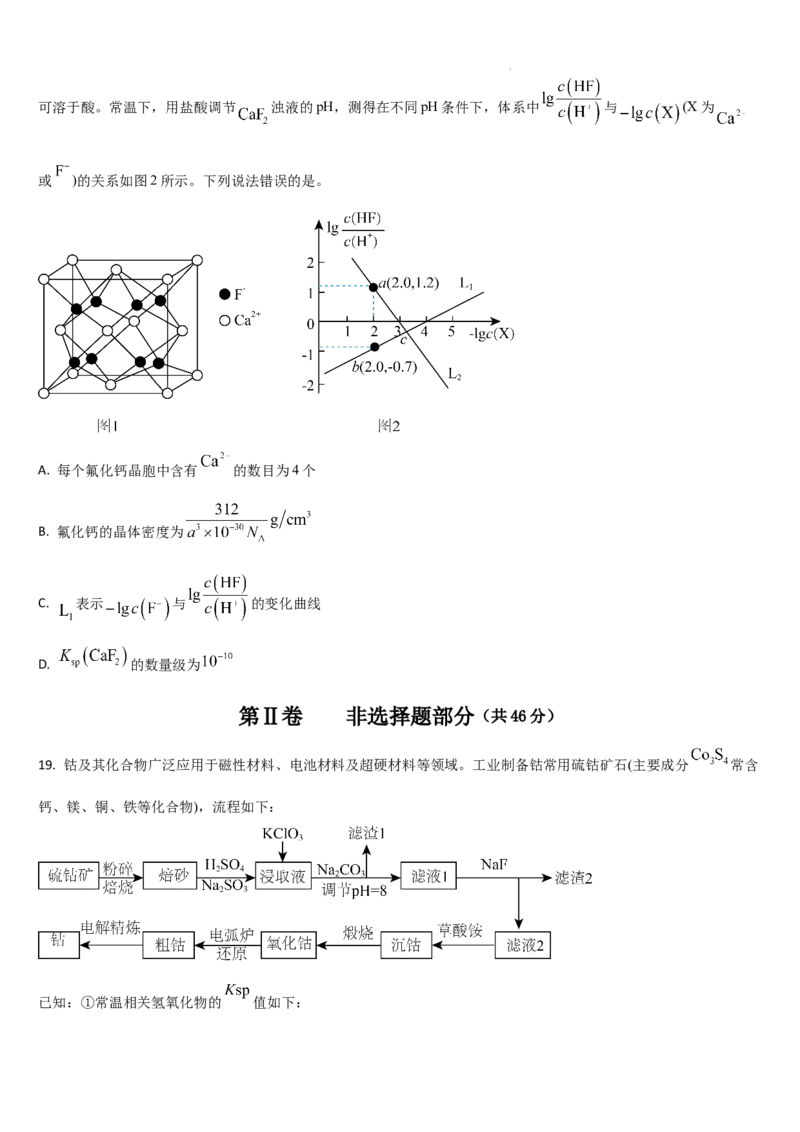
18. 是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm, 表示阿伏加德罗常数的值),难溶于水、
学科网(北京)股份有限公司可溶于酸。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中 与 (X为
或 )的关系如图2所示。下列说法错误的是。
A. 每个氟化钙晶胞中含有 的数目为4个
B. 氟化钙的晶体密度为
C. 表示 与 的变化曲线
D. 的数量级为
第Ⅱ卷 非选择题部分(共46分)
19. 钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。工业制备钴常用硫钴矿石(主要成分 常含
钙、镁、铜、铁等化合物),流程如下:
已知:①常温相关氢氧化物的 值如下:
学科网(北京)股份有限公司物质
②酸性条件下 极难被氧化。
(1)基态钴原子价层电子排布式为_______。
(2)已知钴与铁均为Ⅷ族元素,具有类似的化合价, 中 的化合价_______。
(3)硫酸浸取焙砂的过程中,温度及硫酸的浓度对金属离子浸出的影响如图所示,考虑生产成本和效率,最佳的浸
出温度为_______℃,最佳的硫酸浓度为_______mol/L。
(4)向浸取液中加入 发生的主要反应的离子方程式为_______,滤渣1的主要成分是_______。
(5)电解精炼的过程中,粗钴与电源_______极相连,用硫酸钴溶液作为电解质,控制阴极室 为3~5之间,若
值过低,在纯钴的电极表面产生气体,该气体可能是_______。
A. B. C. D.
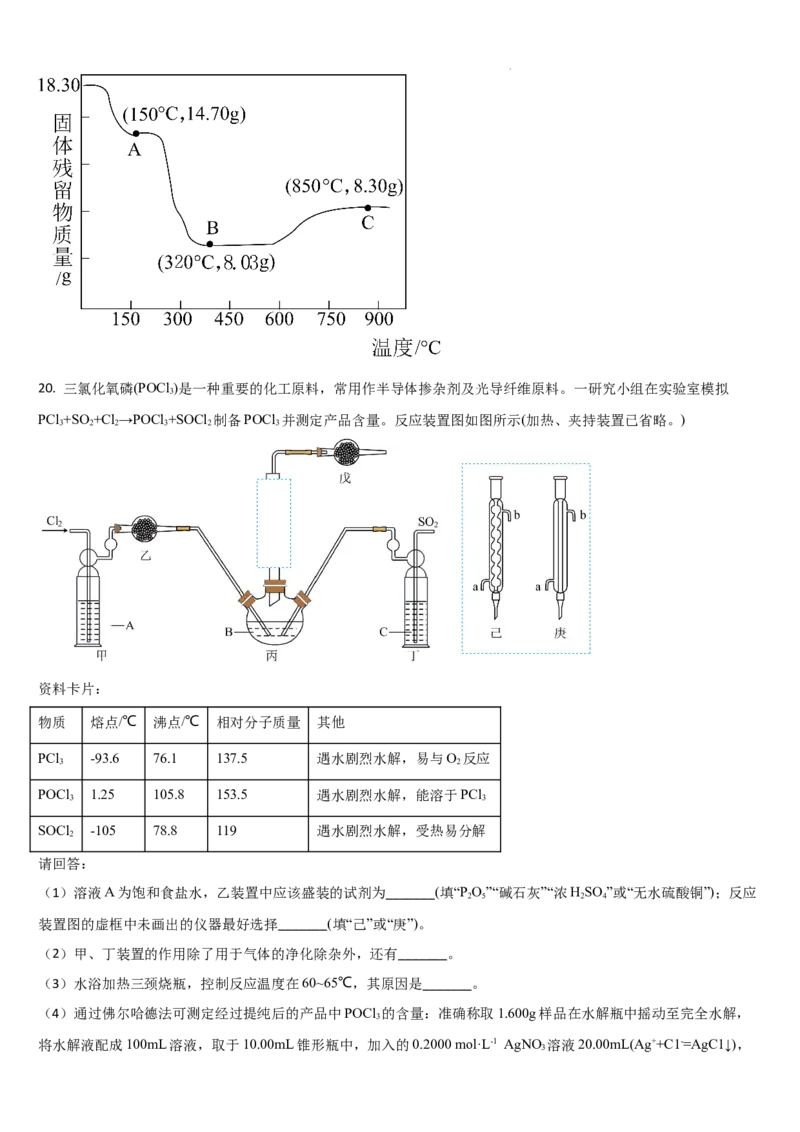
(6)若沉钴中得到二水合草酸钴 ( )热分解质量变化过程如图所示。其中600℃以前是
的
隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,请写出从反应B点到C点 化学方程式_______。
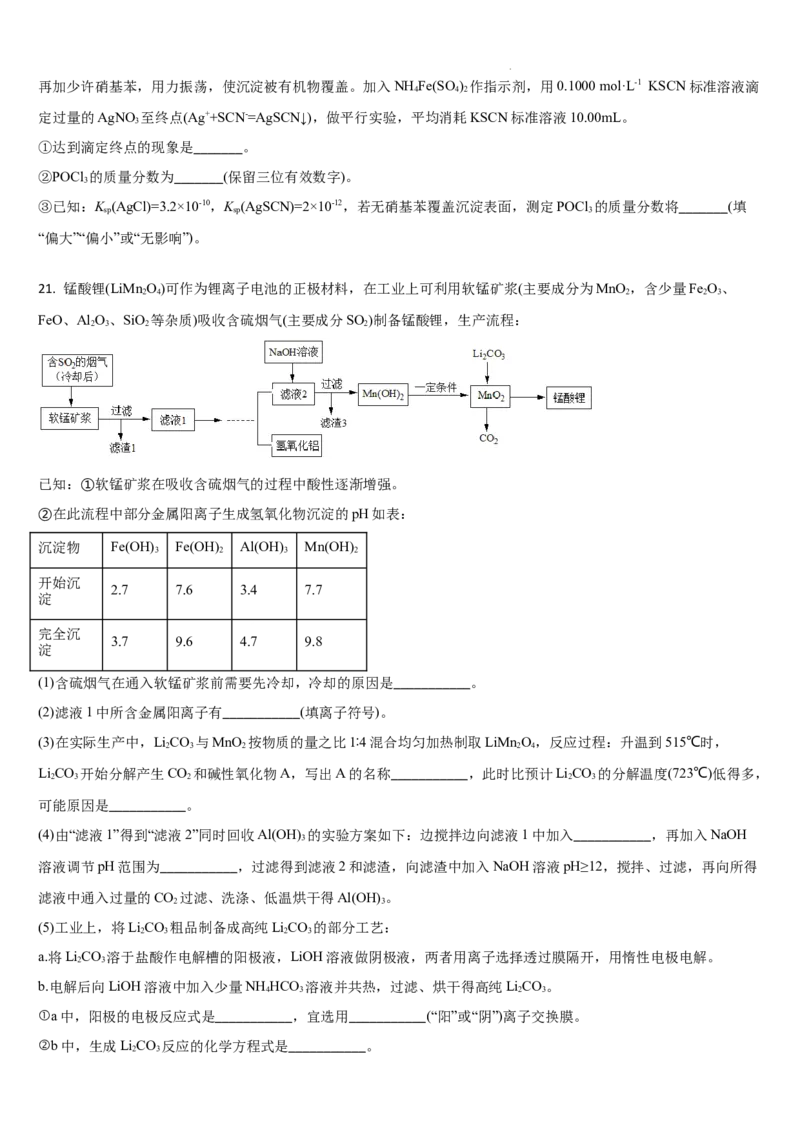
学科网(北京)股份有限公司20. 三氯化氧磷(POCl )是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料。一研究小组在实验室模拟
3
PCl +SO+Cl→POCl +SOCl 制备POCl 并测定产品含量。反应装置图如图所示(加热、夹持装置已省略。)
3 2 2 3 2 3
资料卡片:
物质 熔点/℃ 沸点/℃ 相对分子质量 其他
PCl -93.6 76.1 137.5 遇水剧烈水解,易与O 反应
3 2
POCl 1.25 105.8 153.5 遇水剧烈水解,能溶于PCl
3 3
SOCl -105 78.8 119 遇水剧烈水解,受热易分解
2
请回答:
(1)溶液A为饱和食盐水,乙装置中应该盛装的试剂为_______(填“PO”“碱石灰”“浓HSO ”或“无水硫酸铜”);反应
2 5 2 4
装置图的虚框中未画出的仪器最好选择_______(填“己”或“庚”)。
(2)甲、丁装置的作用除了用于气体的净化除杂外,还有_______。
(3)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是_______。
(4)通过佛尔哈德法可测定经过提纯后的产品中POCl 的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,
3
将水解液配成100mL溶液,取于10.00mL锥形瓶中,加入的0.2000 mol·L-1 AgNO 溶液20.00mL(Ag++C1-=AgC1↓),
3
学科网(北京)股份有限公司再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH Fe(SO ) 作指示剂,用0.1000 mol·L-1 KSCN标准溶液滴
4 4 2
定过量的AgNO 至终点(Ag++SCN-=AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
3
①达到滴定终点的现象是_______。
②POCl 的质量分数为_______(保留三位有效数字)。
3
③已知:K (AgCl)=3.2×10-10,K (AgSCN)=2×10-12,若无硝基苯覆盖沉淀表面,测定POCl 的质量分数将_______(填
sp sp 3
“偏大”“偏小”或“无影响”)。
21. 锰酸锂(LiMn O)可作为锂离子电池的正极材料,在工业上可利用软锰矿浆(主要成分为MnO ,含少量Fe O、
2 4 2 2 3
FeO、Al O、SiO 等杂质)吸收含硫烟气(主要成分SO )制备锰酸锂,生产流程:
2 3 2 2
已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强。
②在此流程中部分金属阳离子生成氢氧化物沉淀的pH如表:
沉淀物 Fe(OH) Fe(OH) Al(OH) Mn(OH)
3 2 3 2
开始沉
2.7 7.6 3.4 7.7
淀
完全沉
3.7 9.6 4.7 9.8
淀
(1)含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是___________。
(2)滤液1中所含金属阳离子有___________(填离子符号)。
(3)在实际生产中,LiCO 与MnO 按物质的量之比1∶4混合均匀加热制取LiMn O,反应过程:升温到515℃时,
2 3 2 2 4
LiCO 开始分解产生CO 和碱性氧化物A,写出A的名称___________,此时比预计LiCO 的分解温度(723℃)低得多,
2 3 2 2 3
可能原因是___________。
(4)由“滤液1”得到“滤液2”同时回收Al(OH) 的实验方案如下:边搅拌边向滤液1中加入___________,再加入NaOH
3
溶液调节pH范围为___________,过滤得到滤液2和滤渣,向滤渣中加入NaOH溶液pH≥12,搅拌、过滤,再向所得
滤液中通入过量的CO 过滤、洗涤、低温烘干得Al(OH) 。
2 3
(5)工业上,将LiCO 粗品制备成高纯LiCO 的部分工艺:
2 3 2 3
a.将LiCO 溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
2 3
b.电解后向LiOH溶液中加入少量NH HCO 溶液并共热,过滤、烘干得高纯LiCO。
4 3 2 3
①a中,阳极的电极反应式是___________,宜选用___________(“阳”或“阴”)离子交换膜。
②b中,生成LiCO 反应的化学方程式是___________。
2 3
学科网(北京)股份有限公司22. 近几年经济发展迅速,汽车数量越来越多,在方便我们的工作和生活的同时,也带来了严重的环境问题,为了消
除汽车尾气对大气环境和人体健康造成的影响,科学家们想了很多处理尾气的方法。
(1)活性炭可用于处理汽车尾气中的NO,有关反应为C(s)+2NO(g) N(g)+CO(g)。
2 2
①判断该反应达到平衡的标志为___________。(填标号)
的
A.容器内气体 物质的量恒定 B.NO、N、CO 的物质的量之比为2:1:1
2 2
C.v (NO)=2v (CO) D.容器内气体密度恒定
正 逆 2
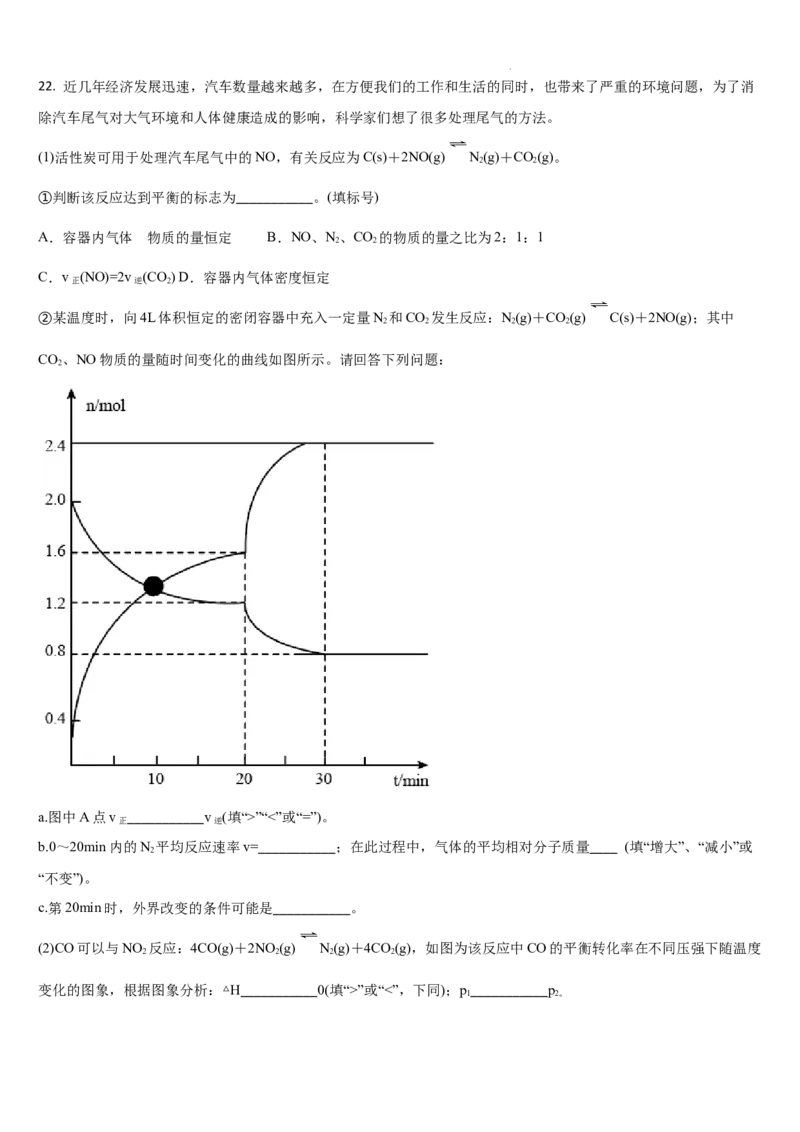
②某温度时,向4L体积恒定的密闭容器中充入一定量N 和CO 发生反应:N(g)+CO(g) C(s)+2NO(g);其中
2 2 2 2
CO、NO物质的量随时间变化的曲线如图所示。请回答下列问题:
2
a.图中A点v ___________v (填“>”“<”或“=”)。
正 逆
b.0~20min内的N 平均反应速率v=___________;在此过程中,气体的平均相对分子质量____ (填“增大”、“减小”或
2
“不变”)。
c.第20min时,外界改变的条件可能是___________。
(2)CO可以与NO 反应:4CO(g)+2NO (g) N(g)+4CO(g),如图为该反应中CO的平衡转化率在不同压强下随温度
2 2 2 2
变化的图象,根据图象分析:△H___________0(填“>”或“<”,下同);p___________p
1 2。
学科网(北京)股份有限公司CACDD DCCDB BBACB DDC
19
【答案】(1)3d74s2
(2)+2、+3 (3) ①. 50℃ ②. 3mol/L
(4) ①. +6Fe2++6H+=6Fe3++Cl-+3H O ②. Fe(OH)
2 3
(5) ①. 正 ②. C
(6)
20
【答案】(1) ①. PO ②. 己
2 5
(2)通过观察产生气泡的速率控制通入气体的流速
(3)温度太低,反应速率太慢;温度太高,PCl 等物质挥发
3
(4) ①. 滴入最后一滴KSCN标准溶液,溶液变红色,且半分钟内不褪色 ②. 95.9% ③. 偏小
21【答案】 ①. 有利于 的吸收,提高含硫烟气中 的吸收率 ②. 、 、 ③. 氧化锂
④. 对LiCO 的分解起到催化作用 ⑤. 足量 ⑥. ⑦. ⑧.
2 3
阳 ⑨.
22答案】 ①. CD ②. > ③. 0.01mol·L-1·min-1 ④. 减小 ⑤. 加催化剂或升温 ⑥. < ⑦.
学科网(北京)股份有限公司< ⑧.
学科网(北京)股份有限公司