文档内容
南开中学 2024 届高三第一次月检测
化学学科试卷 考试时间:60分钟
Ⅰ卷(共36分)
相对原子质量:C:l2 N:14 O:16 Na:23 Mg:24 Al:27 ‘S:32 Fe:56 Cu:64 Ba:137
一、选择题(每题只有一个选项是正确的,每题3分,共36分)
1. 下列应用中涉及到氧化还原反应的是( )
A. 使用明矾对水进行净化 B. 雪天道路上撒盐融雪
C. 暖贴中的铁粉遇空气放热 D. 荧光指示牌被照发光
2. 下列有关碱金属的叙述正确的是( )
A. 随核电荷数的增加,碱金属单质的熔点逐渐降低,密度逐渐增大
B. KOH 的碱性比 CsOH 的强
C. Cs
2
CO₃用酒精灯加热时不易分解
D. 碱金属单质着火时均可用干冰灭火
3. 类推(类比迁移)的思维方法可以预测许多物质的性质。但类比是相对的,不能违背客观
事实。下列类比分析结果不正确的是( )
A. Fe
3
Cl₈根据:化合价规律可表示为FeCl
2
·2FeCl₃,则 Fe
3
I₈也可表示为 FeI
2
·2FeI₃
B. CO₂通入 BaCl₂溶液不产生沉淀,则 CO₂通入 Ba(NO
3
)₂溶液也不产生沉淀
C. Na与O₂加热生成Na
2
O₂, 则K与O₂加热也可能生成K
2
O₂
D. CaC₂能水解: CaC₂+2H₂O→Ca(OH)₂+HC=CH↑,则 Mg₂C₃也能水
解: Mg₂C₃+4H₂O→2Mg(OH)₂↓+C₃H₄↑
4. 下列离子方程式书写不正确的是( )
A. 等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合
Ba2++2OH−+N H++HCO−=BaCO ↓+N H ⋅H O+H O
4 3 3 3 2 2
B. 向次氯酸钙溶液中通入少量二氧化硫 Ca²⁺+2ClO⁻+SO₂+H₂O=CaSO₃↓+2HClO
C. 将2mol/LAlCl₃溶液和 7mol/LNaOH溶液等体积混合;
2Al3++7OH−=Al(OH) ↓+AlO−+2H O
3 2 2
D. 向 Ba(OH)₂溶液中滴加 NaHSO₄溶液至恰好为中性:
Ba2++2OH−+2H++SO2−=BaSO ↓+2H O
4 4 2
第1页/共8页5. 实验室将粗盐提纯并配制 0.1000mol⋅L⁻ ¹的NaCl溶液。下列仪器中,本实验必须用
到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A. ①②④⑥ B. ①④⑤⑥ C. ②③⑦⑧ D. ①⑤⑥⑧
N
6. 设 A表示阿伏加德罗常数的值,下列说法中正确的是( )
①1molBrCl与H₂O 完全反应生成氯化氢和次溴酸, 转移的电子数为NA
②14.2g硫酸钠固体中含有0.1NA个硫酸钠分子
③锌与一定浓硫酸反应,产生标准状况下 SO₂和H₂的混合气体22.4L,锌失去电子
数为2NA
④2gD16O中含有的质子数、中子数、电子数均为 NA
2
⑤标准状况下, 2.24LCl₂全部溶于水所得溶液中的Cl⁻数目为0.1NA
⑥10mL18mol⋅L⁻ ¹的浓硫酸与足量的镁反应时转移的电子数为 0.18N
A
A. ③④ B. ①②③④ C.③④⑤ D. ①②③④⑤⑥
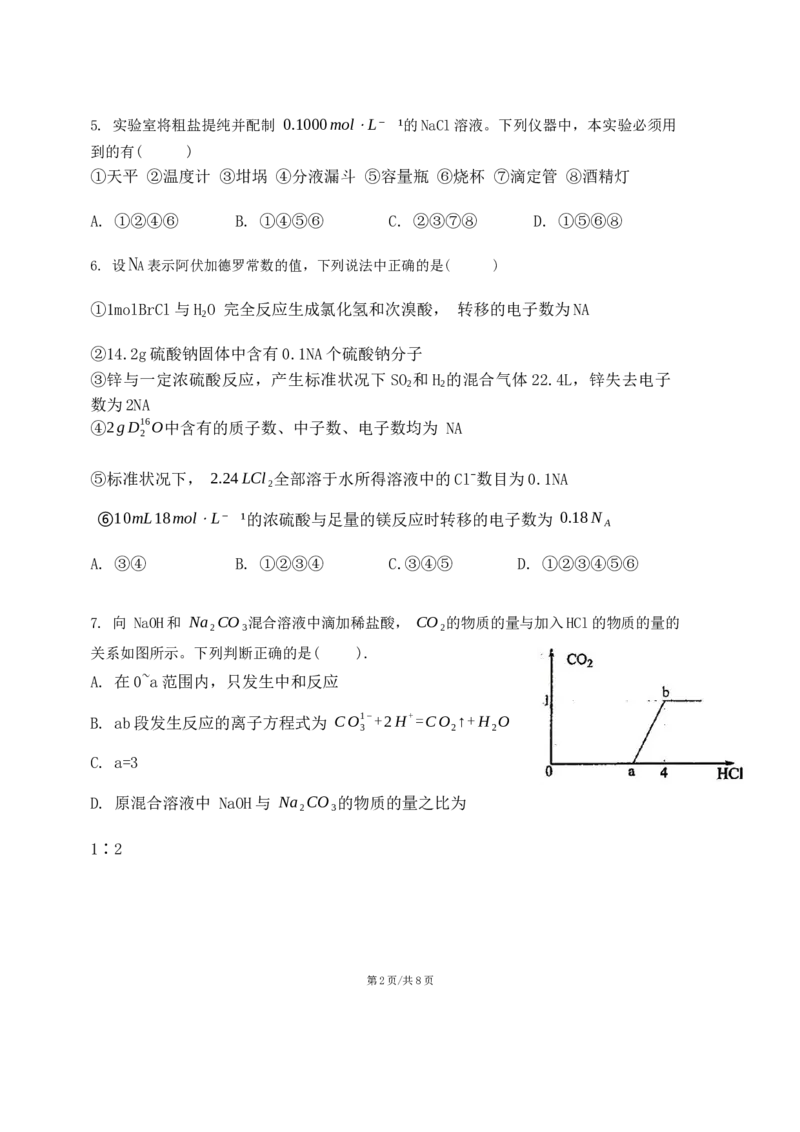
7. 向 NaOH和 Na₂CO₃混合溶液中滴加稀盐酸, CO₂的物质的量与加入HCl的物质的量的
关系如图所示。下列判断正确的是( ).
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为 CO1−+2H+=CO ↑+H O
3 2 2
C. a=3
D. 原混合溶液中 NaOH与 Na₂CO₃的物质的量之比为
1∶2
第2页/共8页8. 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
选
实验 现象 结论
项
某粉末用酒精润湿后,用铂丝
A 火焰呈黄色 该粉末一定为钠盐
蘸取做焰色试验
B 用熔融氯化铝做导电性实验 电流表指针不偏转 氯化铝属于非电解质
将铁粉加入过量稀硝酸中,充有气体生成,溶液呈浅 稀硝酸将 Fe氧化为
C
分反应后滴加 KSCN 溶液 绿色 Fe²⁺
Na₂CO₃与H₂O 发生了
D 向碳酸钠固体中加入少量水 白色粉末变成了晶体
化学反应
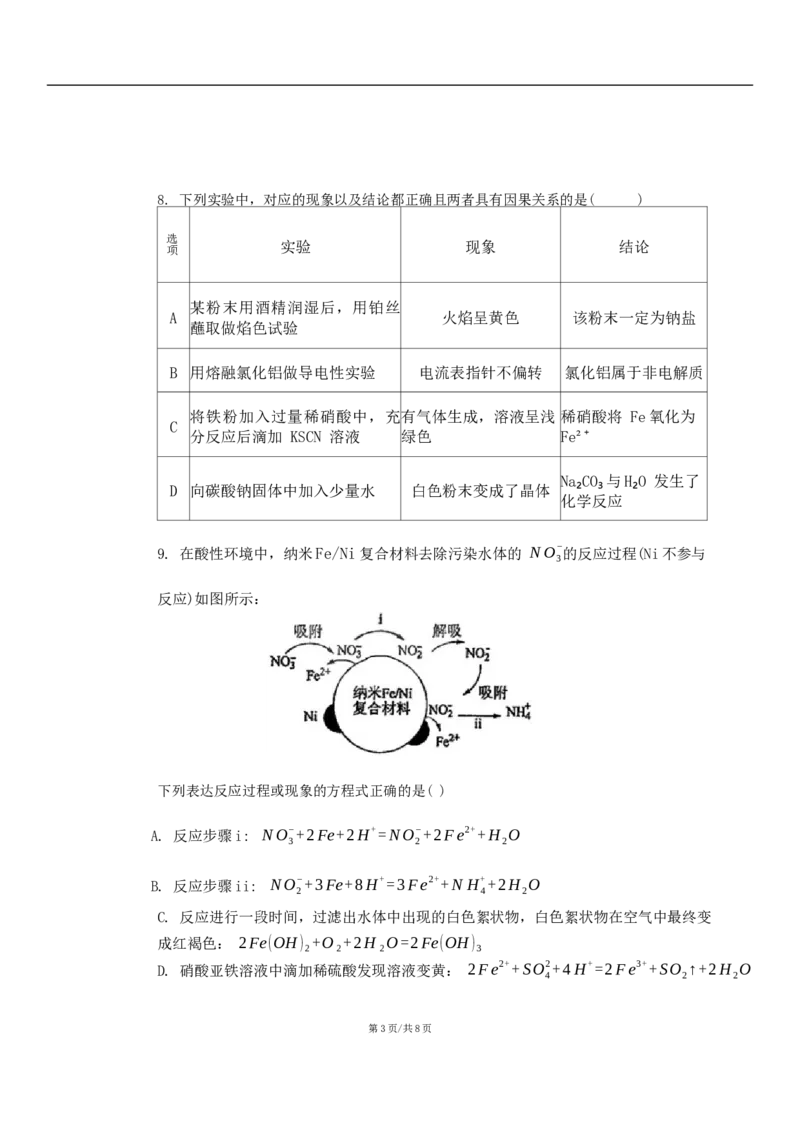
9. 在酸性环境中,纳米Fe/Ni复合材料去除污染水体的 NO− 的反应过程(Ni不参与
3
反应)如图所示:
下列表达反应过程或现象的方程式正确的是( )
A. 反应步骤i: NO−+2Fe+2H+=NO−+2Fe2++H O
3 2 2
B. 反应步骤ii: NO−+3Fe+8H+=3Fe2++N H++2H O
2 4 2
C. 反应进行一段时间,过滤出水体中出现的白色絮状物,白色絮状物在空气中最终变
成红褐色: 2Fe(OH)₂+O₂+2H₂O=2Fe(OH)₃
D. 硝酸亚铁溶液中滴加稀硫酸发现溶液变黄: 2Fe2++SO2+4H+=2Fe3++SO ↑+2H O
4 2 2
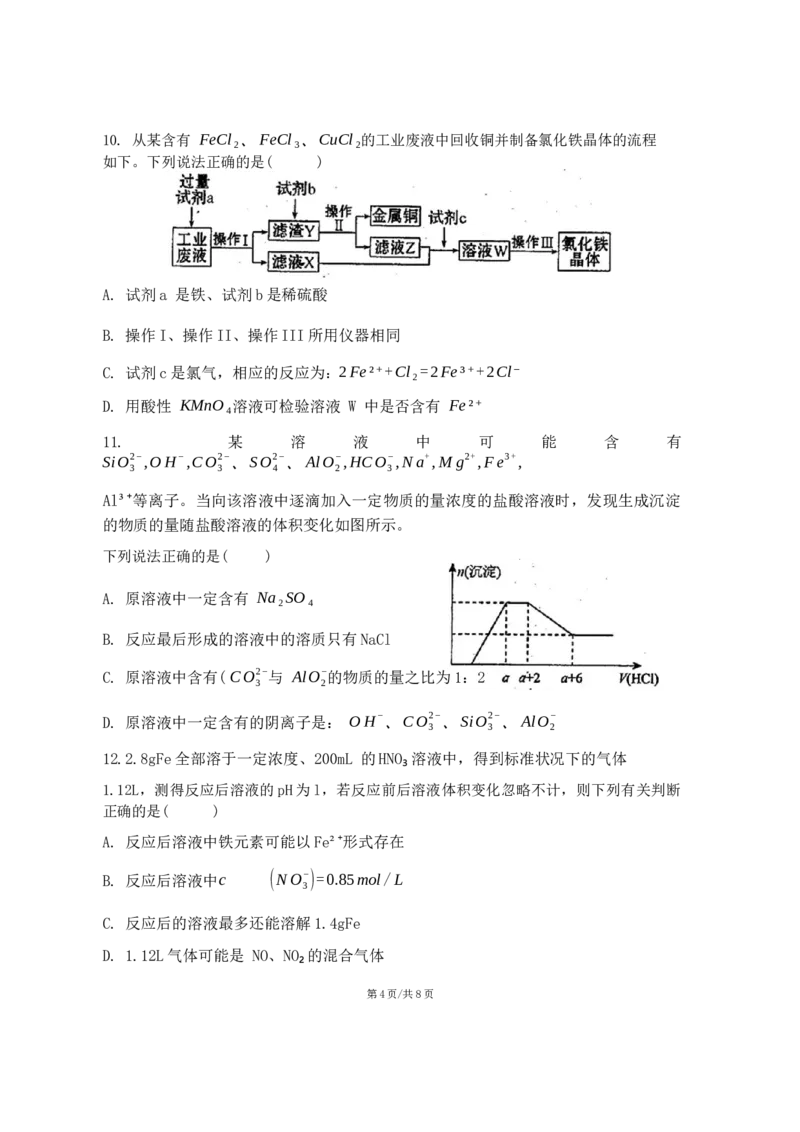
第3页/共8页10. 从某含有 FeCl₂、FeCl₃、CuCl₂的工业废液中回收铜并制备氯化铁晶体的流程
如下。下列说法正确的是( )
A. 试剂a 是铁、试剂b是稀硫酸
B. 操作I、操作II、操作III所用仪器相同
C. 试剂c是氯气,相应的反应为:2Fe²⁺+Cl₂=2Fe³⁺+2Cl⁻
D. 用酸性 KMnO₄溶液可检验溶液 W 中是否含有 Fe²⁺
11. 某 溶 液 中 可 能 含 有
SiO2−,OH−,CO2−、SO2−、AlO−,HCO−,Na+,M g2+,Fe3+,
3 3 4 2 3
Al³⁺等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀
的物质的量随盐酸溶液的体积变化如图所示。
下列说法正确的是( )
A. 原溶液中一定含有 Na₂SO₄
B. 反应最后形成的溶液中的溶质只有NaCl
C. 原溶液中含有( CO2−与 AlO−的物质的量之比为1:2
3 2
D. 原溶液中一定含有的阴离子是: OH−、CO2−、SiO2−、AlO−
3 3 2
12.2.8gFe全部溶于一定浓度、200mL 的HNO₃溶液中,得到标准状况下的气体
1.12L,测得反应后溶液的pH为l,若反应前后溶液体积变化忽略不计,则下列有关判断
正确的是( )
A. 反应后溶液中铁元素可能以Fe²⁺形式存在
B. 反应后溶液中c (NO−)=0.85mol/L
3
C. 反应后的溶液最多还能溶解1.4gFe
D. 1.12L气体可能是 NO、NO₂的混合气体
第4页/共8页Ⅱ卷(共64分)
二、填空题(共4题,共64分)
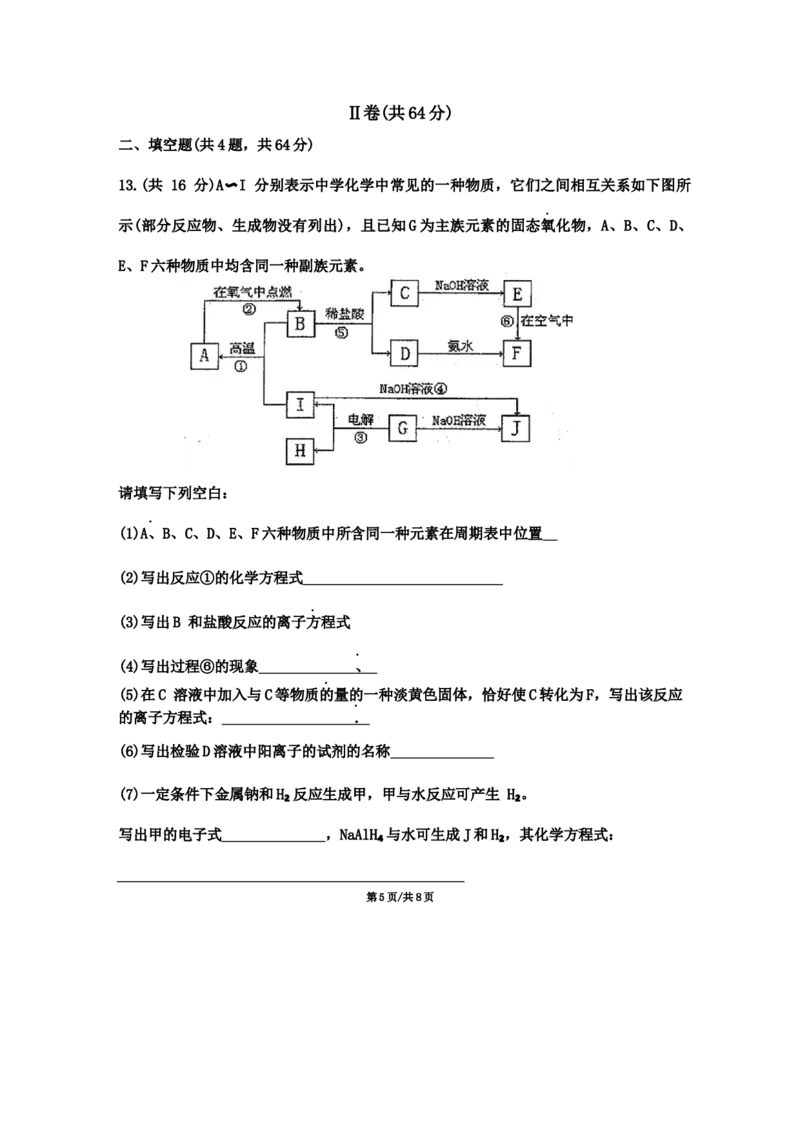
13.(共 16 分)A〜I 分别表示中学化学中常见的一种物质,它们之间相互关系如下图所
示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、
E、F六种物质中均含同一种副族元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置
(2)写出反应①的化学方程式
(3)写出B 和盐酸反应的离子方程式
(4)写出过程⑥的现象 、
(5)在C 溶液中加入与C等物质的量的一种淡黄色固体,恰好使C转化为F,写出该反应
的离子方程式: .
(6)写出检验D溶液中阳离子的试剂的名称
(7)一定条件下金属钠和H₂反应生成甲,甲与水反应可产生 H₂。
写出甲的电子式 ,NaAlH₄与水可生成J和H₂,其化学方程式:
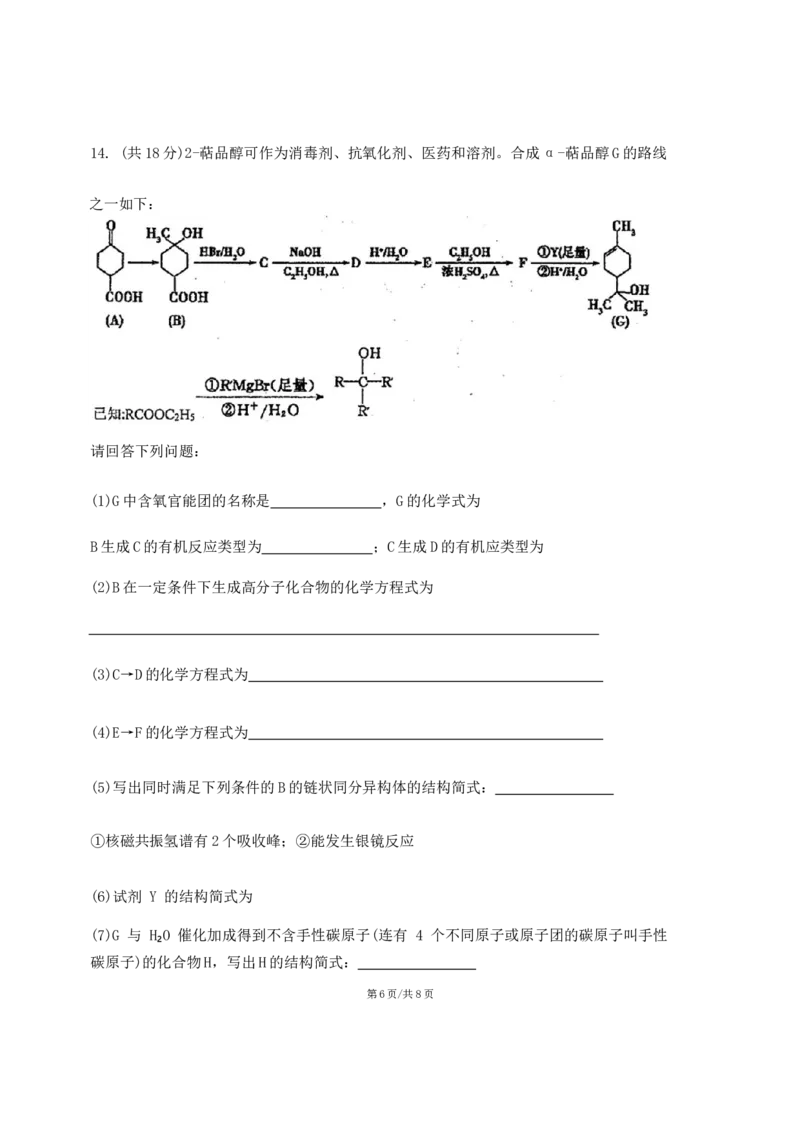
第5页/共8页14. (共18分)2-萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成α-萜品醇G的路线
之一如下:
请回答下列问题:
(1)G中含氧官能团的名称是 ,G的化学式为
B生成C的有机反应类型为 ;C生成D的有机应类型为
(2)B在一定条件下生成高分子化合物的化学方程式为
(3)C→D的化学方程式为
(4)E→F的化学方程式为
(5)写出同时满足下列条件的B的链状同分异构体的结构简式:
①核磁共振氢谱有2个吸收峰;②能发生银镜反应
(6)试剂 Y 的结构简式为
(7)G 与 H₂O 催化加成得到不含手性碳原子(连有 4 个不同原子或原子团的碳原子叫手性
碳原子)的化合物H,写出H的结构简式:
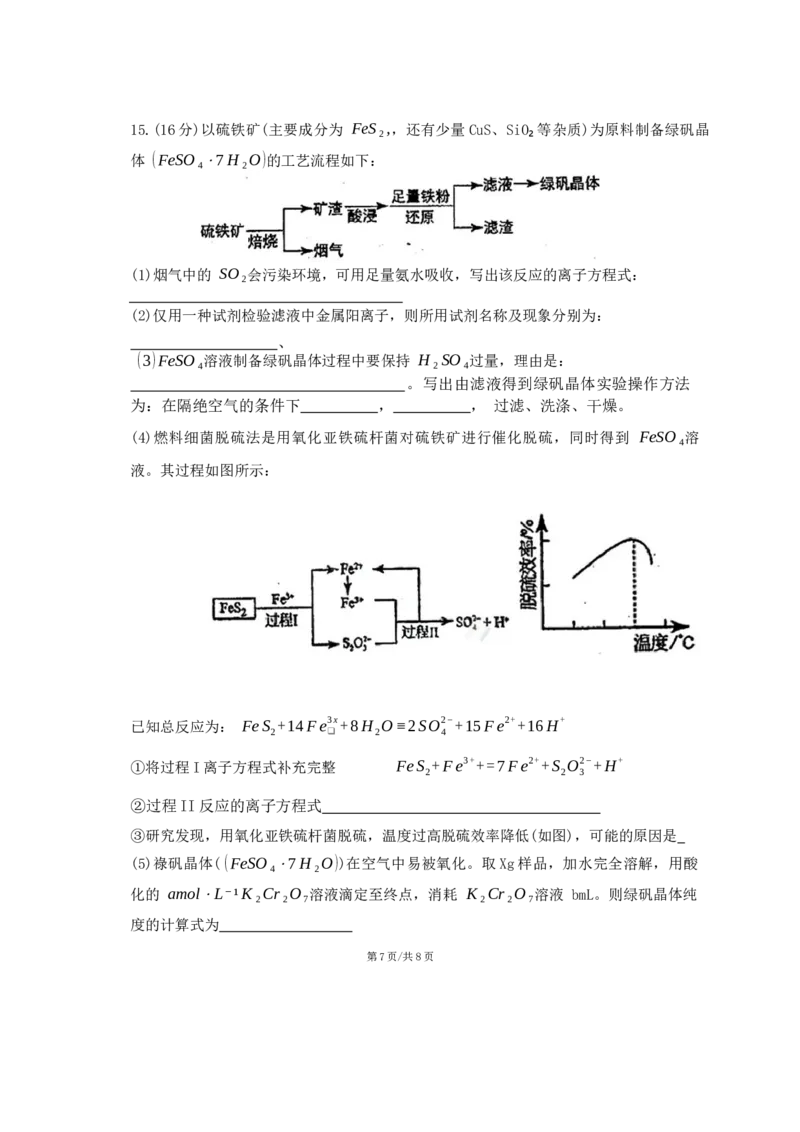
第6页/共8页15.(16分)以硫铁矿(主要成分为 FeS₂,,还有少量CuS、SiO₂等杂质)为原料制备绿矾晶
体 (FeSO₄⋅7H₂O)的工艺流程如下:
(1)烟气中的 SO₂会污染环境,可用足量氨水吸收,写出该反应的离子方程式:
(2)仅用一种试剂检验滤液中金属阳离子,则所用试剂名称及现象分别为:
、
(3)FeSO₄溶液制备绿矾晶体过程中要保持 H₂SO₄过量,理由是:
。写出由滤液得到绿矾晶体实验操作方法
为:在隔绝空气的条件下 , , 过滤、洗涤、干燥。
(4)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到 FeSO₄溶
液。其过程如图所示:
已知总反应为: FeS +14Fe3x+8H O≡2SO2−+15Fe2++16H+
2 ❑ 2 4
①将过程I离子方程式补充完整 FeS +Fe3++=7Fe2++S O2−+H+
2 2 3
②过程II反应的离子方程式
③研究发现,用氧化亚铁硫杆菌脱硫,温度过高脱硫效率降低(如图),可能的原因是
(5)祿矾晶体( (FeSO₄⋅7H₂O))在空气中易被氧化。取Xg样品,加水完全溶解,用酸
化的 amol⋅L⁻¹K₂Cr₂O₇溶液滴定至终点,消耗 K₂Cr₂O₇溶液 bmL。则绿矾晶体纯
度的计算式为
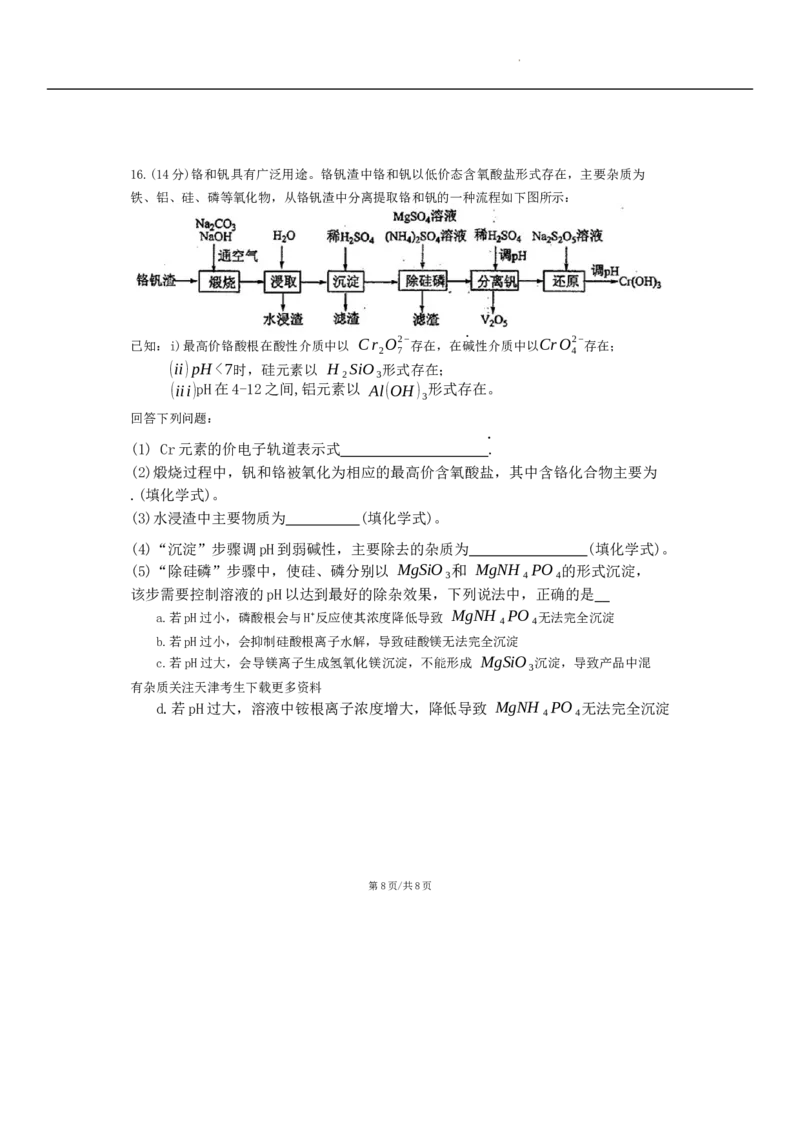
第7页/共8页16.(14分)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为
铁、铝、硅、磷等氧化物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:i)最高价铬酸根在酸性介质中以 Cr O2− 存在,在碱性介质中以CrO2− 存在;
2 7 4
(ii)pH<7时,硅元素以 H₂SiO₃形式存在;
(iii)pH在4-12之间,铝元素以 Al(OH)₃形式存在。
回答下列问题:
(1) Cr元素的价电子轨道表示式 .
(2)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
.(填化学式)。
(3)水浸渣中主要物质为 (填化学式)。
(4)“沉淀”步骤调pH到弱碱性,主要除去的杂质为 (填化学式)。
(5)“除硅磷”步骤中,使硅、磷分别以 MgSiO₃和 MgNH₄PO₄的形式沉淀,
该步需要控制溶液的pH以达到最好的除杂效果,下列说法中,正确的是
a.若pH过小,磷酸根会与H⁺反应使其浓度降低导致 MgNH₄PO₄无法完全沉淀
b.若pH过小,会抑制硅酸根离子水解,导致硅酸镁无法完全沉淀
c.若pH过大,会导镁离子生成氢氧化镁沉淀,不能形成 MgSiO₃沉淀,导致产品中混
有杂质关注天津考生下载更多资料
d.若pH过大,溶液中铵根离子浓度增大,降低导致 MgNH₄PO₄无法完全沉淀
第8页/共8页
学科网(北京)股份有限公司