文档内容
枣庄三中高三年级 10 月月考
化学试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试用时90分钟。答卷前,
考生务必将自己的姓名、准考证号、考试科目填涂在答题卡和答题纸规定的地方。
第Ⅰ卷(选择题 共 40 分)
注意事项:第Ⅰ卷共15小题,1-10每小题2分,11-15每小题4分共40分。在每小题给出的四个选
项中,1-10只有一项是符合题目要求的,11-15每题有一个或两个选项正确。每小题选出答案后,用铅笔
把答题卡上对应题目的答案涂黑。如需改动,用橡皮擦干净后,再选涂其他答案。
可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 Ba137 Ti48
一、选择题:本题共 10小题,每小题 2分,共 20 分。每题只有一个正确选项
1.化学与生活密切相关,下列说法正确的是 ( )
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
2.绿矾(FeSO 7H O)分解可制备铁红,同时产生SO 、SO 和HO。设N 为阿伏加德罗常数的值,下列
4 2 2 3 2 A
说法错误的是 ( )
A.1L1molL1FeSO 溶液含有的阳离子数大于N
4 A
B.0.5mol三聚SO 分子( )中含有σ键数目为6N
3 A
C.绿矾分解生成16gFe O 时,转移电子数为0.2N
2 3 A
D.22.4LSO 溶于水,溶液中H SO 、HSO、SO2的数目总和为N
2 2 3 3 3 A
3.物质的性质决定用途,下列两者对应关系不正确的是 ( )
A.铝有强还原性,可用于制作门窗框架
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
第 1 页 共 10 页
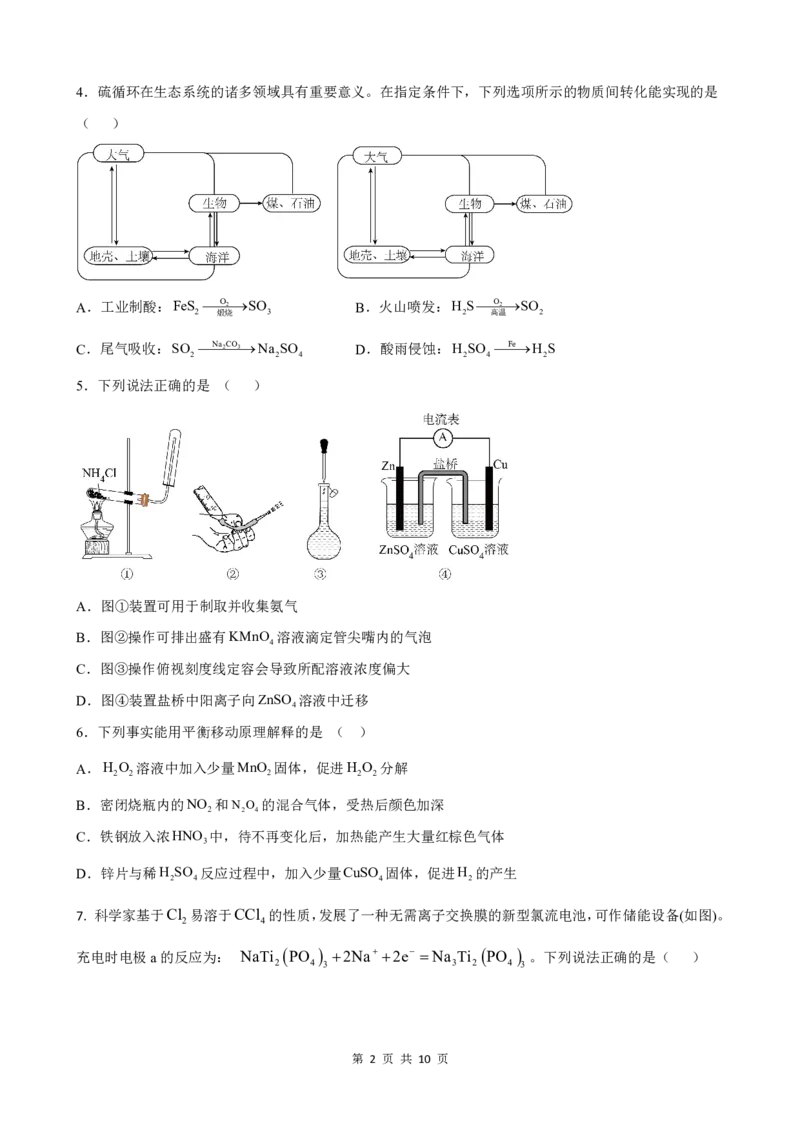
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}4.硫循环在生态系统的诸多领域具有重要意义。在指定条件下,下列选项所示的物质间转化能实现的是
( )
A.工业制酸:FeS O2SO B.火山喷发:H SO2SO
2 煅烧 3 2 高温 2
C.尾气吸收:SO Na2CO3Na SO D.酸雨侵蚀:H SO FeH S
2 2 4 2 4 2
5.下列说法正确的是 ( )
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有KMnO 溶液滴定管尖嘴内的气泡
4
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向ZnSO 溶液中迁移
4
6.下列事实能用平衡移动原理解释的是 ( )
A.H O 溶液中加入少量MnO 固体,促进H O 分解
2 2 2 2 2
B.密闭烧瓶内的NO 和N O 的混合气体,受热后颜色加深
2 2 4
C.铁钢放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D.锌片与稀H SO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
7. 科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。
2 4
充电时电极a的反应为: NaTi PO 2Na 2e Na Ti PO 。下列说法正确的是( )
2 4 3 3 2 4 3
第 2 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}A. 充电时电极b是阳极
B. 放电时NaCl溶液的pH减小
C. 放电时NaCl溶液的浓度减小
D. 每生成1mol Cl ,电极a质量理论上增加23g
2
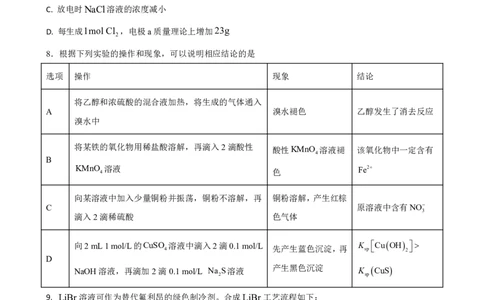
8.根据下列实验的操作和现象,可以说明相应结论的是
选项 操作 现象 结论
将乙醇和浓硫酸的混合液加热,将生成的气体通入
A 溴水褪色 乙醇发生了消去反应
溴水中
将某铁的氧化物用稀盐酸溶解,再滴入2滴酸性
酸性KMnO 溶液褪 该氧化物中一定含有
4
B
KMnO
4
溶液
色
Fe2
向某溶液中加入少量铜粉并振荡,铜粉不溶解,再 铜粉溶解,产生红棕
C 原溶液中含有NO
3
滴入2滴稀硫酸 色气体
向2mL1mol/L的CuSO
4
溶液中滴入2滴0.1mol/L
先产生蓝色沉淀,再
K
sp
CuOH
2
D
NaOH溶液,再滴加2滴0.1mol/L Na S溶液 产生黑色沉淀 K CuS
2 sp
9. LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是 ( )
A. 还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B. 除杂工序中产生的滤渣可用煤油进行组分分离
第 3 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}C. 中和工序中的化学反应为Li CO +2HBr=CO +2LiBr+H O
2 3 2 2
D. 参与反应的n Br :n(BaS):n H SO 为1∶1∶1
2 2 4
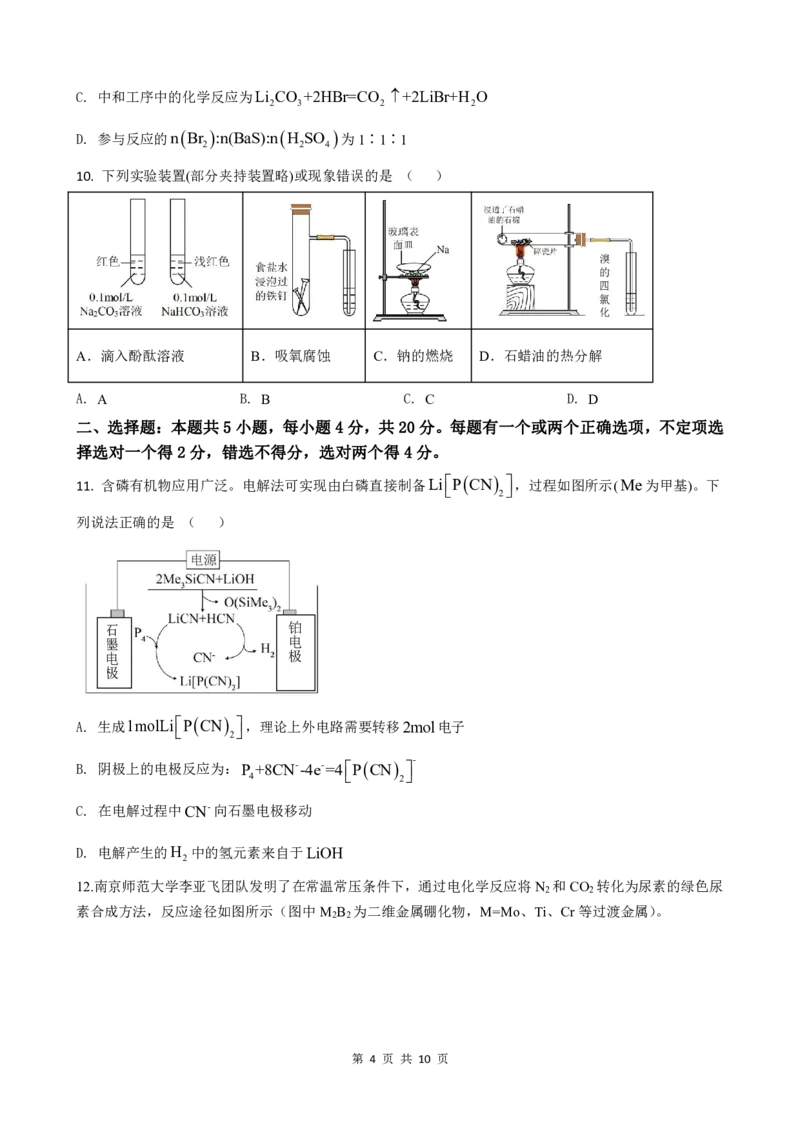
10. 下列实验装置(部分夹持装置略)或现象错误的是 ( )
溴
的
四
氯
化
A.滴入酚酞溶液 B.吸氧腐蚀 C.钠的燃烧 D.石蜡油的热分解
A. A B. B C. C D. D
二、选择题:本题共 5 小题,每小题4 分,共 20分。每题有一个或两个正确选项,不定项选
择选对一个得 2分,错选不得分,选对两个得 4分。
11. 含磷有机物应用广泛。电解法可实现由白磷直接制备Li P CN ,过程如图所示(Me为甲基)。下
2
列说法正确的是 ( )
石 铂
墨 电
电 极
极
A. 生成1molLi
P CN
,理论上外电路需要转移2mol电子
2
B. 阴极上的电极反应为:P +8CN--4e-=4P CN -
4 2
C. 在电解过程中CN-向石墨电极移动
D. 电解产生的H 中的氢元素来自于LiOH
2
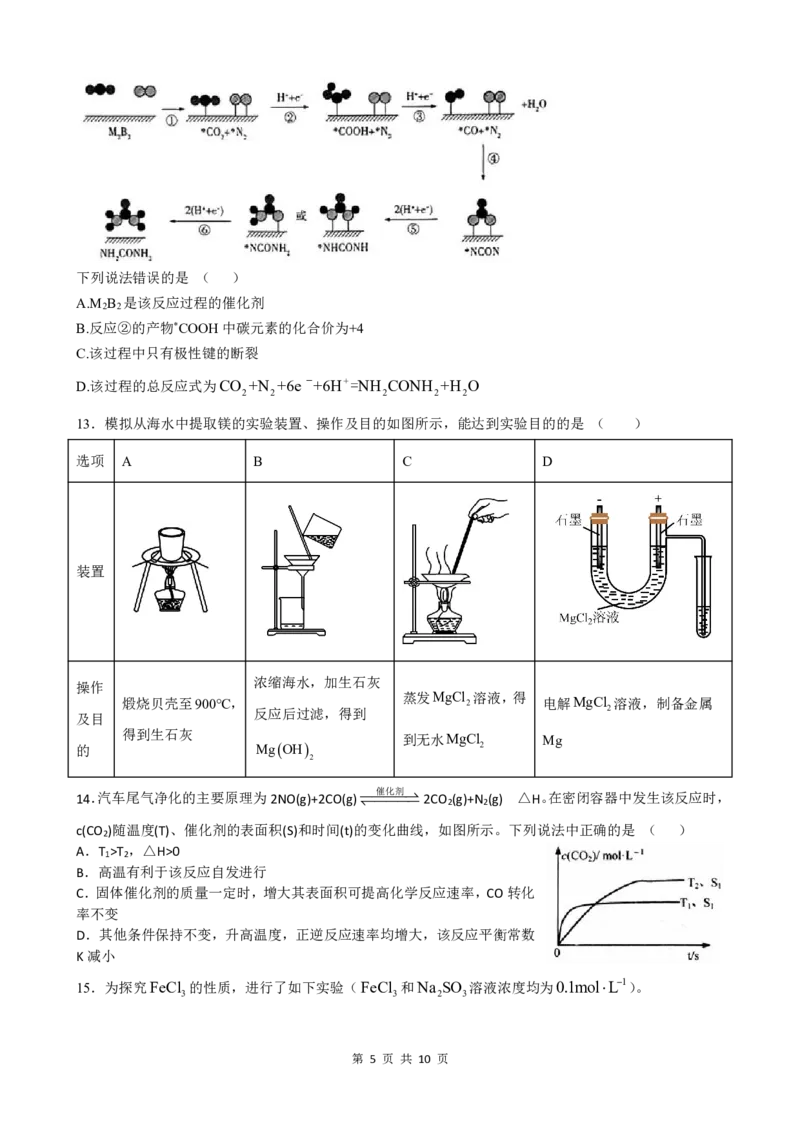
12.南京师范大学李亚飞团队发明了在常温常压条件下,通过电化学反应将N 和CO 转化为尿素的绿色尿
2 2
素合成方法,反应途径如图所示(图中M B 为二维金属硼化物,M=Mo、Ti、Cr等过渡金属)。
2 2
第 4 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}下列说法错误的是 ( )
A.M B 是该反应过程的催化剂
2 2
B.反应②的产物*COOH中碳元素的化合价为+4
C.该过程中只有极性键的断裂
D.该过程的总反应式为CO +N +6eˉ+6H+=NH CONH +H O
2 2 2 2 2
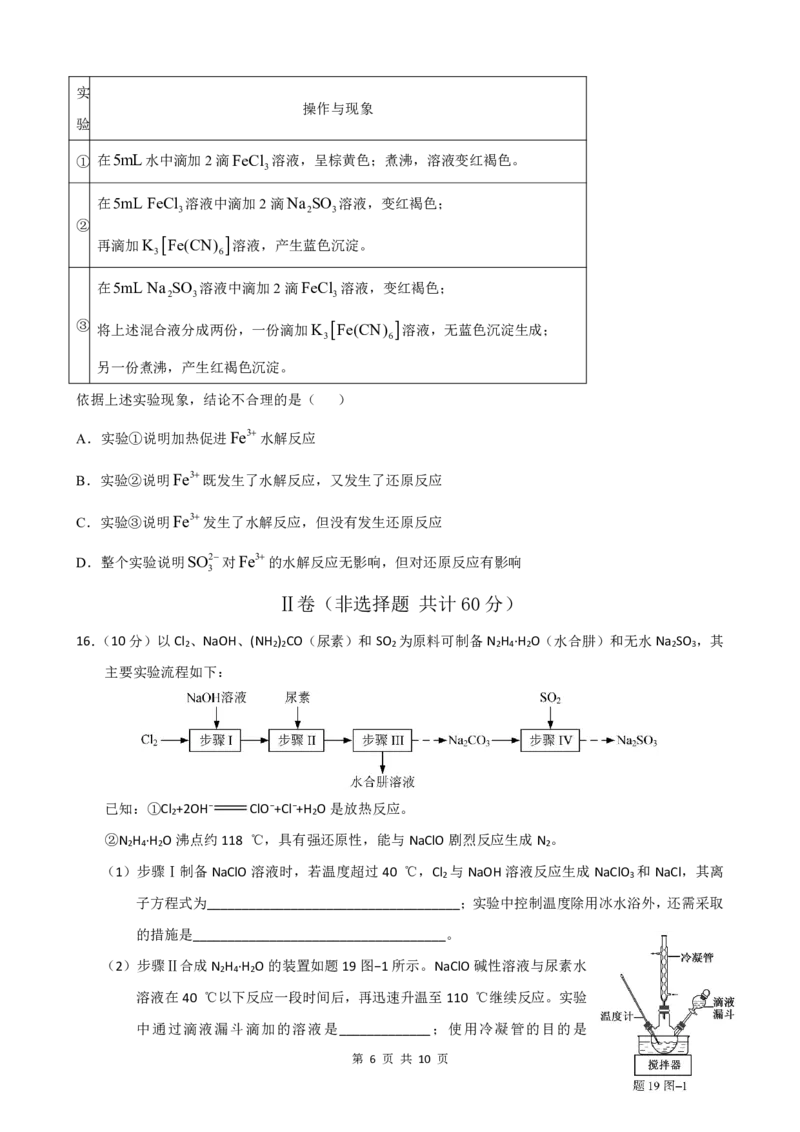
13.模拟从海水中提取镁的实验装置、操作及目的如图所示,能达到实验目的的是 ( )
选项 A B C D
装置
浓缩海水,加生石灰
操作
蒸发MgCl 溶液,得
煅烧贝壳至900℃, 2 电解MgCl 溶液,制备金属
反应后过滤,得到 2
及目
得到生石灰
到无水MgCl Mg
的 MgOH 2
2
催化剂
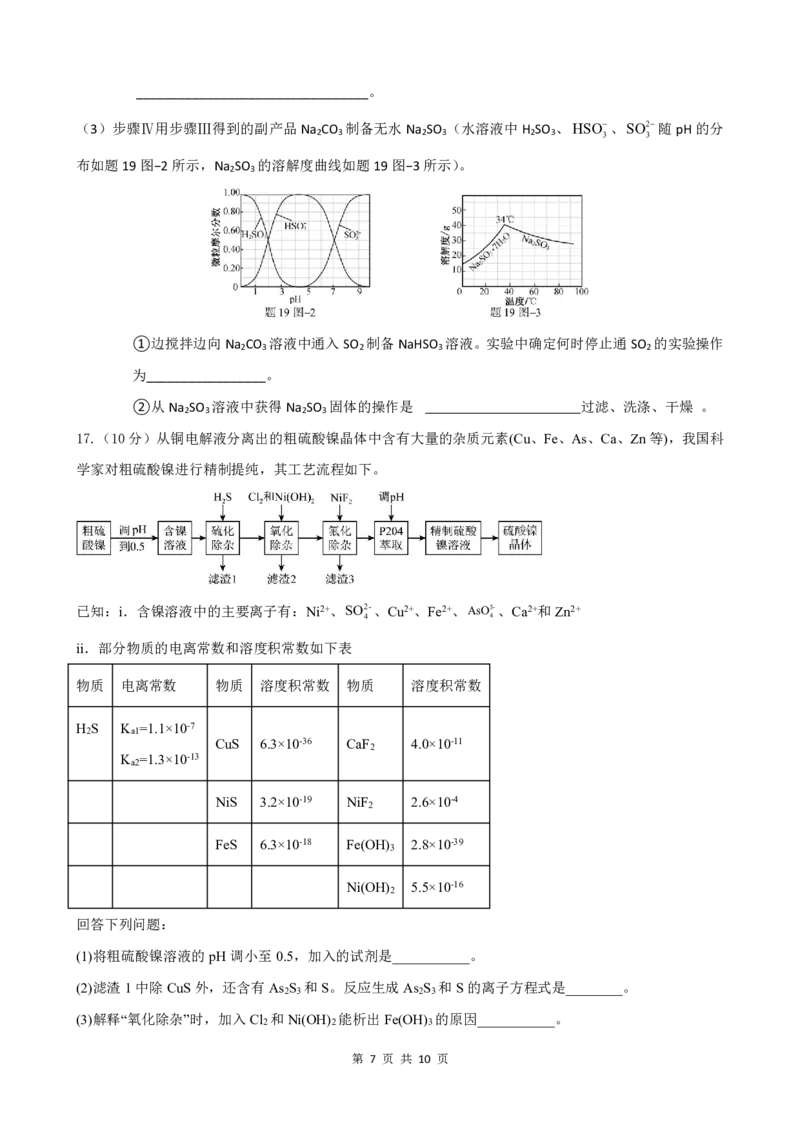
14.汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO 2 (g)+N 2 (g) △H。在密闭容器中发生该反应时,
c(CO )随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。下列说法中正确的是 ( )
2
A.T >T ,△H>0
1 2
B.高温有利于该反应自发进行
C.固体催化剂的质量一定时,增大其表面积可提高化学反应速率,CO转化
率不变
D.其他条件保持不变,升高温度,正逆反应速率均增大,该反应平衡常数
K减小
15.为探究FeCl 的性质,进行了如下实验(FeCl 和Na SO 溶液浓度均为0.1molL1)。
3 3 2 3
第 5 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}实
操作与现象
验
① 在5mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mL FeCl 溶液中滴加2滴Na SO 溶液,变红褐色;
3 2 3
②
再滴加K Fe(CN) 溶液,产生蓝色沉淀。
3 6
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;
2 3 3
③ 将上述混合液分成两份,一份滴加K Fe(CN) 溶液,无蓝色沉淀生成;
3 6
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3水解反应
B.实验②说明Fe3既发生了水解反应,又发生了还原反应
C.实验③说明Fe3发生了水解反应,但没有发生还原反应
D.整个实验说明SO2对Fe3的水解反应无影响,但对还原反应有影响
3
Ⅱ卷(非选择题 共计 60 分)
16.(10分)以Cl 、NaOH、(NH ) CO(尿素)和SO 为原料可制备N H ·H O(水合肼)和无水Na SO ,其
2 2 2 2 2 4 2 2 3
主要实验流程如下:
已知:①Cl +2OH− ClO−+Cl−+H O是放热反应。
2 2
②N H ·H O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N 。
2 4 2 2
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl 与NaOH溶液反应生成NaClO 和NaCl,其离
2 3
子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取
的措施是____________________________________。
(2)步骤Ⅱ合成N H ·H O的装置如题19图−1所示。NaClO碱性溶液与尿素水
2 4 2
溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验
中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是
第 6 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}_________________________________。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na CO 制备无水Na SO (水溶液中H SO 、HSO、SO2随pH的分
2 3 2 3 2 3 3 3
布如题19图−2所示,Na SO 的溶解度曲线如题19图−3所示)。
2 3
①边搅拌边向Na CO 溶液中通入SO 制备NaHSO 溶液。实验中确定何时停止通SO 的实验操作
2 3 2 3 2
为_________________。
②从Na SO 溶液中获得Na SO 固体的操作是 过滤、洗涤、干燥 。
2 3 2 3
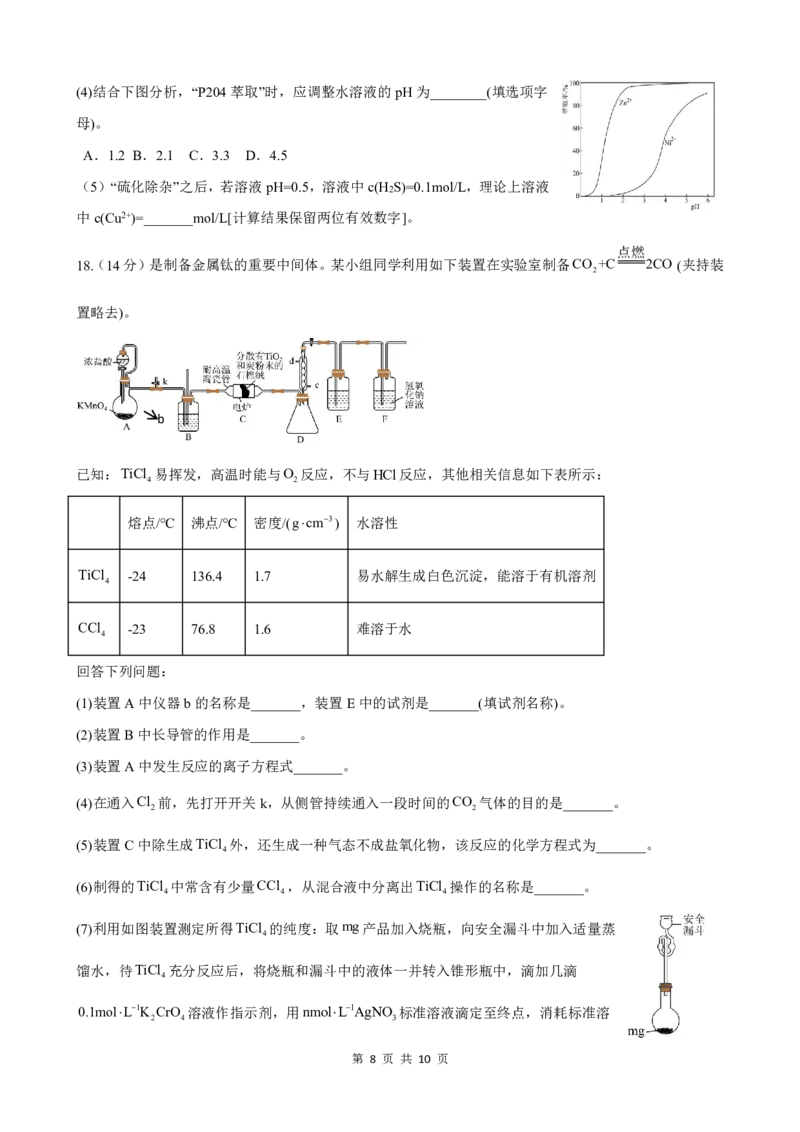
17.(10分)从铜电解液分离出的粗硫酸镍晶体中含有大量的杂质元素(Cu、Fe、As、Ca、Zn等),我国科
学家对粗硫酸镍进行精制提纯,其工艺流程如下。
已知:i.含镍溶液中的主要离子有:Ni2+、SO2-、Cu2+、Fe2+、AsO3-、Ca2+和Zn2+
4 4
ii.部分物质的电离常数和溶度积常数如下表
物质 电离常数 物质 溶度积常数 物质 溶度积常数
H S K =1.1×10-7
2 a1
CuS 6.3×10-36 CaF 4.0×10-11
2
K =1.3×10-13
a2
NiS 3.2×10-19 NiF 2.6×10-4
2
FeS 6.3×10-18 Fe(OH) 2.8×10-39
3
Ni(OH) 5.5×10-16
2
回答下列问题:
(1)将粗硫酸镍溶液的pH调小至0.5,加入的试剂是___________。
(2)滤渣1中除CuS外,还含有As S 和S。反应生成As S 和S的离子方程式是________。
2 3 2 3
(3)解释“氧化除杂”时,加入Cl 和Ni(OH) 能析出Fe(OH) 的原因___________。
2 2 3
第 7 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}(4)结合下图分析,“P204萃取”时,应调整水溶液的pH为________(填选项字
母)。
A.1.2 B.2.1 C.3.3 D.4.5
(5)“硫化除杂”之后,若溶液pH=0.5,溶液中c(H S)=0.1mol/L,理论上溶液
2
中c(Cu2+)=_______mol/L[计算结果保留两位有效数字]。
点燃
18.(14分)是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备CO +C 2CO (夹持装
2
置略去)。
b
已知:TiCl 易挥发,高温时能与O 反应,不与HCl反应,其他相关信息如下表所示:
4 2
熔点/℃ 沸点/℃ 密度/(gcm3) 水溶性
TiCl -24 136.4 1.7 易水解生成白色沉淀,能溶于有机溶剂
4
CCl -23 76.8 1.6 难溶于水
4
回答下列问题:
(1)装置A中仪器b的名称是_______,装置E中的试剂是_______(填试剂名称)。
(2)装置B中长导管的作用是_______。
(3)装置A中发生反应的离子方程式_______。
(4)在通入Cl 前,先打开开关k,从侧管持续通入一段时间的CO 气体的目的是_______。
2 2
(5)装置C中除生成TiCl 外,还生成一种气态不成盐氧化物,该反应的化学方程式为_______。
4
(6)制得的TiCl 中常含有少量CCl ,从混合液中分离出TiCl 操作的名称是_______。
4 4 4
(7)利用如图装置测定所得TiCl 的纯度:取mg产品加入烧瓶,向安全漏斗中加入适量蒸
4
馏水,待TiCl 充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴
4
0.1molL1K CrO 溶液作指示剂,用nmolL1AgNO 标准溶液滴定至终点,消耗标准溶
2 4 3
第 8 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}液VmL。
已知:常温下,K (AgCl)1.81010、K Ag CrO 1.11012,Ag CrO 呈砖红色,
sp sp 2 4 2 4
TiCl (2n)H O=TiO nH O4HCl。
4 2 2 2
①安全漏斗中的水在本实验中的作用除与TiCl 反应外,还有_______;
4
②滴定终点的判断方法是_______;
③产品的纯度为_______(用含m、n和V的代数式表示)。
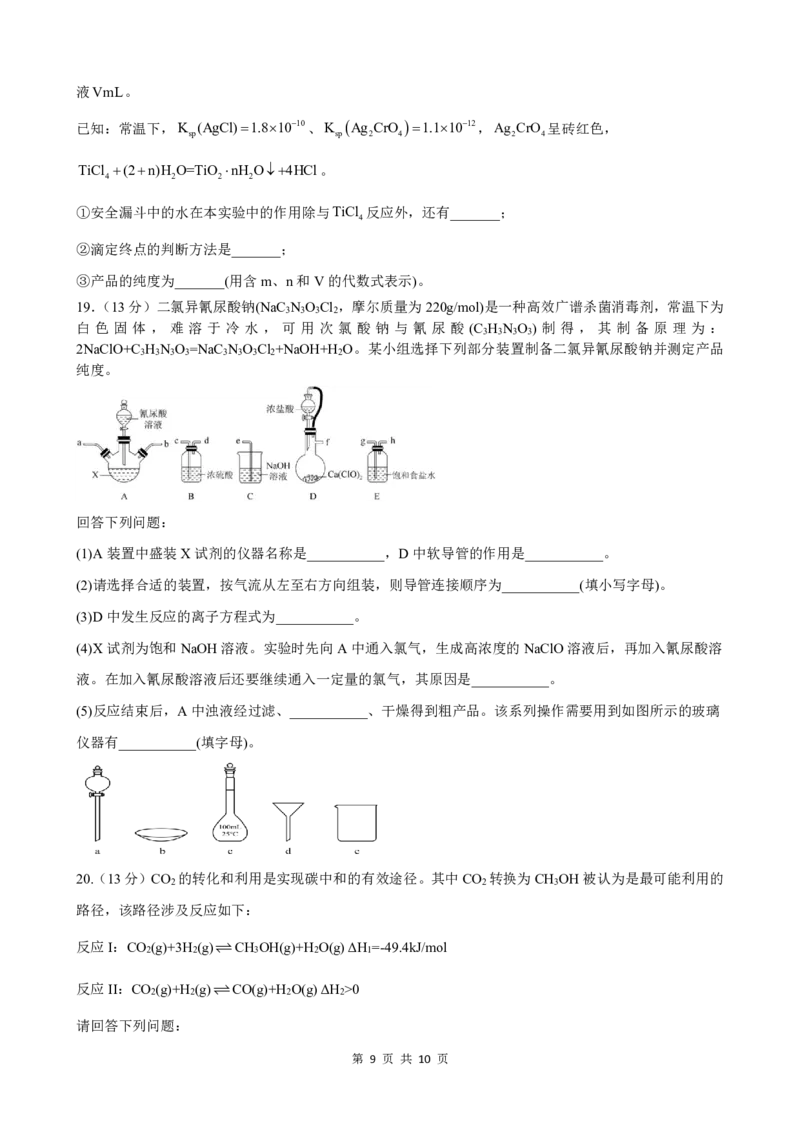
19.(13分)二氯异氰尿酸钠(NaC N O Cl ,摩尔质量为220g/mol)是一种高效广谱杀菌消毒剂,常温下为
3 3 3 2
白 色 固 体 , 难 溶 于 冷 水 , 可 用 次 氯 酸 钠 与 氰 尿 酸 (C H N O ) 制 得 , 其 制 备 原 理 为 :
3 3 3 3
2NaClO+C H N O =NaC N O Cl +NaOH+H O。某小组选择下列部分装置制备二氯异氰尿酸钠并测定产品
3 3 3 3 3 3 3 2 2
纯度。
回答下列问题:
(1)A装置中盛装X试剂的仪器名称是___________,D中软导管的作用是___________。
(2)请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为___________(填小写字母)。
(3)D中发生反应的离子方程式为___________。
(4)X试剂为饱和NaOH溶液。实验时先向A中通入氯气,生成高浓度的NaClO溶液后,再加入氰尿酸溶
液。在加入氰尿酸溶液后还要继续通入一定量的氯气,其原因是___________。
(5)反应结束后,A中浊液经过滤、___________、干燥得到粗产品。该系列操作需要用到如图所示的玻璃
仪器有___________(填字母)。
20.(13分)CO 的转化和利用是实现碳中和的有效途径。其中CO 转换为CH OH被认为是最可能利用的
2 2 3
路径,该路径涉及反应如下:
反应I:CO
2
(g)+3H
2
(g)CH
3
OH(g)+H
2
O(g)ΔH
1
=-49.4kJ/mol
反应II:CO
2
(g)+H
2
(g)CO(g)+H
2
O(g)ΔH
2
>0
请回答下列问题:
第 9 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}(1)若已知H 和CO的燃烧热,计算反应II的ΔH ,还需要的一个只与水有关的物理量为___________。
2 2
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图1(吸附在催化剂表面上的粒子用*标注,TS为
过渡态)。
1
完善该反应机理中相关的化学反应方程式:OH*+ H (g)=___________;以TS3为过渡态的反应,其正反
2
2
应活化能为___________eV。
(3)在恒温恒压下,CO 和H 按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得
2 2
相关数据如下表。
已知:①分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能:
nCH OH
②CH OH的选择性= 3 生成 100%
3
c(CO )
2 消耗
1.8MPa260°C
CO 平衡转化率 甲醇的选择性 达到平衡时间(s)
2
普通反应器(A) 25.0% 80.0% 10.0
分子筛膜催化反应器(B) a>25.0% 100.0% 8.0
①在普通反应器(A)中,下列能作为反应(反应I和反应II)达到平衡状态的判据是___________(填标号)。
A.气体压强不再变化 B.气体的密度不再改变。
C.v (CO )=3v (H )D.各物质浓度比不再改变
正 2 逆 2
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是___________;在反应器(B)
中,CO 的平衡转化率明显高于反应器(A),可能的原因是:___________。
2
③若反应器(A)中初始时n(CO )=1mol,反应I从开始到平衡态的平均反应速率v(CH OH)=___________mol/s;
2 3
反应II的化学平衡常数K (II)=___________(用最简的分数表示);
p
第 10 页 共 10 页
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}枣庄三中高三年级 10 月月考
化学试题答案
1-5 B、D、A、B、C 6-10 B、A、C、A、C 11-15 CD、BC、B、CD、D
△
16【答案】(10分,除标注外每空2分)(1)3Cl+6OH− 5Cl−+ClO−+3HO 缓慢通入
2 3 2
Cl(1分)
2
(2)NaClO碱性溶液(1分) 减少水合肼的挥发
(3)①测量溶液的pH,若pH约为4,停止通SO②加热浓缩、34℃以上趁热过滤
2
17.【答案】(10分 每空2分)
(1)稀硫酸(2)2AsO3-+5HS+6H+=AsS↓+2S↓+8HO
4 2 2 3 2
(3)Cl 将Fe2+氧化为Fe3+,Fe3++3HO⇌ Fe(OH)+3H+,加入的Ni(OH) 和H+反应,使Fe3+的水解
2 2 3 2
平衡向正反应方向移动,生成Fe(OH)(4)C(5)4.4×10-16
3
18题(14分 除标注外每空2分)
(1)蒸馏烧瓶(1分) 浓硫酸 (1分)(2)平衡气压,防止堵塞和倒吸
(3)2MnO+16H++10Cl=2Mn2++5Cl +8H O
4 2 2
(4)排除装置中的空气,防止TiCl 和O 反应 (1分)
4 2
Δ
(5)TiO +2C+2Cl TiCl +2CO(6)蒸馏(1分)
2 2 4
(7)①液封,吸收挥发的HCl气体,避免HCl的损失 ②当加入最后一滴AgNO 标准溶液时,
3
l9nV
溶液恰好出现砖红色沉淀,且半分钟不消失 ③ %
4m
19.(13分 每空2分)【答案】(1)三颈烧瓶(1分) 平衡气压,使液体能够顺利滴下
(2)fghabe(3)ClO-+2H+ Cl-=Cl + H O
2 2
(4)消耗过量的NaOH,促进NaCNOCl 的生成(5)冷水洗涤 de
3 3 3 2
20.(13分 除标注外每空2分)【答案】(1)H
2
O(g)H
2
O(l)的ΔH
(2)H O*(1分) 1.40(3)①BD ②反应I为放热反应、反应II为吸热反应,升高温度,反
2
应I逆向移动、反应II正向移动 在反应器(B)中,能分离出部分水蒸气,导致反应正向移
1
动 ③0.02
141
{#{QQABAYKQgggIABIAAQhCQwFACkGQkAEAAIoOQEAMsAAAgQNABAA=}#}