文档内容
山大附中高三第一次阶段性考试
化学试题
本试卷满分为100 分,考试用时90分钟。
注意事项:
1.答题前,考生先将自己的姓名、考生号、座号填写在相应位置,认真核对条形码上的姓名、
考生号和座号,并将条形码粘贴在指定位置上。
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用0.5毫米黑色
签字笔书写,字体工整、笔迹清楚。
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试题卷
上答题无效.保持卡面清洁,不折叠、不破损。
可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 23 Ag108 S 32 Cl35.5 Cr 52 Fe 56
一、选择题:每小题 2 分,共 30分。每小题只有一个选项符合题意。
1.下列叙述不涉及化学变化的是
A.用热纯碱液去除油污 B.用福尔马林制作动物标本
C.用双氧水清洗伤口 D.用焰色反应鉴别KCl溶液和NaCl溶液
2.下列物质应用错误的是
A.钾钠合金可用于原子反应堆导热剂 B.牺牲阳极保护法可采用废铜保护钢材
C.铝罐槽车可用于运输冷的浓硝酸 D.四氧化三铁用于制备激光打印墨
3.下列物质的化学性质与实际应用的对应关系正确的是
选项 化学性质 实际应用
A Al 是活泼金属 用铝罐贮运浓硝酸
B NaHCO 溶液显弱碱性 用作食品膨化剂
3
C Al(OH) 能与盐酸反应 用作胃酸中和剂
3
D Fe O 能被CO等还原 用作红色颜料
2 3
4.已知N 为阿伏加德罗常数,下列说法正确的是
A
A.25C时,1.0LpH13的BaOH 溶液中含有的 OH数目为0.2N
2 A
B.0.1molH C O 被氧化为CO ,转移的电子数为0.1N
2 2 4 2 A
C.32g乙醇和14g二甲醚(H COCH )组成的混合物中共价键数目为8N
3 3 A
高二化学暑假过关检测 第 1 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}D.lmolCaO 晶体所含离子总数为3N
2 A
5.LiAlH 是重要的还原剂与储氢材料,在120C下的干燥空气中相对稳定,其合成
4
方法为:NaAlH LiClLiAlH NaCl 。下列说法正确的是
4 4
A.该反应可以在水溶液中进行
B.基态锂原子的电子排布式为 1s22s1,核外电子的空间运动状态有2种
C.LiAlH 中Al 原子采用sp3杂化,AlH离子的空间构型为正方形
4 4
D.上述物质中电负性最大的元素与电负性最小的元素形成的化合物,其电子式为
Na
:H
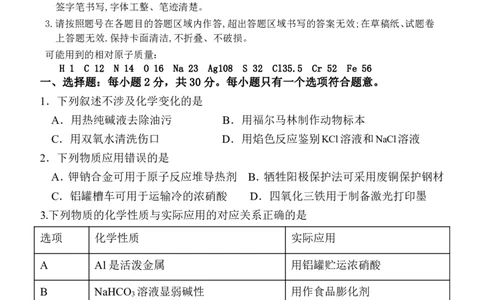
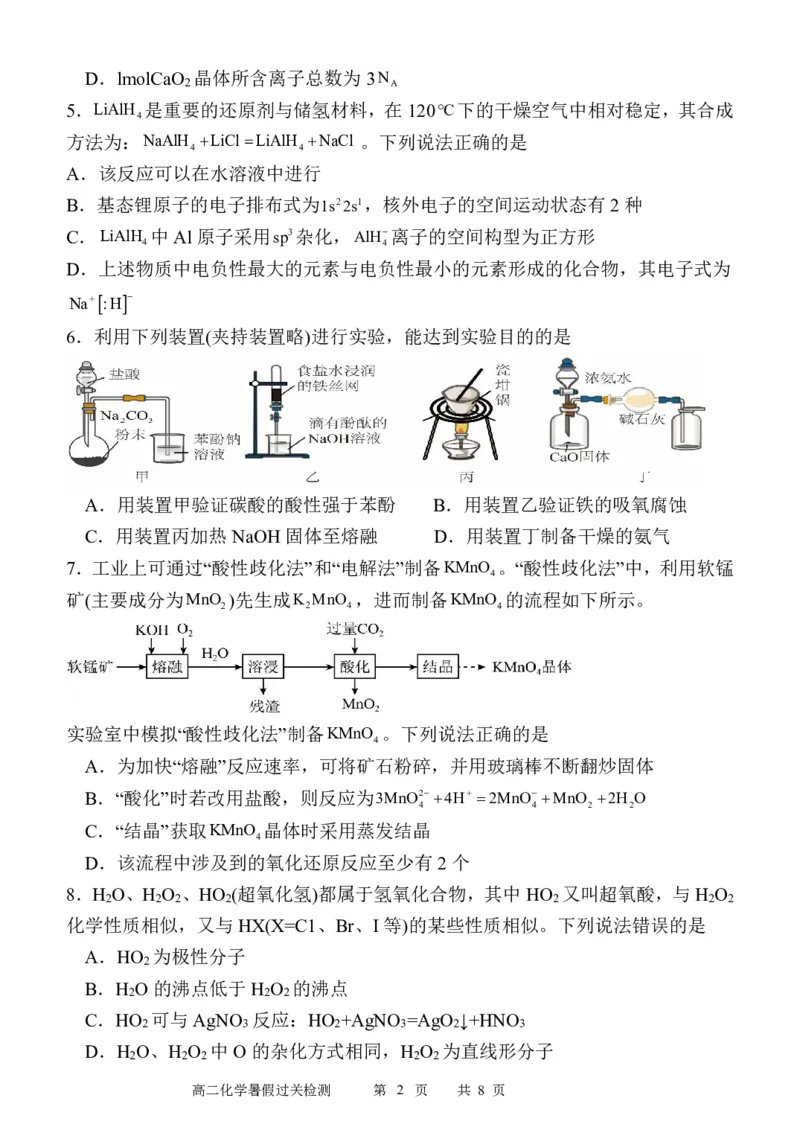
6.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用装置甲验证碳酸的酸性强于苯酚 B.用装置乙验证铁的吸氧腐蚀
C.用装置丙加热NaOH 固体至熔融 D.用装置丁制备干燥的氨气
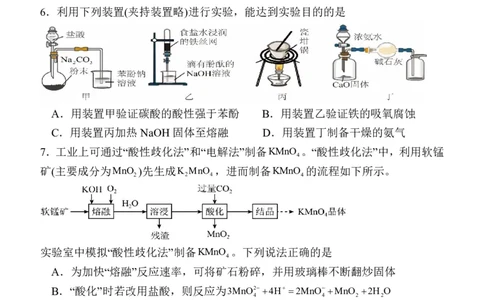
7.工业上可通过“酸性歧化法”和“电解法”制备KMnO 。“酸性歧化法”中,利用软锰
4
矿(主要成分为MnO )先生成K MnO ,进而制备KMnO 的流程如下所示。
2 2 4 4
实验室中模拟“酸性歧化法”制备KMnO 。下列说法正确的是
4
A.为加快“熔融”反应速率,可将矿石粉碎,并用玻璃棒不断翻炒固体
B.“酸化”时若改用盐酸,则反应为3MnO24H 2MnOMnO 2H O
4 4 2 2
C.“结晶”获取KMnO 晶体时采用蒸发结晶
4
D.该流程中涉及到的氧化还原反应至少有2个
8.H O、H O 、HO (超氧化氢)都属于氢氧化合物,其中HO 又叫超氧酸,与H O
2 2 2 2 2 2 2
化学性质相似,又与HX(X=C1、Br、I等)的某些性质相似。下列说法错误的是
A.HO 为极性分子
2
B.H O的沸点低于H O 的沸点
2 2 2
C.HO 可与AgNO 反应:HO +AgNO =AgO ↓+HNO
2 3 2 3 2 3
D.H O、H O 中O的杂化方式相同,H O 为直线形分子
2 2 2 2 2
高二化学暑假过关检测 第 2 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}9.三草酸合铁酸钾(K
3
FeC
2
O
4
3
3H
2
O)是制备铁触媒的主要原料。该配合物在光
光照
照下发生分解:2K Fe C O 3H O 3K C O +2FeC O +2CO ↑+6H O。下列说法
3 2 4 3 2 2 2 4 2 4 2 2
错误的是
A.Fe3+的最高能层电子排布式为 3d5 B.K 3 FeC 2 O 4 3 中铁离子的配位数为 6
C.C O2中 C 原子的杂化方式为 sp2 D.CO 分子中σ键和π键数目比为1:1
2 4 2
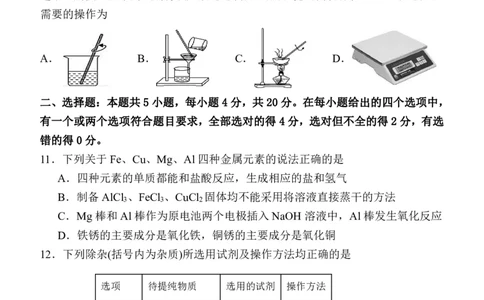
10.某补铁剂每片含硫酸亚铁0.3g(相当于铁60mg),为测定含铁量是否达标,某兴
趣小组用实验室常用试剂将铁元素通过氧化、碱化等步骤转化为Fe O ,该过程不
2 3
需要的操作为
A. B. C. D.
二、选择题:本题共5小题,每小题 4 分,共 20 分。在每小题给出的四个选项中,
有一个或两个选项符合题目要求,全部选对的得 4分,选对但不全的得 2 分,有选
错的得 0分。
11.下列关于Fe、Cu、Mg、Al 四种金属元素的说法正确的是
A.四种元素的单质都能和盐酸反应,生成相应的盐和氢气
B.制备AlCl 、FeCl 、CuCl 固体均不能采用将溶液直接蒸干的方法
3 3 2
C.Mg棒和Al 棒作为原电池两个电极插入NaOH 溶液中,Al 棒发生氧化反应
D.铁锈的主要成分是氧化铁,铜锈的主要成分是氧化铜
12.下列除杂(括号内为杂质)所选用试剂及操作方法均正确的是
选项 待提纯物质 选用的试剂 操作方法
A FeCu 稀硫酸 过滤
B CO SO NaOH溶液 洗气
2 2
C NaCl溶液I CCl 萃取分液
2 4
D NaClNa CO 稀盐酸 蒸发结晶
2 3
13.某低成本储能电池原理如下图所示。下列说法正确的是
高二化学暑假过关检测 第 3 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}A.放电时负极质量减小 B.储能过程中电能转变为化学能
C.放电时右侧 H通过质子交换膜移向左侧
D.放电总反应:PbSO2 2Fe3 PbSO 2Fe2
4 4
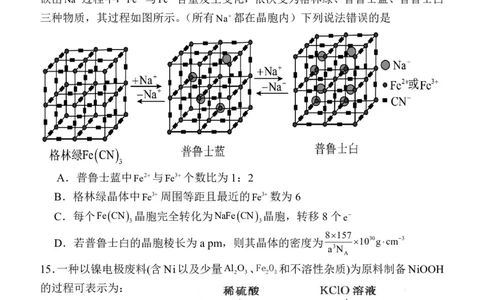
14.某水性钠离子电池电极材料由 Na、 Fe2、Fe3、 CN组成,其立方晶胞嵌入和
嵌出 Na过程中,Fe2与Fe3含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白
三种物质,其过程如图所示。(所有 Na都在晶胞内)下列说法错误的是
A.普鲁士蓝中Fe2与Fe3个数比为1:2
B.格林绿晶体中 Fe3周围等距且最近的 Fe3数为6
C.每个FeCN 晶胞完全转化为NaFeCN 晶胞,转移8个e
3 3
8157
D.若普鲁士白的晶胞棱长为apm,则其晶体的密度为 1030gcm3
a3N
A
15.一种以镍电极废料(含Ni以及少量Al O 、Fe O 和不溶性杂质)为原料制备NiOOH
2 3 2 3
的过程可表示为:
“酸浸”后溶液中的金属离子除Ni2外还有少量的 Al3和 Fe2等,下列说法错误的是
A.氧化性: Ni2 Fe3
B.提高酸浸率可采用升高温度或将废料粉碎
C.除杂过程包括:调节 pH,将 Al3和Fe2转化为沉淀,再过滤除去不溶性杂质
D.检验NiOOH 是否洗涤干净可取洗涤液加入盐酸酸化的BaCl 溶液
2
高二化学暑假过关检测 第 4 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}三.非选择题(共 5个大题,共 60分)
16.(11分)金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生
产,约在 1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应
电解
原理是 2NaCl(熔融) 2Na+Cl ↑。回答下列有关单质钠的问题:
2
(1)保存金属钠的正确方法是___________。
A.放在棕色瓶 B.放在细沙中 C.放在水中D.放在煤油中
(2)Na、NaOH 久置于空气中最终都变为 (填化学式)。
(3)除去碳酸钠粉末中混有的少量碳酸氢钠固体的最适宜的方法为 ,所
涉及到的化学方程式为 。
(4)工业上以NaCl、NH 、CO 等为原料先制得NaHCO ,反应的化学方程式为:
3 2 3
NaCl+NH +CO +H O=NaHCO ↓+NH Cl,进而生产纯碱。
3 2 2 3 4
某活动小组根据上述原理,制备碳酸氢钠。实验装置如图所示(夹持、固定用仪器未
画出)。
乙装置中的试剂是 ;实验中分离出NaHCO 晶体的操作是
3
(填分离操作名称)。
(5)已知该装置是一个电解池,使用时,先向水中加入一勺食盐。电解
过程中NaCl没有参与反应,请分析NaCl在整个装置中起到的作
用 。
17.(12分)某小组同学设计如下实验,研究亚铁盐与H O 溶液的反应。
2 2
【实验 1】试剂:酸化的0.5molL1FeSO 溶液(pH0.2),5%H O 溶液(pH5)
4 2 2
操作 现象
取2mL上述FeSO 溶液于试管中,加入 溶液立即变为棕黄色,稍后,产生气泡。测
4
5滴5%H O 溶液 得反应后溶液pH0.9
2 2
向反应后的溶液中加入KSCN溶液 溶液变红
高二化学暑假过关检测 第 5 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}(1)上述实验中H O 溶液与FeSO 溶液反应的离子方程式是 。
2 2 4
(2)产生气泡的原因是 。
【实验Ⅱ】试剂:未酸化的0.5molL1FeSO 溶液(pH3),5%H O 溶液(pH5)
4 2 2
操作 现象
溶液立即变为棕黄色,产生大量气泡,并放热,反
取2mL5%H O 溶液于试管中,
2 2
应混合物颜色加深且有浑浊。测得反应后溶液
加入 5滴上述FeSO 溶液
4
pH 1.4
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加
4molL1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe O ,经检验还含
2 3
有SO2。检验棕黄色沉淀中SO2的方法是 。
4 4
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H O 溶液氧化Fe2消耗 H ⅱ.Fe2氧化的产物发生了水解
2 2
①根据实验Ⅱ记录否定假设ⅰ,理由是 。
②实验验证假设ⅱ:取 ,加热,溶液变为红褐色,pH下降,证明假设ⅱ成
立。
(5)将FeSO 溶液加入H O 溶液后,产生红褐色胶体,反应的离子方程式
4 2 2
是: 。
18.(13分)阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K FeO
2 4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着 pH减小,稳定性下
降,与水反应放出氧气,K FeO 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,
2 4
同时不会产生有害物质。K FeO 与水反应还能产生具有强吸附性的Fe(OH) 胶体,
2 4 3
可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放 5mgK FeO 即可达到卫生标准
2 4
(1)将K FeO 与水反应的化学方程式补充完整:
2 4
_______K FeO +_______H O=_______Fe(OH) (胶体)+_______O ↑+_______KOH
2 4 2 3 2
(2)Na FeO 可通过多种方法得到。
2 4
高二化学暑假过关检测 第 6 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}Na FeO 可通过Fe(NO ) 溶液与NaClO 溶液在碱性条件下反应制备(NaClO被还
2 4 3 3
原为 NaCl),此反应的离子方程式为 ;Na FeO 可用
2 4
于氧化去除高氯(含高浓度Cl-)废水中的有机物。将Na FeO 溶液酸化时,FeO2迅
2 4 4
速分解而转化为Fe3+并放出O 。酸性溶液中FeO2的氧化性大于Cl 的氧化性。FeO2
2 4 2 4
处理高氯废水中的有机物需在碱性条件下进行,其原因
是 ;
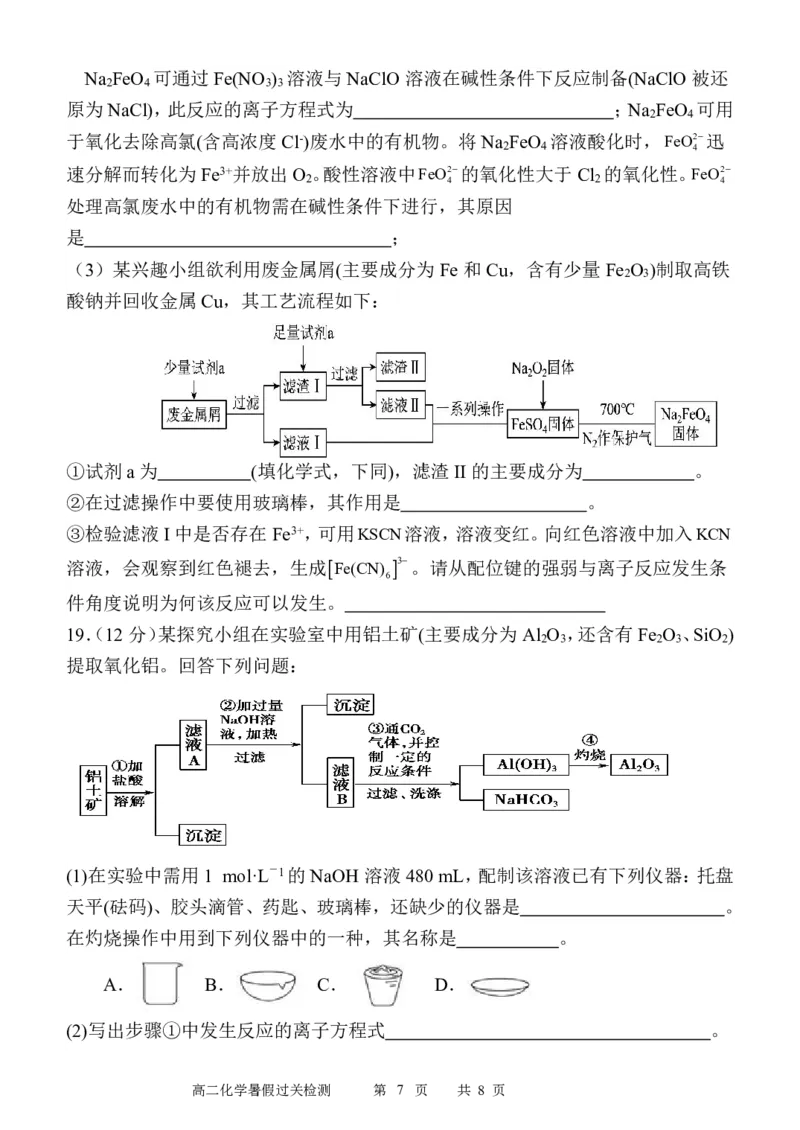
(3)某兴趣小组欲利用废金属屑(主要成分为Fe 和Cu,含有少量Fe O )制取高铁
2 3
酸钠并回收金属Cu,其工艺流程如下:
①试剂 a为 (填化学式,下同),滤渣II 的主要成分为 。
②在过滤操作中要使用玻璃棒,其作用是 。
③检验滤液 I中是否存在Fe3+,可用KSCN溶液,溶液变红。向红色溶液中加入KCN
溶液,会观察到红色褪去,生成
Fe(CN)
3。请从配位键的强弱与离子反应发生条
6
件角度说明为何该反应可以发生。
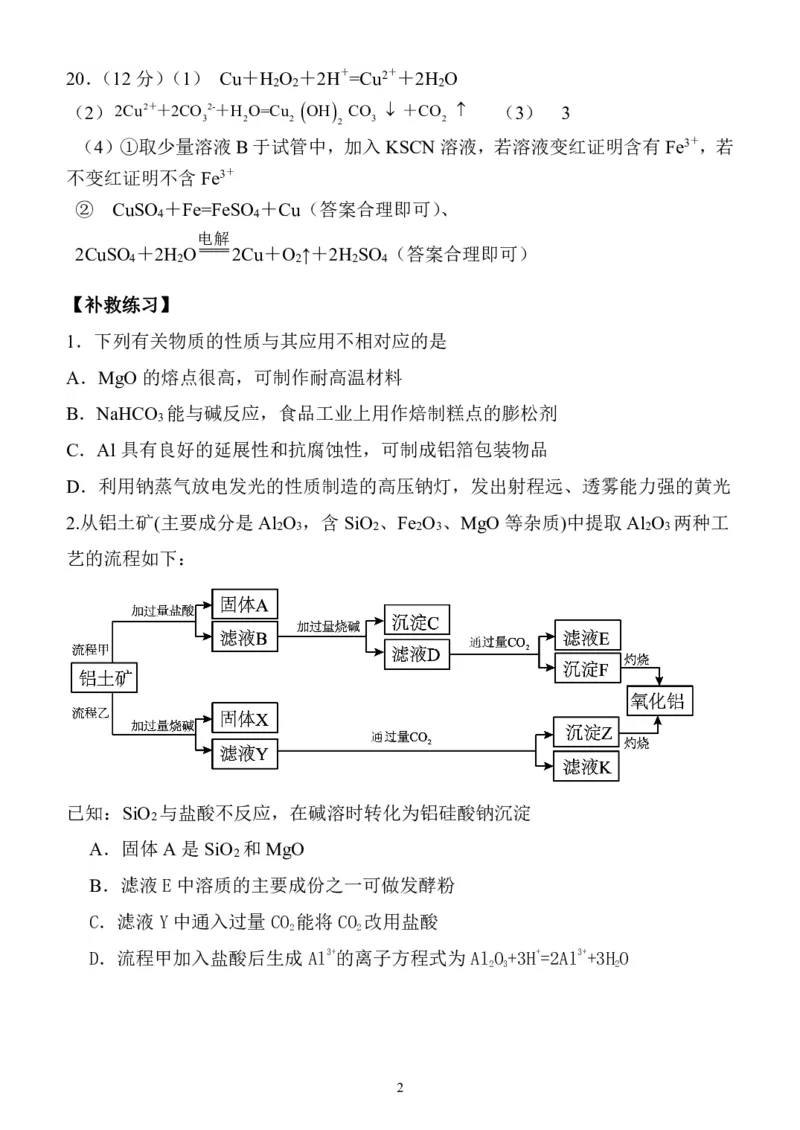
19.(12分)某探究小组在实验室中用铝土矿(主要成分为Al O ,还含有Fe O 、SiO )
2 3 2 3 2
提取氧化铝。回答下列问题:
(1)在实验中需用1 mol·L-1的NaOH 溶液480mL,配制该溶液已有下列仪器:托盘
天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 。
在灼烧操作中用到下列仪器中的一种,其名称是 。
A. B. C. D.
(2)写出步骤①中发生反应的离子方程式 。
高二化学暑假过关检测 第 7 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}(3)操作③中的洗涤操作如何进行? 。
(4)甲同学在实验室中用如图装置制备CO 气体,并通入滤液B 中制备Al(OH) 时,
2 3
结果没有产生预期现象。
乙同学分析认为:甲同学通入CO 的量不足是导
2
致实验失败的原因之一,你认为乙的分析是否合
理? 。若合理,请用离子方程式解释其原
因 (若你认为不
合理,该空不作答)。丙同学分析认为:甲同学通
入的 CO 中含有HCl 气体,也是导致实验失败的
2
原因,在实验中增加某装置可解决这个问题。请帮助丙同学画出该装置图,并注明
试剂名称 。
20.(12分)铜是生活中常见的金属,请回答下列问题:
(1)Cu 不活泼,通常情况下不与稀硫酸反应,但向Cu 和稀硫酸的混合物中滴入H O
2 2
溶液后,溶液很快变蓝色,试写出该反应的离子方程式: 。
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出Cu (OH) CO 绿色固体,试写出该反应
2 2 3
的离子方程式: 。
加热
(3)火法炼铜的原理为Cu S+O 2Cu+SO ,在反应中每生成1molCu,
2 2 2
转移 mol e-。
(4)据报道,有一种叫Thibacillus Ferroxidans 的细菌在有氧气存在的酸性溶液中,可
将黄铜矿 CuFeS 氧化成硫酸盐:4CuFeS +2H SO +17O =4CuSO +2Fe (SO ) +
2 2 2 4 2 4 2 4 3
2H O。利用反应后的溶液,按如下流程可制备胆矾(CuSO ·5H O):
2 4 2
①检验溶液 B 中 Fe3+是否被除尽的实验方法: 。
②在实验室中,设计两个原理不同的方案,从溶液B 中提炼金属铜(要求:一种方
案只用一个反应来完成)。写出两种方案中涉及的化学方程式:
方案一 ;方案二 。
高二化学暑假过关检测 第 8 页 共 8 页
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}高三第一次阶段性考试(化学答案)
一、选择题:本题共10 小题,每小题 2 分,共20 分,每小题只有一个选项符合题
目要求。
1--5.DBCCB 6--10.BDDAC
二、选择题:本题共 5 个小题,每小题 4 分,共 20 分。每小题有一个或两个选项
符合题意,全部选对得 4分,选对但不全的得 2分,有选错的得 0分。
11--15. BC 、CD、BD、A、A
三.非选择题(共 5个大题,共 60分)
16.(11分)(1)D (2)Na CO
2 3
Δ
(3) 加热 、 2NaHCO Na CO +H O+CO ↑
3 2 3 2 2
(4) 饱和碳酸氢钠溶液 、 过滤 (5)增加溶液的导电性
17.(12分)(1)2Fe2++2H++H O 2Fe3+ 2H O
2 2 2
(2)Fe3+催化下H O 分解生成O
2 2 2
(3)取加入盐酸后的黄色溶液少许于试管中,加入BaCl 溶液,产生白色沉淀,说
2
明棕黄色沉淀中含有SO2
4
(4)① 根据实验Ⅱ 记录反应后溶液pH =1.4,酸性增强,假设ⅰ中消耗氢离子,
酸性减弱,pH 应增大,故不合理 ② Fe (SO ) 溶液
2 4 3
(5)2Fe2++4H O+H O 2Fe(OH) (胶体) 2H+
2 2 2 3
18.(13分)(1)4、10、4、3、8;
(2)2Fe3 3ClO10OH 2FeO23Cl5H O ;
4 2
酸性条件下,FeO2
4
自身会分解,且会与 Cl反应产生Cl
2
(3) ①H
2
SO
4
、 Cu ② 引流 ③ CN的配位能力强于 SCN
19.(12分)(1)500mL容量瓶、烧杯 ; 坩埚
(2)Fe O +6H+===2Fe3++3H O,Al O +6H+===2Al3++3H O
2 3 2 2 3 2
(3)向过滤器中加入蒸馏水,使水刚好没过沉淀物,等水自然流尽后,重复操作
2~3次
(4)合理 ; 2OH-+CO ===CO 2-+H O
2 3 2
1
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}20.(12分)(1) Cu+H O +2H+=Cu2++2H O
2 2 2
(2)2Cu2++2CO 2-+H O=Cu OH CO +CO (3) 3
3 2 2 2 3 2
(4)①取少量溶液B于试管中,加入KSCN溶液,若溶液变红证明含有Fe3+,若
不变红证明不含Fe3+
② CuSO +Fe=FeSO +Cu(答案合理即可)、
4 4
电解
2CuSO +2H O 2Cu+O ↑+2H SO (答案合理即可)
4 2 2 2 4
【补救练习】
1.下列有关物质的性质与其应用不相对应的是
A.MgO 的熔点很高,可制作耐高温材料
B.NaHCO 能与碱反应,食品工业上用作焙制糕点的膨松剂
3
C.Al 具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
D.利用钠蒸气放电发光的性质制造的高压钠灯,发出射程远、透雾能力强的黄光
2.从铝土矿(主要成分是Al O ,含SiO 、Fe O 、MgO 等杂质)中提取Al O 两种工
2 3 2 2 3 2 3
艺的流程如下:
已知:SiO 与盐酸不反应,在碱溶时转化为铝硅酸钠沉淀
2
A.固体A是SiO 和MgO
2
B.滤液E中溶质的主要成份之一可做发酵粉
C.滤液 Y中通入过量CO 能将CO 改用盐酸
2 2
D.流程甲加入盐酸后生成Al3+的离子方程式为AlO+3H+=2Al3++3HO
2 3 2
2
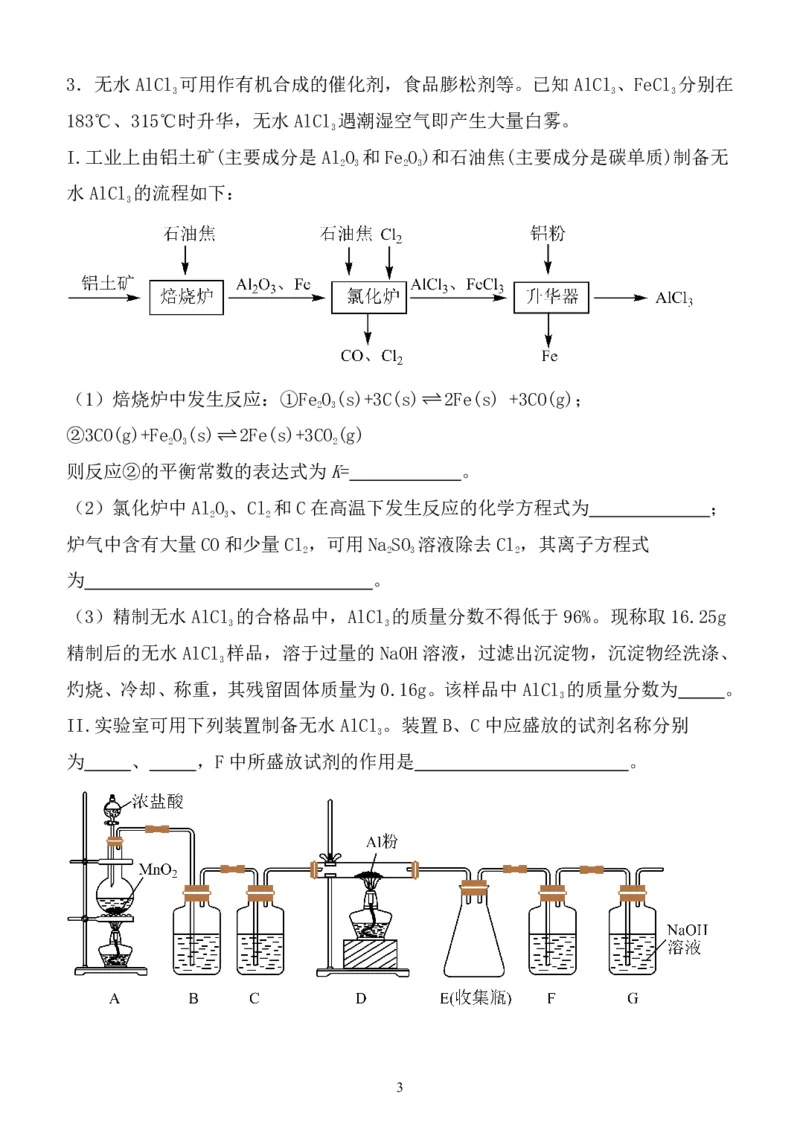
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}3.无水AlCl 可用作有机合成的催化剂,食品膨松剂等。已知AlCl、FeCl 分别在
3 3 3
183℃、315℃时升华,无水AlCl 遇潮湿空气即产生大量白雾。
3
I.工业上由铝土矿(主要成分是AlO 和Fe O)和石油焦(主要成分是碳单质)制备无
2 3 2 3
水AlCl 的流程如下:
3
(1)焙烧炉中发生反应:①FeO(s)+3C(s)2Fe(s) +3CO(g);
2 3
②3CO(g)+Fe O(s)2Fe(s)+3CO(g)
2 3 2
则反应②的平衡常数的表达式为K= 。
(2)氯化炉中 AlO、Cl 和C在高温下发生反应的化学方程式为 ;
2 3 2
炉气中含有大量CO和少量Cl,可用NaSO 溶液除去Cl,其离子方程式
2 2 3 2
为 。
(3)精制无水 AlCl 的合格品中,AlCl 的质量分数不得低于96%。现称取16.25g
3 3
精制后的无水 AlCl 样品,溶于过量的NaOH 溶液,过滤出沉淀物,沉淀物经洗涤、
3
灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl 的质量分数为 。
3
II.实验室可用下列装置制备无水AlCl。装置B、C中应盛放的试剂名称分别
3
为 、 ,F中所盛放试剂的作用是 。
3
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}4.金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的
相关知识回答下列问题:
(1)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na O 后,过滤,
2 2
将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
_______。
A.Mg2+ B.Fe2+ C.A13+ D.Cu2+
(2)高铁酸钠(Na FeO )是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分
2 4
为Fe 和Cu,含有少量 Fe O )制取高铁酸钠并回收金属 Cu,其工艺流程如下:
2 3
①试剂 a为 (填化学式,下同),滤渣II 的主要成分为 。
②在过滤操作中要使用玻璃棒,其作用是 。
③检验滤液 I中是否存在Fe3+的试剂是 。
700C
④制备Na FeO 的反应原理是:2FeSO +6Na O 2Na FeO +2Na O+2Na SO +O 。
2 4 4 2 2 2 4 2 2 4 2
当反应中转移电子总数约为 9.031023时,则生成Na
2
FeO
4
的物质的量为 mol。
(3)纳米铁粉可用于处理废水中的NO-。酸性条件下,纳米铁粉与废水中NO-反应生
3 3
成Fe3+与NH+,其反应的离子方程式是 。
4
4
{#{QQABKYQQggAgQABAABgCAQUyCgKQkBACCAgOgAAAMAAByBFABAA=}#}