文档内容
2022 年湖北省新高考联考协作体高三上学期起点考试
高三化学参考答案
一、单选题(每题有且只有一个正确选项,每小题3分,共45分)
1-5DCDDB 6-10CDBAB 11-15CABCC
二、非选择题(4小题,共55分)
16.(14分)
(1)NH ;SO
3 2
(2)取少量溶液于试管,向试管中加入NaOH溶液,加热,用湿润红色石蕊试纸靠近试管
口,若试纸变蓝,则证明有NH +
4
(3)CO 2-+2SO +H O=2HSO -+CO
3 2 2 3 2
(4)得到NaHSO 过饱和溶液
3
(5)低温蒸发(或减压蒸发,强调温度低即可); 冷却结晶;减少Na S O 在水中的溶解
2 2 5
(6)Na S O +H O+O =Na SO +H SO
2 2 5 2 2 2 4 2 4
17.(14分)
(1)将导管末端插入D中水面以下;将整个装置内的空气排净
(2)三颈烧瓶; Fe2++2HCO - =FeCO ↓+H O+CO ↑
3 3 2 2
(3)K 、K ; 关闭K 、K ,一段时间后打开K
1 3 1 3 2
(4)防止Fe(Ⅱ)被氧化
(5)减小乳酸亚铁溶解度,使之析出,提高产量
(6)否; 偏高,乳酸(根)也能被高锰酸钾氧化,消耗更多高锰酸钾,使铁元素的质
量分数偏高
18.(14分)
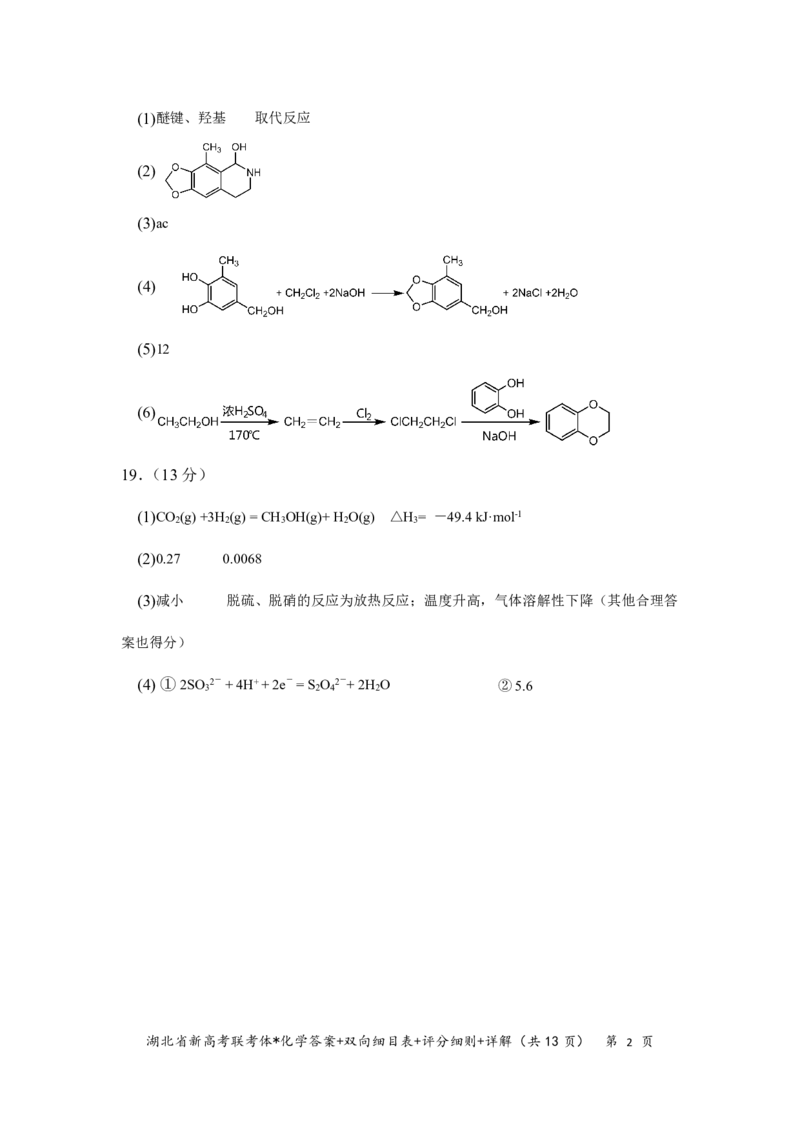
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 1 页(1)醚键、羟基 取代反应
(2)
(3)ac
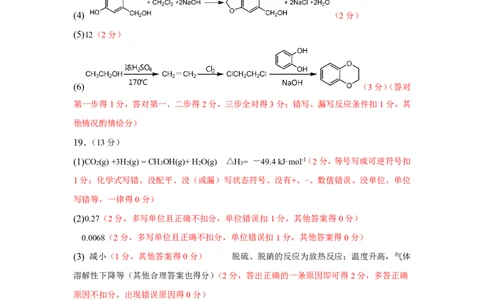
(4)
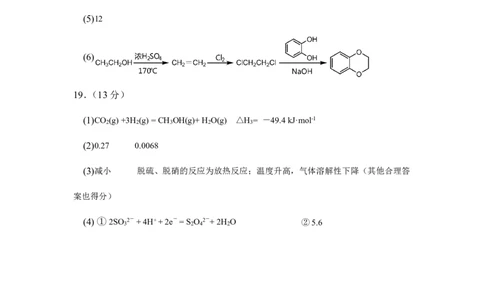
(5)12
(6)
19.(13分)
(1)CO (g)+3H (g)=CH OH(g)+H O(g) △H = -49.4kJ·mol-1
2 2 3 2 3
(2)0.27 0.0068
(3)减小 脱硫、脱硝的反应为放热反应;温度升高,气体溶解性下降(其他合理答
案也得分)
(4) ① 2SO 3 2- + 4H+ + 2e- = S 2 O 4 2-+ 2H 2 O ② 5.6
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 2 页2022 年湖北省新高考联考协作体高三上学期起点考试
高三化学评分细则
1-5DCDDB 6-10CDBAB 11-15CABCC
16.(14分)
(1) NH (1分); SO (1分)
3 2
(2)取少量溶液于试管,向试管中加入NaOH溶液,加热,用湿润红色石蕊试纸靠近试管口,
若试纸变蓝,则证明有NH +(2分,需强调取样,加热,加NaOH溶液以及用湿润红色
4
石蕊试纸,若没有则不给分,若没有实验现象则扣一分,NaOH可换成其他强碱)
(3)CO 2-+2SO +H O=2HSO -+CO(2分,化学计量数错误或化学式书写错误均不给分,若
3 2 2 3 2
CO 打气体符号则扣一分)
2
(4)得到NaHSO 过饱和溶液(2分,强调过饱和溶液)
3
(5)低温蒸发(1分,减压蒸发也可得分,强调温度低即可); 冷却结晶(1分);
减少Na S O 在水中的溶解(2分)
2 2 5
(6)Na S O +H O+O =Na SO +H SO (2分,化学计量数错误或化学式书写错误均不给
2 2 5 2 2 2 4 2 4
分)
17.(14分)
(1)将导管末端插入D中水面以下;将整个装置内的空气排净
(2分,需填写完整,少一项扣一分)
(2)三颈烧瓶(1分);
Fe2++2HCO - =FeCO ↓+H O+CO ↑(2分,化学计量数错误或化学式书写错误均不
3 3 2 2
给分,气体符号和沉淀符号少写一项扣一分)
(3)K 、K (1分); 关闭K 、K ,一段时间后打开K (2分,书写完整可得全分)
1 3 1 3 2
(4) 防止Fe(Ⅱ)被氧化(1分,写防止Fe2+被氧化也可得分)
(5)减小乳酸亚铁溶解度,使之析出,提高产量(2分,强调减小产物损耗)
(6)否(1分); 偏高,乳酸(根)也能被高锰酸钾氧化,消耗更多高锰酸钾,使铁元素
的质量分数偏高(2分)
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 3 页18.(14分)
(1)醚键、羟基 (2分,有错别字不得分) 取代反应(1分,只写“取代”不得分)
(2) (2分)
(3)ac(2分)(答对两个得2分,只选一个且正确得1分,选错、多选得0分)
(4) (2分)
(5)12(2分)
(6) (3分)(答对
第一步得1分,答对第一、二步得2分,三步全对得3分;错写、漏写反应条件扣1分,其
他情况酌情给分)
19.(13分)
(1)CO (g)+3H (g)=CH OH(g)+H O(g) △H = -49.4kJ·mol-1(2分,等号写成可逆符号扣
2 2 3 2 3
1分;化学式写错、没配平、没(或漏)写状态符号、没有+、-、数值错误、没单位、单位
写错等,一律得0分)
(2)0.27(2分,多写单位且正确不扣分,单位错误扣1分,其他答案得0分)
0.0068(2分,多写单位且正确不扣分,单位错误扣1分,其他答案得0分)
(3) 减小(1分,其他答案得0分) 脱硫、脱硝的反应为放热反应;温度升高,气体
溶解性下降等(其他合理答案也得分)(2分,答出正确的一条原因即可得2分,多答正确
原因不扣分,出现错误原因得0分)
(4)① 2SO 2- + 4H+ + 2e- = S O 2-+ 2H O (2 分) ②5.6(2 分,分式答案得 0 分)
3 2 4 2
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 4 页2022 年高三上学期起点考试试题双向细目表
姓名:方针、李锦羽、吴玲丽 电话:17371145935 科目 :化学 学校:天门中学
难 易
度
分
题号 题型 考点(知识点) 能力点 (难、 试题来源 评分标准
值
中 、
易)
化学与生活:合金、氮的 自创结合2022湖北卷1
记忆识别
1 选择题 3 固定、硅与二氧化硅用 易 课本必修一P77必修二
了解
途、维C的性质 P113
有机化学基础:酚的显
理解表达 自创改编结合2022全
2 选择题 3 色、加成反应、共面问 中
应用 国甲卷2题
题、核磁共振氢谱
化学应用元素化合物的
记忆识别 自创结合必修一课后
3 选择题 3 性质:铝与碱的反应、 易
了解 习题 P60P80
油脂的水解
离子共存:SO2-与H+、
2 3 理解表达 自创结合2022湖北卷4
4 选择题 3 Fe3+存在环境、水的电 中
应用 题和课本必修二P44
离、澄清透明
离子方程式书写:少量
理解表达 自创结合2022广东14
5 选择题 3 Cl与SO2-或FeI或石灰 中
2 3 2 应用 题和课本氯气方程
乳,醋酸和84消毒液
实验设计图:CO除杂
2 记忆识别 自创改编结合2022湖
HCl,定容胶头滴管,S、
6 选择题 3 了解实验 易 北卷6和课本周期律实
C、Si非金属性比较,
能力 验
NaO与简易启普发生器
2 2
结构基础知识信息题:
理解表达 自创结合课本选择性
信息液晶的各向异性弹
7 选择题 3 信息处理 中 必修二P69-72、P77和知
性、驱动因素、形状记
能力 网文献
忆、SiO的形态
2
N题:体积未知、反应
A
前后总分子数、sp3杂化 理解表达 自创改编结合2021湖
8 选择题 3 中
总原子数、重水和水质 应用 北卷N 题
A
子数比较
氧化还原反应:氧化剂、记忆识别 自创结合课后习题必
9 选择题 3 易
还原剂、用途、电子式 了解 修一P29P91
物质结构晶胞计算:化 理解表达 自创结合课本选择性
10 选择题 3 学式、最近距离、配位 应用计算 中 必修二P102和2022全
数 能力 国模拟预测结构题
11 选择题 3 元素化合物性质元素周记忆识别 易 自创结合课本选择性
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 5 页期律知识:非极性分子、了解 必修二P80资料
Mg与CO 反应、干冰升
2
华、氢键
综合应用 自创结合2022湖北卷
有机结构、电解质溶液
12 选择题 3 处理信息 中 12题和课本选择性必
理论信息题:共轭酸碱
的能力 修三P72
氨基钠的性质和反应机
理信息题:有机反应类 综合应用 自创结合2022湖北卷
13 选择题 3 型、氨基钠碱性还原性、理解信息 难 13题和课本选择性必
苯胺的碱性与反应、反 的能力 修三 P78
应机理
电化学和电解质溶液理
论:离子浓度大小比较、综合应用
自创改编结合2022湖
14 选择题 3 平衡常数和pH的计算、理解信息 难
南卷16题
再生离子反应、电催化 计算能力
阴极反应
电解质溶液图像信息
题:图像含义、等电点 综合应用 自创结合2022辽宁高
15 选择题 3 的离子数量关系、粒子 理解信息 难 考卷13题和等电点资
带电和移动、平衡常数 计算能 料
计算
侯氏制碱法;工业制备 自创结合2018全国卷
16(1)填空题 2 记忆识别 易 书写正确得两分
二氧化硫 Ⅰ
需强调取样,加热,加NaOH
溶液以及用湿润红色石蕊试
自创结合2018全国卷
16(2)填空题 2 NH +的检验 记忆识别 易 纸,若没有则不给分,若没
4 Ⅰ
有实验现象则扣一分,NaOH
可换成其他强碱
根据溶液环境合理推断 化学计量数错误或化学式书
自创结合2018全国卷
16(3)填空题 2 产物,书写陌生离子反 综合应用 难 写错误均不给分,若CO 打气
Ⅰ 2
应方程式 体符号则扣一分
自创结合2018全国卷 强调过饱和溶液,否则没有
16(4)填空题 2 工艺流程操作理解 综合应用 中
Ⅰ 分
实验操作;洗涤晶体方 自创结合2018全国卷 减压蒸发也可得分,强调温
16(5)填空题 4 综合应用 难
法 Ⅰ 度低即可
陌生氧化还原反应方程 自创结合2018全国卷 化学计量数错误或化学式书
16(6)填空题 2 综合应用 难
式的书写 Ⅰ 写错误均不给分
制备Fe(Ⅱ)防止被氧化 改编自2021·福建龙岩
17(1)填空题 2 记忆识别 易 需填写完整,少一项扣一分
的方法 市·高三一模
化学计量数错误或化学式书
仪器名称 记忆识别 改编自2021·福建龙岩
17(2)填空题 3 中 写错误均不给分,气体符号
陌生离子方程式书写 综合应用 市·高三一模
和沉淀符号少写一项扣一分
改编自2021·福建龙岩
17(3)填空题 3 实验操作 综合应用 难 书写完整可得全分
市·高三一模
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 6 页制备易被氧化物质的方 改编自2021·福建龙岩
17(4)填空题 1 记忆识别 易 写防止Fe2+被氧化也可得分
法 市·高三一模
改编自2021·福建龙岩
17(5)填空题 2 制备晶体的方法 综合应用 中 强调减小产物损耗
市·高三一模
理解表达 改编自2021·福建龙岩
17(6)填空题 3 产品元素含量的测定 难 书写合理即可得分
综合应用 市·高三一模
第一空有错别字不得分;第
18(1)填空题 2,1 官能团名称,反应类型 记忆识别 易 2022湖南模拟创新
二空只写“取代”不得分)
18(2)填空题 2 有机物结构简式 理解表达 中 2022湖南模拟创新 书写正确得2分
答对两个得2分,只选一个且
18(3)填空题 2 有机物官能团的性质 理解表达 中 2022湖南模拟创新 正确得1分,选错、多选得0
分
18(4)填空题 2 有机化学方程式的书写 理解表达 中 2022湖南模拟创新 书写正确得2分
18(5)填空题 2 同分异构体的书写 综合应用 难 2022湖南模拟创新 书写正确得2分
答对第一步得1分,答对第
一、二步得2分,三步全对得
18(6)填空题 3 有机物的转化 综合应用 难 2022湖南模拟创新
3分;错写、漏写反应条件扣
1分,其他情况酌情给分
等号写成可逆符号扣1分;化
学式写错、没配平、没(或
热化学方程式;盖斯定
19(1)填空题 2 计算能力 中 2021广东卷改编 漏)写状态符号、没有+、-、
律
数值错误、没单位、单位写
错等等,一律得0分
答案正确各得2分,多写单位
19(2)填空题 2,2 平衡常数和速率的计算 计算能力 难 2021辽宁卷改编 且正确不扣分,单位错误扣1
分
答出正确的一条原因即可得
图像处理
19(3)填空题 1,2 平衡常数与温度的关系 难 2022四川模拟改编 2分,多答正确原因不扣分,
能力
出现错误原因得0分
19(4)填空题 2,2 电解池原理 综合应用 中 2020贵阳模拟改编 第二空分式答案不得分
说明:试题来源应注明自创,改编,移用(改编和移用要注明出处)
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 7 页2022 年湖北省新高考联考协作体高三上学期起点考试
高三化学答案解析
1.答案D
解析:A硬铝是一种铝合金,属于混合物,不是铝单质,故A错误;
B.自然固氮是将N 转化为含氮化合物,不一定是转化为NH ,比如大气固氮是将N 会转
2 3 2
化为NO,B错误;
C.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于制造晶体管、集
成电路等,而二氧化硅常用于制造光导纤维,C错误;
D维生素C具有强还原性,能还原人体内的活性氧自由基,延缓衰老。故选D。
2、辅酶Q10能提高心肌功能,有效治疗各种心肌病、抗心律失常、心绞痛,心力衰竭,,
其结构简式如下。下列有关辅酶Q 的说法正确的是( )
10
2.答案:C
解析:A.辅酶Q 中没有酚羟基,不能与铁离子发生显色,A项错误;
10
B.辅酶Q 的结构简式可以表示为 ,
10
1分子辅酶Q10能与14个H 发生加成反应,B项错误;
2
C.碳碳双键和碳氧双键均为平面结构,故辅酶Q 中的四个氧原子可以在同一平面内,C项
10
正确;
D.分子中的重复部分就有不同的40种氢原子,应该有43组吸收峰,故D项错误。
3.答案D
解析:A.NaOH与铝粉反应产生氢气故应防明火,正确;
B.油脂在碱性环境下可以水解,加热能加速反应速率故B正确;
C.疏通剂中的强碱长时间存于管道会腐蚀管道,故C正确;
D.洁厕灵主要成分是HCl,会中和NaOH降低效果。故选D
4.答案D
解析:A.S O2-能与氢离子反应不能共存,A错;
2 3
B.铁离子应存在于酸性环境中,B错;
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 8 页
C.水电离产生的 c OH - 10 -12molL1的溶液既可能是酸性溶液也可能是碱性溶液,铝
离子不能存在于碱性环境,C错;
D.离子间不反应可以大量共存,故选D.
5.答案B
解析:A.亚硫酸根过量应该与生产的氢离子继续生成亚硫酸氢根,A错;
B.微溶物石灰乳不拆,B正确;
C.碘离子还原性强于亚铁离子,氯气先氧化碘离子,故C错;
D.醋酸为弱电解质不拆,D错。故选B
6.答案C
解析A.应使用饱和NaHCO 除去氯化氢杂质而不影响二氧化碳的量,A错;
3
B.配制溶液时胶头滴管不能伸入容量瓶瓶内,B错;
C.最高价氧化物对应的水化物酸性强弱可以比较非金属性强弱,C正确;
D.Na O 粉末颗粒小反应快,不能使用该启普发生器控制速率D错;故选C
2 2
7.答案D
解析:A液晶具有各向异性,文中介绍其具有弹性,故A正确;
B液晶的各向异性即在热电光磁等改变的情况下发生形变从而驱动,故B正确;
C液晶弹性体可以恢复到原来的形状即形状记忆功能,故C正确;
D液晶是介于液态和晶态之间的物质状态,固体SiO 有晶体和非晶体之分。故选D。
2
8.答案B
解析:A.溶液体积未知,阴离子数不能确定,A错;
B.32g甲醇为1mol,该分子中C和O均采取sp3杂化,故为2N ,B正确;
A
C.氢气和碘反应前后气体的物质的量不变,所以分子总数等于原来之和为2N ,C错;
A
D.1mol重水和1mol水含有相同质子10N ,D错。故选B.
A
9.答案A
解析:A.碳元素中的同位素原子14C 可用于考古学,A项正确;
B.该反应的氧化剂为KNO 和S,化合价降低被还原做氧化剂,B项错;
3
C.该反应的还原剂为C,化合价升高被氧化做还原剂,C项错;
D.氮气的电子式左右两个氮原子上还分别缺一对孤电子对,D项错。故选A
10.答案B
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 9 页解析:A.通过晶胞为类似NaCl可计算该物质中的化学式为TiN ,A项正确;
B.两个Ti的最近距离是晶胞面对角线的一半即 2apm,B项错误;
C.Ti的配位数类似NaCl上下左右前后为6,C项正确;
D.与N距离相等且最近的N似NaCl有三个面,每个面有4各共有12个,D正确。故选B.
11.答案C
解析:A.干冰为CO 直线形分子为非极性分子,A项正确;
2
B.该实验能继续燃烧说明干冰易升华的特性,B项正确;
C.干冰为CO 存在共价键,不存在氢键,并且氢键不是化学键,C项错误;
2
D.该实验能继续燃烧即镁粉与二氧化碳能发生剧烈的发光发热的化学反应,D正确。故选
C.
12.答案A
解析:A.根据分析,H C H O -是H C H O 的共轭碱,是HC H O 2-的共轭酸,说明其既
2 6 5 7 3 6 5 7 6 5 7
是酸又是碱,故A正确;
B.根据定义可推知,H O+是水的共轭酸,故B错误;
3
C.根据分析,H C H O -的共轭碱是HC H O 2-,故C错误;
2 6 5 7 6 5 7
D.根据分析,H C H O -的共轭酸为H C H O ,故D错误;答案选A。
2 6 5 7 3 6 5 7
13.B
解析:A.有机反应机理中反应①是氯苯上C-Cl断裂,被-NH 取代Cl,属于取代反应;反
2
应②脱去1分子HCl,属于消去反应;反应③属于加成反应;A正确。
B.氨基钠有腐蚀性是因为其强碱性,其粉末易燃、易爆是因为其具有强的还原性,易被氧
化;B错误;
C.苯胺官能团为氨基,具有碱性,能与盐酸反应生产可溶性苯胺盐酸盐;C正确;
D.氯苯与氨基钠在液氨中反应,支持反应必定经过中间体苯炔这一步的事实是:产物苯胺
有两种,氨基连在14C上和连在相邻的12C上的一样多,D正确;故选B。
14.答案C
c(CO2)c(H)
解析:A.由K 3 可知, ,则该
a2 c(HCO)
3
溶液的pH=11,A正确;
B. 再生塔中KHCO 受热分解生成K CO 、H O和CO ,该反应的离子方程式为
3 2 3 2 2
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 10页Δ
2HCO- CO ↑+CO2- +H O,B正确;
3 2 3 2
C.等物质的量混合后根据k值可知K >K ,c(HCO -)>c(CO 2-),故C错;
h1 a1 3 3
D.利用电化学原理,将CO 电催化还原为C H ,阴极上发生还原反应,阳极上水放电生成
2 2 4
氧气和H+,H+通过质子交换膜迁移到阴极区参与反应生成乙烯,铂电极和Ag/AgCl电极均
为阴极,在电解过程中AgCl可以转化为Ag,则阴极的电极反应式为
2CO +12e-+12H+=C H +4H O、AgCl+e-=Ag+Cl-,D正确。
2 2 4 2
15.C
解析:A.氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧
根离子反应,故曲线a表示 NH+CH COOH的分布分数随溶液pH的变化,曲b表示
3 2
NH+CH COO-的分布分数随溶液pH的变化,曲线c表示NH CH COO-的分布分数随溶液pH
3 2 2 2
的变化,故A错;
B.由题知,等电点时,甘氨酸所带正负电荷正好相等,所以主要以NH+CH COOH-形式存在,
3 2
在电场中不发生移动现象,则NH+CH COOH的量应该等于NH CH COO-的量,故三者数
3 2 2 2
量关系为NH+CH COO->NH+CH COOH=NH CH COO-;B.错;
3 2 3 2 2 2
C.甘氨酸的等电点为5.97,为酸性,说明甘氨酸更易解离H+,更易解离的是羧基;在pH
小于5.97的溶液中,甘氨酸的解离向NH+CH COOH方向移动,带有净正电荷,在电场中
3 2
将向阴极移动;C.错;
c NH+CH COOH c OH-
D.NH
3
+CH
2
COO-+H
2
ONH
3
+CH
2
COOH+OH-的平衡常数K=
c
3
NH
2
+CH COO-
,
3 2
25℃时,根据a,b曲线交点坐标(2.35,0.50)可知,pH=2.35时,
c NH
3
+CH
2
COO- =c NH
3
+CH
2
COOH ,则K=c OH- =
c
K
H
w + =10-11.65 ,故D错;故选C.
16.(1)NH ;SO
3 2
分析:反应I、Ⅱ是通过侯氏制碱法制备碳酸钠,反应I制备NaHCO 的化学方程式为
3
NaClCO NH H O=NaHCO NH Cl
2 3 2 3 4 ,反应时先通入氨气,再通入CO 2 ,反应Ⅱ为
NaHCO 加热分解生成Na CO 。FeS 煅烧生成气体SO 。
3 2 3 2 2
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 11页(2)取少量溶液于试管,向试管中加入NaOH溶液,加热,用湿润红色石蕊试纸靠近试管
口,若试纸变蓝,则证明有NH +
4
分析:X离子为NH +。
4
(3)CO 2-+2SO +H O=2HSO -+CO
3 2 2 3 2
分析:向饱和Na CO 溶液中通入SO ,且控制pH=4.1,由题意是为了制备NaHSO 。
2 3 2 3
(4)得到NaHSO 过饱和溶液
3
分析:由于反应Ⅲ得到的NaHSO 不是过饱和溶液,后加碳酸钠固体、并再次充入SO 的目
3 2
的,是为了得到NaHSO 过饱和溶液,结晶得Na S O 晶体。
3 2 2 5
(5)低温蒸发(或减压蒸发,强调温度低即可); 冷却结晶;减少Na S O 在水中的溶解
2 2 5
分析:Na S O 在空气中易氧化、受热易分解,蒸发时需强调低温蒸发;其中洗涤Na S O
2 2 5 2 2 5
时依次用饱和SO 水溶液、无水乙醇,饱和SO 水溶液洗涤的目的是减少Na S O 在水中的
2 2 2 2 5
溶解,减少产品损失。
(6)Na S O +H O+O =Na SO +H SO
2 2 5 2 2 2 4 2 4
分析:实验制得的Na S O 固体中含有少量Na SO 杂质,其可能的原因是Na S O 被空气
2 2 5 2 4 2 2 5
中氧气氧化生成硫酸钠杂质。
17.(1)将导管末端插入D中水面以下;将整个装置内的空气排净
分析:Fe(Ⅱ)易被氧化,制备硫酸亚铁前需要排尽装置内空气,导管末端插入D中水面以下
可形成液封,防止空气进入装置。
(2)三颈烧瓶;Fe2++2HCO -=FeCO ↓+H O+CO ↑
3 3 2 2
分析:C装置中FeSO 和NH HCO 发生反应。
4 4 3
(3)K 、K ; 关闭K 、K ,一段时间后打开K
1 3 1 3 2
分析:首先关闭活塞K ,打开活塞K 、K ,目的是发生反应制备Fe2+,利用产生的氢气排
2 1 3
净装置内的空气,防止Fe2+被氧化;关闭活塞K ,反一段时间后,关闭活塞K ,打开活塞
1 3
K ,利用生成氢气,使B装置中气压增大,将B装置中的硫酸亚铁溶液压入C中,产生FeCO
2 3
沉淀。
(4)防止Fe(Ⅱ)被氧化
分析:Fe2+容易被氧化为Fe3+,加入铁粉可将Fe3+还原为Fe2+。
(5)减小乳酸亚铁溶解度,使之析出,提高产量
分析:乳酸亚铁晶体易溶于水,几乎不溶于乙醇,故加入乙醇可让乳酸亚铁析出更多,提高
产量。
(6)否; 偏高,乳酸(根)也能被高锰酸钾氧化,消耗更多高锰酸钾,使铁元素的质量
分数偏高
分析:乳酸(根)中含有羟基,也可以被酸性高锰酸钾溶液氧化,导致消耗高锰酸钾的量增
大,使计算所得乳酸亚铁的质量偏大。
18.解析:(1)由D的结构可知应在羟基的邻位进行取代反应
(2)由I的结构和已知信息b倒推可知H的结构为:
(3)物质B中含酚羟基,与FeCl 溶液发生显色反应;A中不含醛基,不能发生银镜反应,I
3
中与羟基相连的碳为手性碳原子;I的分子式为:C H NO 故a,c正确
12 15 3,
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 12页(4)C生成D的反应方程式:
(5)由条件a可知有羟基直接连在苯环上,其余的C,O原子单键连接成一个取代基:—OCHCH,
2 3
—CHOCH,—CHCHOH,—CH(OH)CH,分别连在酚羟基的邻、间、对位上,共12种。
2 3 2 2 3
(6)合成路线为:
19解析:(1)由盖斯定律可知:CO(g) +3H(g) = CHOH(g)+ HO(g) △H=-49.4 kJ·mol-1。
2 2 3 2 3
(2)设起始投入xmolCO 和4xmolH ,平衡时CO 的转化率为60%,CH 选择性为50%,则平
2 2 2 4
衡时有0.3xmolCH;0.3xmolCO;0.9xmolHO;0.4xmolCO;2.5xmolH;
4 2 2 2
K=P(CO)×P(HO)/[P(CO)×P(H)]=(0.3x÷4.4x)×(0.9x÷4.4x)/[(0.4x÷4.4x)×(2.5x
P 2 2 2
÷4.4x)]=0.27;CH4的分压变化为(0.3x÷4.4x)×1 - 0 = 0.068MPa,所以用CH 的分压
4
变化表示的速率为:0.0068MPa·min-1
(3)由图可知,纵坐标为平衡分压的负对数,温度升高,纵坐标减小,平衡分压增大,平
衡逆向移动,所以平衡常数减小,依据勒夏特列原理,反应正向放热,温度高气体溶解度减
小也能导致气体分压增加。(4)①由图可知阴极区SO2-生成S O2-,结合阴极得电子书写出
3 2 4
电极反应式:2SO2-+4H++2e-=S O2-+2H O。②NO转化为N 得电子数与电路中转移电子数相
3 2 4 2 2
等,计算可得NO标况下体积V=0.5÷2×22.4=5.6L。
湖北省新高考联考体*化学答案+双向细目表+评分细则+详解(共13页) 第 13页