文档内容
秘密★启用前
2023-2024 学年上期三校联合考试(高 2024 届)
化学试题卷
注意事项:
1.考试时间:75分钟,满分:100分。
2.所有题目必须在答题卡上作答,在试题卷、草稿纸上答题无效。
3.需要填涂的地方,一律用2B铅笔涂满涂黑。需要书写的地方一律用0.5MM黑色签字笔。
4.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。
5.考试结束后,将试题卷和答题卡一并交回。
6.可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ca-40 As-75
Ga-70
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
个选项符合题目要求。
1.2022年10月31日,搭载空间站梦天实验舱的长征五号B遥四运载火箭,在中国文昌
航天发射场准时点火发射成功,下列说法不正确的( )
A.为实验舱提供能量的砷化镓太阳能电池板也可以用单质硅代替
B.具备隔热抗辐射性能的实验舱舷窗玻璃属于传统无机非金属材料
C.火箭箭体使用铝合金材料,可一定程度上减轻火箭的质量
D.运载火箭采用液氢作为燃料,原因是单位质量的燃料完全燃烧时氢气放热较多
2.下列化学用语或图示表达正确的是( )
A.CH 的球棍模型:
4
B.CCl 的电子式:
4
C.丁二烯的键线式:
D.基态Cr原子的价层电子轨道表达式:
3.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.0.1mol肼N H 含有的孤电子对数为0.2N
2 4 A
B.1mol乙酸乙酯在酸性条件下水解,生成乙醇的分子数为N
A
C.常温下,pH=12的NaOH溶液中,OH-的数目为10-2N
A
D.电解饱和食盐水时,若阴阳两极产生气体的总体积为44.8L,则转移电子数为2N
A
试卷第1页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}4.下列离子在指定溶液中一定能大量共存的是
A.有NO存在的强酸性溶液中:NH+、Ba2+、Fe2+、Br-
3 4
B.能使甲基橙变红的溶液中:Na、K、SiO2、S2
3
C.由水电离的c(H+)=10-12mol·L-1的溶液:K+、Ba2+、Cl-、Br-
D.浓氨水中:Ba2、Cu2、Cl、NO
3
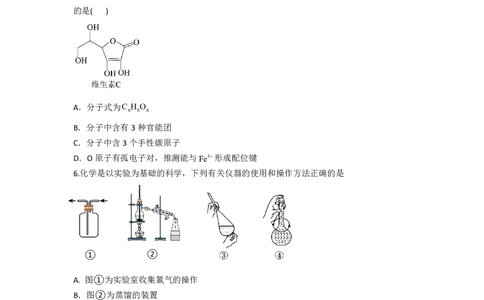
5.汉字传承的载体之一、出土后竹简中的木质素(多元酚)与Fe3+发生配位反应,导致字迹颜
色变深难以辨认,使用维生素C修复可使竹简变回浅色。下列关于维生素C的说法不正确
的是( )
A.分子式为C H O
6 8 6
B.分子中含有3种官能团
C.分子中含3个手性碳原子
D.O原子有孤电子对,推测能与Fe3形成配位键
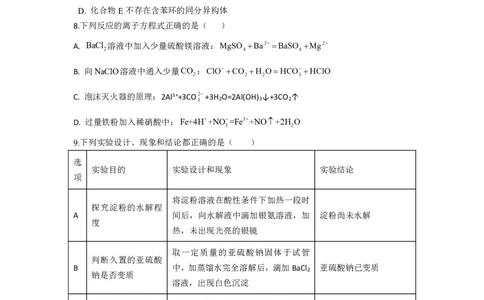
6.化学是以实验为基础的科学,下列有关仪器的使用和操作方法正确的是
① ②
A. 图①为实验室收集氯气的操作
B.图②为蒸馏的装置
C.图③为用四氯化碳萃取碘水中的碘,振荡,放气
D.图④配制溶液定容后摇匀
7.化合物E是一种药用中间体,合成路线如图所示。下列说法正确的是( )
试卷第2页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}A. 化合物A可与NaOH溶液发生反应
B. 化合物A转化成B,A发生还原反应
C. B与C互为同系物
D. 化合物E不存在含苯环的同分异构体
8.下列反应的离子方程式正确的是( )
A. BaCl 溶液中加入少量硫酸镁溶液:MgSO Ba2 BaSO Mg2
2 4 4
B. 向NaClO溶液中通入少量CO :ClOCO H OHCOHClO
2 2 2 3
C. 泡沫灭火器的原理:2Al3++3CO2+3H O=2Al(OH) ↓+3CO ↑
3 2 3 2
D. 过量铁粉加入稀硝酸中:Fe+4H++NO=Fe3++NO+2H O
3 2
9.下列实验设计、现象和结论都正确的是( )
选
实验目的 实验设计和现象 实验结论
项
将淀粉溶液在酸性条件下加热一段时
探究淀粉的水解程
A 间后,向水解液中滴加银氨溶液,加 淀粉尚未水解
度
热,未出现光亮的银镜
取一定质量的亚硫酸钠固体于试管
判断久置的亚硫酸
B 中,加蒸馏水完全溶解后,滴加BaCl 亚硫酸钠已变质
2
钠是否变质
溶液,出现白色沉淀
检验溶液中是否含 向待测液中通入氯气并加入 KSCN 溶
C 溶液中含有Fe2+
Fe2+ 液,溶液变红
探究 AlO 和 HSO 向NaAlO 溶液中滴加NaHSO 溶液, 溶液中AlO结合H的能
2 3 2 3 2
D
反应原理 有白色沉淀生成 力比SO2强
3
10..A、B、C、D、E为20号以前的元素,原子序数逐渐增大。A元素的原子最外层电子排布
式为nsnnpn;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基
试卷第3页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高
能级的电子对数等于其最高能层的电子层数。下列说法正确的是( )
A.简单氢化物的沸点:DCBA
B.同周期元素第一电离能小于C的有5种
C.氧化物对应水化物的酸性:DBA
D.A、D和C、E形成的化合物中可能均含有非极性共价键
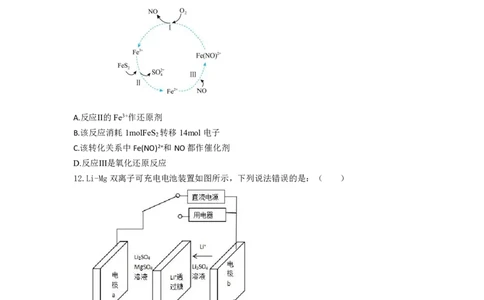
11. 在 酸 性 条 件 下 , 黄 铁 矿 ( ) 催 化 氧 化 的 反 应 方 程 式 为 :
2FeS +7O +2H O=2Fe2++4SO 2-+4H+ 实现该反应的物质间转化如图所示。下列分析正确的是
2 2 2 4
( )
A.反应Ⅱ的Fe3+作还原剂
B.该反应消耗1molFeS 转移14mol电子
2
C.该转化关系中Fe(NO)2+和NO都作催化剂
D.反应Ⅲ是氧化还原反应
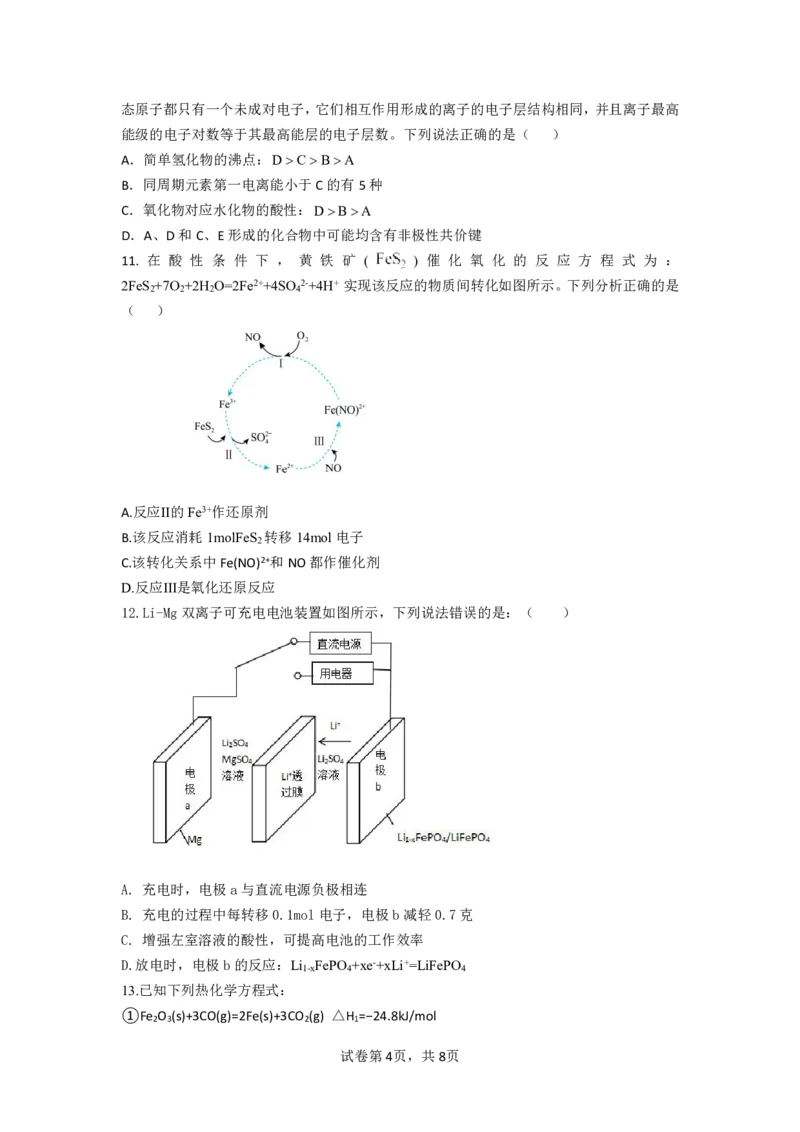
12.Li-Mg双离子可充电电池装置如图所示,下列说法错误的是:( )
A. 充电时,电极a与直流电源负极相连
B. 充电的过程中每转移0.1mol电子,电极b减轻0.7克
C. 增强左室溶液的酸性,可提高电池的工作效率
D.放电时,电极b的反应:Li FePO +xe-+xLi+=LiFePO
1-x 4 4
13.已知下列热化学方程式:
①Fe O (s)+3CO(g)=2Fe(s)+3CO (g) △H =−24.8kJ/mol
2 3 2 1
试卷第4页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}1 2 1
②Fe O (s)+ CO(g)= Fe O (s)+ CO (g) △H =−15.73kJ/mol
2 3 3 4 2 2
3 3 3
③Fe O (s)+CO(g)=3FeO(s)+CO (g) △H =640.4kJ/mol
3 4 2 3
则14gCO气体还原足量FeO固体生成CO 气体时对应的△H约为( )
2
A.−218kJ/mol B.−109kJ/mol C.+218kJ/mol D.+109kJ/mol
14.砷化镓是一种半导体材料,其晶胞结构如图所示,其晶胞参数为anm,晶胞密度为
gcm3。下列说法正确的是( )
A.As位于元素周期表d区
B.砷化镓化学式为GaAs
2
2a
C.Ga与As原子的最近距离为 nm
4
5.81023
D.阿伏加德罗常数可表示为 mol1
a3
二、非选择题:本题共4个小题,共58分
15.(14分)丰富的元素化合物具有丰富的实际用途,完成下列问题。
(1)11.7gNaCl溶于水形成500mL溶液,其物质的量浓度为 mol/L;标况下,
6.72LNH 的质量为 g。
3
(2)在工业上次磷酸(H PO )常用于化学镀银,发生的反应为:4Ag++H PO +2H O=4Ag↓+
3 2 3 2 2
H PO +4H+,请回答下列问题:
3 4
①H PO 中P元素的化合价为 ;反应中H PO 被 填“氧化”或“还原” 。
3 2 3 2
②工业上也可以用电镀的方法镀银,阳极的电极反应式为 。
③H PO 是一元弱酸,其与足量NaOH溶液反应的离子方程式为 。
3 2
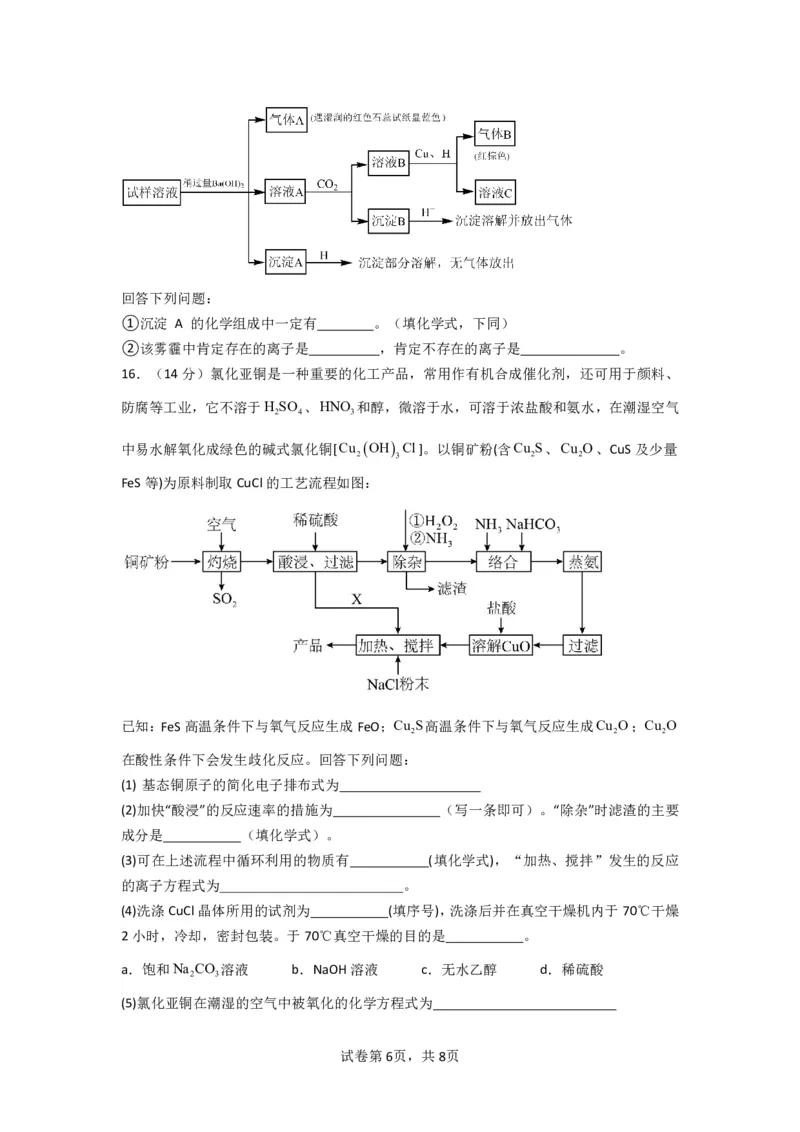
(3)雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有苯、甲苯和如下可溶性无机
离子:K+、NH+、Mg2+、Al3+、SO2-、NO-、Cl-、HCO-。某研究小组收集了该地区的雾霾,
4 4 3 3
经必要的预处理后得到试样溶液,设计并完成了如下实验。
试卷第5页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}回答下列问题:
①沉淀 A 的化学组成中一定有 。(填化学式,下同)
②该雾霾中肯定存在的离子是 ,肯定不存在的离子是 。
16.(14分)氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、
防腐等工业,它不溶于H SO 、HNO 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气
2 4 3
中易水解氧化成绿色的碱式氯化铜[Cu OH Cl]。以铜矿粉(含Cu S、Cu O、CuS及少量
2 3 2 2
FeS等)为原料制取CuCl的工艺流程如图:
已知:FeS高温条件下与氧气反应生成FeO;Cu S高温条件下与氧气反应生成Cu O;Cu O
2 2 2
在酸性条件下会发生歧化反应。回答下列问题:
(1) 基态铜原子的简化电子排布式为
(2)加快“酸浸”的反应速率的措施为 (写一条即可)。“除杂”时滤渣的主要
成分是 (填化学式)。
(3)可在上述流程中循环利用的物质有 (填化学式),“加热、搅拌”发生的反应
的离子方程式为 。
(4)洗涤CuCl晶体所用的试剂为 (填序号),洗涤后并在真空干燥机内于70℃干燥
2小时,冷却,密封包装。于70℃真空干燥的目的是 。
a.饱和Na CO 溶液 b.NaOH溶液 c.无水乙醇 d.稀硫酸
2 3
(5)氯化亚铜在潮湿的空气中被氧化的化学方程式为
试卷第6页,共8页
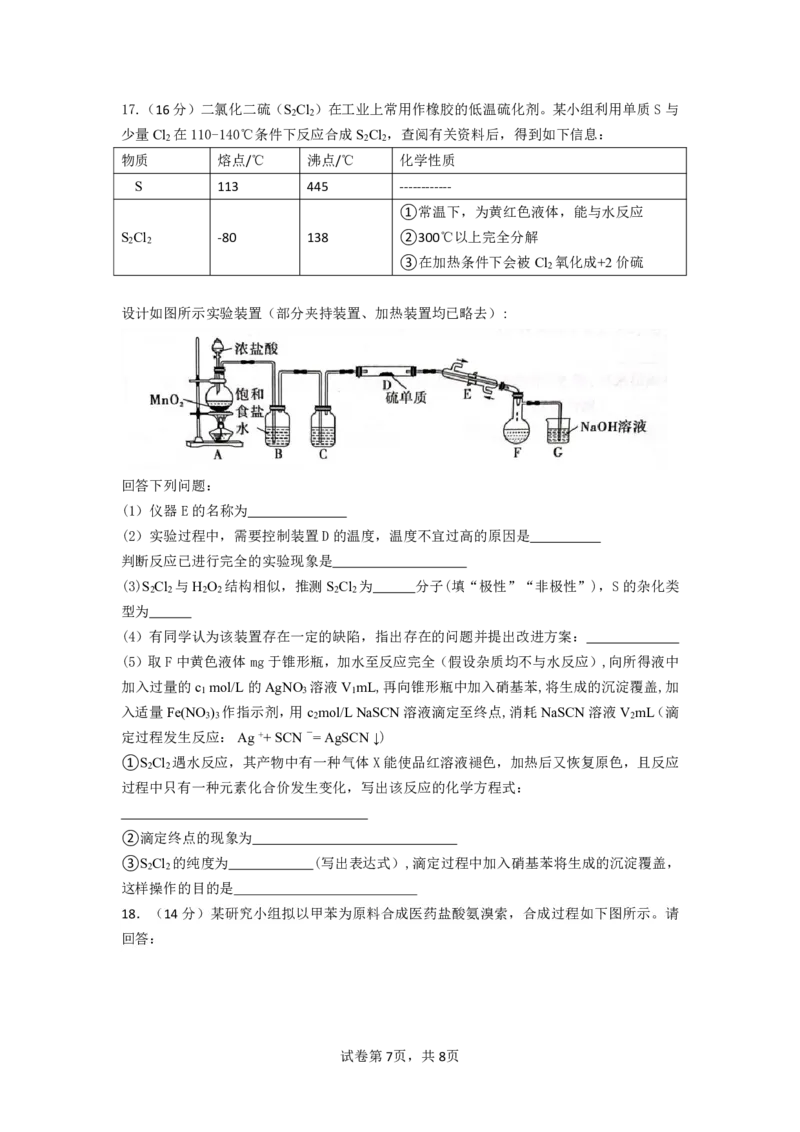
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}17.(16分)二氯化二硫(S Cl )在工业上常用作橡胶的低温硫化剂。某小组利用单质S与
2 2
少量Cl 在110-140℃条件下反应合成S Cl ,查阅有关资料后,得到如下信息:
2 2 2
物质 熔点/℃ 沸点/℃ 化学性质
S 113 445 ------------
①常温下,为黄红色液体,能与水反应
S Cl -80 138 ②300℃以上完全分解
2 2
③在加热条件下会被Cl 氧化成+2价硫
2
设计如图所示实验装置(部分夹持装置、加热装置均已略去):
回答下列问题:
(1)仪器E的名称为
(2)实验过程中,需要控制装置D的温度,温度不宜过高的原因是
判断反应已进行完全的实验现象是
(3)S Cl 与H O 结构相似,推测S Cl 为 分子(填“极性”“非极性”),S的杂化类
2 2 2 2 2 2
型为
(4)有同学认为该装置存在一定的缺陷,指出存在的问题并提出改进方案:
(5)取F中黄色液体mg于锥形瓶,加水至反应完全(假设杂质均不与水反应),向所得液中
加入过量的c mol/L的AgNO 溶液V mL,再向锥形瓶中加入硝基苯,将生成的沉淀覆盖,加
1 3 1
入适量Fe(NO ) 作指示剂,用c mol/LNaSCN溶液滴定至终点,消耗NaSCN溶液V mL(滴
3 3 2 2
定过程发生反应:Ag++SCN-=AgSCN↓)
①S Cl 遇水反应,其产物中有一种气体X能使品红溶液褪色,加热后又恢复原色,且反应
2 2
过程中只有一种元素化合价发生变化,写出该反应的化学方程式:
②滴定终点的现象为
③S Cl 的纯度为 (写出表达式),滴定过程中加入硝基苯将生成的沉淀覆盖,
2 2
这样操作的目的是
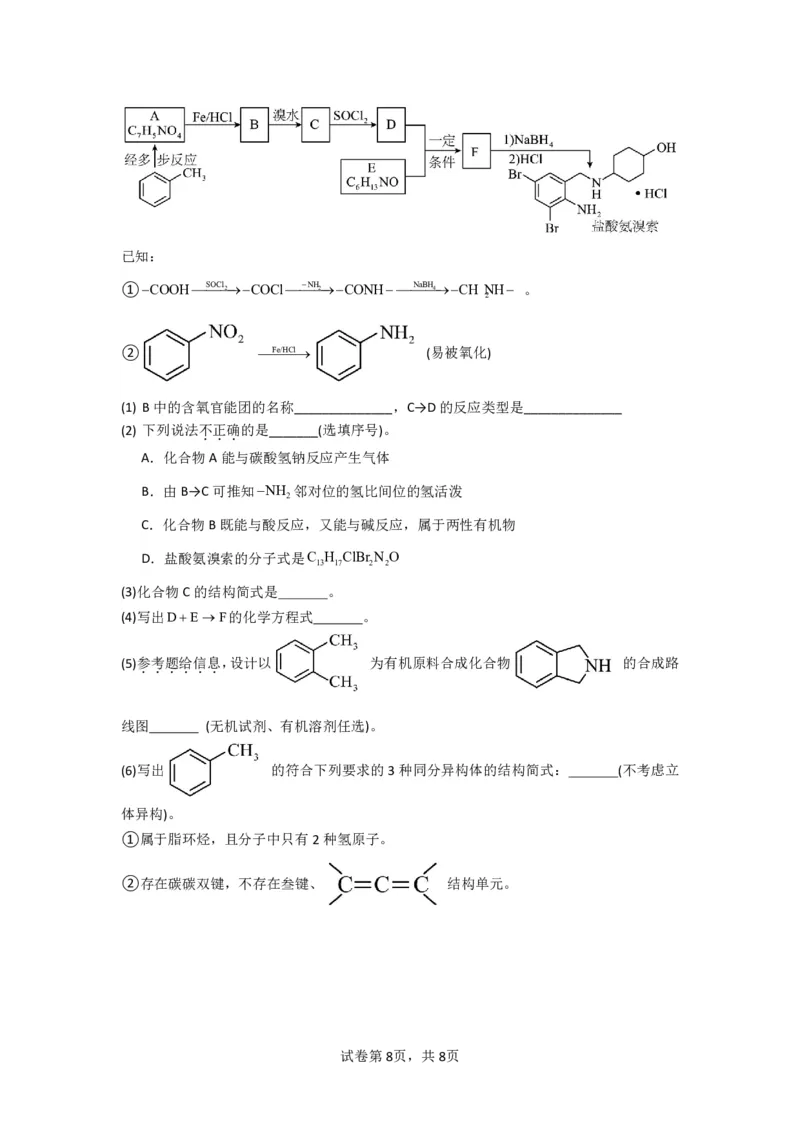
18.(14分)某研究小组拟以甲苯为原料合成医药盐酸氨溴索,合成过程如下图所示。请
回答:
试卷第7页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}已知:
①COOHSOCl2COClNH2CONHNaBH4CH NH 。
2
② Fe/HCl (易被氧化)
(1) B中的含氧官能团的名称______________,C→D的反应类型是______________
(2) 下列说法不 . 正 . 确 . 的是_______(选填序号)。
A.化合物A能与碳酸氢钠反应产生气体
B.由B→C可推知NH 邻对位的氢比间位的氢活泼
2
C.化合物B既能与酸反应,又能与碱反应,属于两性有机物
D.盐酸氨溴索的分子式是C H ClBr N O
13 17 2 2
(3)化合物C的结构简式是 。
(4)写出DEF的化学方程式 。
(5)参
.
考
.
题
.
给
.
信
.
息
.
,设计以 为有机原料合成化合物 的合成路
线图 (无机试剂、有机溶剂任选)。
(6)写出 的符合下列要求的3种同分异构体的结构简式: (不考虑立
体异构)。
①属于脂环烃,且分子中只有2种氢原子。
②存在碳碳双键,不存在叁键、 结构单元。
试卷第8页,共8页
{#{QQABQQQAggAoAAIAAAhCQw2QCgKQkBECACoGQBAIMAAAwBFABAA=}#}