文档内容
哈 32 中 2023~2024 学年度上学期 9 月考试 D.化学变化:硫燃烧、碳酸钙高温分解、氢气与氯气混合气光照下爆炸
化学试题 7.下列应用中涉及到氧化还原反应的是( )
(考试范围物质的分类、离子反应、氧化还原反应 适用班级:高三学年) A.使用明矾对水进行净化 B.雪天道路上撒盐融雪
一、选择题(每小题只有1个选项符合题意,每题4分,共60分)
C.暖贴中的铁粉遇空气放热 D.荧光指示牌被照发光
1.下列消毒剂的有效成分属于盐的是( )。
8.常温下,下列各组离子在给定溶液中能大量共存的是( )
A.高锰酸钾溶液 B.过氧乙酸溶液
A.pH=1的溶液:Fe2+、Mg2+、SO2-、NO-
C.双氧水 D.医用酒精 4 3
B.pH=12的溶液:K+、Na+、NO-、CO2-
2.《天工开物》中记载:“凡乌金纸由苏、杭造成,其纸用东海巨竹膜为质。用豆油 3 3
点灯,闭塞周围,只留针孔通气,熏染烟光而成此纸,每纸一张打金箔五十度……”下 C.pH=7的溶液:Na+、Cu2+、S2-、Cl-
列说法错误的是( )。 D.pH=7的溶液:Al3+、K+、Cl-、HCO-
3
审 出 A.“乌金纸”的“乌”与豆油不完全燃烧有关 9.在给定条件下,下列所示的转化关系均能实现的是
题 题
B.“巨竹膜”为造纸的原料,主要成分是纤维素 H O(g)
人 人 A.Fe 2 FeO Fe(SO)
: : 高温 2 3 2 4 3
C.豆油的主要成分油脂属于天然高分子化合物
李 李
O
凤 凤 D.打金成箔,说明金具有良好的延展性 B.Si 2 SiO HSiO
桂 桂 加热 2 2 3
3. 下列物质属于弱电解质的是( )。
C.Al(OH) AlO NaAlO
A.CO B.HO C.HNO D.NaOH 3 2 3 2
2 2 3
O
4.下列化学用语正确的是( )。 D.Na 2 NaO NaCO
点燃 2 2 3
A.NaHCO的电离:NaHCO=Na++H++CO2-
3 3 3
10.下列过程中的化学反应,相应的离子方程式正确的是( )
B.HS-的电离:HS-+HO HO++S2-
2 3
A.用碳酸钠溶液处理水垢中的硫酸钙:CO2-+CaSO=CaCO+SO2-
C.NaClO的电离:NaClO Na++ClO- 3 4 3 4
D.NHCl水解方程式:NH++HO=NH•HO+H+ B.过量铁粉加入稀硝酸中:Fe+4H++NO-=Fe3++NO↑+2HO
4 4 2 3 2 3 2
5.仅能表示唯一化学反应的离子方程式是( )。 C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO+2HO
2 2
A.Zn+2H+=Zn2++H↑
2 D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
B.CHCOOH+OH―=CHCOO―+HO
3 3 2 11.某白色粉末样品,可能含有.NaSO、NaSO、NaSO 和NaCO.取少量样品进行如
2 4 2 3 2 2 3 2 3
C.Ba2++2OH―+2H++SO2―=BaSO↓+2HO
4 4 2
下实验:①溶于水,得到无色透明溶液;②向①的溶液中滴加过量稀盐酸,溶液变浑浊,
D.CHCOOH+NH·HO=CHCOO―+NH++HO
3 3 2 3 4 2
有刺激性气体逸出.离心分离;③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
6.下列有关物质分类或归类正确的是( )。 2
该样品中确定存在的是
A.混合物:盐酸、漂白粉、氯水、液氯
B.化合物:CaCl、NaOH、HCl、O A.NaSO 、NaSO B.NaSO 、NaSO
2 2 2 4 2 2 3 2 3 2 2 3
C.同素异形体:C 、干冰、金刚石、石墨
60
第 1 页 共 4 页
学科网(北京)股份有限公司C.NaSO 、NaCO D.NaSO 、NaCO ①钠与水反应:
2 4 2 3 2 3 2 3
12. 下列鉴别或检验不能达到实验目的的是
②铁与水蒸气反应:
A. 用石灰水鉴别NaCO 与NaHCO
2 3 3
③二氧化氮与水的反应:
B. 用KSCN溶液检验FeSO 是否变质
4
④碳酸氢钠受热分解的反应:
C. 用盐酸酸化的BaCl 溶液检验NaSO 是否被氧化
2 2 3
D. 加热条件下用银氨溶液检验乙醇中是否混有乙醛 (3)完成下列物质的水解离子方程式
13.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A ①Al (SO ) :
2 4 3
A.标准状况下,22.4L HCl气体中H+数目为N
A
②Na CO (两步):
2 3
B.28 g CH 分子中含有的σ键数目为4 N
2 4 A
C.1.8 g 18O中含有的中子数为N
A
D.pH=12的NaCO 溶液中OH-数目为0.01 N (4)配平下列化学方程式
2 3 A
14.下列物质的应用中,利用了氧化还原反应的是( ) ① KNO + FeCl + HCl — KCl + FeCl + NO↑ + H O
3 2 3 2
A.用石灰乳脱除烟气中的SO
2
② ClO-+ Fe(OH) + OH- — Cl- + FeO24- + HO
3 2
B.用明矾[KAl(SO)·12HO]处理污水
4 2 2
17.(共8分)某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、Mg2+
C.用盐酸去除铁锈(主要成分FeO·xHO)
2 3 2
和Mn2+)。实现镍、钴、镁元素的回收。
D.用84消毒液(有效成分NaClO)杀灭细菌
15.下列反应的现象描述与离子方程式都正确的是( )。
A.锌片插入硝酸银溶液中,有银析出:Zn+Ag+=Zn2++Ag
B.氢氧化钡溶液与稀硫酸反应,有白色沉淀生成:SO2-+Ba2+=BaSO↓
4 4
C.氢氧化铜加到盐酸中,无明显现象:Cu(OH)+2H+=Cu2++2HO
2 2
D.碳酸钡中加入稀盐酸,固体溶解,生成无色无味气体:BaCO↓+2H+=Ba2++CO↑+HO
3 2 2
二、非选择题(共40分)
16.(共22分)完成下列方程式
(1)完成下列物质的电离方程式
①NaHSO(在水溶液中):
4
②)H S:
2
已知:
(2)完成下列物质的化学方程式
第 2 页 共 4 页物质
FeOH CoOH NiOH MgOH
3 2 2 2
K 1037.4 1014.7 1014.7 1010.8
sp
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,用石灰乳调节pH4,Mn2被H SO 氧化为MnO ,该反应的离
2 5 2
子方程式为_______(H SO 的电离第一步完全,第二步微弱);
2 5
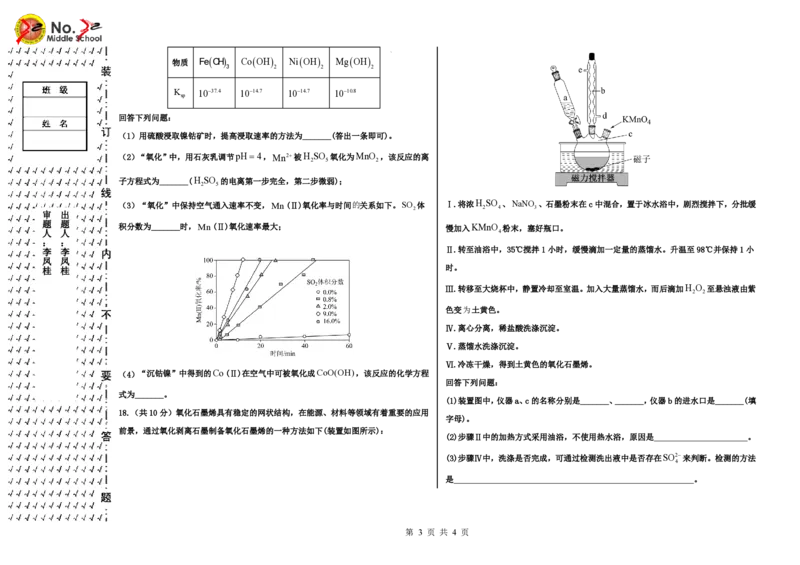
(3)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。SO 体 Ⅰ.将浓H SO 、NaNO 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓
2 2 4 3
审 出
题 题
积分数为_______时,Mn(Ⅱ)氧化速率最大; 慢加入KMnO 粉末,塞好瓶口。
人 人 4
: :
李 李 Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小
凤 凤
时。
桂 桂
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H O 至悬浊液由紫
2 2
色变为土黄色。
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
(4)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程
回答下列问题:
式为_______。
(1)装置图中,仪器a、c的名称分别是_______、_______,仪器b的进水口是_______(填
18.(共10分)氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用
字母)。
前景,通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示):
(2)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是 。
(3)步骤Ⅳ中,洗涤是否完成,可通过检测洗出液中是否存在SO2来判断。检测的方法
4
是 。
第 3 页 共 4 页
学科网(北京)股份有限公司哈 32 中 2023~2024 学年度上学期 9 月考试
(4) 4Co(OH) +O =4CoO(OH)+2H O
2 2 2
化学试题 答案
18、(共10分)
(考试范围物质的分类、离子反应、氧化还原反应 适用班级:高三学年)
(1) 滴液漏斗 三颈烧瓶 d
二、选择题(每小题只有1个选项符合题意,每题5分,共60分)
(2) 反应温度接近水的沸点,油浴更易控温
1.A 2.C 3.B 4.B 5.D 6.D 7.C 8.B 9.C 10.A 11.A 12.A 13.C 14.D 15.D
二、非选择题(共40分)
(3).取少量洗出液,滴加BaCl ,没有白色沉淀生成
2
16、(共22分)完成下列方程式
(1)① NaHSO
4
===Na++H++SO2
4
-
② H S H++HS-
2
(2)①2Na+2H O===2NaOH+H ↑。
2 2
高温
②3Fe+4H O(g)=====Fe O +4H 。
2 3 4 2
③3NO +H O===2HNO +NO
2 2 3
△
④2NaHCO =====Na CO +H O+CO ↑。
3 2 3 2 2
(3)①Al3++3H O Al(OH) +3H+
2 3
②CO2
3
-+H
2
O HCO-
3
+OH-、HCO-
3
+H
2
O H
2
CO
3
+OH-。
(4)配平下列化学方程式
① 1 KNO + 3 FeCl + 4 HCl = 1 KCl + 3 FeCl + 1 NO↑ + 2 H O
3 2 3 2
② 3 ClO-+ 2 Fe(OH) 3 + 4OH- = 3 Cl- + 2 FeO2 4 - + 5 H 2 O
17、(共8分)
(1)适当增大硫酸浓度或适当升高温度或将镍钴矿粉碎增大接触面积
(2)H O+Mn2++HSO-=MnO +SO2-+3H+
2 5 2 4
(3) 9.0%
第 4 页 共 4 页