文档内容
第一章 有机化合物的结构特点与研究方法
第一节 研究有机化合物的一般方法
第2课时 元素分析与有机化合物结构的确定
1.(2020·广东执信中学高二月考)研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→
确定分子式→确定结构式。以下用于研究有机物的方法错误的是( )
A.蒸馏常用于分离提纯互溶的液态有机混合物
B.李比希元素分析仪可以确定有机物的分子结构
C.利用红外光谱仪可以区分乙醇和二甲醚
D.质谱仪通常用于测定有机物的相对分子质量
【答案】B
【详解】
A.蒸馏常用于分离互溶的沸点相差较大的液体,故常用于提纯液态有机混合物,A正确;
B.李比希元素分析仪可以确定有机物的元素组成,分子的最简式,甚至可以确定有机物的分子式,但是
不能确定有机物的结构,B错误;
C.利用红外光谱仪可以测出共价物质分子中含有的化学键、官能团,乙醇和二甲醚中所含的化学键类型
不完全相同,故可以区分乙醇和二甲醚,C正确;
D.质谱仪通常用于测定有机物的相对分子质量,质荷比的最大值=相对分子质量,D正确。
故答案为:B。
2.(2020·广西南宁三中高二期中)有机物A分子的质谱图如图所示。现将9.0g有机物A在足量O 中充
2
分燃烧,生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为
O。下列有关说法正确的是
2A.从质谱图可看出,A的摩尔质量是45g/mol
B.A的实验式为C HO
2 5
C.若A能与NaHCO 溶液反应放出气体,则它可能的结构有2种
3
D.若A只含有一种官能团,则它可能的结构多于2种
【答案】D
【分析】
浓硫酸吸水,碱石灰吸收二氧化碳,分别增重5.4g和13.2g,5.4g水的物质的量为 =0.3mol,
n(H)=0.6mol,13.2g二氧化碳的物质的量为 =0.3mol,n(C)=n(CO)=0.3mol,此有机物9.0g含O
2
元素质量:9.0g-0.6g-0.3×12g=4.8g,n(O)= =0.3mol,故n(C):n(H):n(O)=0.3mol:0.6mol:
0.3mol=1:2:1,即实验式为CHO,设分子式为(CHO) ,由质谱仪可知,A的相对分子质量为90,可得
2 2 n
30n=90,解得:n=3,故有机物A为C HO,据此分析解答。
3 6 3
【详解】
A.从质谱图可看出,最大质荷比为90,A的摩尔质量是90g/mol,故A不符合题意;
B.根据分析,A的实验式为CHO,故B不符合题意;
2
C.根据分析可知,有机物A为C HO,若A能与NaHCO 溶液反应放出气体,说明分子中含有羧基,则
3 6 3 3
它可能的结构有CHCH(OH)COOH、CH (OH)CHCOOH、CHOCH COOH等,不止2种,故C不符合题
3 2 2 3 2
意;
D.若A只含有一种官能团,它可能的结构有 、 、 等,结构多
于2种,故D符合题意;
答案选D。
3.(2014·湖南高二期末)某烃中碳和氢的质量比是24:5,该烃在标准状况下的密度为2.59g/L,其分子式
为( )A.C H B.C H C.C H D.C H
2 6 4 10 5 10 7 8
【答案】B
【详解】
某烃中碳和氢的质量比是24:5,设碳、氢元素组成的化合物的化学式为C H,则12×x:1×y=24:5,解得
x y
x:y=2:5,即化合物的最简式为C H,烃在标况下的密度是2.59g/L,则M=22.4L/mol×2.59g/L=58g/
2 5
mol,设分子式为(C H),则(12×2+1×5)×n=58,所以n=2,所以分子式为:C H ,答案选B。
2 5 n 4 10
4.(2021·吉林长春外国语学校高二期中)标准状况下1mol某烃完全燃烧时,生成89.6LCO ,又知
2
0.1mol此烃能与标准状况下4.48LH 加成,则此烃的结构简式是
2
A.CHCH=CHCH B.CHCHCH=CH C.CH=CHCH=CH D.CH=CHCH=CHCH
3 3 3 2 2 2 2 2 3
【答案】C
【详解】
标准状况下,1mol某烃完全燃烧时,生成89.6L二氧化碳,其物质的量是 =4mol,则1分子该
烃含有4个碳原子,0.1mol此烃能与标准状况下4.48LH 加成,消耗氢气的物质的量是
2
=0.2mol,则一分子该烃含有两个碳碳双键,
故选:C。
5.(2020·钦州市第四中学高二月考)某有机物在O 中充分燃烧,生成36g水和44gCO,则该有机物的
2 2
组成必须满足的条件是( )
A.分子式一定是CH B.分子式一定是CHO
4 4
C.分子式可能是CH 或CHO D.以上说法均不正确
4 4
【答案】C
【分析】
有机物在氧气中充分燃烧,生成的CO 和HO的物质的量之比为 : =1:2,则确定有机
2 2
物分子中C、H个数之比为1:4,有机物可能是CH,也可能是CHO。
4 4
【详解】
有机物在氧气中充分燃烧,生成的CO 和HO的物质的量之比为 : =1:2,则确定有机
2 2物分子中C、H个数之比为1:4,不能确定是否含有氧元素,则有机物可能是CH,也可能是CHO,故选:
4 4
C。
6.(2020·浙江诸暨中学高二月考)下列最简式中,没有相对分子质量也可以确定分子式的是
A.CH B.CH C.C H D.C H
2 2 3 2 5
【答案】D
【分析】
因为碳氢化合物或含氧衍生物中碳成4条键,所以氢原子数一定为偶数,而且根据烷烃通式可得,最多氢
原子数=2n+2(n是碳原子数),氧原子不影响氢原子数目,据此分析。
【详解】
A.最简式为CH,可以是C H 或C H(环丁二烯)或C H 或C H(苯乙烯),没有相对分子质量无法确定分
2 2 4 4 6 6 8 8
子式,A错误;
B.任何烯烃最简式都是CH,没有相对分子质量无法确定分子式,B错误;
2
C.最简式为C H,可以是C H 或C H 或C H 等,没有相对分子质量无法确定分子式,C错误;
2 3 4 6 8 12 12 18
D.最简式是C H,氢原子为偶数,若氢原子为10,分子式为C H ,已达饱和结构,所以分子式一定是
2 5 4 10
C H ,D正确。
4 10
答案选D。
7.(2020·天津高三期中)用来测定某一固体是否是晶体的仪器是
A.质谱仪 B.红外光谱仪 C.pH计 D.X射线衔射仪
【答案】D
【详解】
A.质谱仪通常用来测定有机物的相对分子质量,相对分子质量=质荷比的最大值,A不符合题意;
B.红外光谱仪通常用来测定有机物分子中的化学键和官能团,从而测定有机物结构式,B不符合题意;
C.pH计用来测量溶液的酸碱性,C不符合题意;
D.同一条件下,当单一波长的X-射线通过晶体和非晶体时,摄取的图谱是不同的,非晶体图谱中看不到
分立的班点或明锐的谱线,故可用x-射线衍射仪来区分晶体和非晶体,D符合题意。
答案选D。
8.(2020·云南省玉溪第一中学高二期中)下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比不为
3:2的是( )
A. B. C.正丁烷 D.【答案】A
【详解】
A. 的结构简式为CH-CH=CH-CH ,分子中存在2种不同性质的氢原子,氢原子个数比为
3 3
6:2=3:1,A符合题意;
B. 分子中有2种不同性质的氢原子,氢原子个数比为6:4=3:2,B不合题意;
C.正丁烷的结构简式为CHCHCHCH,分子中存在2种不同性质的氢原子,氢原子个数比为6:4=3:2,
3 2 2 3
C不合题意;
D. 分子中存在2种不同性质的氢原子,氢原子个数比为6:4=3:2,D不合题意;
故选A。
9.(2020·陕西安康·)某化合物由碳、氢、氧三种元素组成,其红外光谱图表明有C-H键、O-H键、C-O
键的红外吸收峰,该有机物的相对分子质量是60,其核磁共振氢谱只有3组峰,则该有机物的结构简式是
( )
A.CHCHOCH B.CHCH(OH)CH
3 2 3 3 3
C.CHCHCHOH D.CHCHCHO
3 2 2 3 2
【答案】B
【分析】
结合有机物的相对分子质量为60,该有机物分子中有分子中含有C-H键、O-H键、C-O键,分子式可能为
C HO 或C HO,核磁共振氢谱中有3组峰,分子中就有3种H原子,据此分析。
2 4 2 3 8
【详解】
A.CHCHOCH 结构中不含O-H键,A错误;
3 2 3
B.CHCH(OH)CH 相对分子质量为60,分子中含有C-H键、O-H键、C-O键,有3种H原子,满足条件,
3 3
B正确;
C.CHCHCHOH有4种H原子,C错误;
3 2 2
D.CHCHCHO相对分子质量为58,有C-H键、C=O键,不含O-H键、C-O键,D错误;
3 2
答案选B。
【点睛】
等效氢原子的判断是此题的易错点,核磁共振氢谱中有几组峰就有几种氢原子,在结构简式中的判断方法
是取代等效氢法:同碳原子上的氢等效,同碳原子上的甲基氢等效 ,处在对称位置的相同原子团上的氢等效。以此区分B、C选项。
10.(2019·民勤县第一中学高二期中)分子式为C HO的有机物有两种同分异构体:乙醇(CHCHOH)和
2 6 3 2
甲醚(CHOCH ),则通过下列方式或方法不可能将二者区别开来的是( )
3 3
A.红外光谱 B.核磁共振氢谱 C.元素分析法 D.与钠反应
【答案】C
【分析】
乙醇(CHCHOH)和甲醚(CHOCH ) 的元素组成相同,而官能团不同、H的种类不同,以此解答该题。
3 2 3 3
【详解】
A.含化学键、官能团不同,则红外光谱可区分,故A不选;
B.乙醇含3种H,甲醚含1种H,则核磁共振氢谱可区分,故B不选;
C.乙醇和甲醚的元素组成相同,则元素分析法不能区分,故C选;
D.乙醇与钠反应生成氢气,而甲醚不能,可区分,故D不选;
故选C。
11.(2019·民勤县第一中学高二期中)燃烧0.1mol某有机物得0.2molCO 和0.3molHO,由此得出的结论
2 2
不正确的是( )
A .该有机物分子中可能含有氧原子
B.该有机物中碳、氢元素原子数目之比为1∶3
C.该有机物分子中不可能含有碳碳双键
D.该有机物分子的结构简式为CH—CH
3 3
【答案】D
【分析】
根据元素守恒和原子守恒,推出0.1mol有机物中含有0.2molC和0.6molH,即1mol该有机物分子中有
2molC原子和6molH原子,据此分析。
【详解】
A.题中无法确认有机物的质量或相对分子质量,因此无法确认有机物中是否含氧元素,该有机物分子中
可能存在氧原子,故A正确;
B.根据上述分析可知,该有机物中碳、氢元素原子数目之比为2:6=1:3,故B正确;
C.1mol该有机物中含有2molC和6molH,该有机物分子式C HO,不饱和度为0,即不含碳碳双键,故
2 6 x
C正确;
D.题中无法确认有机物的质量或相对分子质量,因此无法确认有机物中是否含氧元素,即无法确认有机物结构简式,故D错误;
答案选D。
【点睛】
有机物分子式的确定,利用原子守恒和元素守恒,推出有机物中C原子的物质的量和H原子的物质的量,
然后根据有机物的质量,确认是否含有氧元素,从而求出有机物的实验式,最后利用有机物的相对分子质
量,求出有机物的分子式。
12.(2020·钦州市第四中学高二月考)下列说法中正确的是( )
A. 在核磁共振氢谱中有7个吸收峰
B.红外光谱图只能确定有机物中所含官能团的种类和数目
C.质谱法不能用于相对分子质量的测定
D.核磁共振氢谱、红外光谱和质谱法都可用于分析有机物结构
【答案】D
【详解】
A. 此物质有3种不同化学环境的氢原子,在核磁共振氢谱中有3个吸收峰,
故A错误;
B. 红外光谱只能确定官能团的种类,不能确定其数目,故B错误;
C. 质谱图中,用最大质荷比可确定有机物的相对分子质量,故C错误;
D. 核磁共振氢谱、红外光谱和质谱都可用于分析有机物结构,故D正确;
故选D。
13.(2020·广东执信中学高二月考)化学上常用燃烧法确定有机物的组成,如下图所示装置是用燃烧法确
定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质
量确定有机物的组成。
完成下列问题:
(1)A中发生反应的化学方程式为_______________(2)B装置的作用是_______________
(3)燃烧管C中CuO的作用是______________,
(4)产生的氧气按从左向右流向,燃烧管C与装置D、E的连接顺序是:C→____→___
(5)准确称取1.8g烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加2.64g,E管质量增加1.08g,
则该有机物的实验式是______.
(6)实验测得X的蒸气密度是同温同压下氢气密度的45倍,则X的分子式为______
(7)1molX分别与足量Na、NaHCO 反应放出的气体在相同条件下的体积比为1:1,X 的核磁共振氢谱
3
如下(峰面积之比为1:1:1:3),X的结构简式为_______________
【答案】2HO 2HO+O↑ 吸收氧气中的水蒸气(或答:干燥氧气) 使有机物不完全燃烧
2 2 2 2
的产物全部转化为CO 和 HO E D CHO C HO
2 2 2 3 6 3
【分析】
A装置中二氧化锰催化过氧化氢分解产生氧气,用B干燥氧气,样品在C中燃烧,在CuO的作用下不完全
燃烧的产物转化为CO,然后用E吸收有机物燃烧产生的水,E增加的质量即为燃烧产生的水的质量,最
2
后用D吸收二氧化碳,D增加的质量即为二氧化碳的质量,通过E、D中水、二氧化碳的质量计算有机样
品中O的质量,通过计算C、H、O的物质的量之比确定实验式,通过测定X蒸气密度确定X的分子式,
再测定X的核磁共振氢谱确定X的结构,据此解答。
【详解】
(1) A装置的作用是制备氧气,可用二氧化锰催化过氧化氢分解产生氧气,反应的化学方程式为2HO
2 2
2HO+O↑,故答案为:2HO 2HO+O↑;
2 2 2 2 2 2
(2)B装置的作用是除去氧气中的水蒸气,避免测定有机物燃烧产生的水不准确,故答案为:吸收氧气中的
水蒸气(或答:干燥氧气);(3)有机物可能燃烧不完全,CuO的作用是使有机物不完全燃烧的产物全部转化为CO 和 HO,故答案为:
2 2
使有机物不完全燃烧的产物全部转化为CO 和 HO;
2 2
(4)D中碱石灰既能吸收水,又能吸收二氧化碳,因此要先连接E,仪器连接顺序为C→E→D,故答案为:
E;D;
(5)D管质量增加2.64g克说明生成了2.64g二氧化碳,n(CO)= =0.06mol,m(C)
2
=0.06mol×12g/mol=0.72g;E管质量增加1.08g,说明生成了1.08g的水,n(HO)= =0.06mol,m
2
(H)=0.06mol×2×1g/mol=0.12g;从而可推出含氧元素的质量为:1.8g-0.72g-0.12g=0.96g,n(O)=
=0.06mol, N(C):N(H):N(O)=0.06mol:0.12mol:0.06mol=1:2:1,故该有机物的实
验式为CHO,故答案为:CHO;
2 2
(6)CH O的相对质量为30,X的蒸气密度是同温同压下氢气密度的45倍,则X的相对分子质量为
2
45×2=90,则X的分子式为C HO,故答案为:C HO;
3 6 3 3 6 3
(7) 1molX分别与足量Na、NaHCO 反应放出的气体在相同条件下的体积比为1:1,则分子中含一个羟基
3
和一个羧基,X 的核磁共振氢谱出现4组峰且峰面积之比为1:1:1:3,则X的结构简式为 ,
故答案为: 。
14.(2020·江西师大附中高一月考)实验室用燃烧法测定某氨基酸(C HON)的分子组成,取w g该氨基
x y z p
酸放在纯氧中充分燃烧,生成CO、HO和N。现用如图所示装置进行实验(铁架台.铁夹.酒精灯等未画
2 2 2
出),请回答有关问题:(1)实验中止水夹a是关闭的,b是开启的。但实验开始时,首先要打开夹a,关闭夹b,通一段时间的纯氧,
这样做的目的是______________________。
(2)以上装置中需要加热的有________(填装置代号)。操作时应先点燃_______处的酒精灯。
(3)装置A中发生反应的化学方程式为__________________。
(4)实验中测得N 的体积为V mL(已知密度),为确定此氨基酸的分子式,还需要得到的数据有_______ (填
2
字母)。
A.生成二氧化碳气体的质量 B.生成水的质量
C.通入氧气的质量 D.该氨基酸的相对分子质量
(5)如果将装置B、C的连接顺序变为C、B,该实验的目的能否达到______ ( 能或不能)简述理由
__________________________。
【答案】将装置中的空气排净 A和D D C HON+(x+ - )O xCO+ HO+ N
x y z p 2 2 2 2
ABD 不能 因为烧碱将同时吸收CO 和HO两种气体,使实验结果缺少必要的数据,无法确定该氨
2 2
基酸的分子组成
【分析】
根据题意可知,用燃烧法测定某种氨基酸(C HON)的分子组成,用纯氧气将C HON 完全氧化成二氧化
x y z p x y z p
碳、水和氮气,用浓硫酸吸收水,用碱石灰吸收二氧化碳,用铜网吸收未反应的氧气,用排水量气法测得
氮气的体积,为了准确测得各成分的质量,实验开始先用氧气将装置中的空气排尽,同时应按先吸收水,
再吸收二氧化碳,再除氧气,最后测氮气的体积,根据元素守恒可计算出C HON 的组成,以此解答该题;
x y z p
【详解】
(1)空气中的氮气会产生干扰,实验开始时,首先要打开夹a,关闭夹b,通一段时间的纯氧,可以将装置
中的N 排净,避免它对实验造成干扰,之后,则需关闭止水夹a,打开b;
2
(2)氨基酸和氧气的反应,以及铜网和氧气的反应都需要加热,因此需要加热的装置有AD;操作时应先点
燃D处的酒精灯,吸收未反应的氧气,保证最终收集的气体为N;
2
(3)在装置A中氨基酸和氧气在加热时发生氧化反应,化学方程式是:C HON+(x+ - )O
x y z p 2
xCO+ HO+ N;
2 2 2
(4)根据上面的分析可知,为了确定此氨基酸的分子式,除了准确测量N 的体积外,还需得到氨基酸的摩
2尔质量、生成二氧化碳气体的质量、生成水的质量,故合理选项是ABD;
(5)如果将装置中的B、C连接顺序变为C、B,因为碱石灰将同时吸收水蒸气与CO,得不到二者各自的质
2
量,无法计算C元素与H元素的含量,使实验结果缺少必要的数据,无法确定该氨基酸的分子组成。
15.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究
A的组成与结构,进行了如下实验:
实验步骤 解释或实验结论
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H 的45 通过计算填空:(1)A的相对分
2
倍 子质量为:________
(2)将此9.0 g A在足量纯O 中充分燃烧,并使其产物依次缓缓通
2 (2)A的分子式为:________
过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g
(3)另取A 9.0 g,跟足量的NaHCO 粉末反应,生成2.24 LCO (标 (3)用结构简式表示A中含有的
3 2
准状况),若与足量金属钠反应则生成2.24 L H (标准状况) 官能团:__________、________
2
(4)A的1H核磁共振谱如图
(4)A中含有________种氢原子
(5)综上所述,A的结构简式________
【答案】90 C HO -COOH -OH 4 CHCH(OH)COOH
3 6 3 3
【分析】
(1)有机物和氢气的密度之比等于相对分子质量之比;
(2)浓硫酸可以吸收水,碱石灰可以吸收二氧化碳,根据元素守恒来确定有机物的分子式;
(3)羧基可以和碳酸氢钠发生化学反应生成二氧化碳,羟基可以和金属钠发生化学反应生成氢气;
(4)核磁共振氢谱图中有几个峰值则含有几种类型的等效氢原子,峰面积之比等于氢原子的数目之比;
(5)根据分析确定A的结构简式。
【详解】
(1)有机物质的密度是相同条件下H 的45倍,所以有机物的相对分子质量为45×2=90,故答案为90;
2(2)浓硫酸增重5.4g,则生成水的质量是5.4g,生成水的物质的量是 =0.3mol,所含有氢原子
的物质的量是0.6mol,碱石灰增重13.2g,所以生成二氧化碳的质量是13.2g,所以生成二氧化碳的物质的
量是 = 0.3 mol,所以碳原子的物质的量是0.3 mol,由于有机物是0.1mol,所以有机物中碳原子
个数是3,氢原子个数是6,根据相对分子质量是90,所以氧原子个数是3,即分子式为:C HO,
3 6 3
故答案为C HO;
3 6 3
(3)只有羧基可以和碳酸氢钠发生化学反应生成二氧化碳,生成2.24LCO (标准状况),则含有一个羧
2
基(-COOH),醇羟基(-OH)可以和金属钠发生反应生成氢气,与足量金属钠反应生成2.24LH (标
2
准状况),则含有羟基数目是1个,
故答案为-COOH和-OH;
(4)根据核磁共振氢谱图看出有机物中有4个峰值,则含4种类型的等效氢原子,氢原子的个数比是3:
1:1:1,
故答案为4;
(5)综上所述,A的结构简式为CHCH(OH)COOH。
3
16.(2020·常州市第二中学高二月考)按要求填空
(1)0.2mol 有机物和 0.4mol O 在密闭容器中燃烧后的产物为 CO、CO 和 HO(g).产物经过浓硫酸后,
2 2 2
浓硫酸的质量增加 10.8g;再通过灼热 CuO 充分反应后,固体质量减轻 3.2g;最后气体再通过碱石灰被
完全吸收,碱石灰质量增加 17.6g。该有机物 A 的分子式为:______;
(2) 化合物 B 和 C 的分子式都是 C HBr , B 的核磁共振氢谱如下图所示,则 B 的结构简式为_____;
2 4 2
请预测 C 的核磁共振氢谱上有_______种信号;
(3)有机物 B 的分子式为 C HO,其红外光谱图如图所示,试推测该有机物的可能结构(试写出两
4 8 2
种)______、__________。【答案】C HO BrHC-CHBr 2
2 6 2 2 2
【详解】
(1)有机物燃烧生成水10.8g,物质的量为 ;令有机物燃烧生成的CO为x,则:
, ,x=5.6g ,CO的物质的量为 ,根据碳
元素守恒可知CO与CuO反应生成的CO 的物质的量为0.2mol,质量为0.2mol×44g/mol=8.8g,有机物燃烧
2
生成的CO 的质量为17.6g−8.8g=8.8g,物质的量为 ,根据碳元素守恒可知,1mol有
2
机物含有碳原子物质的量为2mol,根据氢元素守恒可知,1mol有机物含有氢原子物质的量为
,根据氧元素守恒可知,1mol有机物含有氧原子物质的量为
,所以有机物的分子式为C HO;
2 6 2
(2) 化合物 B 和 C 的分子式都是 C HBr ,从B的核磁共振氢谱知 B分子内只有1种氢,故B的结构
2 4 2
简式为BrHC-CHBr;C与B是同分异构体,则C的的结构简式为HC-CHBr ,C 分子内有2种氢,故C
2 2 3 2
的核磁共振氢谱上有2种信号;
(3)有机物 B 的分子式为 C HO,B的不饱和度为1,由红外光谱图知,B分子内有两个 —CH,且不对
4 8 2 3称,都含有 C=O 、 C—O—C ,该有机物的可能结构为 、 。
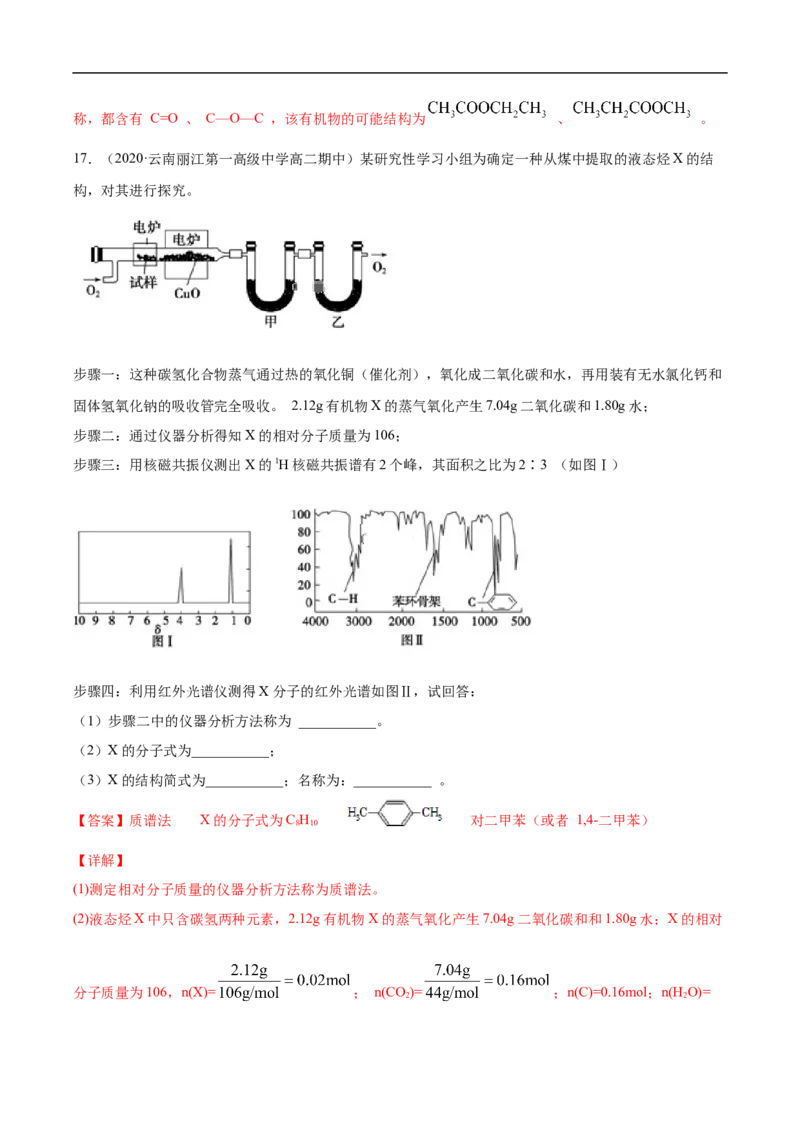
17.(2020·云南丽江第一高级中学高二期中)某研究性学习小组为确定一种从煤中提取的液态烃X的结
构,对其进行探究。
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和
固体氢氧化钠的吸收管完全吸收。 2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3 (如图Ⅰ)
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
(1)步骤二中的仪器分析方法称为 ___________。
(2)X的分子式为___________;
(3)X的结构简式为___________;名称为:___________ 。
【答案】质谱法 X的分子式为C H 对二甲苯(或者 1,4-二甲苯)
8 10
【详解】
(1)测定相对分子质量的仪器分析方法称为质谱法。
(2)液态烃X中只含碳氢两种元素,2.12g有机物X的蒸气氧化产生7.04g二氧化碳和和1.80g水;X的相对
分子质量为106,n(X)= ; n(CO)= ;n(C)=0.16mol;n(H O)=
2 2,n(H)=0.2mol,所以X的分子式为C H ;
8 10
(3)根据X分子的红外光谱如图,X的结构中含有 ,核磁共振谱有2个峰,其面积之比为2∶3,X
的结构简式为 ;名称为对二甲苯。