文档内容
第一章 原子结构与性质
第二节 原子结构与元素的性质
第2课时 元素周期律
培优第一阶——基础过关练
1.(2022·福建省宁化第六中学高二阶段练习)已知X、Y元素同周期,且电负性X > Y,下列说法错误的
是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能可能Y小于X
C.原子半径:X > Y
D.X元素气态氢化物的稳定性大于Y元素气态氢化物的稳定性
2.(2022·浙江大学附属中学高二期末)下列说法正确的是
A.原子核外电子发生跃迁不一定吸收能量
B.从左到右,同周期元素原子的电负性逐渐增大
C.所有元素中氟的第一电离能最大
D.价电子排布为5s25p4的元素位于第五周期第ⅣA族,是p区元素
3.(2021·四川省安岳县兴隆中学高二阶段练习)下列各组比较正确的是
A.第一电离能:B>Al>Ga B.电负性:F>N>O
C.离子半径:K+>Cl->S2- D.原子半径:P>O>N
4.(2022·福建省泉州实验中学高二期中)在元素周期表中,存在“对角线规则”,如下表。比如铍元素
与铝元素的单质及其化合物的性质相似。下列说法正确的是
A.Be的氯化物是共价化合物
B.比较逐级电离能,铍元素与铝元素都是第四电离能突然变大
C. 与过量的NaOH溶液反应生成
D. 溶液呈中性
5.(2022·福建·三明一中高二阶段练习)短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判
断下列说法正确的是
元素最高价氧化物的水化物 X Y Z W
分子式 HZO
3 4
0.1 mol·L-1溶液对应的pH 1.00 13.00 1.57 0.70
A.元素电负性: ZZ
6.(2022·云南·富宁县第一中学高二开学考试)以下有关元素性质的说法中不正确的是
A.①Na、K、Rb,②N、P、As,③O、S、Se,④Na、P、O元素的电负性依次递增的是④
B.下列原子中,①1s22s22p63s23p1,②1s22s22p63s23p2,③1s22s22p63s23p3,④1s22s22p63s23p4对应的第一电
离能最大的元素是④
C.某短元素的逐级电离能(kJ∙mol−1)分别为738、1451、7733、10540、13630、17995、21703,该元素可能
在第三周期ⅡA族
D.以下原子中,①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4半径最大的是①
7.(2022·上海交大附中高二开学考试)元素X的各级电离能数据如下:
57 1483
1817 2745 11578 18378
8 1
则元素X的常见化合价是
A.+1 B.+2 C.+3 D.+6
8.(2022·山东潍坊·高二期末)已知X、Y是主族元素,表中数据 为逐级电离能(单位 )。下
列说法错误的是
元素
X 500 4600 6900 9500
Y 580 1800 2700 11600
A.元素Y是ⅢA族元素
B.X单质还原性比Y的强
C.元素X的常见化合价是 价
D.若元素Y处于第3周期,其单质可与冷水剧烈反应
9.(2022·浙江·杭州市源清中学高二期中)下列说法正确的是
A.氧原子的电子排布图: 最外层违背了洪特规则
B.在基态多电子原子中,p能级电子的能量一定高于s能级电子的能量
C.因O的电负性比N的大,故O的第一电离能比N的大
D.根据原子核外电子排布的特点Cu在元素周期表中位于s区
10.(2022·江苏省如东高级中学高三开学考试)有反应P+16H O+10CuSO =10Cu+4H PO +10H SO 。下
4 2 4 3 4 2 4
列说法正确的是
A.第一电离能大小:I(P)r(S2-) D.酸性强弱:HPO >H SO
3 4 2 4
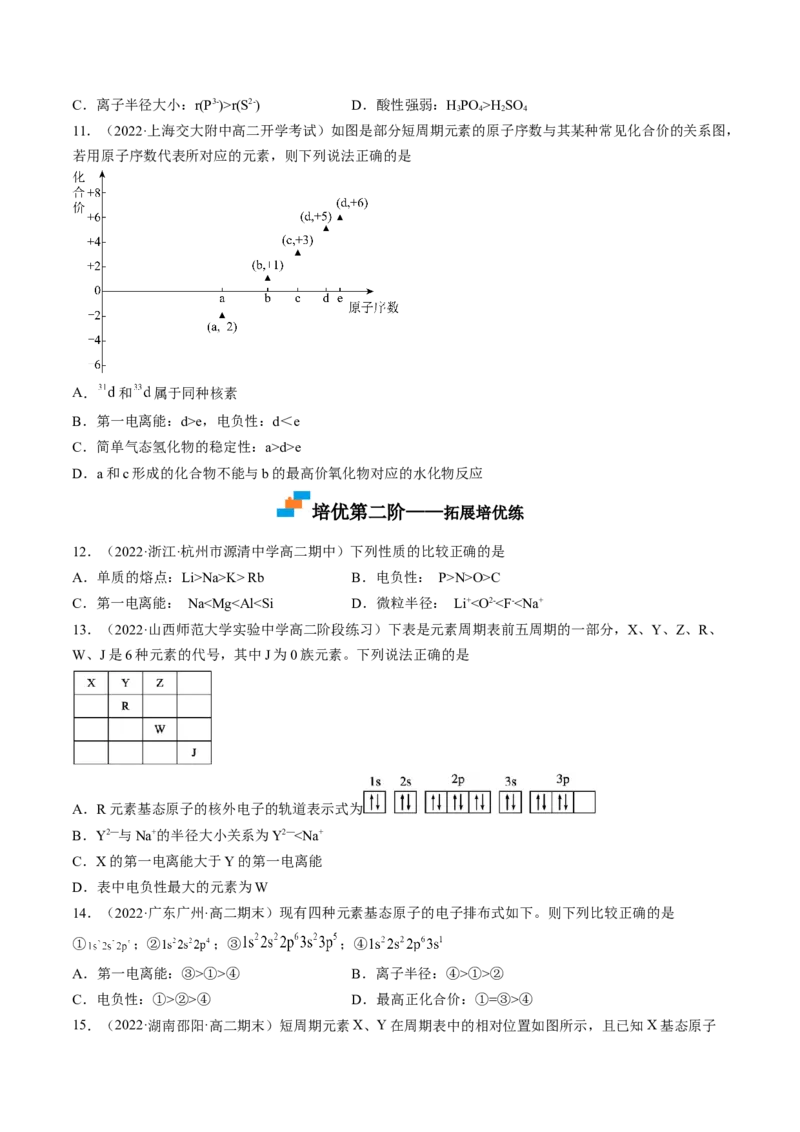
11.(2022·上海交大附中高二开学考试)如图是部分短周期元素的原子序数与其某种常见化合价的关系图,
若用原子序数代表所对应的元素,则下列说法正确的是
A. 和 属于同种核素
B.第一电离能:d>e,电负性:d<e
C.简单气态氢化物的稳定性:a>d>e
D.a和c形成的化合物不能与b的最高价氧化物对应的水化物反应
培优第二阶——拓展培优练
12.(2022·浙江·杭州市源清中学高二期中)下列性质的比较正确的是
A.单质的熔点:Li>Na>K> Rb B.电负性: P>N>O>C
C.第一电离能: Na①>④ B.离子半径:④>①>②
C.电负性:①>②>④ D.最高正化合价:①=③>④
15.(2022·湖南邵阳·高二期末)短周期元素X、Y在周期表中的相对位置如图所示,且已知X基态原子的价电子排布为 ,下列说法不正确的是
A.X在周期表中位于第二周期第IIIA族 B.原子半径
C.X元素的电负性大于Y D.X元素的第一电离能大于Y
16.(2022·安徽滁州·高二阶段练习)X、Y、Z、W四种短周期元素,原子半径依次增大,X和Y位于同
一周期,可组成多种化合物,其中一种是红棕色的大气污染物。Z的最高价氧化物对应的水化物是中强碱。
下列有关说法正确的是
A.简单离子半径:
B.第一电离能:
C.电负性:
D.W与X组成的化合物中一定不含有共价键
17.(2022·江苏·金沙中学高一阶段练习)几种短周期元素的原子半径及主要化合价如表:
元素代号 X Y Z W
原子半径/nm 0.143 0.102 0.075 0.074
主要化合价 +3 +6、-2 +5、-3 -2
下列叙述正确的是
A.X元素位于周期表的第二周期ⅢA族 B.Y的简单氢化物比W的稳定
C.第一电离能:I(Z)>I (W)>I (Y) D.Z的含氧酸酸性一定比Y的强
1 1 1
18.(2022·浙江宁波·高三开学考试)X、Y、Z、W为原子序数依次增大的短周期主族元素。X与Z同族,
Z的原子序数是X的2倍,Y离子在同周期内离子半径最小。下列说法正确的是
A.离子半径:W>Z>Y>X
B.W元素是同周期中第一电离能最大的元素
C.HX分子间存在氢键,因此稳定性:HX>HZ
2 2 2
D.元素X和W的某些单质或化合物可作为工业生产上的脱色剂、消毒剂
19.(2022·新疆·乌市八中高二期末)根据要求完成。
(1)基态氟原子氟原子有_______种不同能量的电子,价电子排布图为_______。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:_______; 中有_______种运动
状态不同的电子。
(3)基态硼原子的核外电子排布图为_______。
(4)基态K原子中,核外电子占据最高能层的符号是_______,占据该能层电子的电子云轮廓图形状为
_______。(5)锰元素在周期表中的位置为_______;属于_______区元素(填“s”“p”“d”“ds”或“f”)。铜、锌两种元素的
第一电离能、第二电离能如表所示:
电离能/
铜 746 1958
锌 906 1733
铜的第二电离能(I)却大于锌的第二电离能,其主要原因是_______。
2
20.(2021·湖北·华中师范大学潜江附属中学高二阶段练习)回答下列问题:
(1)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性小的元素是____;
26号元素价层电子排布式为____;L原子核外电子占有9个轨道,而且有一个未成对电子,L是____元素。
(2)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
①基态硒原子的价层电子排布式为____。
②锗、砷、硒三种元素的第一电离能大小排序为____。
(3)①Cu元素基态原子的价层电子排布式为____。
②下列说法正确的是____(填字母)。
A.第一电离能:As>Ga
B.电负性:As>Ga
C.原子半径:As>Ga
21.(2022·河南·高二期中)元素周期律是指元素的性质随着原子序数的递增而呈周期性变化的规律。如
图是第三周期各元素第一电离能与原子序数的关系。
回答下列问题:
(1)I (Mg)>I (Al)的原因是_______。
1 1
(2)同一周期由左向右元素第一电离能的变化特点是_______ ;第二周期元素(原子序数3-10)具有类似的变
化规律,可见各周期元素第一电离能的这种变化特点体现了元素性质的_______变化规律。
(3)在同周期元素中氩元素的第一电离能最大的原因是_______。
(4)根据上述变化特点,推测As、Se、Br三种元素第一电离能由大到小的顺序是_______。
(5)已知第三周期某元素各级电离能数据如下,该元素是_______(填元素符号)。电离能 I I I I …
1 2 3 4
181
I/kJ·mol-1 578 2745 11578 …
n
7
22.(2021·北京师大附中高二期末)合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决
了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________,占据最高能级电子的电子云轮廓图为___________形。
②NH 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________。
3
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al O、KO、CaO、MgO、Cr O 等氧化
2 3 2 2 3
物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________。
②比较Mg、Ca第一电离能的大小:___________。O的第一电离能小于N,原因是___________。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
元素 Na Mg Al
496 738 578
4562 1451 1817
电离能(kJ/mol)
6912 7733 2745
9543 10540 11575
结合数据说明Mg的常见化合价为+2价的原因:___________。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反
应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________,铁在元素周期表中的位置___________。
②比较Li+与H-的半径大小关系:r(Li+)___________r(H-)(填“>”或“<”)。
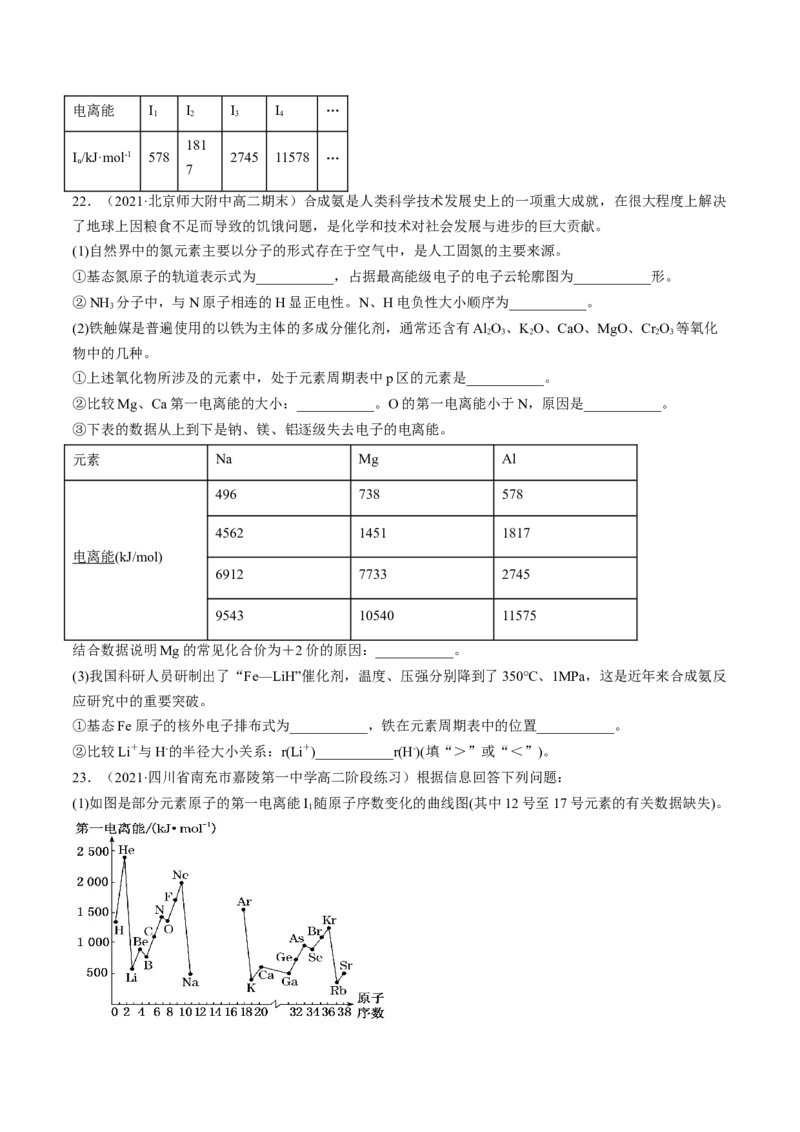
23.(2021·四川省南充市嘉陵第一中学高二阶段练习)根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I 随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
1①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
___________<Al<___________(填元素符号);
②图中Ge元素中未成对电子有___________个;
③图中的C和N可以形成分子(CN) ,该分子中键与键之间的夹角为180°,并有对称性,分子中每个原子
2
最外层均满足8电子稳定结构,其结构式为___________,1个分子中含有___________个π键。
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 Al B Be C Cl F Li
电负
2.0 1.5 2.5 3.0 4.0 1.0
性
元素 Mg N Na O P S Si
电负
1.2 3.0 0.9 3.5 2.1 2.5 1.8
性
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价
键。
①通过分析电负性值变化规律,确定Al元素电负性值的最小范围____;
②判断下列物质是离子化合物还是共价化合物:
A.LiN B.PCl C.MgCl D.SiC
3 3 2
I.属于离子化合物的是____;II.属于共价化合物的是____;