文档内容
南宁二中 2024 届高三化学 5 月月考化学答案
1. 【答案】D【详解】A.青砖青瓦在烧制的过程中,粘土中含有的铁未被完全氧化,还含有二价铁,A正确;
B.铜绿是因为铜与空气中的 、 、 反应生成 ,B正确;C.桂平乳泉井酒酿造过程中要得
到高度数的白酒,需要涉及蒸馏的操作,C正确;壮族服饰的主要原材料棉、麻的成分为纤维素,点燃没有烧焦
羽毛的气味,D错误。
2.A
3.【答案】D【详解】A.配制一定物质的量浓度的溶液,定容后,反复上下颠倒,摇匀,A项正确;B.聚四氟乙
烯活塞的耐腐蚀性能好,所以可以用于碱式滴定管,即可以用氢氧化钠标准溶液滴定未知浓度的盐酸,B项正确;
C.可在坩埚中进行钠与氧气加热时的反应,C项正确;D.因为反应后仍有浓硫酸,需将反应后的混合物沿烧杯
内壁注入水中,边加边搅拌,D项错误;故选D。
4.【答案】B【详解】A.碘和四氯化碳是非极性分子,而水是极性分子,根据相似相溶原理,碘易溶于四氯化
碳而难溶于水,A正确;NaO、MgO、Al O 的离子键成分百分数减少,是因为金属元素和氧元素的电负性差值依
2 2 3
次减小,故B错误;C.对羟基苯甲酸的沸点高于邻羟基苯甲酸,对羟基苯甲酸中,羟基和羧基位于对位,可以形
成分子间氢键,而分子间氢键会增强分子间的作用力,从而使沸点升高,C正确;D.水晶柱面上的固态石蜡在不
同方向熔化的快慢不同是因为原子有序排列,D正确;
5.【答案】C【分析】由题意可知,Y的简单氢化物与其最高价含氧酸反应会产生白烟,则Y为N元素;基态X原
子s轨道上的电子数是p轨道上的2倍,X的原子序数比Y小,则X的电子排布式为:1s22s22p2,为C元素;Z与
C形成的某化合物为CCl 或CS,由于四种元素中只有一种元素的单质为气态,则Z为S元素;基态W原子有1
4 2
个未成对电子,为K元素。【详解】三种离子的原子半径S>K>N,A错误;B.C的氢化物有多种,沸点可能最
大,B错误;C三种最简单氢化物的中心原子均为sp3杂化,孤电子对越多,键角越小,C正确;D.KH是离子化
合物,D错误。
6.【答案】C【详解】A.由图知,分子中含有醚键、碳碳双键、酰胺基三种官能团,A错误;B.由图知,该分子
中的碳碳双键一个为顺式结构,一个为反式结构,B错误;C.结构中有碳碳双键,可以发生加聚反应,结构中有
酰胺基,可以发生水解反应,C正确;D1mol该物质最多消耗5molH ,D错误。
2
7. 【答案】C【详解】A.HO 溶液中含HO,氧原子数目大于N A错误;B.一个CO 中含有两个C=O键,则有
2 2 2 A, 2
两个Π键,标准状况下22.4LCO 的物质的量为 ,含σ键的数目为2N ,B错误C.H原子
2 A
中没有质子,20gDO物质的量为1mol,含有中子数目为10N ,C正确;D.NH OCN中铵根内N元素为-3价,生
2 A 4
成氮气转移6个电子,则1molNH OCN参与反应时转移电子数为6N ,D错误。
4 A
8.【答案】A由分析可知,滤渣的主要成分是铁、镁,故A错误;,碱溶过程中发生的是NaOH和Al的反应,即:
1
学科网(北京)股份有限公司2Al+2NaOH+6H O=2Na[Al(OH) ]+3H ↑,故“碱溶”步骤中发生反应的离子方程式为2Al+2OH-+6H O=2[Al(OH) ]-
2 4 2 2 4
+3H ↑,B正确;C.二氧化碳也能与偏铝酸钠溶液反应生成氢氧化铝沉淀,则可以用过量的二氧化碳代替碳酸氢铵
2
得到氢氧化铝沉淀,故C正确;氢氧化铝沉淀溶于稀硫酸后,加入硫酸钾,蒸发浓缩、冷却结晶、过滤、洗涤、
干燥得到明矾,故D正确。
9.【答案】D【详解】A.一般用质谱法测定有机物的相对分子质量,测定分子空间结构最普遍的方法X射线衍
射,A不符合题意;B.向浓度均为0.1mol/LMgCl 和AlCl 溶液中滴加浓氨水至过量都得到白色沉淀,无法对比
2 3
Mg和Al的金属性,B错误;C.对 增压平衡右移,反应容器压缩容积,混合气体的颜色变深,
是因为体积减小,二氧化氮浓度增大引起的,与平衡移动无关,故C错误;D.向5mL0.2mol/LMgCl 溶液中滴加
2
少量NaOH溶液,氢氧化钠全部转化成氢氧化镁,振荡充分后,再滴加几滴0.2mol/LCuCl 溶液,如果白色沉淀转
2
化成蓝色沉淀,说明氢氧化镁的溶度积大于氢氧化铜的溶度积,故D正确。
10.【答案】C【分析】当K连接 时,b极区溶液能捕获通入的 ,右侧为b极,充电时b为阴极,得电子发生
还原反应,a为阳极失电子发生氧化反应;放电时a为正极发生还原反应,得电子,b为负极发生氧化反应,失电
子,据此分析解题。【详解】A.K连接 时,为电解池,阴极得电子,发生还原反应, b极发生反应:
,A正确;B.K连接 时,a为阳极,与连接电源正极
相连,B正确;C.K连接 时,为原电池,a极为正极,发生还原反应,得电子, ,a
极区 的值减小,C错误;D.该装置通过“充电”和“放电”OH-浓度调控b极区溶
液pH,捕获和释放 ,D正确;故选C。
11.【答案】D【详解】NaSO 水解为可逆反应,反应为SO 2-+H O HSO -+2OH-
2 3 3 2 3
12.【答案】B【详解】A.该晶体中存在金属阳离子,所以该合金属于共价晶体晶体,故A错误;C.由晶胞结
构可知,位于顶点的铁原子与位于体对角线上镁原子的距离最近,则铁原子的配位数为8,故C错误;D.由晶胞
结构可知,晶胞中位于顶点和面心的铁原子个数为8× +6× =4,位于体内的镁原子个数为8,位于体心和棱的中
2
学科网(北京)股份有限公司心位置的氢分子个数为12× +1=4,氢后化学式为FeMg H,故D错误;
2 2
13.【答案】C【分析】反应Ⅰ为吸热反应,反应Ⅱ和反应Ⅲ是放热反应,升高温度反应Ⅰ平衡正向移动,反应Ⅱ
和反应Ⅲ平衡逆向移动,CO和H 的摩尔分数增大,且H 的摩尔分数大于CO,曲线b代表 ,a代表CO,以此
2 2
解答。【详解】A.由盖斯定律可知,反应Ⅰ+反应Ⅲ可得反应Ⅱ,
=-163.9 ,该反应为放热反应,低温下有利于反应Ⅱ正向进行,
A正确;B.由分析可知,曲线b代表 ,B正确;C.由分析可知,曲线b代表 ,a代表CO,当
x(CO)=x(CO )时,温度高于500℃,x(H )>x(HO),反应I的平衡常数K= ,p点温度
2 2 2 p
低于500℃,反应I是吸热反应,温度降低平衡常数减小,则P点时反应I的K<1,C错误;D.由图可知,高温
p
时反应I进行程度很大,反应II、III程度很小接近于0,CH 含量很少接近于0,则平衡不受压强影响,适当增大
4
体系压强, 保持不变,D正确;故选C。
14.【答案】B【分析】由图可看出随HCl通入,曲线Z呈下降趋势,代表 ,曲线X先增后
减,代表 ,曲线Y呈逐渐增大趋势,代表 。【详解】A.根据分析,随着盐酸的加入,
曲线Y呈增大趋势,代表 的变化趋势,A错误;B.由图可知,P 所示溶液,氯化氢和乙二胺之比
3
为1.6∶1,此时溶液中的成份为:C H NCl 和C HNCl,由于1mol 电离产生1mol 和2mol
2 10 2 2 2 9 2
,则此时 ,B正确;C.由图可知,P 所示溶液,氯化氢和乙二胺之比为2∶1,
4
此时溶液中的成份为C H NCl,根据物料守恒可知, ,C错误;
2 10 2 2
D.乙二胺中, , ,图中曲线X与曲线Z的交点
3
学科网(北京)股份有限公司, ,则 ,曲线X与Y的交点
, ,则 ,图中M点是曲线Y与Z的交点,存在
,则 ,故
, ,
, , ,M点 ,
D错误;故选B。
15.【答案】(除标明外,每空2分)
(1)适当加热(或将固体原料粉碎或适当增大硫酸的浓度等)(任答一个)
(2)5.7
(3)6mol/L(1分) 2mol/L(1分)
(4)
(5)
(6)2 (其他化简形式只要正确都可)
16.【答案】(除标明外,每空2分)
(1) 高温(1分)
(2) III(1分) 恒温减压时平衡①、③右移,甲烷平衡转化率增大
(3)温度在500摄氏度以前,温度对②反应影响更大,所以n(CO)增大,温度高于500摄氏度,温度对①反应影
2
响更大,所以n(CO)减小
2
(4)
(5)
17.【答案】(除标明外,每空2分)
(1)催化剂(1分)形成共沸物带出水,促进平衡正向移动,提高产率(2分)
(2) (2分)
(3) 分水器中油水分界层位置保持不变(2分)
(4)分液漏斗(2分)
(5)除掉残留的硫酸等酸性物质(2分)
(6)75(2分)
(7)c(2分)
18.【答案】(除标明外,每空2分)
(1)醚键和氨基
(2)保护羰基不被还原
4
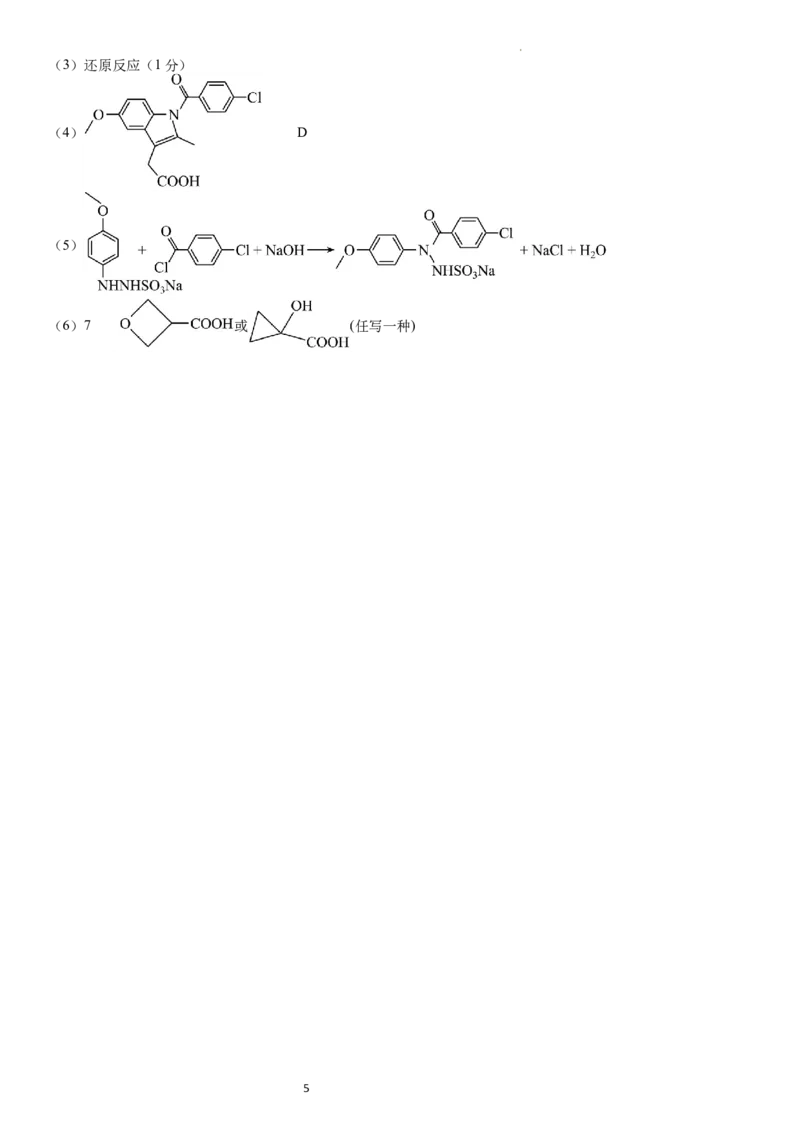
学科网(北京)股份有限公司(3)还原反应(1分)
(4) D
(5)
(6)7 或 (任写一种)
5
学科网(北京)股份有限公司