文档内容
期末复习检测卷一
一、单选题
1.(广西桂林市2022-2023学年高一上学期期末考试化学试题)硒( )元素位于元
素周期表第四周期,与硫同族。以下对于硒( )的相关说法不正确的是
A.Se的原子序数是34 B.Se的原子半径大于S
C.Se的最高化合价为+6价 D. 的还原性比 弱
2.(2023秋·辽宁葫芦岛·高二统考期末)下列化学用语正确的是
A.乙醇的结构式:
B.水的电子式:
C.基态铬原子( )的价层电子排布式:
D.基态氧原子的轨道表示式:
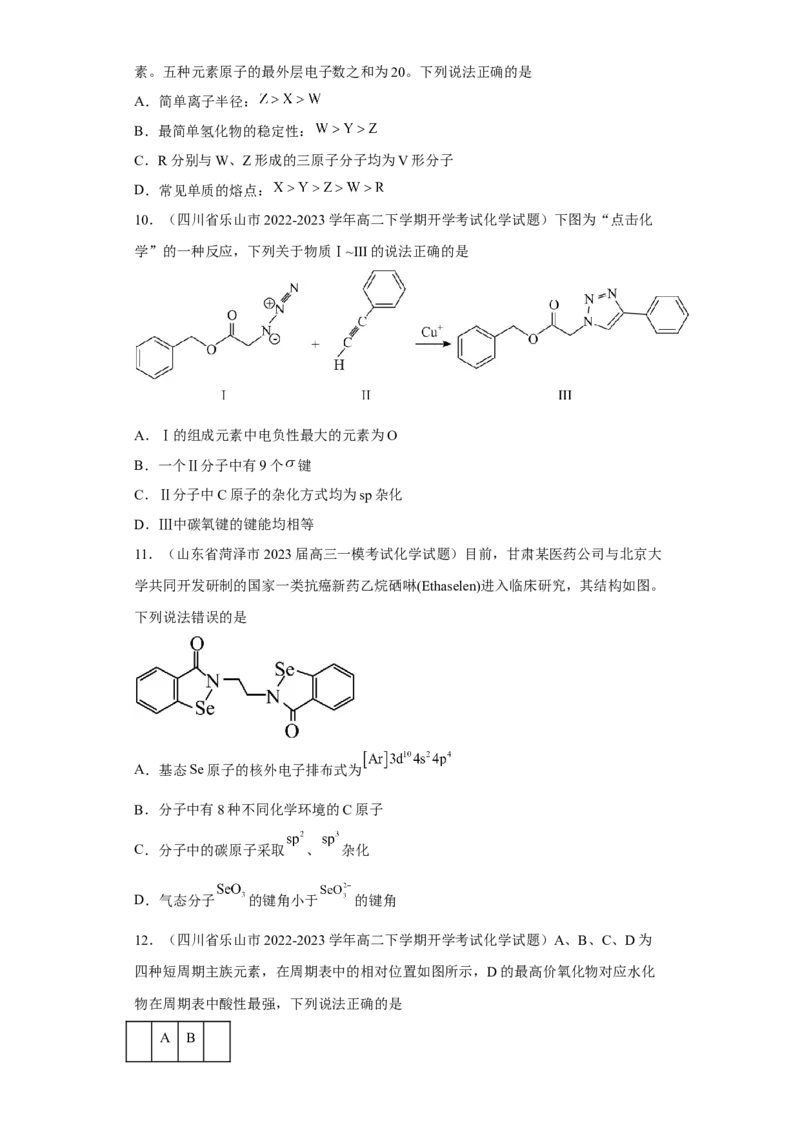
3.(天津市南开区2022-2023学年高二上学期阶段性质量监测化学试题)嫦娥5号月
球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确
的是
A.原子半径:Al<Si B.第一电离能:Mg<Ca
C.Fe位于元素周期表的p区 D.这六种元素中,电负性最大的是O
4.(山东省菏泽市2023届高三一模考试化学试题)居里夫妇用α粒子( )轰击某金
属原子 得到 ,基态Y原子3p能级半充满。 具有放射性,很快衰变为 :, 。下列说法正确的是
A.第一电离能:XB>C
B.非金属性:D>C>B
C.C与D形成的化合物为分子晶体
D.离子 中中心原子的价电子对数为3
13.(2022秋·吉林长春·高三校考阶段练习)下列物质中属于分子晶体,而且既含σ
键又含π键的是
A.KSCN B.CO C.HO D.Al(OH)
2 2 2 3
14.(2022秋·重庆北碚·高二西南大学附中校考开学考试)下列说法正确的是
A.SiO 晶体中最小环是十二元环
2
B.石墨和金刚石中碳原子的杂化类型相同,属于同种晶体类型
C.金刚石比石墨更稳定
D.12g金刚石中含有的C—C数目为1.5N
A
15.(2023·湖南常德·高三常德市鼎城区第一中学校考阶段练习)X、Y、Z、W是元
素周期表中原子序数依次增大的前四周期元素,某科研团队研究发现,X、Y、W形成
的晶体有超导性,该新型超导晶体的一个晶胞如图所示,晶胞参数为apm。已知X是
形成化合物种类最多的元素,Y和W的最外层电子数相同,但不同族,W的次外层电
子数是最外层的8倍,Z是主族元素,其最高价氧化物的水化物可以用于净水,下列
说法正确的是
A.Y的第一电离能小于Z的第一电离能
B.Z的最高价氧化物的水化物可以与X最高价氧化物的水化物反应
C.晶胞中与Y最近的W原子有6个
D.晶体密度为 g/cm3
16.(2023秋·湖北武汉·高三统考期末)O和S为ⅥA族元素,下列说法正确的是
4
原创精品资源学科网独家享有版权,侵权必究!
试卷第4页,共3页A.O元素、S元素可形成多种同分异构体 B. 和 均可和 形成配位键
C. 与 均是强酸 D. 与 中S原子的杂化方式相同
17.(2023秋·上海徐汇·高三上海市西南位育中学校考期末)下列固体熔化时破坏共
价键的是
A.冰 B.铝 C.二氧化硅 D.烧碱
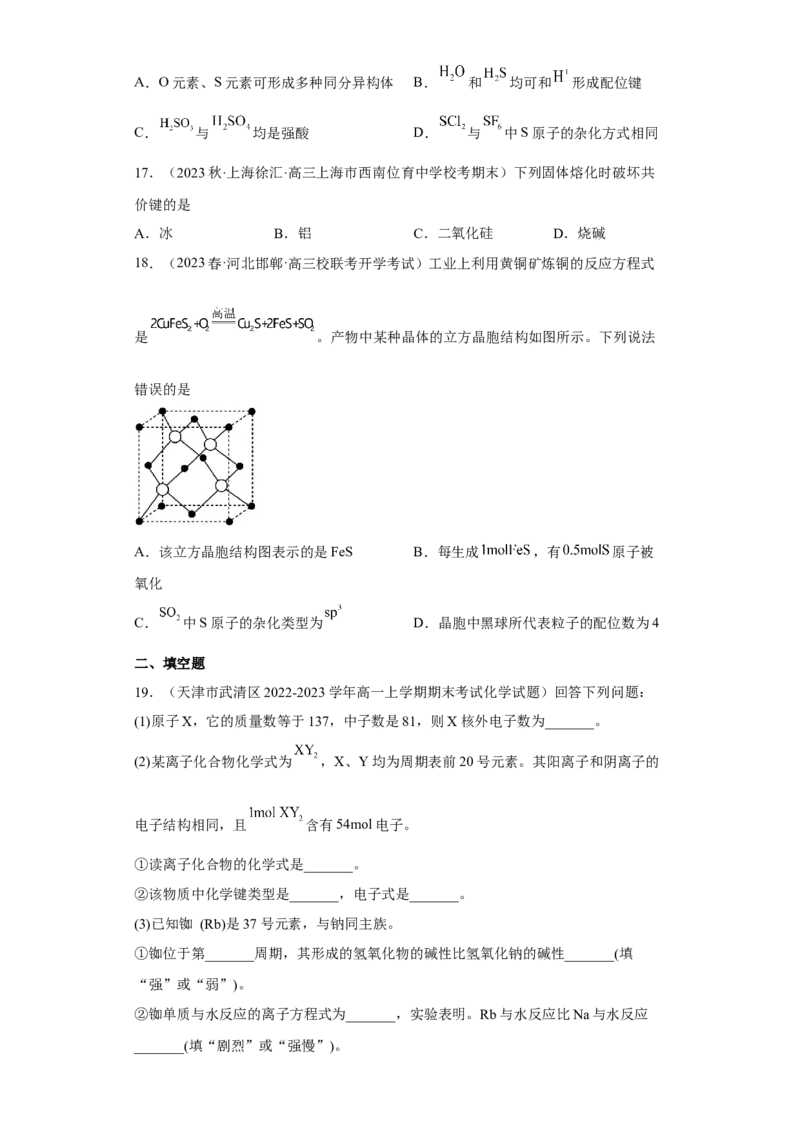
18.(2023春·河北邯郸·高三校联考开学考试)工业上利用黄铜矿炼铜的反应方程式
是 。产物中某种晶体的立方晶胞结构如图所示。下列说法
错误的是
A.该立方晶胞结构图表示的是FeS B.每生成 ,有 原子被
氧化
C. 中S原子的杂化类型为 D.晶胞中黑球所代表粒子的配位数为4
二、填空题
19.(天津市武清区2022-2023学年高一上学期期末考试化学试题)回答下列问题:
(1)原子X,它的质量数等于137,中子数是81,则X核外电子数为_______。
(2)某离子化合物化学式为 ,X、Y均为周期表前20号元素。其阳离子和阴离子的
电子结构相同,且 含有54mol电子。
①读离子化合物的化学式是_______。
②该物质中化学键类型是_______,电子式是_______。
(3)已知铷 (Rb)是37号元素,与钠同主族。
①铷位于第_______周期,其形成的氢氧化物的碱性比氢氧化钠的碱性_______(填
“强”或“弱”)。
②铷单质与水反应的离子方程式为_______,实验表明。Rb与水反应比Na与水反应
_______(填“剧烈”或“强慢”)。20.(2023秋·天津河北·高二天津外国语大学附属外国语学校校考期末)能源、材料
与生产生活和社会发展密切相关。
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半
导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、
GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:_______。
(2)P、S、Ga电负性从大到小的顺序为_______。
(3)As元素的第一电离能_______(填“大于”“小于”或“等于”)Se元素的第一电离
能。
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:_______。
(5)写出3p轨道上只有2个未成对电子的元素的符号:_______、_______。
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键
形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能
量。
化学键 H—H N—H N≡N
键能/(kJ/mol) 436 391 945
(6)已知: ,根据上表中所列键能数据可计
算出a=_______。
21.(2023·全国·高三专题练习)完成下列问题
(1)配体氨基乙酸根 受热分解可产生 和 , 中 键和 键数
目之比是_______。
(2)已知: 是强还原剂,与水反应能生成 。 中含有 键与
键的数目之比为_______,该离子中C的杂化方式为_______。
(3) 的结构如图所示。 原子的杂化类型为_______, 配体
bpy分子中含有 键的数目为_______ 。
6
原创精品资源学科网独家享有版权,侵权必究!
试卷第6页,共3页22.(2022秋·浙江杭州·高二学军中学校考期中)依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
A.简单离子的还原性: P3->O2->F-
B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种
C.焰色试验与电子跃迁有关
D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形
(2)基态氟原子的第一电离能_______基态氮原子的第一电离能(填大于、小于或等于)的
原因是_______。
(3)基态Mn2+的价电子排布式为_______。
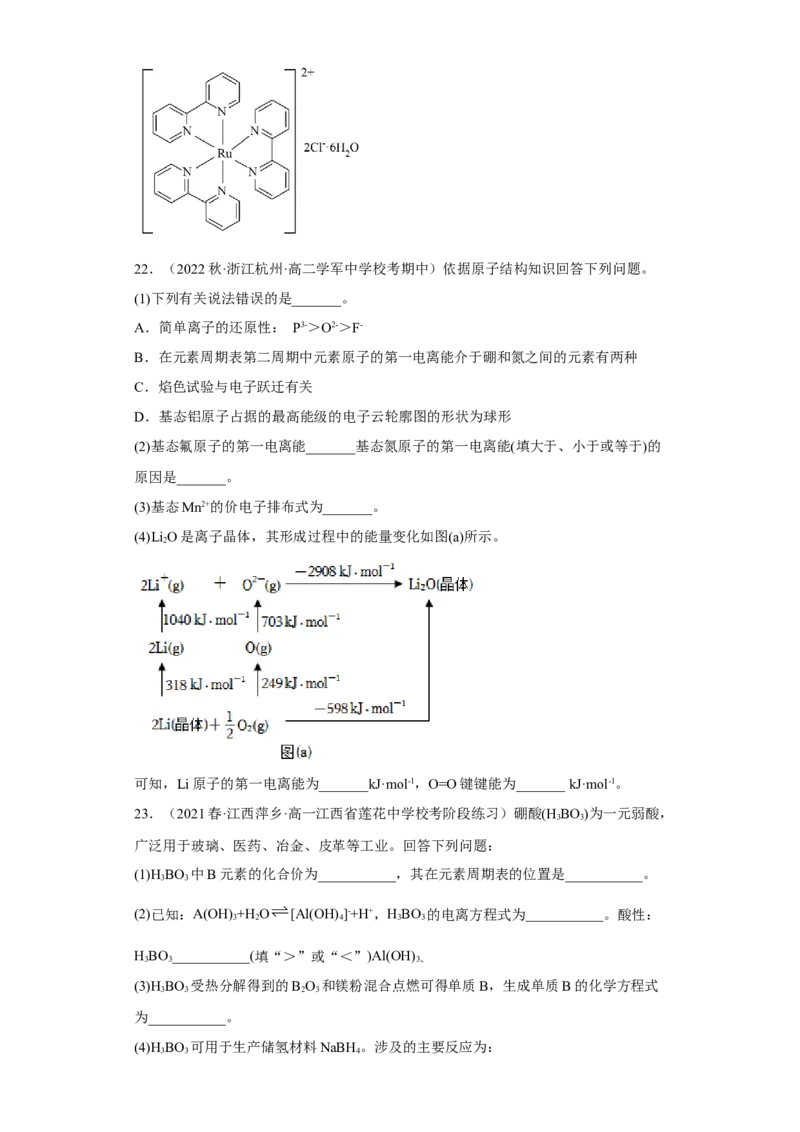
(4)Li O是离子晶体,其形成过程中的能量变化如图(a)所示。
2
可知,Li原子的第一电离能为_______kJ·mol-1,O=O键键能为_______ kJ·mol-1。
23.(2021春·江西萍乡·高一江西省莲花中学校考阶段练习)硼酸(H BO)为一元弱酸,
3 3
广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
(1)H BO 中B元素的化合价为___________,其在元素周期表的位置是___________。
3 3
(2)已知:A(OH) +H O [Al(OH) ]-+H+,HBO 的电离方程式为___________。酸性:
3 2 4 3 3
HBO___________(填“>”或“<”)Al(OH)
3 3 3。
(3)H BO 受热分解得到的B O 和镁粉混合点燃可得单质B,生成单质B的化学方程式
3 3 2 3
为___________。
(4)H BO 可用于生产储氢材料NaBH 。涉及的主要反应为:
3 3 4I.HBO+3CH OH→B(OCH )+3H O
3 3 3 3 3 2
II.B(OCH )+4NaH→NaBH +3CH ONa
3 3 4 3
①NaH的电子式为___________。
②在碱性条件下,NaBH 与CuSO 溶液反应可得Cu和Na[B(OH) ],其中H元素由-1
4 4 4
价升高为+1价,该反应的离子方程式为___________。
24.(2018春·湖北襄阳·高一襄阳四中阶段练习)H、C、N、C、Na、S、Fe是中学化
学中常见的元素,请根据题意回答与这些元素有关的问题:
(1)Fe元素在元素周期表中的位置:___________________;
(2) 写出(CN) 的电子式:___________________;
2
(3)用电子式表示NaN 的形成过程: ___________________;
3
(4)各种氮氧化物(NO、NO )是主要的大气污染物之一,治理氨氧化物(NO )废气的
2 x
方法之一是用NaOH溶液进行吸收,其反应原理可表示如下:
NO +NO+2NaOH=2NaNO +H O 2NO + 2NaOH =NaNO +NaNO +H O
2 2 2 2 2 3 2
现有NO 与NO 的混合气体,将其通入50 mL 2 mol/L的NaOH 溶液中,恰好完全吸
2
收,测得溶液中含有NO 0.02 mol,混合气体中v(NO): v(NO )=_________;
2
(5) 向FeI 溶液中不断通入Cl,溶液中I-、I、IO 、Fe3+、Fe2+等粒子物质的量随
2 2 2
n(Cl )/n(FeI )的变化可用下图简单表示
2 2
当n(Cl )/n(FeI )=6.5 时,溶液中n(Cl-):n(IO )=_________;
2 2
8
原创精品资源学科网独家享有版权,侵权必究!
试卷第8页,共3页