文档内容
第一章单元检测试卷(原卷版)
可能用到的原子量:H 1 N 14 O 16 S 32
第Ⅰ卷
一、选择题:本题共20个小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列关于胶体和溶液的说法中正确的是( )
A.胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀
B.胶体与悬浊液的本质区别是胶体是均一透明的,而悬浊液是浑浊的
C.光线通过时,胶体发生丁达尔效应,溶液则不能发生丁达尔效应
D.只有胶状物如胶水、果冻类的物质才能称为胶体
2.下列叙述中正确的是( )
A.在离子方程式中盐都要以离子形式表示
B.离子反应也可能属于氧化还原反应
C.酸碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应都可以用H++OH- HO表示
2
D.复分解反应必须同时具备离子反应发生的三个条件才能进行
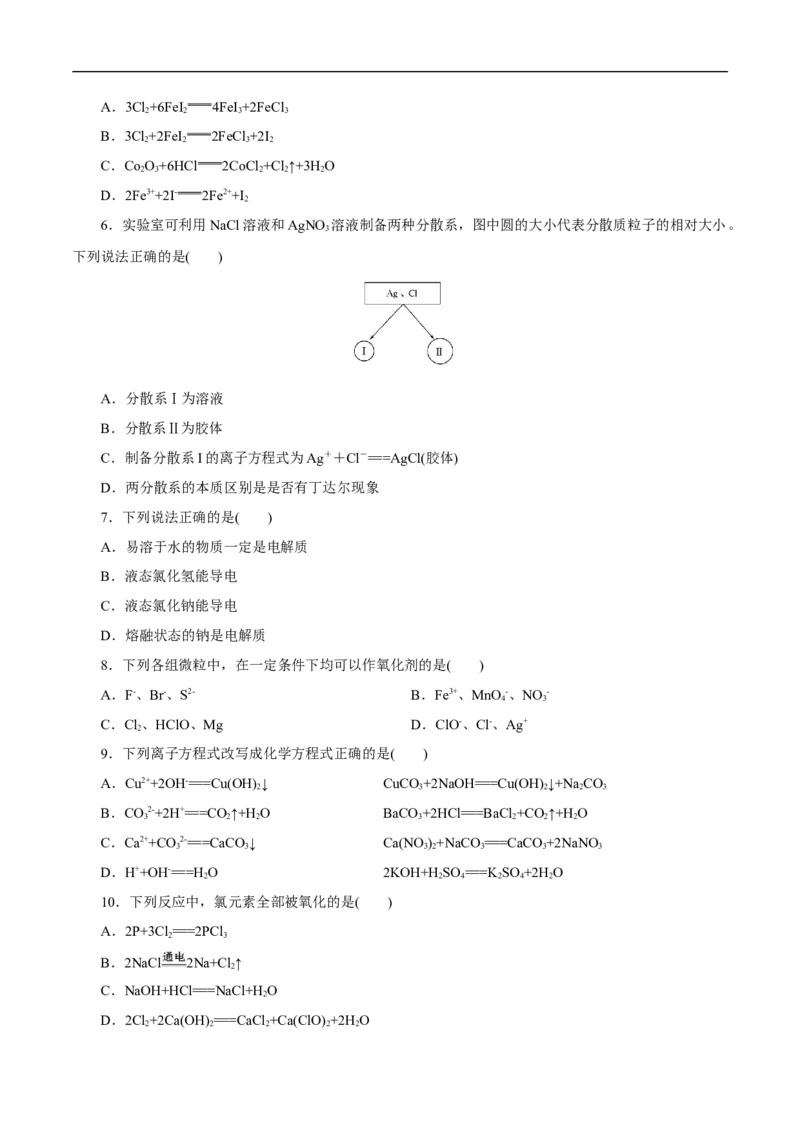
3.下列操作过程中一定有氧化还原反应发生的是( )
4.下列离子能大量共存的是( )
A.使无色酚酞溶液呈红色的溶液中:Na+、K+、S 、C
O2- O2-
4 3
B.无色透明的溶液中:Cu2+、K+、S 、N
O2- O-
4 3
C.含有大量Ba(NO ) 的溶液中:Mg2+、N 、S 、Cl-
3 2 H+ O2-
4 4
D.使紫色石蕊溶液呈红色的溶液中:Na+、K+、C 、N
O2- O-
3 3
5.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 氧化性依次减弱。下列反应在水
2 3 2 3 2 3 2
溶液中不可能发生的是( )A.3Cl+6FeI 4FeI+2FeCl
2 2 3 3
B.3Cl+2FeI 2FeCl +2I
2 2 3 2
C.Co O+6HCl 2CoCl +Cl↑+3H O
2 3 2 2 2
D.2Fe3++2I- 2Fe2++I
2
6.实验室可利用NaCl溶液和AgNO 溶液制备两种分散系,图中圆的大小代表分散质粒子的相对大小。
3
下列说法正确的是( )
A.分散系Ⅰ为溶液
B.分散系Ⅱ为胶体
C.制备分散系I的离子方程式为Ag++Cl-===AgCl(胶体)
D.两分散系的本质区别是是否有丁达尔现象
7.下列说法正确的是( )
A.易溶于水的物质一定是电解质
B.液态氯化氢能导电
C.液态氯化钠能导电
D.熔融状态的钠是电解质
8.下列各组微粒中,在一定条件下均可以作氧化剂的是( )
A.F-、Br-、S2- B.Fe3+、MnO -、NO -
4 3
C.Cl、HClO、Mg D.ClO-、Cl-、Ag+
2
9.下列离子方程式改写成化学方程式正确的是( )
A.Cu2++2OH-===Cu(OH) ↓ CuCO+2NaOH===Cu(OH) ↓+Na CO
2 3 2 2 3
B.CO2-+2H+===CO ↑+H O BaCO +2HCl===BaCl +CO ↑+H O
3 2 2 3 2 2 2
C.Ca2++CO 2-===CaCO ↓ Ca(NO )+NaCO ===CaCO +2NaNO
3 3 3 2 3 3 3
D.H++OH-===H O 2KOH+H SO ===K SO +2H O
2 2 4 2 4 2
10.下列反应中,氯元素全部被氧化的是( )
A.2P+3Cl ===2PCl
2 3
B.2NaCl 2Na+Cl ↑
2
C.NaOH+HCl===NaCl+HO
2
D.2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2H O
2 2 2 2 211.下列叙述中正确的是( )
序号 氧化剂 还原剂 其他反应物 氧化产物 还原产物
① Cl FeBr FeCl
2 2 3
② KMnO HO HSO O MnSO
4 2 2 2 4 2 4
③ KClO HCl(浓) Cl Cl
3 2 2
④ KMnO HCl(浓) Cl MnCl
4 2 2
A.表中第①组反应中FeCl 是还原产物
3
B.氧化性比较:KMnO >Cl>Fe3+>Br >Fe2+
4 2 2
C.还原性比较:HO>Mn2+>Cl-
2 2
D.④组中的HCl既作还原剂,又起到酸的作用。
12.下列反应中,电子转移发生在同种物质的同种元素之间的是( )
A.2HS+SO =3S+2HO B.2KMnO KMnO +MnO +O↑
2 2 2 4 2 4 2 2
C.2KClO 2KCl+3O↑ D.Cu O+HSO =CuSO+Cu+HO
3 2 2 2 4 4 2
13.下列变化必须加入氧化剂才能实现的是
A. CuO→CuSO B.CO→CO C.Fe→Fe O D.KClO→O
4 2 3 4 3 2
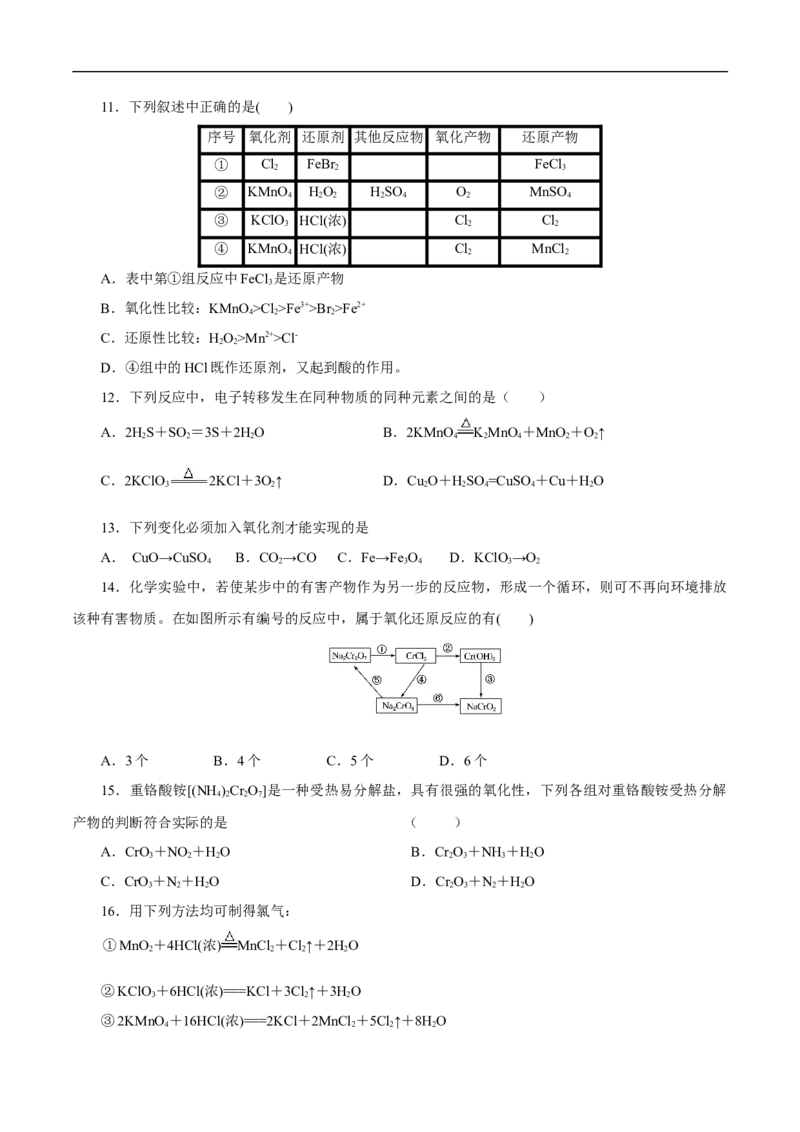
14.化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放
该种有害物质。在如图所示有编号的反应中,属于氧化还原反应的有( )
A.3个 B.4个 C.5个 D.6个
15.重铬酸铵[(NH )Cr O]是一种受热易分解盐,具有很强的氧化性,下列各组对重铬酸铵受热分解
4 2 2 7
产物的判断符合实际的是 ( )
A.CrO+NO +HO B.Cr O+NH +HO
3 2 2 2 3 3 2
C.CrO+N+HO D.Cr O+N+HO
3 2 2 2 3 2 2
16.用下列方法均可制得氯气:
①MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
②KClO+6HCl(浓)===KCl+3Cl↑+3HO
3 2 2
③2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A.6∶5∶6 B.1∶3∶5 C.15∶5∶3 D.1∶6∶10
17.把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。下列说法正确的是( )
A.反应物微粒是S、SO、OH-
B.该反应可能在酸性条件下进行
C.氧化剂与还原剂的质量比为2∶1
D.每生成2个S2-反应转移的电子数为6
18.LiAlH 是金属储氢材料,遇水能剧烈反应释放出H ,LiAlH 在125℃时分解为LiH、H 和Al。下
4 2 4 2
列说法正确的是( )
A.LiAlH 中Al的化合价为-5价
4
B.LiAlH 与水反应时,LiAlH 作氧化剂
4 4
C.1 mol LiAlH 在125℃时完全分解,每生成2个H 分子转移4个电子
4 2
D.LiH是反应的还原产物
19.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中形成无色溶液,其化学方程式为:
PbSO (s)+2CHCOONH(aq)===(CH COO) Pb(aq)+(NH )SO (aq)。当在(CHCOO) Pb溶液中通入HS时,
4 3 4 3 2 4 2 4 3 2 2
有黑色沉淀PbS生成,表示这个反应的离子方程式正确的是( )
A.(CHCOO) Pb+HS===PbS↓+2CHCOOH
3 2 2 3
B.Pb2++HS===PbS↓+2H+
2
C.Pb2++2CHCOO-+HS===PbS↓+2CHCOOH
3 2 3
D.Pb2++2CHCOO-+2H++S2-===PbS↓+2CHCOOH
3 3
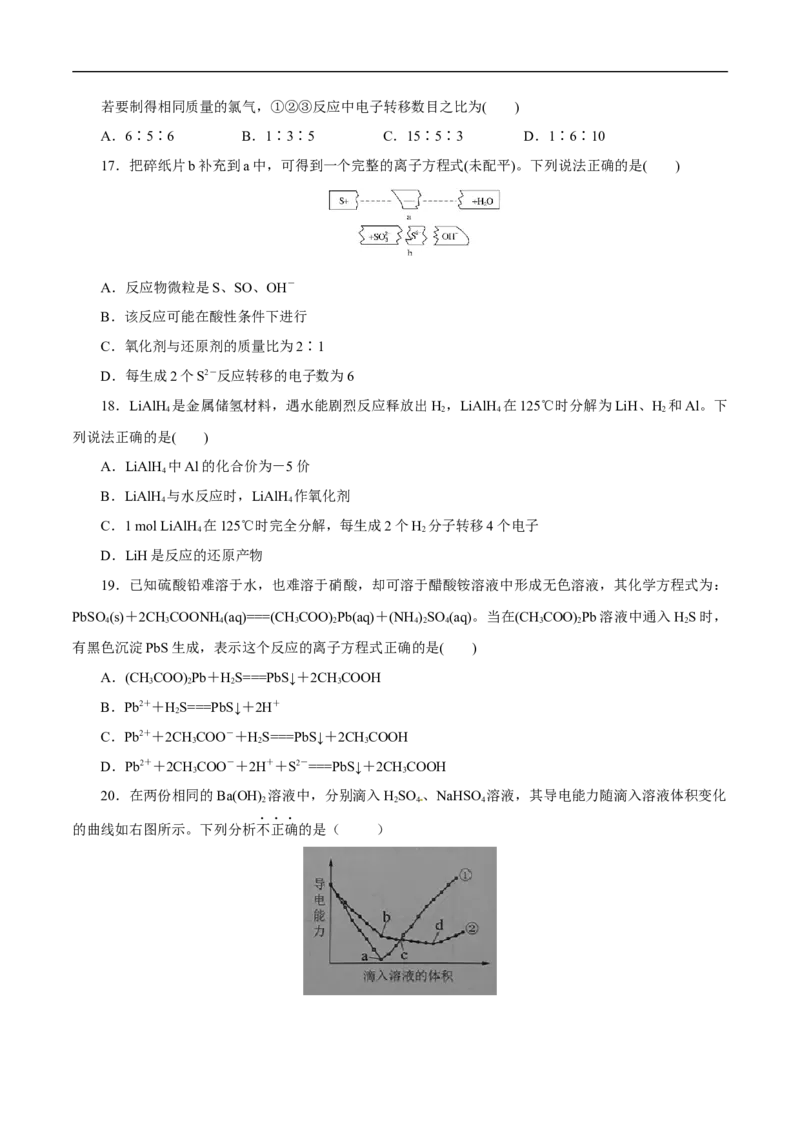
20.在两份相同的Ba(OH) 溶液中,分别滴入HSO 、NaHSO 溶液,其导电能力随滴入溶液体积变化
2 2 4 4
的曲线如右图所示。下列分析不正确的是( )A.①代表滴加HSO 溶液的变化曲线
2 4
B.b点,溶液中大量存在的离子是Na+、OH–
C.曲线①的c点和曲线②的c点所代表的溶液酸碱性相同
D.a、d两点对应的溶液均显中性
第Ⅱ卷
21.(14分)现有以下物质:
NaCl BaSO
① 晶体;②干冰;③ 液态的醋酸;④ 铜;⑤ 4固体;⑥ 蔗糖;⑦ 酒精;⑧ 熔融的
KNO
3;⑨HCl。请回答下列问题(填序号)
(1)以上物质能导电的是 。
(2)以上物质属于电解质的是 。
(3)以上物质属于非电解质的是 。
(4)物质⑨HCl具有 (填写“氧化性”、“还原性”或者“氧化性和还原
性”),理由是 。物质④铜在氧化还原反应中应该
只能表现 (填“氧化性”和“还原性”),写出一个关于HCl的化学反应方程式,该反应
中HCl表现了Cu所不具有的性质 。
22.(8分)将HS和空气的混合气体通入FeCl 、FeCl 、CuCl 的混合溶液中反应回收S,其物质转
2 3 2 2
化如图所示。
(1)写出CuCl 与HS反应的离子方程式:___________________________________________。
2 2
(2)通过上述流程图的分析,整个流程的总反应为 ; 23.
(16分)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO 有毒性,将含该物质的
2
废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
□NaNO + □KI + □ →□NO↑ + □I + □K SO + □Na SO + □
2 2 2 4 2 4
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:(3)用上述反应来处理NaNO 并不是最佳方法,其原因是 。从环保
2
角度来讲,要处理NaNO ,所用的物质的 (填“氧化性”或“还原性”)应该比 KI更
2
(填“强”或“弱”)。
(4)简便鉴别亚硝酸钠和氯化钠的方法是 。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线
桥表示其电子转移的方向和数目。
H SO
24.(6分)在一烧杯中盛有稀 2 4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央(如图所
H SO Ba(OH)
示)。向该烧杯里缓缓注入与稀 2 4等密度的 2溶液至恰好完全反应。在此实验过程中
(1)烧杯里观察到的实验现象有:
① ,② 。
(2)写出实验过程中反应的离子方程式 。
25.(16分)把Cl 通入浓氨水中,发生如下反应:3Cl + 8NH = 6NH Cl + N
2 2 3 4 2
(1)用双线桥表示反应的电子转移方向和数目:
(2)发生化学反应的Cl 与NH 的分子数之比为: ,反应中发生电子转移的Cl 与NH 的分
2 3 2 3
子数之比为:
(3)写出NH Cl在溶液中的电离方程式 ,在其溶液中分散质粒
4
子的直径范围为
(4)若反应中有6.8克氨发生氧化反应,则反应中有生成氮气的质量为