文档内容
鲁科版(2019)必修第一册第二章第3节 氧化还原反应课
时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.已知 晶体和足量浓盐酸可发生如下反应: (浓)
(未配平),下列说法错误的是
A.氧化性:
B.氧化剂与还原剂物质的量之比为
C. 只是还原剂
D.反应中每转移 电子,产生 气体(标准状况)
2. 是一种优良的饮用水处理剂,可用 、 、 混合共熔反应制
得: 。下列关于该反应的说法不正确
的是
A. 是还原剂, 为还原产物
B.在熔融条件下氧化性:
C.每生成 ,转移
D. 在处理饮用水过程中起氧化、杀菌、脱色、除味、净水等作用
3.生物浸出是用细菌等微生物从固体中浸出金属离子,有速率快、浸出率高等特点。
氧化亚铁硫杆菌是一类在酸性环境中加速 氧化的细菌,其浸出ZnS矿机理如图所
示。下列说法错误的是A.浸出过程中,反应I和反应II两步反应都是氧化还原反应
B.在反应I和反应II两步反应过程中化合价没有变化的元素只有H、Zn
C.反应II的方程式:
D.理论上反应I中每消耗 可浸出
4.下列对图示的解释不正确的是
A B C D
NaCl形成示意图
H
2
在Cl
2
中燃烧
向Ba(OH) 溶液中
NaCl固体溶解形成
2
水合离子
加入稀硫酸
白雾可能是HCl遇 a点Ba(OH) 与
2
水蒸气形成 HSO 恰好完全中和
2 4
A.A B.B C.C D.D
5.下列变化中不涉及氧化还原反应的是
A.钢铁的冶炼 B.实验室用大理石制备
C.钢铁的腐蚀 D.食物的腐败
6.下列氧化还原反应中,电子转移的方向和数目均正确的是
A. B.
C. D.
7. 可以发生反应: ,下列说法正确的是
A. 中O显负价
试卷第2页,共3页B. 既是氧化剂又是还原剂
C.标准状况下,若生成 ,则转移 电子
D.该反应可说明 还原性强于
8.氧化还原反应与四种基本类型反应的关系如下图,则下列化学反应属于阴影部分的
是
A. B.
C. D.
9. 是国际上公认的新一代高效、安全、环保的杀菌消毒剂。利用 (Fe的化合
价为+2)制备 和用 除去水体中 的反应如下:
反应①:
反应②:
下列说法正确的是
A.反应①中, 是还原剂,发生还原反应
B.反应中①,每生成1mol ,反应转移1mol电子
C.由反应①可知:氧化产物只有
D.由反应②可知酸性: 大于HCl
10.下列叙述正确的是
A.金属单质在氧化还原反应中一定做还原剂
B.非金属单质在氧化还原反应中一定做氧化剂
C.金属阳离子在氧化还原反应中一定做氧化剂D.某元素由游离态变为化合态,该元素一定被氧化
11.下列离子方程式正确的是
A.利用 溶液腐蚀铜质电路板:
B. 溶液与过量NaOH溶液反应:
C.将足量的氯气通入 溶液中:
D.将 气体通入NaClO溶液中:
12.已知:①绿茶中含有大量的鞣酸;②鞣酸亚铁溶液为无色,鞣酸铁溶液为蓝黑色,
概据如图所示的实验流程分析,下列叙述错误的是
A.绿茶叶水与FeSO 反应生成的鞣酸亚铁易被氧化成鞣酸铁而呈蓝黑色
4
B.维生素C可将鞣酸铁还原成鞣酸亚铁
C.④中发生的反应只有1个
D.服用补铁剂时不能喝绿茶
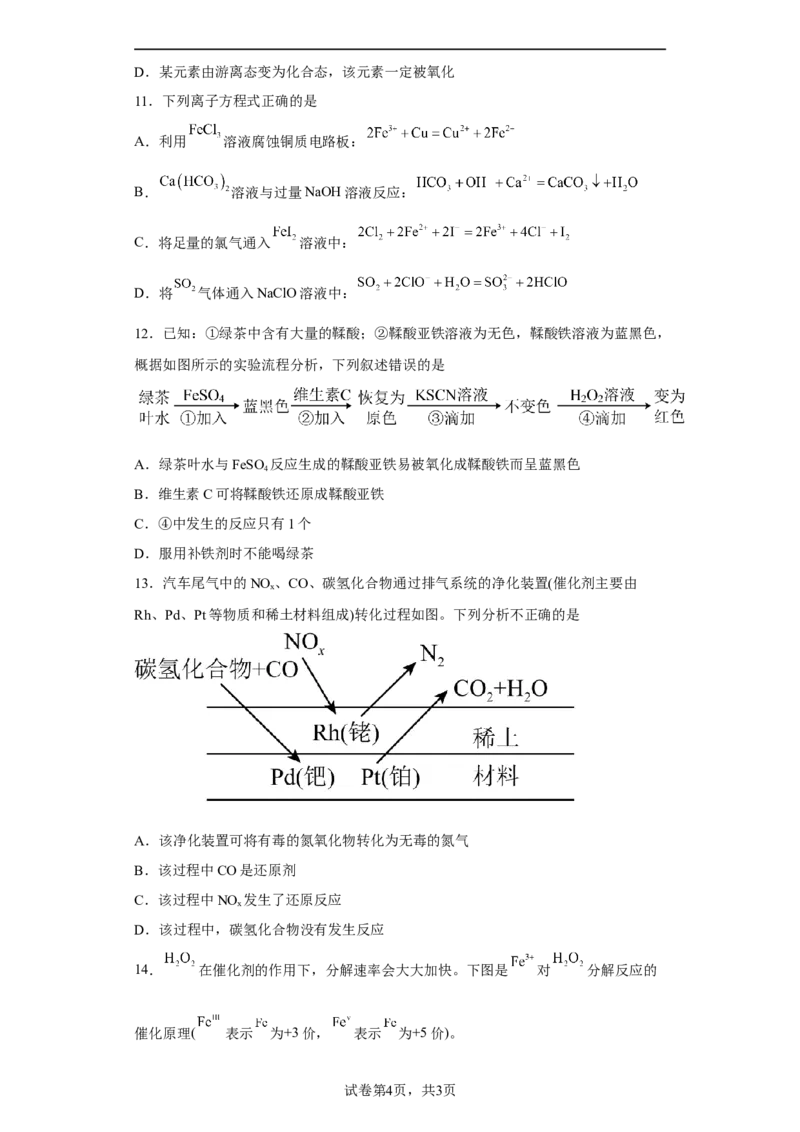
13.汽车尾气中的NO 、CO、碳氢化合物通过排气系统的净化装置(催化剂主要由
x
Rh、Pd、Pt等物质和稀土材料组成)转化过程如图。下列分析不正确的是
A.该净化装置可将有毒的氮氧化物转化为无毒的氮气
B.该过程中CO是还原剂
C.该过程中NO 发生了还原反应
x
D.该过程中,碳氢化合物没有发生反应
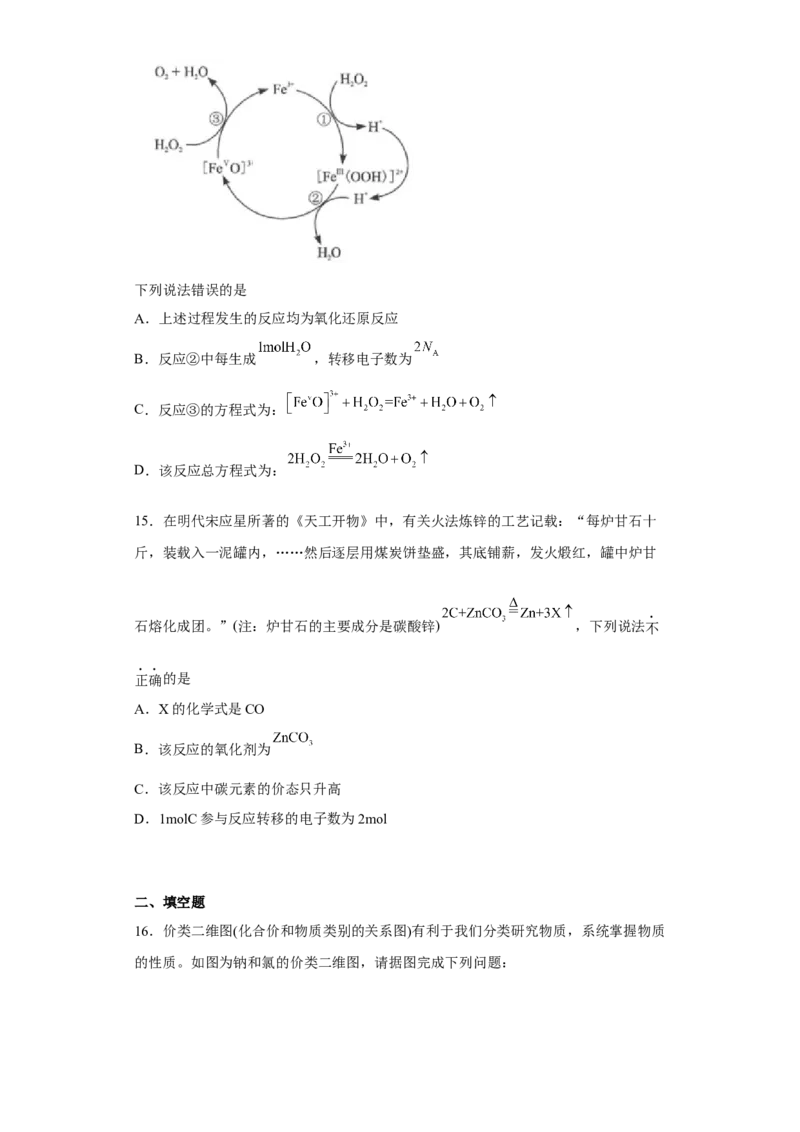
14. 在催化剂的作用下,分解速率会大大加快。下图是 对 分解反应的
催化原理( 表示 为+3价, 表示 为+5价)。
试卷第4页,共3页下列说法错误的是
A.上述过程发生的反应均为氧化还原反应
B.反应②中每生成 ,转移电子数为
C.反应③的方程式为:
D.该反应总方程式为:
15.在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十
斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘
石熔化成团。”(注:炉甘石的主要成分是碳酸锌) ,下列说法不
正确的是
A.X的化学式是CO
B.该反应的氧化剂为
C.该反应中碳元素的价态只升高
D.1molC参与反应转移的电子数为2mol
二、填空题
16.价类二维图(化合价和物质类别的关系图)有利于我们分类研究物质,系统掌握物质
的性质。如图为钠和氯的价类二维图,请据图完成下列问题:(1)分别由 和 形成的等物质的量的氯气的质量之比为__________。
(2) 属于__________(填“酸性”或“碱性”)氧化物,与 相遇会生成
__________(填化学式)。
(3) A、B两处分别对应的物质是__________、__________。(填化学式)
(4)A可用于自来水消毒,是因为该物质具有__________性,与氯气相比,其用于消毒
的优点有__________。
(5)将 和 按一定比例混合后,用稀硫酸酸化,能够生成一种刺激性气味的
气体,写出该反应的离子方程式__________。
(6)研究发现, 具有漂白性是因为 不稳定,会分解释放出活性氧原子 ,
具有很强的氧化性,可将部分有颜色的物质氧化成无色(或白色)物质,则下列与
性质相似的物质是__________。(填序号)
① ② ③活性炭
17.请回答下列问题:
(1)CrO 是一种酸根离子,Fe(CrO ) 中铁元素的化合价为_______,Fe(CrO ) 属于
2 2 2 2
_______(填“酸”、“碱”、“盐”或“氧化物")。
(2)新型纳米材料氧缺位铁酸盐(MFe O,3”“<”或“=”)Cl。
3 2
②ClO,在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下
2
列试剂中,可将ClO 转化为 的是_______(填字母)。
A.FeSO B.O C.KMnO
4 3 4
③在一定条件下,RO 和Cl 可发生如下反应:RO +Cl+OH-=RO +2Cl-+HO,
2 2 2
由以上反应可知在上述过程中RO 被_______(填“氧化”或“还原”);RO 中元素R
的化合价是_______。
20.针对以下A~D四个涉及HO 的反应填空:
2 2
A.NaO+2HCl=H O+2NaCl
2 2 2 2
B.Ag O+HO=2Ag+O↑+HO
2 2 2 2 2
C.2HO=2H O+O↑
2 2 2 2
D.3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O
2 2 2 4 3 2 4 2 4 2
(1)H O 仅体现氧化性的是_______(填序号,下同),HO 仅体现还原性的是_______,
2 2 2 2
HO 既体现氧化性又体现还原性的是_______,HO 既不作氧化剂又不作还原剂的是
2 2 2 2
_______。
(2)标出反应D中电子转移的方向和数目_______,反应中氧化剂是_______,被氧化的
元素是_______,还原产物是_______。
三、实验题
21.铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
氯化铁:熔点为 ,沸点为 ;易吸收空气中的水分而潮解。工业上采用向
的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为 ,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯
化亚铁。
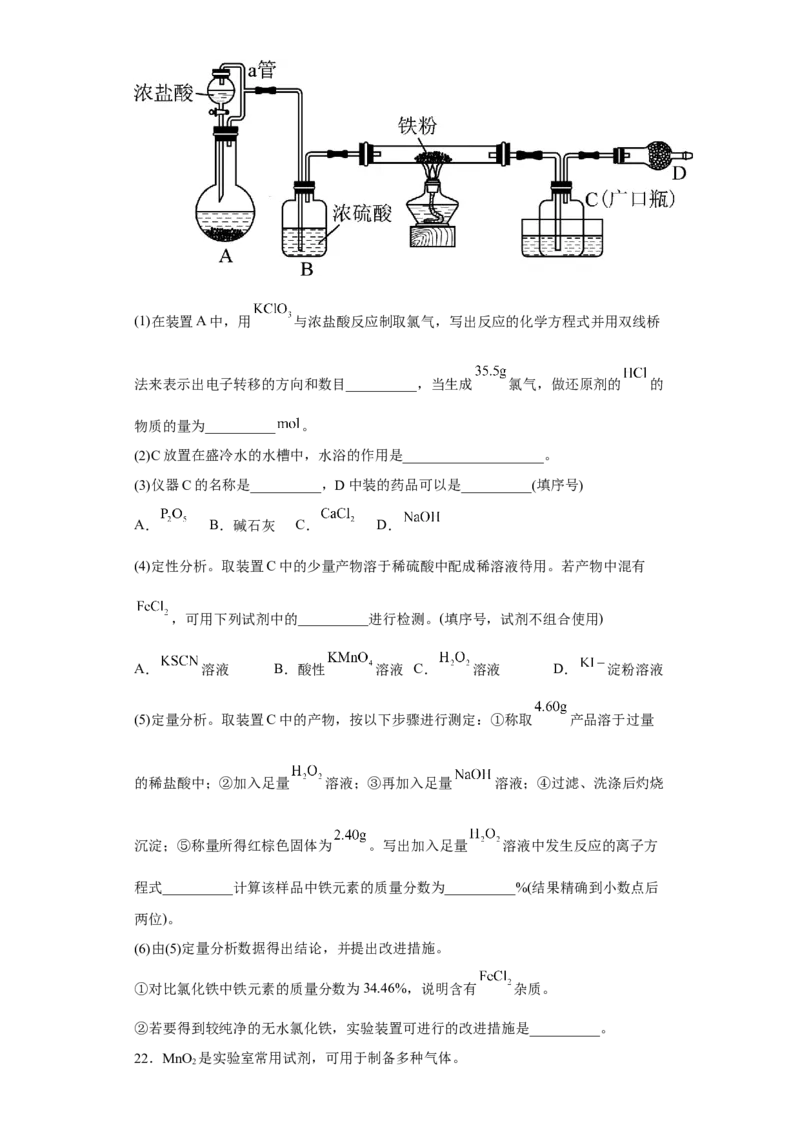
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回
答下列问题:
试卷第8页,共3页(1)在装置A中,用 与浓盐酸反应制取氯气,写出反应的化学方程式并用双线桥
法来表示出电子转移的方向和数目__________,当生成 氯气,做还原剂的 的
物质的量为__________ 。
(2)C放置在盛冷水的水槽中,水浴的作用是____________________。
(3)仪器C的名称是__________,D中装的药品可以是__________(填序号)
A. B.碱石灰 C. D.
(4)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有
,可用下列试剂中的__________进行检测。(填序号,试剂不组合使用)
A. 溶液 B.酸性 溶液 C. 溶液 D. 淀粉溶液
(5)定量分析。取装置C中的产物,按以下步骤进行测定:①称取 产品溶于过量
的稀盐酸中;②加入足量 溶液;③再加入足量 溶液;④过滤、洗涤后灼烧
沉淀;⑤称量所得红棕色固体为 。写出加入足量 溶液中发生反应的离子方
程式__________计算该样品中铁元素的质量分数为__________%(结果精确到小数点后
两位)。
(6)由(5)定量分析数据得出结论,并提出改进措施。
①对比氯化铁中铁元素的质量分数为34.46%,说明含有 杂质。
②若要得到较纯净的无水氯化铁,实验装置可进行的改进措施是__________。
22.MnO 是实验室常用试剂,可用于制备多种气体。
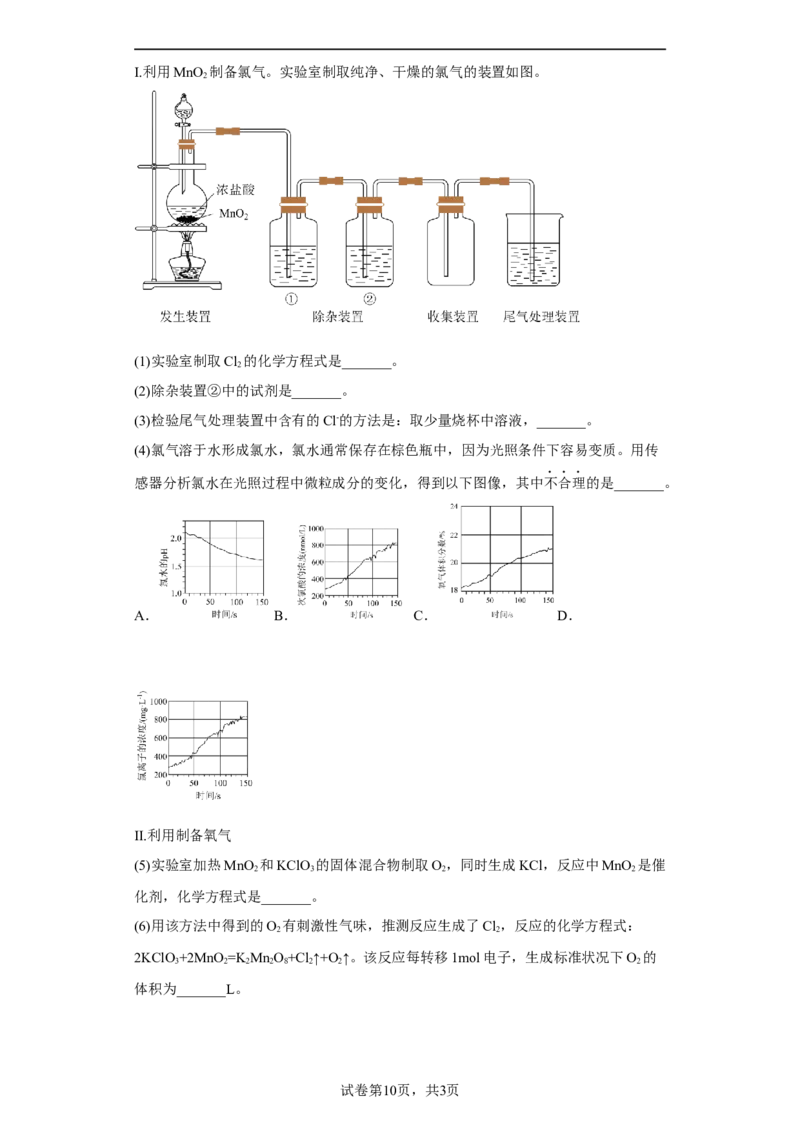
2Ⅰ.利用MnO 制备氯气。实验室制取纯净、干燥的氯气的装置如图。
2
(1)实验室制取Cl 的化学方程式是_______。
2
(2)除杂装置②中的试剂是_______。
(3)检验尾气处理装置中含有的Cl-的方法是:取少量烧杯中溶液,_______。
(4)氯气溶于水形成氯水,氯水通常保存在棕色瓶中,因为光照条件下容易变质。用传
感器分析氯水在光照过程中微粒成分的变化,得到以下图像,其中不合理的是_______。
A. B. C. D.
Ⅱ.利用制备氧气
(5)实验室加热MnO 和KClO 的固体混合物制取O,同时生成KCl,反应中MnO 是催
2 3 2 2
化剂,化学方程式是_______。
(6)用该方法中得到的O 有刺激性气味,推测反应生成了Cl,反应的化学方程式:
2 2
2KClO+2MnO=K MnO+Cl↑+O ↑。该反应每转移1mol电子,生成标准状况下O 的
3 2 2 2 8 2 2 2
体积为_______L。
试卷第10页,共3页参考答案:
1.C
【详解】A.氧化剂的氧化性大于氧化产物的氧化性,该反应中氯酸钾是氧化剂、HCl是
还原剂,则氯气是氧化产物,所以氧化性KClO >Cl ,故A正确;
3 2
B.反应中,6molHCl中有5mol被氧化,则氧化剂与还原剂的物质的量之比为1:5,故B正
确;
C.该反应中Cl元素化合价由+5价、-1价变为0价,则Cl 既是还原产物又是氧化产物,
2
故C错误;
D.KClO+6HCl(浓)=KCl+3Cl +3H O反应中Cl元素化合价由+5价、-1价变为0价,所以
3 2 2
反应中每转移5mol电子,产生3mol氯气,体积为22.4L/mol 3mol=67.2L气体(标准状
况),故D正确;
故答案为:C。
2.C
【详解】A. , 化合价升高,被氧化,作还原剂, ,
化合价降低,被还原,作氧化剂,生成物为还原产物,A正确;
B.根据氧化性:氧化剂>氧化产物,,所以氧化性: ,B正确;
C. ,化合价升高3价,每生成 ,转移 ,C错误;
D. 具有强氧化性,在处理饮用水过程中起氧化、杀菌、脱色等,其还原产物
水解生成 胶体,具有吸附性,能达到净水的目的,D正确;
故选C。
3.D
【详解】A.反应I和反应II两步反应都是氧化还原反应,A正确;
B.在反应I和反应II两步反应过程中化合价变化的元素为O、Fe、S,化合价没有变化的
元素有H、Zn,B正确;
C.由图中转化可知反应Ⅱ的方程式为2Fe3++ZnS═Zn2++2Fe2++S,C正确;
D.没有注明标况,无法根据气体体积计算,D错误;
故选D。4.A
【详解】A.Na与Cl 反应,生成NaCl,电子转移的方向和数目可表示为
2
,A不正确;
B.H 在Cl 中燃烧,生成的HCl易溶于水,遇空气中的水蒸气产生白雾,B正确;
2 2
C.向Ba(OH) 溶液中加入稀硫酸,当二者刚好完全反应时发生反应Ba(OH) + H SO =
2 2 2 4
BaSO↓+ 2H O,此时溶液中离子浓度很小,导电能力接近0,对应图中的a点,C正确;
4 2
D.NaCl固体溶解水,Na+、Cl-都形成水合离子,但通常仍以Na+和Cl-表示,电离方程式
为 ,D正确;
故选A。
5.B
【详解】A.钢铁的冶炼时发生反应Fe O+3CO 2Fe+3CO ,涉及氧化还原反应,A不符
2 3 2
合题意;
B.实验室用大理石制备CO,发生反应CaCO +2HCl=CaCl +H O+CO↑,不涉及氧化还原
2 3 2 2 2
反应,B符合题意;
C.钢铁的腐蚀时,Fe最终转化为铁锈,涉及氧化还原反应,C不符合题意;
D.食物的腐败时,食物中的油脂、蛋白质等发生氧化反应,涉及氧化还原反应,D不符
合题意;
故选B。
6.B
【详解】A.该反应中Cl化合价从+5价降低为-1价,共得到 个电子,同理O共失去
个电子,A错误;
B.该反应中Mg化合价从0价升高为+2价,共失去 个电子,同理O共得到
个电子,B正确;
C.该反应中Cu化合价从+2价降低为0价,共得到 个电子,C化合价从0价升高到
答案第2页,共2页+4价,共失去4个电子,C错误;
D.该反应中O化合价从0价降低到-2价,共得到 个电子,D错误;
故答案选B。
7.C
【分析】HS+4OF=SF +2HF+4O 中,HS中S的化合价为-2价,OF 中O元素化合价为
2 2 2 6 2 2 2 2
+1价,F为-1价,SF 中,S的化合价为+6价,F为-1价,HF中H为+1价,F为-1价,据
6
此结合氧化还原反应的规律分析解答。
【详解】A.OF 中F只有负价为-1价,则O元素化合价为+1价,A错误;
2 2
B.OF 中只有氧元素化合价降低,故它只作氧化剂,B错误;
2 2
C.由化学方程式可知,每生成4mol ,反应转移8mol电子,则 转移0.4mol电
子,C正确;
D.由化学方程式可知,OF 中氧元素化合价降低,OF 作氧化剂,O 作还原产物,因此
2 2 2 2 2
无法比较二者的还原性强弱,D错误;
故选C。
8.A
【分析】从图中可以得出,阴影部分的反应,不属于化合反应、不属于分解反应、不属于
置换反应,但属于氧化还原反应。
【详解】A.反应 属于燃烧反应,属于氧化还原反应,但不属
于化合反应、不属于分解反应、不属于置换反应,A符合题意;
B.反应 的反应物只有一种,属于分解反应,B不符合题意;
C.反应 的生成物只有一种,属于化合反应,C不符合
题意;
D.反应 中,单质Fe与可溶性铜盐反应,生成Cu和可溶性亚铁盐,
属于置换反应,D不符合题意;
故选A。9.B
【详解】A.反应①中 中铁元素从+2价变为+3价,硫素从-1价变为+6价,则FeS 为
2
还原剂,发生氧化反应,A错误;
B.由反应①方程式可得关系式: ,故每生成1mol ,反应转移1mol
电子,B正确;
C.由反应①可知, 中铁元素和硫素化合价均升高,则氧化产物为: 、
,C错误;
D.反应②是氧化还原反应,不能比较反应物和产物的酸性,D错误;
故本题选B。
10.A
【详解】A.金属单质只能失电子不能得电子,所以金属单质在氧化还原反应中一定做还
原剂,A正确;
B.非金属单质在氧化还原反应中既可得电子,也可失电子,所以不一定做氧化剂,B不正
确;
C.金属阳离子在氧化还原反应中也可能失电子,如Fe2+与氯气等氧化剂反应,所以不一定
做氧化剂,C不正确;
D.某元素由游离态变为化合态,其可能失电子,也可能得电子,所以该元素不一定被氧
化,D不正确;
故选A。
11.A
【详解】A.利用 溶液腐蚀铜质电路板: ,A正确;
B. 溶液与过量NaOH溶液反应:
,B错误;
C.足量的氯气通入 溶液中,Fe2+、I-比例为1:2,离子方程式为
答案第4页,共2页,C错误;
D. 气体与NaClO溶液发生氧化还原反应,D错误;
故选A。
12.C
【详解】A.鞣酸亚铁溶液为无色,鞣酸铁溶液为蓝黑色,在绿茶叶水中加入FeSO ,出现
4
蓝黑色,说明鞣酸亚铁易被氧化,A正确;
B.向蓝黑色溶液中加入维生素C,溶液由蓝黑色恢复原色,说明维生素C能将鞣酸铁还
原成鞣酸亚铁,表现还原性,B正确;
C.④中发生的反应有维生素C、Fe2+被HO 氧化、Fe3+与SCN-的络合反应等,反应不止2
2 2
个,C错误;
D.因为绿茶叶水中的鞣酸与补铁剂中的Fe2+反应生成鞣酸亚铁,鞣酸亚铁不稳定,易被氧
化为鞣酸铁,故服用补铁剂时不能喝绿茶,D正确;
故选C。
13.D
【详解】A.根据图示信息,NO 经过该净化装置转化为无毒的氮气,A正确;
x
B.CO经过该净化装置转化为CO,C元素化合价升高,为还原剂,B正确;
2
C.NO 经过该净化装置转化为无毒的氮气,反应中N元素化合价降低,被还原,发生还
x
原反应,C正确;
D.该过程中,碳氢化合物经过该净化装置转化为CO、HO,发生了化学反应,D错误;
2 2
故选D。
14.A
【详解】A.反应①中元素化合价没有变化,所以不属于氧化还原反应,反应②③中有元
素化合价变化,属于氧化还原反应,A错误;
B.反应②中铁元素化合价从+3价升高到+5价,所以每生成 ,转移电子数为 ,
B正确;
C.反应③中双氧水被氧化生成氧气,铁元素化合价降低,反应的方程式为:
,C正确;
D.根据流程图可知反应物是双氧水,生成物是水和氧气,铁离子作催化剂,所以该反应总方程式为: ,D正确;
答案选A。
15.C
【详解】A.根据元素守恒,X的化学式是 ,A正确;
B. ,元素化合价降低,被还原作氧化剂,B正确;
C. , 碳元素的化合价又升高,又降低,C错误;
D.根据反应方程式中的化合价变化, ,2molC参与反应转移的电子数为4mol电
子,1molC参与反应转移的电子数为2mol,D正确;
故选C。
16.(1)
(2) 碱性
(3)
(4) (强)氧化 高效、安全、无异味
(5)
(6)②
【详解】(1) 的相对原子质量是35, 的相对原子质量是37,分别由 和
形成的等物质的量的氯气的质量之比为35:37;
(2) 能与元素反应生成氯化钠和水, 属于碱性氧化物; 是酸性氧化物,
与 相遇会生成 。
(3)A是+4价氧化物,Na没有+4价,A是氯的+4价氧化物,A是 ,B是碱,B表示
;
答案第6页,共2页(4)A处是高价态氯的氧化物,该物质具有强氧化性,与氯气相比,相同质量的该物质被
还原时,能得到更多的电子,氧化能力更强,消毒能力大大增加;同时更安全:不会产生
对人体有害的有机氯化物,排除了氯气本身的毒性,也减少了消毒时残留的氯气的气味。
(5)在酸性条件下,Cl-、 发生归中反应生成氯气,该反应的离子方程式为
;
(6)根据题意,物质不稳定,且分解时能产生氧气,故选②。
17.(1) +2价 盐
(2) 胶体 氧化还原
(3) Fe O Cu O
2 2
(4)b
(5)+3
【详解】(1)根据CrO 可判断Fe(CrO ) 中铁元素的化合价为+2价,Fe(CrO ) 是金属阳
2 2 2 2
离子与酸根离子组成的盐类,故答案为:+2价;盐。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于胶体,铁酸盐
MFe O 经过高温反应得到MFe O 的反应中因为M=Mn,Zn,Ni.且均为+2价,所以铁元素
2 4 2 x
一定变价,该反应属于氧化还原反应,故答案为:胶体;氧化还原。
(3)在酸性条件下。Fe O 容易转化为Fe2+,铁元素化合价降低,Fe O 作氧化剂,另应
2 2
该有元素化合价升高的元素,故6种粒子Fe O 、Fe3+、H+、HO、Cu O、Cu2+中应该选择
2 2 2
Cu O→Cu2+,则该反应中还原剂是Cu O,故答案为:Fe O ;Cu O。
2 2 2 2
(4)NaSO 中S的化合价为+2价,制备NaSO 时选用的反应物是含S元素,则根据氧
2 2 3 2 2 3
化还原反应中的“归中反应”规律,反应物中S元素的化合价应一个大于+2价、一个小于
+2价,只有NaSO +S符合,故答案为:b。
2 3
(5)S元素的化合价由+4价升高为+6价,Cr元素的化合价由+6价降低,设还原产物中Cr
元素的化合价为x,由电子守恒可知:0.024L0.05mol/L(6-4)=0.02L 0.02mol/L2(6-x),解得x =+3,故答案为:+3。
18.(1) < NaHCO
3
(2) 2H++CaCO =Ca2++CO↑+HO 还原
3 2 2
【详解】(1)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,碳酸钠受热不分解,因此热
稳定性:NaHCO <NaCO,实验室可用如图装置验证,A中温度高,B中温度比A中温
3 2 3
度低,在低温下分解,在高温下不分解,则可以说明高温下的物质热稳定性好,因此试管
B中应装入的固体是NaHCO ;故答案为:<;NaHCO 。
3 3
(2)①从物质类别上看,HCl属于酸,能与大理石反应,酸和盐反应生成新酸和新盐,则
相应的离子方程式为2H++CaCO =Ca2++CO↑+HO;故答案为:2H++CaCO =Ca2++
3 2 2 3
CO↑+HO。
2 2
②从化合价角度看, 处于最低价,只能升高,因此 具有还原性;故答案为:还原。
19.(1) 胶体 丁达尔效应
(2)A
(3) 1:1 > A 氧化 +6
【详解】(1)气溶胶是微粒分散到空气中形成的胶体,胶体能产生丁达尔效应,可用丁达
尔效应鉴别溶液和胶体,故答案为:胶体;丁达尔效应;
(2)A. 漂白粉的有效成分是具有强氧化性的次氯酸钙,故A正确;
B. 苏打水不具有强氧化性,也不能使蛋白质变性,因此不能用作杀灭新型冠状病毒活体的
消毒剂,故B错误;
C. 氯气常用于自来水的杀菌消毒,其中起杀菌消毒作用的是氯气与水反应生成的次氯酸,
故C错误;
D. “84”消毒液(NaClO)与洁厕灵(HCl)混合两者反应生成有毒的氯气,会降低杀菌消毒的效
果,故D错误;
故答案为:A;
(3)2NaClO+4HCl=2ClO ↑+Cl↑+2H O+2NaCl①该反应中,氯酸钠中Cl元素化合价降低
3 2 2 2
被还原成二氧化氯,HCl中氯元素化合价升高被氧化成氯气,结合反应可知被氧化与被还
原的氯原子之比为1:1,反应中氯酸钠作氧化剂,氯气为氧化产物,氧化性:氧化剂>氧
化产物,因此氯酸钠氧化性大于氯气,故答案为:1:1;>;
答案第8页,共2页②ClO 转化为 ,由化合价可知Cl元素化合价降低,被还原,应加还原剂才能实现,结
合选项硫酸亚铁具有强的还原性可做还原剂,臭氧和高锰酸钾常做氧化剂,故答案为:
A;
③结合反应可知氯气在反应中转化成氯离子,作氧化剂,则RO 应做还原剂,被氧化;
RO 中O为-2价,结合各元素的代数和为-2可知,R的价态应为+6,故答案为:氧化;
+6;
20.(1) D B C A
(2) HO Cr HO
2 2 2
【详解】(1)A.反应NaO+2HCl=H O+2NaCl为复分解反应,元素的化合价都不发生
2 2 2 2
改变;
B.在反应Ag O+HO=2Ag+O↑+HO中,HO 中O元素由-1价升高到0价,HO 作还
2 2 2 2 2 2 2 2 2
原剂;
C.反应2HO=2H O+O↑为分解反应,且属于氧化还原反应,HO 中所含O元素化合价一
2 2 2 2 2 2
部分升高,一部分降低;
D.反应3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O中,HO 中所含O元素化合价降
2 2 2 4 3 2 4 2 4 2 2 2
低,作氧化剂,Cr (SO ) 作还原剂。
2 4 3
由以上分析可知,HO 仅体现氧化性的是D,HO 仅体现还原性的是B,HO 既体现氧化
2 2 2 2 2 2
性又体现还原性的是C,HO 既不作氧化剂又不作还原剂的是A。答案为:D;B;C;
2 2
A;
(2)反应D为3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O,HO 作氧化剂,
2 2 2 4 3 2 4 2 4 2 2 2
Cr (SO ) 作还原剂,电子转移的方向和数目为
2 4 3
,反应中氧化剂是HO,被氧化的元素
2 2是Cr,还原产物是HO。答案为: ;
2
HO;Cr;HO。
2 2 2
21.(1)
(2)将 蒸气冷却凝华为固体收集
(3) 球形干燥管 BD
(4)B
(5) 36.52
(6)在 装置间增加一个装有饱和食盐水的洗气装置,除去 中混有的
【分析】在装置A中,用 与浓盐酸反应制取氯气,生成的氯气中混有水和氯化氢气
体,通过装置B干燥氯气,氯气和铁在加热条件下发生反应生成氯化铁,通过装置C收集
氯化铁,D是尾气处理装置,以此解答。
【详解】(1)在装置A中,用 与浓盐酸反应制取氯气,Cl元素由+5价下降到0价,
又由-1价上升到0价,用双线桥法来表示出电子转移的方向和数目为:
;由方程式可知,若6molHCl参与反应,5molHCl做
还原剂,生成3mol氯气,当生成35.5g氯气,物质的量为 =0.5mol,做还原剂的
答案第10页,共2页HCl的物质的量为0.5mol× = mol,故答案为: ; ;
(2)氯化铁的熔点为306℃,沸点为315℃,C放置在盛冷水的水槽中,冷水浴的作用是
将 蒸气冷却凝华为固体收集,故答案为:将 蒸气冷却凝华为固体收集;
(3)由仪器D的结构可知名称是球形干燥管;氯气有毒需要尾气处理,又因为氯化铁易
吸收空气中的水分而潮解,所以D中装的药品是碱石灰或固体NaOH, 和CaCl 可以
2
吸水,但是不能吸收氯气,故答案为:球形干燥管;BD;
(4)KSCN溶液、KI-淀粉溶液可以用来检验Fe3+,由于溶液中存在大量Fe3+,因此
溶液和Fe2+反应的现象不明显,酸性 溶液可以用来检验Fe3+中混有的Fe2+,现象是
酸性高锰酸钾溶液褪色,故答案为B;
(5)双氧水能把亚铁离子氧化为铁离子,离子方程式为:2Fe2++H O+2H+=2Fe3++2H O,
2 2 2
加入氢氧化钠转化为氢氧化铁沉淀,灼烧转化为氧化铁,物质的量是 =
0.015mol,根据铁元素守恒可知铁元素的质量是0.015mol×2×56g/mol=1.68g,则该样品中
铁元素的质量分数为 ×100%≈36.52%,故答案为:2Fe2++H O+2H+=2Fe3++2H O;
2 2 2
36.52;
(6)由于生成的氯气中含有氯化氢,氯化氢能与铁反应生成氯化亚铁,则若要得到较纯净
的无水氯化铁,可采取的“装置”改进措施是在AB装置间增加一个装有饱和食盐水的洗
气装置,除去Cl 中混有的HCl,故答案为:在 装置间增加一个装有饱和食盐水的洗气
2
装置,除去 中混有的 。
22.(1)MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(2)浓硫酸(3)滴加用稀硝酸酸化的硝酸银溶液,有白色沉淀生成
(4)B
(5)2KClO 2KCl+3O ↑
3 2
(6)2.24L
【分析】实验室用MnO 与浓盐酸在加热下反应制取Cl,由于浓盐酸易挥发,制得的Cl
2 2 2
中混有HCl和水蒸气。用装置①中的饱和食盐水除去HCl,用装置②中的浓硫酸干燥Cl;
2
用向上排空气法收集Cl,Cl 尾气用NaOH溶液吸收。
2 2
【详解】(1)实验室用MnO 与浓盐酸在加热条件下制取Cl,化学方程式是
2 2
MnO +4HCl(浓) MnCl +Cl↑+2H O。答案为:MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2 2 2 2 2
(2)由分析可知,除杂装置②用于干燥Cl,所盛试剂是浓硫酸。答案为:浓硫酸;
2
(3)检验尾气处理装置中含有的Cl-,可使用硝酸银溶液,方法是:取少量烧杯中溶液,
滴加用稀硝酸酸化的硝酸银溶液,有白色沉淀生成。答案为:滴加用稀硝酸酸化的硝酸银
溶液,有白色沉淀生成;
(4)在氯水中,发生如下反应:Cl+H O H++Cl-+HClO、2HClO 2HCl+O ↑。
2 2 2
A.随着氯水放置时间的不断增长,HClO不断分解,Cl 与水反应不断进行,最终氯水转
2
化为稀盐酸,氢离子浓度增大,溶液的pH减小,A合理;
B.在光照条件下,HClO不断分解,Cl 与水的反应不断进行,所以HClO的浓度不断减小,
2
最终为0,氯水转化为稀盐酸,B不合理;
C.随着反应的进行,HClO不断分解生成O,Cl 不断减少,O 不断增多,所以氧气的体
2 2 2
积分数不断增大,C合理;
D.随着反应的进行,氯水转化为稀盐酸,Cl-浓度不断增大,D合理;
故选B。答案为:B;
(5)实验室加热MnO 和KClO 的固体混合物制取O,同时生成KCl,反应中MnO 是催
2 3 2 2
化剂,化学方程式是2KClO 2KCl+3O ↑。答案为:2KClO 2KCl+3O ↑;
3 2 3 2
(6)从化学方程式:2KClO+2MnO=K MnO+Cl↑+O ↑可以看出,Cl元素从+5价降低到
3 2 2 2 8 2 2
0价,Mn元素从+4价升高到+7价,O元素从-2价升高到0价,则可建立如下关系式:O
2
答案第12页,共2页——10e-,该反应每转移1mol电子,生成标准状况下O 的体积为0.1mol×22.4L/mol=2.24L
2
L。答案为:2.24L。
【点睛】处理氯气尾气时,可用使用碱性溶液,也可以使用还原性溶液。答案第14页,共2页