文档内容
第一章第三节氧化还原反应小题狂做--人教版(2019)必修
第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.根据下列反应:(1) ;(2) ,判断离子
的还原性由强到弱的顺序是
A. B. C. D.
2.春秋初期,绍兴一带是南方的一个冶铁中心, 其炼铁方法是在1000°C左右的温度
下Fe O 发生一系列的反应生成含较多杂质的海绵铁。其中主要化学反应为:
2 3
3CO+Fe O 2Fe+3CO ,下列说法正确的是
2 3 2
A.海绵铁是一种纯净物
B.Fe O 中铁元素的化合价为+2价
2 3
C.上述反应中涉及的氧化物有3种
D.炼铁过程中,木炭只是作为燃料使用
3.在一个密闭容器中放入A、B、M、Q四种物质,在一定条件下发生化学反应,一
段时间后,测得有关数据如下表,下列说法中,不正确的是
物质 A B M Q
3
反应前质量(g) 18 1 2
2
1
反应后质量(g) X (未知) 26 2
2
A.反应后物质A的质量为13gB.该变化的基本反应类型是分解反应
C.反应中B、M的质量比为5∶4
D.物质Q可能是该反应的催化剂
4.在氧化还原反应中,氧化剂得到的电子总数等于还原剂失的去电子总数,这个规律
称为电子得失守恒。在一定条件下, 发生了以下反应: +Cl+2OH-=
2
+2Cl-+H O下列说法错误的是
2
A.n=2 B. 中R的价态为+6价
C. 中R的价态为+5价 D. 是氧化产物
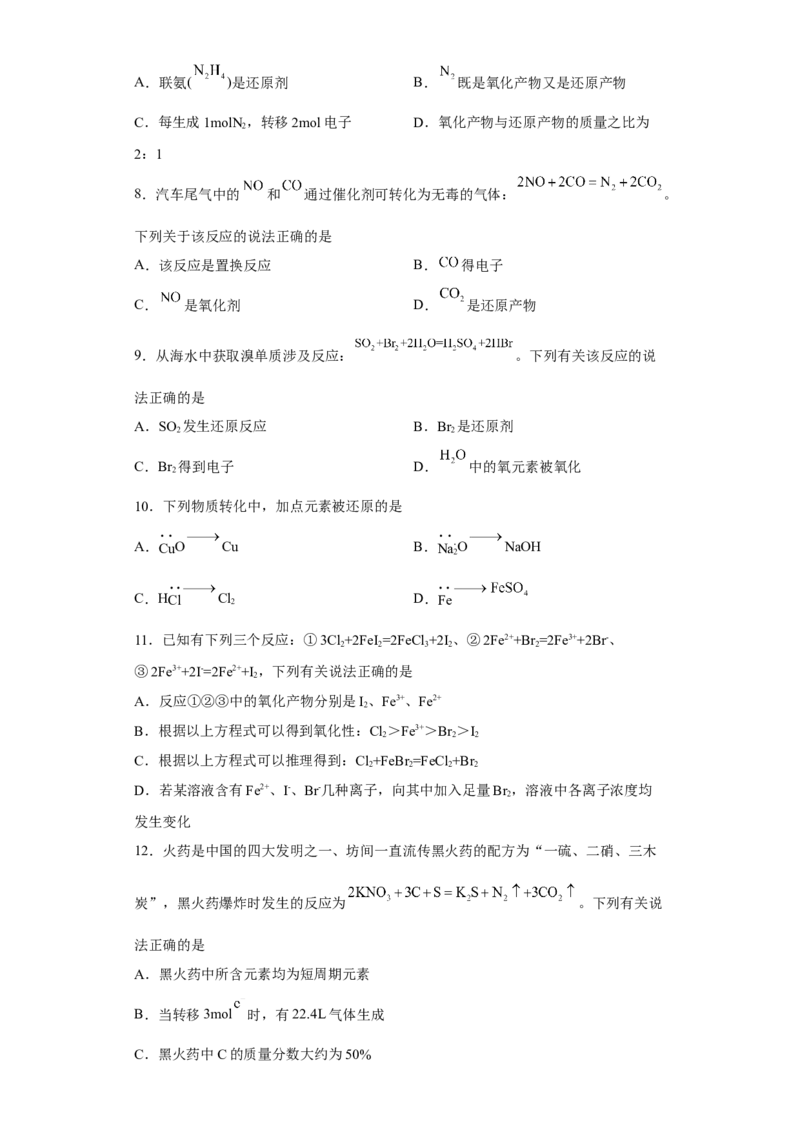
5.一种“地康法”制取氯气的反应原理如图所示,下列说法错误的是
A.反应Ⅰ属于复分解反应 B.反应Ⅱ中 为还原剂
C.由图可知该条件下, 的氧化性强于 的 D.若要制得 ,则消耗
的体积为
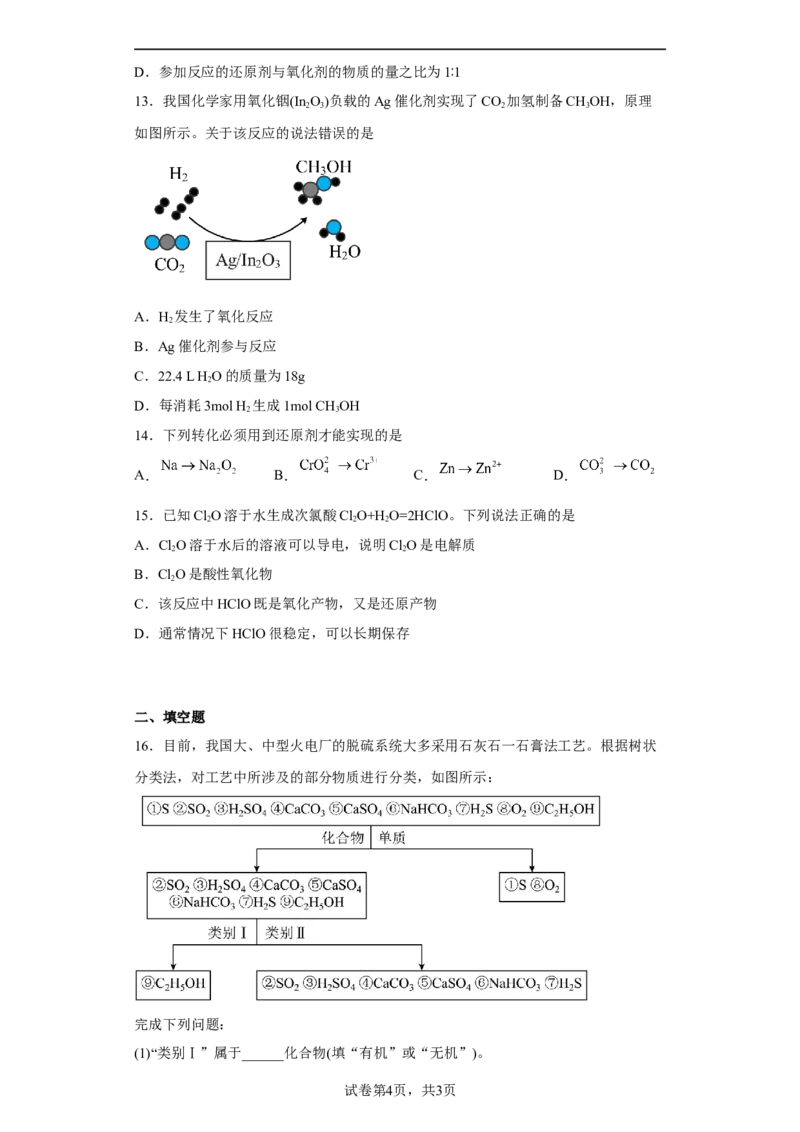
6.下列变化中,与氧化还原反应无关的是
A.食物的腐败 B.钢铁的锈蚀 C.钟乳石的形成 D.燃料的燃烧
A.A B.B C.C D.D
7.2022年11月30日,神舟十五号航天员与神舟十四号航天员首次实现“太空会师”。
火箭推进剂联氨( )与NO 反应的化学方程式为 ,下列说
2 4
法错误的是
试卷第2页,共3页A.联氨( )是还原剂 B. 既是氧化产物又是还原产物
C.每生成1molN ,转移2mol电子 D.氧化产物与还原产物的质量之比为
2
2:1
8.汽车尾气中的 和 通过催化剂可转化为无毒的气体: 。
下列关于该反应的说法正确的是
A.该反应是置换反应 B. 得电子
C. 是氧化剂 D. 是还原产物
9.从海水中获取溴单质涉及反应: 。下列有关该反应的说
法正确的是
A.SO 发生还原反应 B.Br 是还原剂
2 2
C.Br 得到电子 D. 中的氧元素被氧化
2
10.下列物质转化中,加点元素被还原的是
A.CuO Cu B.NaO NaOH
2
C.HCl Cl
2
D.Fe
11.已知有下列三个反应:①3Cl+2FeI =2FeCl +2I 、②2Fe2++Br =2Fe3++2Br-、
2 2 3 2 2
③2Fe3++2I-=2Fe2++I ,下列有关说法正确的是
2
A.反应①②③中的氧化产物分别是I、Fe3+、Fe2+
2
B.根据以上方程式可以得到氧化性:Cl>Fe3+>Br >I
2 2 2
C.根据以上方程式可以推理得到:Cl+FeBr =FeCl +Br
2 2 2 2
D.若某溶液含有Fe2+、I-、Br-几种离子,向其中加入足量Br ,溶液中各离子浓度均
2
发生变化
12.火药是中国的四大发明之一、坊间一直流传黑火药的配方为“一硫、二硝、三木
炭”,黑火药爆炸时发生的反应为 。下列有关说
法正确的是
A.黑火药中所含元素均为短周期元素
B.当转移3mol 时,有22.4L气体生成
C.黑火药中C的质量分数大约为50%D.参加反应的还原剂与氧化剂的物质的量之比为1∶1
13.我国化学家用氧化铟(InO)负载的Ag催化剂实现了CO 加氢制备CHOH,原理
2 3 2 3
如图所示。关于该反应的说法错误的是
A.H 发生了氧化反应
2
B.Ag催化剂参与反应
C.22.4 L H O的质量为18g
2
D.每消耗3mol H 生成1mol CHOH
2 3
14.下列转化必须用到还原剂才能实现的是
A. B. C. D.
15.已知ClO溶于水生成次氯酸ClO+HO=2HClO。下列说法正确的是
2 2 2
A.ClO溶于水后的溶液可以导电,说明ClO是电解质
2 2
B.ClO是酸性氧化物
2
C.该反应中HClO既是氧化产物,又是还原产物
D.通常情况下HClO很稳定,可以长期保存
二、填空题
16.目前,我国大、中型火电厂的脱硫系统大多采用石灰石一石膏法工艺。根据树状
分类法,对工艺中所涉及的部分物质进行分类,如图所示:
完成下列问题:
(1)“类别Ⅰ”属于______化合物(填“有机”或“无机”)。
试卷第4页,共3页(2)“类别Ⅱ”中,属于酸式盐的是______(填编号)。
(3)SO 通入足量NaOH溶液反应的离子方程式为______。
2
(4)脱疏反应之一SO +CaCO =CaSO +CO ,该反应______氧化还原反应(填“属于”或
2 3 3 2
“不属于”);通入空气将CaSO 浆液转化为石膏CaSO·2H O的化学方程式为______。
3 4 2
(5)将SO 通入饱和HS溶液中发生SO +2H S=3S↓+2H O,氧化产物与还原产物的物质
2 2 2 2 2
的量之比为______,测得溶液的电导率随通入SO 体积的变化曲线如图所示(电导率是
2
衡量电解质溶液导电能力大小的物理量),则二者恰好完全反应的点是图中的______点
(填“a”“b”或“c”)。
17.把Cl 通入浓氨水中,发生如下反应:3Cl +8NH=6NHCl +N 。
2 2 3 4 2
(1)用双线桥表示反应的电子转移方向和数目:_______。
(2)发生化学反应的Cl 与NH 的分子数之比为_______,反应中发生电子转移的Cl 与
2 3 2
NH 的分子数之比为_______。
3
(3)写出NH Cl在溶液中的电离方程式_______,在其溶液中分散质粒子的直径范围为
4
_______。
(4)若反应中有6.8克氨发生氧化反应,则反应中有生成氮气的质量为_______。
(5)在一个密闭容器中放入以下四种物质,在一定条件下发生化学反应,一段时间后,
测得有关数据如下:
物质 M N Q P
反应前质量(g) 50 1 3 12
反应后质量(g) x 26 3 30
①该变化的基本反应类型是_______反应;
②物质Q在反应中起的作用是_______。
18.已知下列反应:
①Cl+2NaBr=2NaCl+Br ;
2 2
②2KI+Br =2KBr+I ;
2 2
(1)Cl 、Br 、I 三种物质的氧化性由强到弱的顺序是______。
2 2 2
(2)判断Cl 与KI能否发生反应:_____(不能请填“否”,能请写出反应的离子方程式)。
2(3)已知实验室制取氯气的反应为MnO +4HCl(浓) MnCl +Cl↑+2H O,由此分析,
2 2 2 2
MnO 在反应中______(填“得到”或“失去”)电子,已知Mn的相对原子质量是55,
2
当有87gMnO 发生_____(填“氧化”或“还原”)反应时,同时有______gHCl发生
2
_____(填“氧化”或“还原”)反应。
(4)在硫酸溶液中,NaClO 和NaSO 能按粒子个数比1∶2完全反应,生成一种棕黄色气
3 2 3
体ClO,同时NaSO 转化为NaSO ,该反应是否是氧化还原反应?______(填“是”
2 2 3 2 4
或“否”)请写出该反应的化学方程式:______。
19.已知: ,按要求完成下列空格。
(1)用单线桥标明电子转移方向和数目_______。
(2)该反应中氧化剂是_______。
(3)该反应中被氧化的HCl与参加反应的HCl的物质的量之比为_______。
20.氧化还原反应是中学化学的重要内容。回答下列问题:
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为 。
该反应中氧化剂为_______,还原产物为_______。
(2)用单线桥法表示电子转移的方向和数目:________
被氧化和被还原的氯原子的个数之比为_______。
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,
配平该离子方程式:__________
_______ _______ _______ _______ _______ _______
试卷第6页,共3页参考答案:
1.C
【详解】还原性还原剂大于还原产物;① 中碘离子为还原剂、亚铁
离子为还原产物,则还原性碘离子大于亚铁离子;② 中亚铁离子
为还原剂、溴离子为还原产物,则还原性亚铁离子大于溴离子;
故选C。
2.C
【详解】A.海绵铁有较多杂质,是化合物,A错误;
B.Fe O 中铁元素的化合价为+3价,B错误;
2 3
C.上述反应中涉及的氧化物有一氧化碳、二氧化碳和氧化铁3种,C正确;
D.炼铁过程中,木炭燃烧提供热量和提供还原性环境,碳和一氧化碳都是很好的还原剂,
D错误;
故选C。
3.B
【分析】由数据可知,Q反应前后质量不变,不是反应物或生成物;由质量守恒知A反应
后为13g,A、M是反应物,B是生成物;
【详解】A.由质量守恒知A反应后为13g,A正确;
B.该变化有两种反应物,一种生成物,该变化的基本反应类型是化合反应,B错误;
C.反应中B、M的质量比为25∶20=5∶4,C正确;
D.物质Q反应前后质量不变,可能是该反应的催化剂,D正确;
故选B。
4.C
【分析】1molCl 得2mole-,化合价降低生成氯离子,氯气是氧化剂;根据电子得失守恒知
2
1mol 失去2mole-生成 ,故 中R元素为+4价,n=2;
【详解】A.由分析知n=2,A正确;
B. 中R的价态为+6价,B正确;
C. 中R的价态为+4价,C错误;D. 失去电子化合价升高发生氧化反应生成 , 是氧化产物,D正确;
故选C。
5.D
【分析】反应I为氧化铜与HCl反应生成氯化铜和水的过程;反应II为氯化铜与氧气反应
生成氧化铜 氯气的过程,其化学方程式为: ,据此分析。
【详解】A.反应I为氧化铜与HCl反应生成氯化铜和水的过程,属于复分解反应,A正确;
B.反应II 中Cl元素化合价从-1价升高到0价,被氧化,所以 作还原剂,B正
确;
C.氧化剂的氧化性大于氧化产物的氧化性,根据反应II可知, 的氧化性强于 的氧
化性,C正确;
D.未指明是否为标准状况,无法准确计算消耗 的体积,D错误;
故选D。
6.C
【详解】A.食物的腐败发生氧化还原反应,A错误;
B.钢铁的锈蚀发生氧化还原反应,B错误;
C.钟乳石的形成不发生氧化还原反应,C正确;
D.燃烧为氧化还原反应,D错误;
故选C。
7.C
【详解】A.联氨( )中氮化合价升高,因此联氨是还原剂,故A正确;
B. 是联氨中氮化合价升高得到,也是NO 中氮化合价降低得到,因此 既是氧化产
2 4
物又是还原产物,故B正确;
C.根据方程式分析转移8mol电子生成3mol氮气,因此每生成1molN ,转移 mol电子,
2
故C错误;
D.3mol氮气中有2mol氮气是化合价升高得到,有1mol氮气是化合价降低得到,因此氧
答案第2页,共2页化产物与还原产物的质量之比为2:1,故D正确。
综上所述,答案为C。
8.C
【详解】A.置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,因
此该反应不是置换反应,故A错误;
B.反应中碳化合价升高,因此 失去电子,故B错误;
C.反应中氮化合价降低,因此 是氧化剂,故C正确;
D.碳化合价升高得到 ,因此 是氧化产物,故D错误。
综上所述,答案为C。
9.C
【详解】A.由题干反应方程式可知,SO 中硫元素化合价由+4价升高到+6价,化合价升
2
高被氧化,故SO 发生氧化反应,A错误;
2
B.由题干反应方程式可知,Br的化合价由0价降低到-1价,被还原,故Br 是氧化剂,B
2
错误;
C.由题干反应方程式可知,Br的化合价由0价降低到-1价,被还原,Br 得到电子,C正
2
确;
D.由题干反应方程式可知,HO中的氧元素的化合价未改变,故HO既不被氧化也不被
2 2
还原,D错误;
故答案为:C。
10.A
【详解】A.过程CuO Cu中Cu的化合价降低,被还原,A符合题意;
B.过程NaO NaOH中Na的化合价没有改变,故既不被氧化也不被还原,B不合题
2
意;
C.过程HCl Cl
2
中Cl的化合价升高,被氧化,C不合题意;
D.过程Fe FeSO
4
中Fe的化合价升高,被氧化,D不合题意;
故答案为:A。
11.D【分析】氧化还原反应中,元素化合价升高,被氧化,对应的物质做还原剂,对应的产物
为氧化产物;同理,元素化合价降低,被还原,对应的物质做氧化剂,对应的产物为还原
产物,据此结合氧化还原反应的规律分析解答。
【详解】A.根据氧化还原反应的特征和规律可知,①中FeCl 和I 均为氧化产物,
3 2
②Fe3+为氧化产物,③中的氧化产物为I,故A错误;
2
B.氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,在反应①中Cl>Fe3+和C1
2 2
>I,在反应②中,Br >Fe3+,在反应③中,Fe3+>I,氧化性顺序是Br >Fe3+>I,无法判
2 2 2 2 2
断:C1 >Br ,故B错误;
2 2
C.由反应②可知,还原性:Br-<Fe2+,C1 和FeBr 反应时,氯气先氧化亚铁离子,再氧
2 2
化溴离子,故C错误;
D.根据上述反应可知,还原性:Br-<Fe2+<I-,若某溶液含有Fe2+、I-、Br-几种离子,向其
中加入足量Br ,溶液中碘离子会被氧化为碘单质,亚铁离子会被氧化为铁离子,溴单质被
2
还原为溴离子,导致溴离子浓度增大,即溶液中各离子浓度均发生变化,D正确;
故选D。
12.D
【详解】A.黑火药中钾元素是长周期元素,故A错误;
B.根据方程式分析转移12mol电子,生成4mol气体,当转移3mol 时,生成1mol气体,
由于不清楚是否为标准状况下,因此无法计算气体的体积,故B错误;
C.根据黑火药的配比是1mol硫、2mol硝酸钾、3mol碳,则黑火药中C的质量分数
,故C错误;
D.根据方程式分析碳化合价升高,则参加反应的还原剂是碳共3mol,氮和硫化合价降低,
则参加反应的氧化剂是硫和硝酸钾共3mol,因此参加反应的还原剂与氧化剂的物质的量之
比为1∶1,故D正确。
综上所述,答案为D。
13.C
【详解】A.氢元素化合价升高,因此H 发生了氧化反应,故A正确;
2
B.用氧化铟(InO)负载的Ag催化剂,Ag催化剂参与反应,反应前后质量不变、化学性质
2 3
不变,故B正确;
答案第4页,共2页C.22.4 L H O物质的量不是1mol,因此质量不为18g,故C错误;
2
D.根据方程式3H+CO CHOH+HO,则每消耗3mol H 生成1mol CHOH,故
2 2 3 2 2 3
D正确;
综上所述,答案为C。
14.B
【详解】A.钠化合价升高发生氧化反应,需要氧化剂,故A不符合题意;
B.铬元素化合价降低,发生还原反应,需要还原剂,故B符合题意;
C.锌化合价升高发生氧化反应,需要氧化剂,故C不符合题意;
D.元素化合价没有改变,不需要氧化剂、还原剂,故D不符合题意;
故选B。
15.B
【详解】A.ClO溶于水后的溶液可以导电,但由于ClO溶于水生成了HClO,HClO电离
2 2
而导电,因此只能说ClO是非电解质,故A错误;
2
B.根据题中ClO+HO=2HClO ,可知ClO能与NaOH反应生成NaClO,与碱反应生成盐
2 2 2
和水的是酸性氧化物,故B正确;
C.ClO+HO=2HClO,反应中没有化合价变化,因此该反应不是氧化还原反应,故C错误;
2 2
D.通常情况下HClO不稳定,见光易分解,因此HClO不能长期保存,故D错误。
综上所述,答案为B。
16.(1)有机
(2)⑥
(3)SO +2OH-=SO +H O
2 2
(4) 不属于 2CaSO+O +4H O=2CaSO·2H O
3 2 2 4 2
(5) 2∶1 b
【详解】(1)由题干分类图示信息可知,“类别Ⅰ”中为C HOH即酒精、乙醇,其属于
2 5
有机化合物,故答案为:有机;
(2)酸式盐是指在水溶液中除了电离出金属阳离子或铵根离子和酸根离子之外,还电离出
H+的化合物,故“类别Ⅱ”中,属于酸式盐的是NaHCO ,故答案为:⑥;
3
(3)SO 通入足量NaOH溶液反应的方程式为:2NaOH+SO =Na SO +H O,故其离子方程
2 2 2 3 2式为:SO +2OH-=SO +H O,故答案为:SO +2OH-=SO +H O;
2 2 2 2
(4)已知脱疏反应之一SO +CaCO =CaSO +CO ,反应中没有元素的化合价发生改变,则
2 3 3 2
该反应不属于氧化还原反应,通入空气将CaSO 浆液转化为石膏CaSO·2H O的化学方程
3 4 2
式为:2CaSO+O +4H O=2CaSO·2H O,故答案为:2CaSO+O +4H O=2CaSO·2H O;
3 2 2 4 2 3 2 2 4 2
(5)已知化合价升高被氧化生成的产物为氧化产物,而化合价降低被还原生成的产物为还
原产物,则将SO 通入饱和HS溶液中发生SO +2H S=3S↓+2H O,氧化产物与还原产物的
2 2 2 2 2
物质的量之比为2:1,SO 和HS二者恰好完全反应时溶液中自由移动的离子浓度几乎为
2 2
0,根据溶液的电导率随通入SO 体积的变化曲线图可知,二者恰好完全反应的点是图中的
2
b,故答案为:2:1;b。
17.(1)
(2) 3∶8 3∶2
(3) 小于1nm
(4)5.6g
(5) 分解 催化剂
【详解】(1)化学反应3Cl+8NH=6NHCl+N 中,Cl元素化合价由0→-1价,N元素化合
2 3 4 2
价由-3价→0价,氧化还原反应氧化剂与还原剂得失电子数目相等,表现为化合价升降总
数相等,用双线桥标出电子转移的方向和数目可为 ;
(2)该反应3Cl+8NH=6NHCl+N ,发生化学反应的Cl 与NH 的分子数之比为3∶8,有
2 3 4 2 2 3
1/4的氨气作还原剂,所以发生电子转移的Cl 与NH 的分子数之比为=3:8×1/4=3:2,则
2 3
反应中发生电子转移的Cl 与NH 的分子数之比为3∶2,答案为:3∶8,3∶2;
2 3
(3)NH Cl是可溶性的强电解质,在水中的电离方程式为 ,溶液中的分
4
答案第6页,共2页散质粒子的直径应该小于1nm,答案为: ,1nm;
(4)6.8克氨的物质的量为6.8g/17g/mol=0.4mol,根据原子守恒可知0.4molNH 完全氧化
3
得到的N 的物质的量为0.2mol,质量为0.2mol×28g/mol=5.6g,答案为:5.6g;
2
(5)①根据质量守恒可知:X+26+3+30=50+1+3+12,解得:X=7,反应中M的质量减小,
Q、P的质量增加,则该反应为M分解生成Q和P的反应,属于分解反应,答案为:分解
反应;
②根据表中数据可知,Q在反应前后的质量不变,则Q在反应中作催化剂,答案为:催化
剂。
18.(1)Cl >Br >I
2 2 2
(2)Cl +2I-=I +2Cl-
2 2
(3) 得到 还原 73 氧化
(4) 是 2NaClO+4Na SO +H SO =ClO↑+5Na SO +H O
3 2 3 2 4 2 2 4 2
【详解】(1)氧化剂的氧化性大于氧化产物的氧化性,则根据反应
①Cl+2NaBr=2NaCl+Br 可知,氧化性:Cl>Br ;又根据反应②2KI+Br =2KBr+I 可知,
2 2 2 2 2 2
氧化性:Br >I,所以氧化性:Cl>Br >I;
2 2 2 2 2
(2)根据第(1)问可知,氧化性:Cl>Br >I,所以Cl 与KI能发生反应,反应的离子
2 2 2 2
方程式为:Cl+2I-=I +2Cl-;
2 2
(3)MnO +4HCl(浓) MnCl +Cl↑+2H O,MnO 中的Mn元素化合价从+4价降低到+2价,
2 2 2 2 2
得到电子被还原;87gMnO 的物质的量为 =1mol,根据关系式 (被
2
氧化)可知,所以当1molMnO 作氧化剂,发生还原反应时,有2molHCl被氧化,发生氧
2
化反应,其质量为 =73g,故答案为:得到;还原;73;氧化;
(4)根据题干信息可知,NaClO 转化为ClO,Cl元素化合价从+5价降低到+1价,化合价
3 2
降低 ,NaSO 转化为NaSO ,S元素化合价升高2,则该反应属于氧化还原反应,根
2 3 2 4
据氧化还原反应的配平原则可知,上述反应中ClO与NaSO 的化学计量数之比为1:4,根
2 2 3据元素守恒可知,该反应为:2NaClO+4Na SO +H SO =ClO↑+5Na SO +H O。
3 2 3 2 4 2 2 4 2
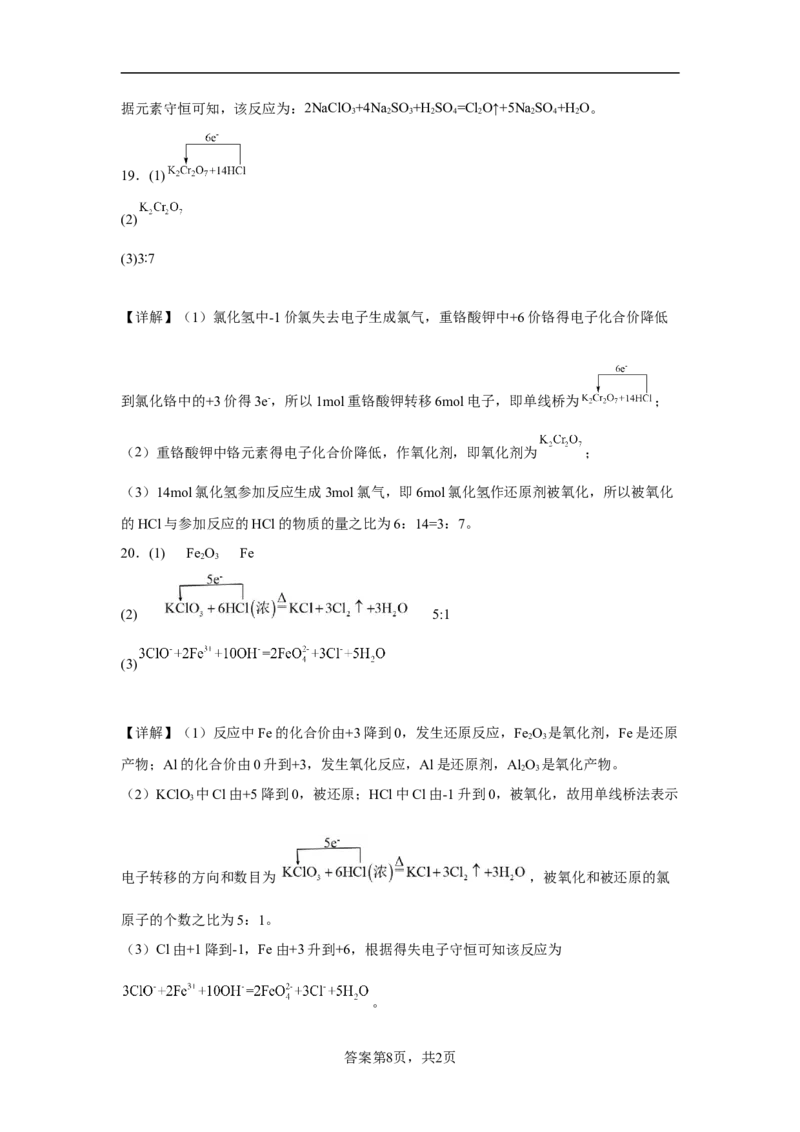
19.(1)
(2)
(3)3∶7
【详解】(1)氯化氢中-1价氯失去电子生成氯气,重铬酸钾中+6价铬得电子化合价降低
到氯化铬中的+3价得3e-,所以1mol重铬酸钾转移6mol电子,即单线桥为 ;
(2)重铬酸钾中铬元素得电子化合价降低,作氧化剂,即氧化剂为 ;
(3)14mol氯化氢参加反应生成3mol氯气,即6mol氯化氢作还原剂被氧化,所以被氧化
的HCl与参加反应的HCl的物质的量之比为6:14=3:7。
20.(1) Fe O Fe
2 3
(2) 5:1
(3)
【详解】(1)反应中Fe的化合价由+3降到0,发生还原反应,Fe O 是氧化剂,Fe是还原
2 3
产物;Al的化合价由0升到+3,发生氧化反应,Al是还原剂,Al O 是氧化产物。
2 3
(2)KClO 中Cl由+5降到0,被还原;HCl中Cl由-1升到0,被氧化,故用单线桥法表示
3
电子转移的方向和数目为 ,被氧化和被还原的氯
原子的个数之比为5:1。
(3)Cl由+1降到-1,Fe由+3升到+6,根据得失电子守恒可知该反应为
。
答案第8页,共2页