文档内容
号考
名姓
级班
校学
线
订
装
封
密
题
答
要
不
内
线
封
密
河北区 2023-2024 学年度高三年级总复习质量检测(一) 4.如图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子总数等于B的
化 学
质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是
注注意意事事项项::1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,
A C
用橡皮擦干净后,再选涂其它答案标号。
B
2.I卷共12题,每题3分,共36分。在每题列出的四个选项中,只有一项是最符
合题目要求的。以下数据可供解题时参考:
A.B为第二周期元素
可能用到的相对原子质量:H1 C12 N14 O16 Na23 Al27 S32 Cl35.5
B.第一电离能:C>A
Cu64
C.A、C元素简单氢化物的稳定性:A>C
第 I 卷 共 36 分
D.C元素的最高价氧化物对应的水化物酸性很强
一一、、单单选选题题
1.2024年2月第十四届全国冬季运动会在内蒙古召开,见证了中国冰雪运动的“热辣滚烫”。 5.下列有关叙述正确的是
下列说法不 . 正 . 确 . 的是 A.235 U和238 U是同一种核素
92 92
A.场馆的照明、运行均由光伏发电和风力发电提供,有利于实现碳达峰
B.O 和O 互为同素异形体
B.速滑竞赛服采用的聚氨酯材料是一种有机高分子材料 2 3
C.冬运会场馆建设大量使用到了太阳能,太阳能电池板的主要材料是二氧化硅
C.由于氢键的作用,H O的稳定性强于H S
2 2
D.冬运会采用了先进的二氧化碳制冰技术,比传统制冷剂氟利昂更加环保
2. 化学与生产、生活密切相关,下列说法不 . 正 . 确 . 的是 D.硫原子核外电子轨道表示式为:
A.氧化亚铁常用作油漆的红色颜料
B.苯甲酸及其钠盐常用作食品防腐剂 6.我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、
C.油脂除食用外还可用于生产肥皂 PbO 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜
2
D.家庭用洁厕灵与“84消毒液”不能同时使用
料,下列物质性质与用途具有对应关系的是
3.SiO +4HF=SiF ↑+2H O在半导体生产工业中有着重要的应用,用化学用语表示反应
2 4 2
A.石墨能导电,可用作润滑剂
中的相关粒子,其中正确的是
B.单晶硅熔点高,可用作半导体材料
A.F-的结构示意图: B.水分子的比例模型:
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
C.SiF
4
的电子式: D.中子数为15的Si原子:2
1
9
4
Si D.含铅化合物颜色丰富,可用作电极材料
高三化学 第1页 (共8页) 高三化学 第2页 (共8页)
{#{QQABKQ4UogiAQpAAARgCAQXwCgGQkBCACAoGxAAMoAAACQFABAA=}#}密
封
线
内
不
要
答
题
密
封
装
订
线
7.宇航员王亚平曾在天宫课堂直播泡腾片水球实验。泡腾片中含有柠檬酸(结构简式如图)
10.碳酸氢铵在食品工业中常用于制作蓬松的面点和糕点。室温下,通过下列实验来探
下列有关柠檬酸的说法不正确的是
...
究NH HCO 的性质:
4 3
A.柠檬酸的分子式为C H O
6 8 7
实验1:测得0.1mol·L-1NH HCO 溶液的pH=9.68
4 3
B.柠檬酸有两种不同的官能团
实验2:向浓度为0.1mol·L-1NH HCO 溶液中加入足量NaOH,有刺激性气味气体产生
4 3
C.柠檬酸分子中有手性碳原子
实验3:浓度均为2.0mol·L-1NH HCO 溶液和NaCl溶液等体积混合,有晶体析出,过
4 3
D.1mol该有机物最多与3molNaOH反应
滤
8.氮化硅(Si N )因其在高温和高频条件下的优异性能,成为现代微电子领域的重要材料。
3 4 下列说法正确的是
工业上用石英砂和原料气(含N 和少量O )制备Si N 的操作流程如下(已知:粗硅中含 2 2 3 4
A.实验1可以用pH试纸进行测定
少量Fe、Cu的单质及化合物;常温下Si N 除与氢氟酸反应外不与其他酸反应),下列
3 4
叙述不正确的是 B. 由实验1可得:c(HCO 3 -)>c(NH 4 +)>c(OH-)>c(H+)
...
C. 实验2中发生反应的离子方程式:NH + + OH-=NH ↑ + H O
4 3 2
D. 实验3中析出的晶体为NaHCO
3
11.MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中不
.
正确的是
..
A.“还原”时焦炭主要被氧化为CO
2 A.MOH是一种弱碱
高温
B.“高温氮化”反应的化学方程式为:3Si+2N 2===== Si 3 N 4 B.在x点,c(M+)=c(R+)
C.“操作X”可将原料气通过灼热的铜粉 C.在x点,ROH完全电离
D.“稀酸Y”可选用稀硝酸
D.稀释前,c(ROH)>10c(MOH)
12.科学家称他们正在研制的铝电池未来有望取代锂电池。银铝电池具有能量密度高的
9.下列实验方案中,能达到实验目的的是
优点,电池装置如图;电池放电时的反应为:
选项 实验目的 实验方案
除去C H 气体中的少量H S
2Al+3AgO(氧化高银)+2NaOH+3H
2
O=2Na[Al(OH)
4
]+3Ag下列说法正确的是
2 2 2
A 将混合气体通入足量CuSO 溶液中,并干燥
气体 4 A.Al电极发生还原反应
在Na S O 溶液中滴加盐酸酸化的BaCl 溶液观 B.阳离子交换膜允许阳离子和电子通过
2 2 3 2
B 验证Na S O 是否氧化变质
2 2 3
察是否产生白色沉淀
C.当导线中通过3mol电子时,负极区溶液质量减小42g
向较浓的FeCl 溶液中滴入少量酸性KMnO 溶
C 证明Fe2+有还原性 2 4 D.正极电极反应式为AgO+2e-+2H+=Ag+H 2 O
液,观察KMnO 溶液紫色是否褪去
4
向NaCl与NaBr混合溶液中滴加AgNO 溶液,
3
D 比较:Ksp(AgBr) <Ksp(AgCl)
观察是否出现淡黄色沉淀
高三化学 第3页 (共8页) 高三化学 第4页 (共8页)
{#{QQABKQ4UogiAQpAAARgCAQXwCgGQkBCACAoGxAAMoAAACQFABAA=}#}号考
名姓
级班
校学
线
订
装
封
密
题
答
要
不
内
线
封
密
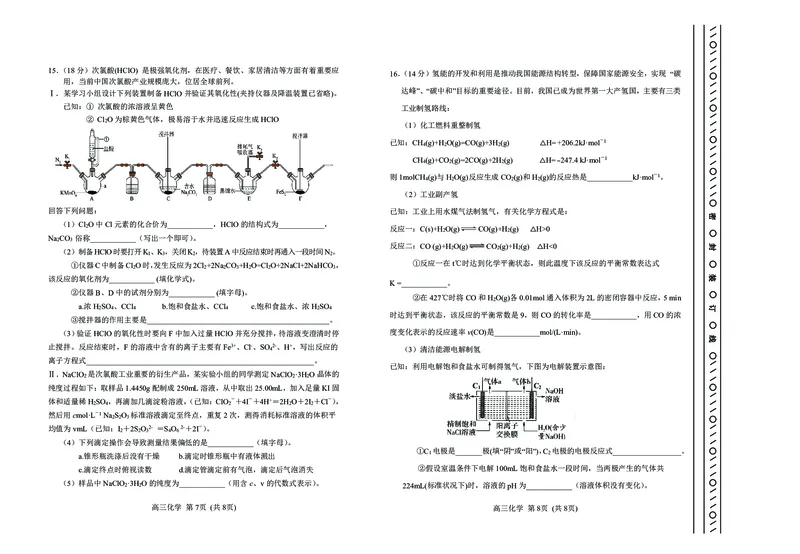
第 II 卷 共 64 分 14.(18分)血栓栓塞类疾病漏诊、误诊、致残率高,是危害患者健康的重要疾病之一。
华法林(物质F)可用于预防血栓栓塞类疾病,某种合成华法林的路线如图所示,请回
注注意意事事项项::
答相关问题:
1.用黑色字迹的签字笔或钢笔将答案写在“答答题题卡卡”上。
2.II卷共4题,共64分。
二二、、填填空空题题
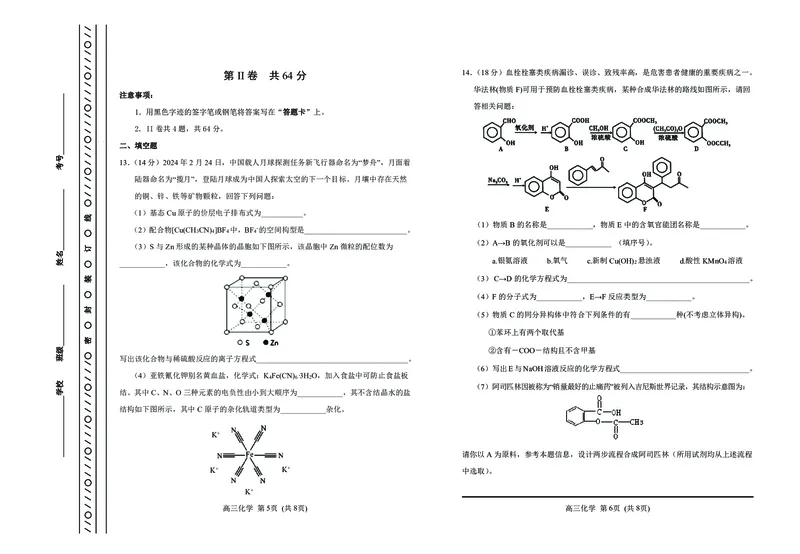
13.(14分)2024年2月24日,中国载人月球探测任务新飞行器命名为“梦舟”,月面着
陆器命名为“揽月”,登陆月球成为中国人探索太空的下一个目标。月壤中存在天然
的铜、锌、铁等矿物颗粒,回答下列问题:
(1)基态Cu原子的价层电子排布式为___________。
(1)物质B的名称是____________,物质E中的含氧官能团名称是____________。
(2)配合物[Cu(CH CN) ]BF 中,BF -的空间构型是___________________________。
3 4 4 4
(2)A→B的氧化剂可以是____________ (填序号)。
(3)S与Zn形成的某种晶体的晶胞如下图所示,该晶胞中Zn微粒的配位数为
____________,该化合物的化学式为____________。
a.银氨溶液 b.氧气 c.新制Cu(OH)
2
悬浊液 d.酸性KMnO
4
溶液
(3)C→D的化学方程式为________________________________________________。
(4)F的分子式为____________,E→F反应类型为____________。
(5)物质C的同分异构体中符合下列条件的有____________种(不考虑立体异构)。
①苯环上有两个取代基
②含有-COO-结构且不含甲基
写出该化合物与稀硫酸反应的离子方程式________________________________________。
(6)写出E与NaOH溶液反应的化学方程式__________________________________。
(4)亚铁氰化钾别名黄血盐,化学式:K Fe(CN) .3H O,加入食盐中可防止食盐板
4 6 2
(7)阿司匹林因被称为“销量最好的止痛药”被列入吉尼斯世界记录,其结构示意图为:
结。其中C、N、O三种元素的电负性由小到大顺序为____________,其不含结晶水的盐
结构如下图所示,其中C原子的杂化轨道类型为____________杂化。
K+
请你以A为原料,参考本题信息,设计两步流程合成阿司匹林(所用试剂均从上述流程
K+ K+ 中选取)。
K+
高三化学 第5页 (共8页) 高三化学 第6页 (共8页)
{#{QQABKQ4UogiAQpAAARgCAQXwCgGQkBCACAoGxAAMoAAACQFABAA=}#}密
封
线
内
不
要
答
题
密
封
装
订
线
15.(18分)次氯酸(HClO) 是极强氧化剂,在医疗、餐饮、家居清洁等方面有着重要应
16.(14分)氢能的开发和利用是推动我国能源结构转型,保障国家能源安全,实现 “碳
用,当前中国次氯酸产业规模庞大,位居全球前列。
Ⅰ.某学习小组设计下列装置制备HClO并验证其氧化性(夹持仪器及降温装置已省略)。
达峰”、“碳中和”目标的重要途径。目前,我国已成为世界第一大产氢国,主要有三类
已知:① 次氯酸的浓溶液呈黄色 工业制氢路线:
② Cl O为棕黄色气体,极易溶于水并迅速反应生成HClO
2
(1)化工燃料重整制氢
已知:CH (g)+H O(g)=CO(g)+3H (g) H=+206.2kJ·mol-1
4 2 2
CH (g)+CO (g)=2CO(g)+2H (g) △H=-247.4kJ·mol-1
4 2 2
则1molCH (g)与H O(g)反应生成CO (g)和H△(g)的反应热是____________kJ·mol-1。
4 2 2 2
(2)工业副产氢
回答下列问题: 已知:工业上用水煤气法制氢气,有关化学方程式是:
(1)Cl O中Cl元素的化合价为____________,HClO的结构式为____________,
2 反应一:C(s)+H O(g) CO(g)+H (g) H>0
2 2
Na CO 俗称____________(写出一个即可)。
2 3
反应二:CO(g)+H O(g) CO (g)+H (g)△ H<0
(2)制备HClO时要打开K、K,关闭K,待装置A中反应结束时再通入一段时间N。 2 2 2
1 3 2 2
①仪器C中制备Cl O时,发生反应为2Cl +2Na CO +H O=Cl O+2NaCl+2NaHCO ,
①反应一在t℃时达到化学平衡状态,△则此温度下该反应的平衡常数表达式
2 2 2 3 2 2 3
该反应的氧化剂为____________(填化学式)。
K=____________。
②仪器B、D中的试剂分别为____________(填字母)。
②在427℃时将CO和H O(g)各0.01mol通入体积为2L的密闭容器中反应,5min
2
a.浓H SO 、CCl b.饱和食盐水、CCl c.饱和食盐水、浓H SO 2 4 4 4 2 4
时达到平衡状态,该反应的平衡常数是9,则CO的转化率是____________,用CO的浓
③搅拌器的作用主要是________________________________________________。
(3)验证HClO的氧化性时要向F中加入过量HClO并充分搅拌,待溶液变澄清时停 度变化表示的反应速率v(CO)是____________mol/(L·min)。
止搅拌。反应结束时,F的溶液中含有的离子主要有Fe3+、Cl-、SO
4
2-、H+,写出反应的
(3)清洁能源电解制氢
离子方程式____________________________________________________________。
已知:利用电解饱和食盐水可制得氢气,下图为电解装置示意图:
Ⅱ.NaClO 是次氯酸工业重要的衍生产品,某实验小组的同学测定NaClO ·3H O晶体的
2 2 2
纯度过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固 C 1 C 2
体和适量稀H SO ,再滴加几滴淀粉溶液,(已知:ClO -+4I-+4H+=2H O+2I +Cl-),
2 4 2 2 2
然后用cmol·L-1Na S O 标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平
2 2 3
均值为vmL(已知:I +2S O 2- =S O 2-+2I-)。
2 2 3 4 6
(4)下列滴定操作会导致测量结果偏低的是____________(填字母)。
①C 电极是_______极(填“阴”或“阳”),C 电极的电极反应式__________________。
a.锥形瓶洗涤后没有干燥 b.滴定时锥形瓶中有液体溅出 1 2
c.滴定终点时俯视读数 d.滴定管滴定前有气泡,滴定后气泡消失 ②假设室温条件下电解100mL饱和食盐水一段时间,当两极产生的气体共
(5)样品中NaClO 2 ·3H 2 O的纯度为____________(用含c、v的代数式表示)。 224mL(标准状况下)时,溶液的pH为____________(溶液体积没有变化)。
高三化学 第7页 (共8页) 高三化学 第8页 (共8页)
{#{QQABKQ4UogiAQpAAARgCAQXwCgGQkBCACAoGxAAMoAAACQFABAA=}#}