文档内容
必修第一册 第一章 第二节 离子反应 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1.下列说法中正确的是( )
A.所有的反应都属于离子反应
B.在离子反应中,所有离子的浓度都是减小的
C.离子反应必须在溶液中进行,非溶液中不能发生离子反应
D.在离子反应方程式中,等号左右的原子种类和数目以及电荷数必须相等
2.下表中物质的分类组合完全正确的是( )
选项 A B C D
强电解质 KNO HSO BaSO HClO
3 2 4 4 4
弱电解质 HF CaCO HClO CHCOONH
3 3 4
非电解质 SO 金属Al HO C HOH
2 2 2 5
3.下列物质中,导电性最差的是( )
A.熔融氢氧化钠 B.石墨棒 C.盐酸 D.固态氯化钠
4.离子方程式BaCO +2H+===CO ↑+HO+Ba2+中的H+不能代表的物质是( )
3 2 2
①HCl ②HSO ③HNO ④NaHSO ⑤CHCOOH
2 4 3 4 3
A.①③ B.①④⑤ C.②④⑤ D.①⑤
5.能正确表示下列化学反应的离子方程式的是( )
A.小苏打溶液中加入少量NaOH溶液:H++OH-===HO
2
B.铁跟稀硫酸反应:2Fe+6H+===2Fe3++3H↑
2
C.硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH-===Cu(OH) ↓
2
D.氧化铁与稀硫酸反应:Fe O+6H+===2Fe3++3HO
2 3 2
6.下列反应可用离子方程式“H++OH-===H O”表示的是( )
2
A.NaHSO 溶液与Ba(OH) 溶液混合
4 2
B.NH Cl溶液与Ca(OH) 溶液混合
4 2
C.HNO 溶液与KOH溶液混合
3
D.NaHPO 溶液与NaOH溶液混合
2 4
7.在无色透明强酸性溶液中,能大量共存的离子组是( )
A.K+、Cu2+、NO -、SO 2- B.K+、Ca2+、Cl-、CO2-
3 4 3
C.Zn2+、NH +、NO -、Cl- D.K+、Na+、MnO -、SO 2-
4 3 4 4
8.如表是某矿物质饮用水的部分标签说明
1
学科网(北京)股份有限公司主要成分
钾离子(K+) 20~27.3 mg·L-1
氯离子(Cl-) 30~34.2 mg·L-1
镁离子(Mg2+) 20.2~24.9 mg·L-1
硫酸根离子(SO 2-) 24~27.5 mg·L-1
4
则该饮用水中还可能较大量存在( )
A.OH- B.Ag+ C.Na+ D.Ca2+
9.甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录结果如下:
甲:KSO 、BaCl 、NaCl 乙:NaCl、Ba(OH) 、KCO
2 4 2 2 2 3
丙:HCl、KCO、NaCl 丁:KSO 、NaCO、KCl
2 3 2 4 2 3
其中记录结果合理的是( )
A.甲 B.乙 C.丙 D.丁
10.某地甲、乙两厂排放的污水中各含有下列8种离子中的4种(两厂废水所含离子不同):Ag+、
Ba2+、Fe2+、Na+、Cl-、SO 2-、NO -、OH-。若两厂单独排放污水都会造成严重的水污染,如将
4 3
两厂的污水按一定比例混合,沉淀后污水便能变得无色澄清,溶质主要含硝酸钠,污染程度大
大降低。根据所给信息有以下几种说法,你认为正确的是 ( )
A.Na+和NO -来自同一工厂 B.Cl-和NO -一定来自同一工厂
3 3
C.Ag+和Na+可能来自同一工厂 D.SO 2-和OH-一定来自同一工厂
4
二、填空题(本题包括5个小题,共60分)
11.(18分)在以下10种物质中 ①SO ②Ag ③CHCOOH ④NaOH固体 ⑤氯化氢
3 3
⑥KSO 固体 ⑦蔗糖 ⑧BaSO 固体 ⑨CuSO 溶液 ⑩NH 。
2 4 4 4 3
(1)溶于水能导电,但本身属于非电解质的是(填序号,下同) ;
(2)难溶于水,熔化状态能导电的强电解质是 ;
(3)固体和液体都不导电,只能在水溶液中导电的强电解质是 ;弱电解质是 。
(4)易溶于水,但不能导电的非电解质是 ;
(5)本身可以导电,但既不是电解质又不是非电解质的是 ;
(6)在水溶液里和熔化状态都能导电的电解质是 ;
(7)在溶液中以离子形式存在的是 ;
(8)NaOH溶液导电性一定比CHCOOH溶液强吗? 。
3
12.(10分)写出与下列离子方程式相对应的化学方程式
①Cu2++2OH-==Cu(OH) ↓
2
②H++OH-==H O
2
2
学科网(北京)股份有限公司⑤2H++CaCO ==Ca2++H O+CO↑
3 2 2
④2H++CO 2-== H O+CO↑
3 2 2
⑤Cu2++Fe==Fe2++Cu
13.(8分)向Ba(OH) 溶液中逐滴加入稀硫酸,请完成下列问题:
2
(1)写出反应的离子方程式_______________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是____________________。
A.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至溶液显中性
4 2
B.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至SO恰好完全沉淀
4 2
C.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至过量
4 2
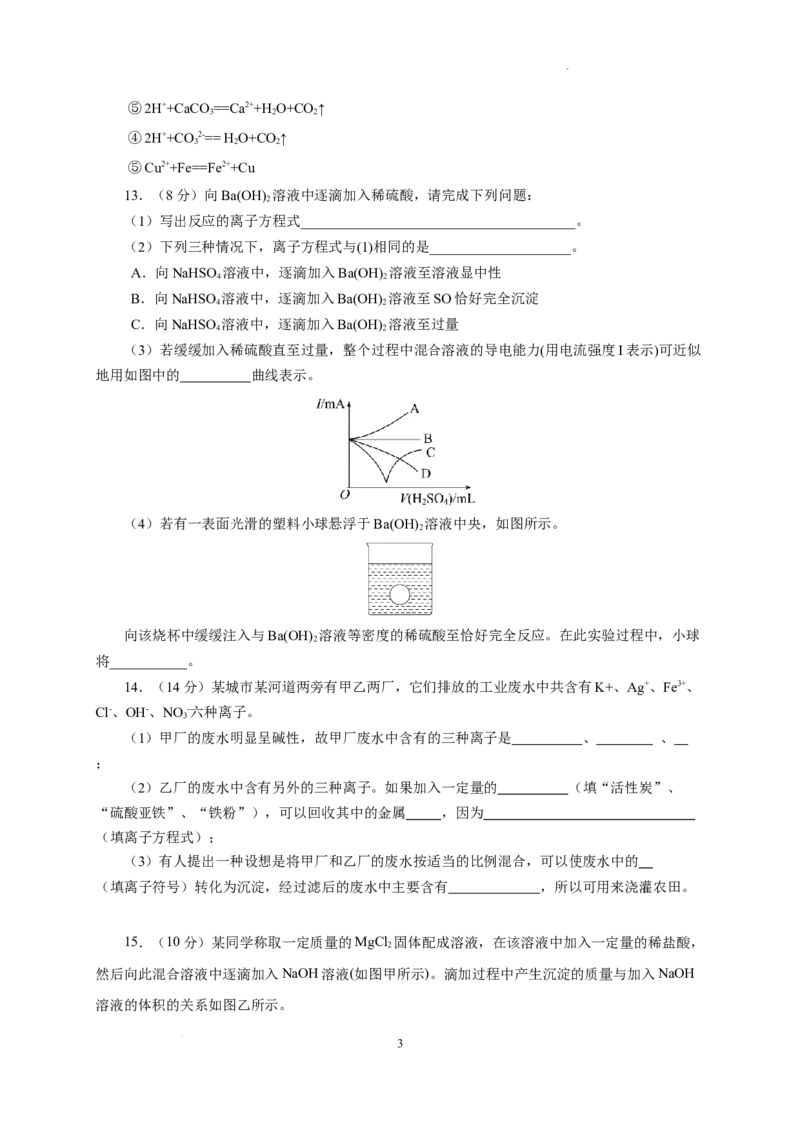
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似
地用如图中的 曲线表示。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH) 溶液中央,如图所示。
2
向该烧杯中缓缓注入与Ba(OH) 溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球
2
将___________。
14.(14分)某城市某河道两旁有甲乙两厂,它们排放的工业废水中共含有K+、Ag+、Fe3+、
Cl-、OH-、NO -六种离子。
3
(1)甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子是 、 、
;
(2)乙厂的废水中含有另外的三种离子。如果加入一定量的 (填“活性炭”、
“硫酸亚铁”、“铁粉”),可以回收其中的金属 ,因为
(填离子方程式);
(3)有人提出一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的
(填离子符号)转化为沉淀,经过滤后的废水中主要含有 ,所以可用来浇灌农田。
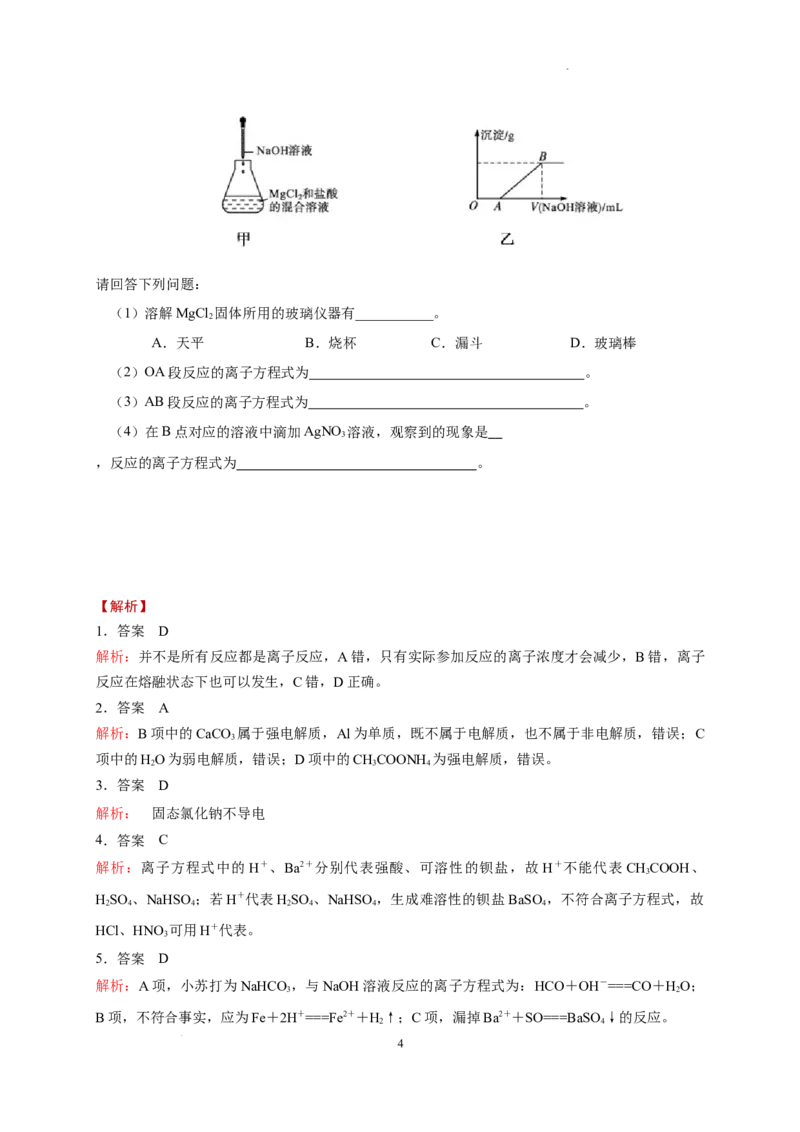
15.(10分)某同学称取一定质量的MgCl 固体配成溶液,在该溶液中加入一定量的稀盐酸,
2
然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH
溶液的体积的关系如图乙所示。
3
学科网(北京)股份有限公司请回答下列问题:
(1)溶解MgCl 固体所用的玻璃仪器有___________。
2
A.天平 B.烧杯 C.漏斗 D.玻璃棒
(2)OA段反应的离子方程式为 。
(3)AB段反应的离子方程式为 。
(4)在B点对应的溶液中滴加AgNO 溶液,观察到的现象是
3
,反应的离子方程式为 。
【解析】
1.答案 D
解析:并不是所有反应都是离子反应,A错,只有实际参加反应的离子浓度才会减少,B错,离子
反应在熔融状态下也可以发生,C错,D正确。
2.答案 A
解析:B项中的CaCO 属于强电解质,Al为单质,既不属于电解质,也不属于非电解质,错误;C
3
项中的HO为弱电解质,错误;D项中的CHCOONH 为强电解质,错误。
2 3 4
3.答案 D
解析: 固态氯化钠不导电
4.答案 C
解析:离子方程式中的H+、Ba2+分别代表强酸、可溶性的钡盐,故 H+不能代表CHCOOH、
3
HSO 、NaHSO ;若H+代表HSO 、NaHSO ,生成难溶性的钡盐BaSO ,不符合离子方程式,故
2 4 4 2 4 4 4
HCl、HNO 可用H+代表。
3
5.答案 D
解析:A项,小苏打为NaHCO ,与NaOH溶液反应的离子方程式为:HCO+OH-===CO+HO;
3 2
B项,不符合事实,应为Fe+2H+===Fe2++H↑;C项,漏掉Ba2++SO===BaSO ↓的反应。
2 4
4
学科网(北京)股份有限公司6.答案 C
解析: A项,NaHSO 溶液与Ba(OH) 溶液混合时,除了H+与OH-反应外,还有SO与Ba2+反应
4 2
生成BaSO 沉淀;B项,NH Cl溶液与 Ca(OH) 溶液混合产生NH ·H O;C项,HNO 溶液与KOH
4 4 2 3 2 3
溶液混合,为可溶性强酸与强碱反应生成可溶性盐和水的类型,符合该离子方程式;D项,
NaHPO 不能拆写成H+。
2 4
7.答案 C
解析: Cu2+、MnO - 有颜色,B中Ca2+、CO2- 不能共存
4 3
8.答案 C
解析:该饮用水中存在Cl-,故Ag+不能大量共存,Mg2+与OH-不能大量共存,SO与Ca2+生成微
溶物不能大量共存。
9.答案 D
解析: 甲会形成BaSO 沉淀而不能共存;乙会形成BaCO 沉淀而不能共存;丙会产生CO 气体而
4 3 2
不能共存。
10.答案 D
解析: Ag+所在的厂污水不应该有Cl-、SO 2-、OH- ,又根据溶液的电中性原则,剩下的NO - 一
4 3
定在该厂,而另个厂污水中有Cl-、SO 2-、OH-,则Ba2+、Fe2+不能存在,而Na+一定存在,这样分
4
成两组的情况是:Cl-、SO 2-、OH-、Na+在一起,NO - 、Ag+ 、Ba2+、Fe2+在一起。
4 3
11.解析:(1)①⑩ (2)⑧ (3)⑤、③ (4)⑦
(5)②⑨ (6)④⑥ (7)④⑤⑥ (8)不一定
12.解析: ①CuSO +2NaOH==Cu(OH) ↓+NaSO
4 2 2 4
②HCl+NaOH==HO+NaCl
2
⑤2HCl+CaCO ==CaCl+H O+CO↑
3 2 2 2
④2HCl +NaCO== NaCl+H O+CO↑
2 3 2 2
⑤CuSO +Fe==FeSO +Cu
4 4
13.解析:(1)Ba2++2OH-+2H++SO= BaSO↓+2H O
4 2
(2)A (3)C (4)下沉
14.解析:(1)K+ Cl- OH-
(2)铁粉 Ag 2 Ag+ + Fe = 2 Ag + Fe2+
(3)Ag+、Cl-、Fe3+、OH- K+、NO -
3
15.解析:(1)BD (2)OH-+H+=H O
2
(3)Mg2++2OH-=Mg(OH) ↓
2
(4)有白色沉淀生成 Ag+ + Cl- = AgCl↓
5
学科网(北京)股份有限公司6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司