文档内容
黄山市 2024 届高中毕业班第二次质量检测
化学试题
(考试时间:75分钟 满分:100分)
注意事项:
1.答卷前,务必将自己的姓名和座位号填写在答题卡和试卷上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,务必擦净后再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16 Fe56 Cu64 Ga70 Br80
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.下列古诗文中蕴含着一定的化学知识或原理,下列有关说法错误的是
A.“榆荚只能随柳絮,等闲撩乱走空园”中柳絮的主要成分和棉花相同
B.《物理小识·金石类》:“有硇水(硝酸)者,剪银塊投之,则旋而为水”,该过程涉及化还原反应
C.“雨过天青云破处,这般颜色做将来”中所描述瓷器的青色不是来自氧化铁
D.“纷纷灿烂如星陨,赫赫喧豗似火攻”中烟花是某些金属的焰色试验,属于化学变化
2.化学与人类生活密切相关,下列说法错误的是
A.二氧化硫可作漂白剂、防腐剂,还是一种食品添加剂
B.葡萄糖制备“碳量子点”是一种绿色、低成本的方法
C.研发催化剂将二氧化碳转化为甲醇,有助于我国2060年前实现碳中和的目标
D.三星堆青铜大立人以合金为材料,其深埋于地下生锈是发生了析氢腐蚀
3.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.电解精炼铜时,阳极质量减少64g,电路中转移电子数可能是2N
A
B.1molCaC 晶体和1molCaH 晶体含有的离子数目均为2N
2 2 A
C.1molHOOCCH COOH与足量乙醇在一定条件下反应,生成的酯基的数目为2N
2 A
D.F−解能力弱于NH+ ,1L1mol⋅L−1的NH F溶液中HF和NH ❑ + 的总数大于N
4 4 4 A
4.下列化学用语正确的是
❑ Ti
A.基态 22 原子的轨道表示式:
H σ
2
B.用电子云轮廓图表示 中的 键形成的示意图:
SO VSEPR
3
C. 的 模型:
2− −1−
D. 甲基 丁醇的键线式:
阅读下列材料,完成5-6小题。
CO 的综合利用具有重要意义。CO 的捕集方法众多,可以形成NaHCO 、(NH ) CO 、尿素
2 2 3 4 2 3
[CO(NH ) ]等重要化合物,CO 还可以催化转化为高附加值化学品
2 2 2
CO、CH 、C H OH、HCOOH等。用活化铜催化剂电解CO 可以制备乙醇。
4 2 5 2
5.下列说法正确的是A.(NH ) CO 是共价化合物 B.CO(NH ) 与NH CNO属于同素异形体
4 2 3 2 2 4
C.Cu位于元素周期表的d区 D.键角大小:CH T
B.Q、X、Y组成的化合物的水溶液一定显酸性
C.RZ 为非极性分子
3
D.该离子液体中含非极性键,不含配位键
9.下列实验操作、现象和结论均正确的是
选项 操作 现象 结论
A 向某钠盐粉末上滴加浓盐酸,将产生的气体 溶液褪色 气体一定是SO
2
通入品红溶液
B 向Na SiO 溶液中滴加盐酸 产生浑浊 Cl的非金属性比Si强
2 3
C 将SO 、SO 混合气体通入BaCl 溶液中 生成白色沉淀 沉淀是BaSO 、BaSO
3 2 2 3 4
D 向硫酸铜溶液中依次加入足量氨水和适量乙最终析出深蓝色晶体乙醇降低硫酸四氨合铜晶体的溶
醇 解度
H+/Δ
γ− γ− +H O
HOCH CH CH COOH ⇌ 2
10.由 羟基丁酸生成 丁内酯的反应如下: 2 2 2 ,在
298K下,γ−羟基丁酸水溶液的初始浓度为0.180mol⋅L−1,随着反应的进行,测得γ−丁内酯的浓度随
时间变化的数据如下表所示。下列说法错误的是t/min 21 50 80 100 120 160 220 ∞
c/(mol⋅L−1) 0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
A.其他条件相同时,升高温度,化学反应速率加快
B.在80∼100min内,以γ−丁内酯的浓度变化表示的反应速率为5.0×10−4mol⋅L−1 ⋅min❑ −1
C.120min时γ−羟基丁酸的转化率为60%
D.298K时该反应的平衡常数K=2.75
11.利用pH传感器探究NaOH溶液与硫酸、硫酸铜混合溶液发生反应时离子反应的先后顺序,绘得三份
曲线图如图所示。已知实验使用的NaOH溶液浓度和滴速相同;硫酸溶液和硫酸铜溶液浓度相同;混合溶
液中两溶质的浓度也相同。
下列说法错误的是
A.混合溶液中滴加NaOH溶液,硫酸先于硫酸铜发生反应
B.b图CuSO
4
溶液pH接近5的原因是:Cu2++2H
2
O⇌Cu(OH)
2
+2H+
C.w点:c(Na+)>c(SO2−)>c(Cu2+)
4
D.pq段铜离子浓度保持不变
3−
12.一种用 氯丙烯( )电解合成环氧氯丙烷( )的装置如图所示。该装置无需使用隔
膜,且绿色高效,图中X为Cl或Br,工作时X−和OH−同时且等量放电。下列说法错误的是
(说明:X−−e−=X⋅)
A.电解一段时间后,装置中OH−物质的量增大
B.每转移2mole−,生成1mol环氧氯丙烷
C.若X为Br,也可电解制得环氧氯丙烷
D.该装置工作时不需要补充X−
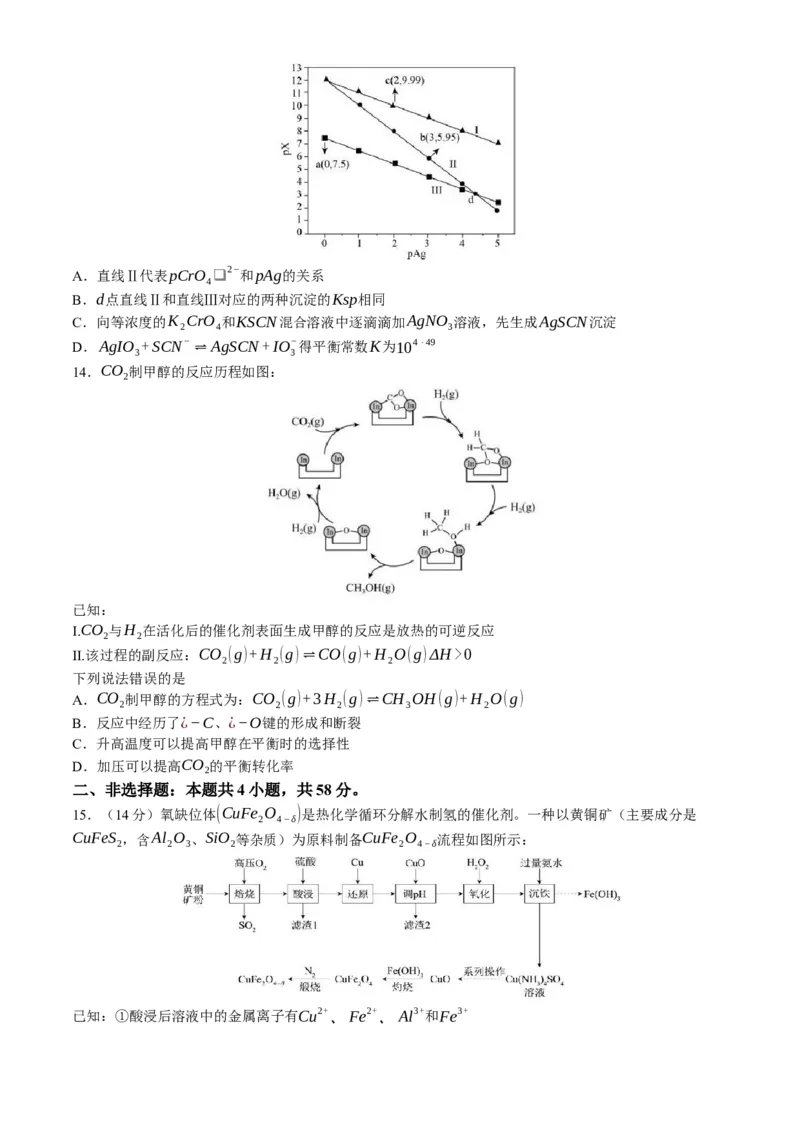
13.室温下向含KSCN、KIO 和K CrO 的溶液中滴加AgNO 溶液,混合液中
3 2 4 3
pX{[pX=−lgc(X)],X=IO−、SCN−、CrO2− }和pAg[pAg=−lgc(Ag+)]的关系如图所示。已知:
3 4
Ksp(AgSCN)0
2 2 2
下列说法错误的是
A.CO 制甲醇的方程式为:CO (g)+3H (g)⇌CH OH(g)+H O(g)
2 2 2 3 2
B.反应中经历了¿−C、¿−O键的形成和断裂
C.升高温度可以提高甲醇在平衡时的选择性
D.加压可以提高CO 的平衡转化率
2
二、非选择题:本题共4小题,共58分。
15.(14分)氧缺位体(CuFe O )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是
2 4−δ
CuFeS ,含Al O 、SiO 等杂质)为原料制备CuFe O 流程如图所示:
2 2 3 2 2 4−δ
已知:①酸浸后溶液中的金属离子有Cu2+ 、Fe2+ 、Al3+和Fe3+②25∘C时已知几种金属离子沉淀的pH如表所示:
金属氢氧化物 Fe(OH) Al(OH) Cu(OH) Fe(OH)
3 3 2 2
开始沉淀的pH 1.9 3.4 6.4 7.0
完全沉淀的pH 3.2 4.7 7.6 9.0
请回答下列问题:
(1)CuFeS “焙烧”时生成三种氧化物,其中金属氧化物的化学式为 。
2
(2)焙烧产物中的SO 在有氧条件下利用石灰石浆液吸收可制得一种副产品 。(填化学式)
2
(3)流程中,若无“还原”工序,造成的后果是 。
(4)已知Cu(NH ) Cl 有两种同分异构体,则“沉铁”过程中生成的[Cu(NH ) ] 2+ 的空间结构是
3 2 2 3 4
。
(5)“灼烧”工序的化学方程式是 ,“煅烧”时通入N 的作用是 。
2
(6)“煅烧”CuFe O 得到氧缺位体(CuFe O )时,不同温度范围内,发生变价的金属元素不同,某
2 4 2 4−δ
温度下制得的氧缺位体质量为原质量的99%,则δ= 。
(7)氧缺位体催化分解水制氢可分为两步:
第一步: (完成方程式);
第二步:2CuFe O =2CuFe O +δO ↑。
2 4 2 4−δ 2
16.(14分)2−溴戊二酸二甲酯(相对分子质量为239)是某抗癌药物的重要中间体,其制备的反应原理
如图所示:
制备装置如图所示(夹持装置已略去):
实验步骤如下:
步骤一:制备
将10.0g戊二酸(相对分子质量为132)加入到三颈烧瓶中,再向其中加入三氯甲烷25mL,搅拌均
匀,保持78∘C条件下,依次缓慢滴加12mL氯化亚砜、3滴催化剂、液溴,随后回流。回流完毕后,将三
颈烧瓶置于冰盐浴中,将溶液温度降到−10∘C后,缓慢滴加25mL甲醇(沸点64.7∘C),保持滴加过程
中温度不超过0∘C。
步骤二:除杂
向三颈烧瓶中加入25mL饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用25mL饱
和氯化钠溶液洗涤3次。洗涤完毕,用无水硫酸镁干燥,过滤。
步骤三:提纯
过滤后的液体置于热浴容器中(外温170∘C),接上精馏装置,进行减压蒸馏。
步骤四:收集
收集100∘C∼110∘C的馏分,得到10.86g无色透明油状液体。
回答下列问题:(1)使用装置A的优点是 。
(2)步骤一中采取“温度降到−10∘C”“缓慢滴加”这些措施的可能原因有 。
a.减缓反应速率b.防止高温下发生复杂的有机副反应
c.避免原料挥发,使反应物充分反应
(3)步骤二中用饱和氯化钠溶液洗涤的目的是 。
(4)步骤三中使用减压蒸馏的目的是 。
(5)中间产物Ⅰ比戊二酸的沸点低很多的原因是 。反应中生成戊二酰氯的同时得到
两种有刺激性气味的气体,该反应的化学方程式为 。
(6)从环保角度分析,该实验装置存在明显不足之处,解决的办法是 。
(7)本实验的产率是 。
A.30% B.50% C.60% D.80%
17.(15分)氨是最基本的化工原料,常用于制液氮、氨水、硝酸、铵盐和胺类等。
(1)工业合成氨是人类科学技术的一项重大突破,其反应如下:
N (g)+3H (g)⇌2NH (g)ΔH=−92.0kJ/mol
2 2 3
根据下列键能数据,结合上述反应数据,计算N−H的键能是 kJ⋅mol−1。
化学键 N≡N H−H
键能/(kJ⋅mol−1) 946 436
(2)合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前需经过铜氨液处
2 2 3
理,目的是除去其中CO,其反应为:[Cu(NH ) ] ++CO+NH ⇌[Cu(NH ) CO] + ΔH<0。
3 2 3 3 3
+
①配离子[Cu(NH ) CO] 的中心离子是 ,配位数是 。
3 3
②铜氨溶液吸收CO适宜的生产条件: 温、 压。(填“高”“低”)
(3)恒温恒压条件下,向容器中通入1molN 和3molH ,合成氨反应用摩尔分数表示的平衡常数
2 2
1
K = ,达到平衡时N 的转化率为 。(保留3位有效数字)(已知反应的
x 27 2
xc ⋅xd n
aA(g)+bB(g)⇌cC(g)+dD(g)K = C D ,物质ⅰ的摩尔分数x = ⅰ 。√5=2.24。)
x xa ⋅xb ⅰ n
A B 总
(4)制备(NH ) SO 时所需的NH 可以通过反应合成,但缺SO ❑ 2−。有学者倡议:常温下,把石膏矿
4 2 4 3 4
中Ca(Ⅱ)转化为难溶的CaCO ,留下的SO2 和NH+ 形成(NH ) SO 。反应方程式如下:
3 4 4 4 2 4
CaSO (s)+2NH ⋅H O(aq)+H CO (aq)⇌(NH ) SO (aq)+CaCO (s)+2H O(l),化学平衡常数
4 3 2 2 3 4 2 4 3 2
为Kc,用下列相关K的符号来表示Kc= 。通过计算反应的Kc判断以上倡议
(填“可行”或“不可行”)。
(已知Ksp(CaCO )=2.5×10−9 、Ksp(CaSO )=9.0×10−6 、K❑ (NH ⋅H O)=1.8×10−5 、H CO
3 4 b 3 2 2 3
的Ka =4.0×10−7 、Ka =5.0×10−11 、Kw=1.0×10−14)
1 2
(5)NH 与镓(Ga)在高温下生成GaN,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,
3
顶点和面心的碳原子被Ga原子代替。①以晶胞边长为单位长度建立的坐标系可以表示晶胞中的原子位置,称作原子坐标。B原子坐标为
(3 3 1)
, , ,则A原子坐标为 。
4 4 4
②若N 为阿伏伽德罗常数的值,GaN晶胞中N原子与N原子之间最短的核间距离是bnm,则GaN晶体的
A
密度为 g⋅cm−3(只列计算式)。
18.(15分)G是一种辅酶类似物,其合成路线如下:
已知:Ph−是苯基
回答下列问题:
(1)B中的官能团名称是 。
(2)A生成B的反应中LiAlH 的作用是 。
4
(3)C含有羟基,分子式为C H NO Cl,则C的结构简式为 。C生成D的反应类型是
11 14 2
。
(4)E生成F的化学方程式为 。
(5)X与D互为同分异构体,符合下列条件。X可能的结构简式为 (任写一
种)。
①含有苯环
②含有硝基(−NO )和碳碳双键
2
③核磁共振氢谱显示有四组峰,峰面积之比为6:3:2:2
CH NHNH
3 2
(6)参照述合成线,以 和 为原料计制备 。该物质的合成路线为
。